| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
| 靶点 |
L-asparagine synthetase(Ki= 0.0023 M)
Aminomalonic acid targets L-asparagine synthetase from mouse pancreas and Leukemia 5178Y/AR. It is a formally competitive inhibitor versus L-aspartic acid with Ki = 0.0015 M for the partially purified enzyme from mouse pancreas [2]. For the tumoral enzyme from Leukemia 5178Y/AR, Ki = 0.0023 M when competing with L-aspartic acid [2]. Against the mouse pancreatic enzyme, inhibition patterns with ATP, L-glutamine, and ammonia gave Ki values of 0.0021 M, 0.0022 M, and 0.0022 M, respectively [2]. |
|---|---|
| 体外研究 (In Vitro) |
氨基丙二酸(Ama)已从大肠杆菌蛋白和人动脉粥样硬化斑块中分离出来。Ama 的存在具有重要的生物学意义,因为丙二酸部分可能赋予蛋白质钙结合特性。Ama 通过厌氧碱性水解获得,并通过色谱行为、定量酸介导脱羧生成甘氨酸以及明确的气相色谱/质谱检测进行鉴定。天然存在的 Ama 的色谱、化学和质谱性质与合成化合物完全相同。氨基酸分析和气相色谱/质谱分析还表明,在人动脉粥样硬化斑块的碱性水解产物中存在 β-羧基天冬氨酸和 γ-羧基谷氨酸。Ama 与 β-羧基天冬氨酸和 γ-羧基谷氨酸的比例为 20:1:10,每 1000 个甘氨酸残基中 Ama 的含量为 0.2。氨基丙二酸(Ama)是一种相对不稳定的少量氨基酸,存在于细菌或组织等复杂结构中。这或许可以解释为何尽管进行了深入研究,它此前仍未被发现[1]。
氨基丙二酸是白血病5178Y/AR细胞和鼠胰腺中L-天冬酰胺合成酶的强效体外抑制剂;该化合物与L-天冬氨酸呈竞争性抑制(肿瘤酶和胰腺酶的Ki值分别为0.0023 M和0.0015 M)[2]。 氨基丙二酸对白血病5178Y/AR细胞和鼠胰腺中的L-天冬酰胺合成酶表现出相当的体外抑制效力。在浓度分别为 0.1、0.5、0.75、1.0、2.0、3.0、4.0、5.0、8.0 和 10.0 mM 时,L5178Y/AR 的平均抑制率分别为 17%、33%、40%、45%、60%、63%、70%、75%、87% 和 89%,小鼠胰腺的平均抑制率分别为 19%、42%、50%、55%、60%、69%、77%、81%、87% 和 87% [2]。 二硫苏糖醇 (0.1–10 mM) 不拮抗氨基丙二酸的抑制作用。经含二硫苏糖醇和 EDTA 的 Tris-HCl 缓冲液彻底透析后,超过 90% 的原始酶活性得以恢复,表明抑制作用是可逆的 [2]。 氨基丙二酸 (5 mM) 未能刺激部分纯化的胰腺 L-天冬酰胺合成酶 (1,520 nmol/mg 蛋白/h) 对 L-谷氨酰胺的分解,而 L-天冬氨酸 (4,620 nmol/mg 蛋白/h) 则能做到这一点。当加入到含有等摩尔L-天冬氨酸的完整体系中时,5 mM氨基丙二酸可抑制L-谷氨酰胺的酰胺化反应37% [2]。体外实验表明,氨基丙二酸可由其前药酶促生成:二乙氨基丙二酸(酯酶催化)、酮丙二酸(转氨酶催化)和氨基丙二酰胺(L-亮氨酸氨肽酶或L-天冬酰胺酶催化)[2]。在人黑色素瘤细胞系中,与正常人黑色素细胞(HEMn-LP)相比,低转移性(A375、G361)和高转移性(A2058、SK-MEL-28)细胞中的氨基丙二酸水平显著升高,且其水平随转移潜能的增加而逐渐升高 [3]。 |
| 体内研究 (In Vivo) |
由于氨基丙二酸在体内作为L-天冬酰胺合成酶抑制剂不稳定且无活性,因此尝试通过其前体将其递送至目标作用位点:二酰胺(2-氨基丙二酰胺)、二酯(二乙氨基丙二酸酯)和酮酸(酮丙二酸)。体外实验表明,这些假定的“前药”均可被哺乳动物和细菌酶代谢为氨基丙二酸。体内实验表明,口服或腹腔注射氨基丙二酰胺后,在24小时内的任何时间点均未能抑制肿瘤L-天冬酰胺合成酶的活性。二酯和酮酸也同样无活性。然而,利用特殊技术可以证明,二酰胺能够显著抑制L-天冬氨酸酰胺化和/或掺入蛋白质的L-天冬酰胺残基。对氨基丙二酸进行化学修饰以引入不可逆反应功能是必要的[2]。
向小鼠静脉注射氨基丙二酸(剂量计算为达到瞬时浓度接近1 mM)后,在给药后10分钟和30分钟采集组织样本时,肿瘤或胰腺中的L-天冬酰胺合成酶活性未受到显著抑制[2]。 口服前药氨基丙二酰胺(饲料中添加1%,持续10天)或腹腔注射(500 mg/kg)氨基丙二酰胺、二乙氨基丙二酸或酮丙二酸,在24小时内对L5178Y/AR肿瘤或小鼠胰腺中L-天冬酰胺合成酶的抑制率不超过30%[2]。 然而,在小鼠中,腹腔注射氨基丙二酰胺(500 mg/kg)或二乙氨基丙二酸(500 mg/kg ip)在注射 L-[U-14C]天冬氨酸前 1 小时,肿瘤中蛋白质结合的 L-天冬酰胺残基的比活性分别降低了 40% 和 53%(二乙氨基丙二酸的 p < 0.05)[2]。 |
| 酶活实验 |
测定了由小鼠胰腺部分纯化的L-天冬酰胺合成酶(比活性0.07 IU/mg蛋白)催化的ATP-焦磷酸交换。在45 µL的最终体积中,将0.00077 µmol [32P]焦磷酸钠(0.723 µCi)与添加剂混合于0.5 M Tris-HCl缓冲液(pH 7.6)中,并加入5 µL酶。在37°C下孵育15分钟后,将反应体系冷冻。然后,将10 µL孵育混合物加入10 µL 0.2 M焦磷酸钠缓冲液(pH 9.2)中,再加入1 mL 80%乙醇,离心,并计数100 µL上清液。交换速率:[32P]焦磷酸钠 + ATP + MgCl2 = 40.2 nmol/mg蛋白/h;加 L-天冬氨酸 (5 mM) = 478.3;加 L-谷氨酰胺 (5 mM) = 200.7;加两者 = 481.5;单独加氨基丙二酸 (10 mM) = 438.8;加氨基丙二酸 (10 mM) + L-谷氨酰胺 (5 mM) = 571.9 [2].
为了测试氨基丙二酸的酰胺化反应,将含有 L-[U-14C]谷氨酰胺 (0.25 µCi)、0.025 M 氨基丙二酸(溶于 pH 8.4 的 Tris-HCl 缓冲液)、0.05 M ATP(含 0.15 M MgCl2)和部分纯化的胰 L-天冬酰胺合成酶的反应混合物在 37°C 下孵育 30 分钟。采用 L-谷氨酸脱羧酶法、纸层析法(异丙醇:HCl:水 4:1:1)或高压电泳法(0.1 M 磷酸钠缓冲液,pH 6.8,3000 V,1 小时)测定 L-[U-14C]谷氨酸的生成量。氨基丙二酸并未刺激谷氨酰胺的分解,其效果未超过对照组[2]。 采用 L-谷氨酸脱氢酶法测定氨的生成量,评估了各种酶(每种 0.05 mg)对氨基丙二酰胺(0.1 M,溶于 Tris-HCl 缓冲液,pH 2.6、7.0 和 8.4)的分解作用。L-亮氨酸氨肽酶的 NH3 释放速率为 1,808 nmol/mg 蛋白/h;胡萝卜软腐欧文氏菌 L-天冬酰胺酶的释放速率为该酶的 15%。其他酶(酰基酶、菠萝蛋白酶、羧肽酶、胰凝乳蛋白酶原、纤维蛋白溶素、无花果蛋白酶、木瓜蛋白酶、胃蛋白酶、凝血酶、胰蛋白酶)的含量均低于5% [2]。 在37°C下,用L-[4-14C]天冬氨酸和L-谷氨酸草酰乙酸转氨酶(0.05 mg)对酮丙二酸(0.03 M)进行1小时的转氨反应,并通过放射性测定法进行监测;酮丙二酸的Km为6.2 mM,Vmax为3.2 mmol/mg蛋白/min [2]。 |
| 细胞实验 |
在对数生长期后期收获需氧培养的大肠杆菌,用冷的0.14 M KCl溶液重悬洗涤两次。将细胞与两倍重量的氧化铝和TM缓冲液(50 mM Tris-HCl/10 mM MgCl₂,pH 7.5)在0℃下研磨破碎,TM缓冲液缓慢加入至最终体积为2.5 ml/g细胞。低速离心(10,000 rpm,40℃,15 min;Sorvall'SS-34转子)后,取上清液进行澄清(18,000 rpm,3℃,25 min;Spinco type 30转子),转移至干净的离心管中,然后进行高速离心(40,000 rpm,3℃,7.5 h;Spinco type 42.1转子)。用移液器吸取最终上清液的上三分之二清澈部分。采用氯化锂/碘液法去除RNA (7)。用10%三氯乙酸在冰上沉淀胞质蛋白1小时,然后离心(在15 ml Cbrex管中,40℃下以8000 rpm离心20分钟;Sorvall SS-34转子)。沉淀物用冷的95%乙醇彻底洗涤,再次离心,并在真空下短暂干燥。将样品(0.3 g)在氮气氛围下,于110℃下用3 ml 2 M KOH水解24小时。取自死后人主动脉的中度钙化动脉粥样硬化斑块样品,冷冻后反复切碎并交替冷冻。未去除钙盐。将所得颗粒(0.3-0.5 g)在氮气氛围下于 110℃ 的 2 M KOH 溶液中水解 24 小时 [1]。在体外,测定了 L5178Y/AR 细胞(对 L-天冬酰胺酶具有抗性)和小鼠胰腺粗提物中 L-天冬酰胺合成酶的活性,测定条件为存在或不存在不同浓度(0.1-10 mM)的氨基丙二酸。L-谷氨酰胺和 L-天冬氨酸的最终浓度分别为 0.013 M 和 0.00037 M。抑制率的计算方法如文献 [2] 所述。ATP-焦磷酸交换实验采用小鼠胰腺部分纯化的酶(比活性为 0.07 IU/mg)。制备物中L-天冬氨酰、L-谷氨酰和L-天冬酰胺酰tRNA合成酶的比活性分别为2.45、0和74.19 nmol/mg蛋白/h [2]。
在人黑色素瘤细胞系(A375、G361低转移细胞系;A2058、SK-MEL-28高转移细胞系)中,将细胞培养于含10%胎牛血清和1%青霉素-链霉素的适宜培养基中,在细胞汇合度达到约90%时收集细胞并冻干。提取氨基丙二酸,并通过GC-MS进行鉴定。氨基丙二酸的含量从正常黑色素细胞到低转移细胞再到高转移细胞逐渐升高[3]。 |
| 动物实验 |
携带1 cm L5178Y/AR肿瘤结节的雄性BDF1小鼠分别接受生理盐水、氨基丙二酰胺(4 g/kg)或二乙氨基丙二酸(4 g/kg)的口服治疗。一小时后,所有小鼠均接受腹腔注射L-[4-14C]天冬氨酸(50 µCi/只)。放射性同位素注射一小时后,处死小鼠,取出肿瘤和胰腺,并在9倍体积的冰冷0.05 M Tris-HCl缓冲液(pH 8.4)中匀浆。蛋白质组分用高氯酸沉淀,乙醇洗涤,在37℃下用蛋白酶(0.1% w/v,溶于含1 mM CaCl₂的0.01 M Tris-HCl缓冲液,pH 8.4)消化24小时,然后加热并离心。采用放射性测定法测定了L-天冬酰胺残基的比活性[2]。
在体内分解研究中,小鼠腹腔注射氨基丙二酰胺(500 mg/kg)或生理盐水。1小时后,取出肾脏和肝脏,并用氨基酸分析仪分析50%乙醇提取物,以检测推测的单酰胺[2]。 在抑制研究中,小鼠在处死前5-19天饲喂含1%氨基丙二酰胺的粉状饲料。将组织在3倍体积的0.05 M Tris-HCl(pH 8.4)中匀浆,并测定L-天冬酰胺合成酶活性[2]。 |
| 药代性质 (ADME/PK) |
氨基丙二酸极不稳定,易发生自发脱羧和酶促脱羧反应。它在体内不稳定且惰性,是L-天冬酰胺合成酶的抑制剂[2]。氨基丙二酸在酸性条件下(1.0 M HCl,100°C,1 小时)可脱羧生成甘氨酸[1]。前药二乙氨基丙二酸、氨基丙二酰胺和酮丙二酸在体外可被哺乳动物和细菌酶代谢为氨基丙二酸:酯酶将二乙氨基丙二酸裂解为单乙氨基丙二酸,然后裂解为氨基丙二酸;L-谷氨酸草酰乙酸转氨酶将酮丙二酸转氨。 L-亮氨酸氨肽酶和L-天冬酰胺酶将氨基丙二酰胺分解为氨基丙二酸[2]。在小鼠肝脏和肾脏匀浆中,氨基丙二酰胺分解的表观亲和常数分别为84 mM和102 mM[2]。
|
| 参考文献 |
|
| 其他信息 |
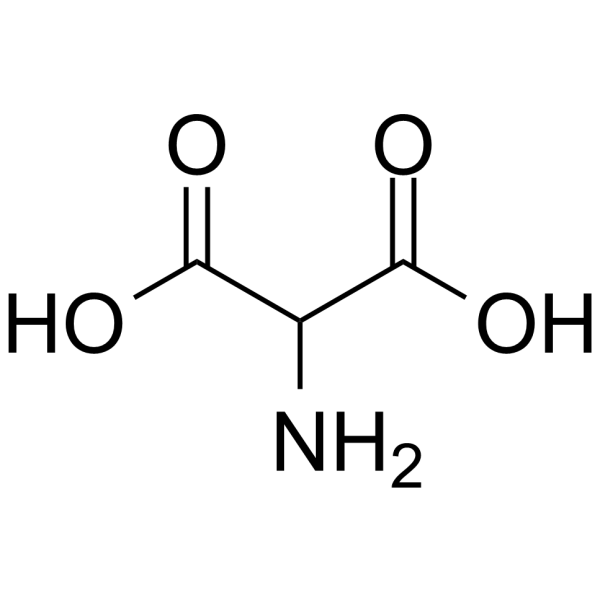
氨基丙二酸 (AMA) 是一种氨基二羧酸,由丙二酸分子中的亚甲基氢原子被氨基取代而形成。它是人和大型蚤(Daphnia magna)体内的代谢产物。其功能与丙二酸相关;它是氨基丙二酸 (1-) 的共轭酸。AMA 是大肠杆菌(K12 菌株、MG1655 菌株)中发现或产生的代谢产物。据报道,秀丽隐杆线虫中也存在 AMA,相关数据可供参考。
氨基丙二酸(2-羧基甘氨酸)是 3-羧基天冬氨酸 (Asa) 和 4-羧基谷氨酸 (Gla) 的同系物。此前仅在自然界中偶尔发现过(例如,鱼类引诱剂阿卡明、抗生素马洛霉素)[1]。 在动脉粥样硬化斑块中,氨基丙二酸与Asa与Gla的比例为20:1:10,每1000个甘氨酸残基中氨基丙二酸的含量为0.2。斑块中氨基丙二酸的存在意义重大,因为它可能赋予蛋白质钙结合特性,而钙结合似乎是动脉粥样硬化发展的初始事件[1]。氨基丙二酸残基,即使位于蛋白质内部,也可能像Gla残基一样促进钙结合,因为肽键的羧基可以与游离羧基结合,从而实现丙二酸型螯合[1]。在黑色素瘤中,氨基丙二酸被确定为一种潜在的新型生物标志物,可用于区分不同转移阶段。其来源可能与蛋白质合成缺陷、自由基对蛋白质的损伤或丝氨酸羟甲基转移酶(SHMT)的生成有关[3]。 |
| 分子式 |
C3H5NO4
|
|---|---|
| 分子量 |
119.0761
|
| 精确质量 |
119.021
|
| CAS号 |
1068-84-4
|
| PubChem CID |
100714
|
| 外观&性状 |
White to off-white solid
|
| 密度 |
1.7±0.1 g/cm3
|
| 沸点 |
402.6±40.0 °C at 760 mmHg
|
| 熔点 |
240-245°C
|
| 闪点 |
197.3±27.3 °C
|
| 蒸汽压 |
0.0±2.0 mmHg at 25°C
|
| 折射率 |
1.545
|
| 来源 |
Endogenous metabolite
|
| LogP |
-0.27
|
| tPSA |
100.62
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
2
|
| 重原子数目 |
8
|
| 分子复杂度/Complexity |
107
|
| 定义原子立体中心数目 |
0
|
| SMILES |
O([H])C(C([H])(C(=O)O[H])N([H])[H])=O
|
| InChi Key |
JINBYESILADKFW-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C3H5NO4/c4-1(2(5)6)3(7)8/h1H,4H2,(H,5,6)(H,7,8)
|
| 化学名 |
2-aminopropanedioic acid
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
H2O : ~8.33 mg/mL (~69.95 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 5 mg/mL (41.99 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶。 (<60°C).
请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 8.3977 mL | 41.9886 mL | 83.9772 mL | |
| 5 mM | 1.6795 mL | 8.3977 mL | 16.7954 mL | |
| 10 mM | 0.8398 mL | 4.1989 mL | 8.3977 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。