| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
CXCR4; Inflammation/Immunology
The targets of Baohuoside I are CXC chemokine receptor 4 (CXCR4) and nuclear factor κB (NF-κB)[1] The targets of Baohuoside I are c-Jun N-terminal kinase (JNK) and p38 mitogen-activated protein kinase (p38MAPK)[2] |
|---|---|
| 体外研究 (In Vitro) |
CXCR4 抑制剂 baohuoside I 在 12–25 μM 时可抑制 CXCR4 的表达。 baohuoside I (0-25 μM) 以剂量依赖性方式抑制 NF-κB 激活和 CXCL12 引起的宫颈癌细胞的侵袭。保活苷 I 还可以防止乳腺癌细胞侵袭性生长[1]。分别在24小时、11.5小时、48小时和72小时时,baohuoside I降低A549细胞的活力,IC50分别为25.1 μM、11.5 μM和9.6 μM。在 A549 细胞中,baohuoside I (25 μM) 刺激 p38MAPK 和 JNK 信号级联,增加 ROS 水平,并抑制 caspase 级联 [2]。保霍苷 I(3.125、6.25、12.5、25.0 和 50.0 µg/mL)对食管鳞癌 Eca109 细胞的增殖有显着的剂量依赖性抑制,48 小时的 IC50 为 4.8 µg/mL[3]。
1. 在人宫颈癌 HeLa 细胞中,Baohuoside I 以剂量和时间依赖方式下调 CXCR4 表达,孵育 12 小时即可观察到抑制效果,最低有效浓度为 12.5 μM,25 μM 作用 24 小时可显著抑制 CXCR4 表达[1] 2. 在乳腺癌 MDA-MB-231 细胞、肝癌 HepG2 细胞、胰腺癌 HPAC 细胞中,25 μM Baohuoside I 作用 24 小时可下调 CXCR4 表达,其中对 MDA-MB-231 细胞的抑制效果最显著,且在该细胞中呈剂量依赖抑制 CXCR4 表达[1] 3. Baohuoside I 对 CXCR4 的下调并非通过蛋白酶体或溶酶体降解途径实现,而是发生在转录水平,以剂量依赖方式降低 CXCR4 mRNA 水平[1] 4. 在 HeLa 细胞中,Baohuoside I 以剂量依赖方式抑制 NF-κB 的组成型激活[1] 5. 25 μM Baohuoside I 预处理可有效抑制 CXCL12 诱导的 HeLa 细胞和 MDA-MB-231 细胞侵袭[1] 1. 对人非小细胞肺癌 A549 细胞具有细胞毒性,以时间和浓度依赖方式抑制细胞活力,24 h、48 h、72 h 的半数抑制浓度(IC50)分别约为 25.1 μM、11.5 μM、9.6 μM[2] 2. 诱导 A549 细胞凋亡,25 μM 处理 24 h 后,凋亡细胞比例从对照组的 8.9±1.1% 升高至 58.5±2.5%,亚 G1 期细胞比例从 0.13±0.02% 升高至 18.31±0.9%,TUNEL 染色显示阳性细胞显著增加[2] 3. 导致 A549 细胞线粒体膜电位(DWM)下降,绿色/红色荧光强度比增至对照组的 4 倍,且能促进线粒体中细胞色素 c(Cytc)释放到细胞质中[2] 4. 上调 A549 细胞中 BAX/Bcl-2 比率,激活 caspase 3 和 caspase 9,导致聚腺苷二磷酸核糖聚合酶(PARP)降解[2] 5. 诱导 A549 细胞过量产生活性氧(ROS),25 μM 处理 12 h 后,DCF 阳性细胞比例从 4.1±0.9% 增至 64.3±2.9%,ROS 生成在 6 h 开始升高并持续至 24 h[2] 6. 以浓度和时间依赖方式激活 A549 细胞中 JNK 和 p38MAPK 通路,9 h 时可检测到 JNK 和 p38MAPK 的磷酸化激活,且持续至 24 h,ERK 磷酸化水平无明显变化[2] 7. ROS 清除剂 NAC(1 mM)预处理可显著逆转 Baohuoside I 诱导的 ROS 积累(降至 23.4±2.7%)、线粒体膜电位下降、细胞凋亡(降至 25.9±3.1%)和细胞死亡(从 59.6±2.6% 降至 27.2±3.3%),并抑制 JNK 和 p38MAPK 通路激活[2] 8. 泛 caspase 抑制剂 Z-VAD-FMK(50 μM)预处理只能部分抑制 Baohuoside I 诱导的 A549 细胞凋亡[2] 9. p38MAPK 抑制剂 SB203580(25 μM)和 JNK 抑制剂 SP600125(25 μM)与 25 μM Baohuoside I 共孵育 24 h,可有效减弱 A549 细胞凋亡[2] 1. 对人食管鳞状细胞癌 Eca109 细胞具有增殖抑制作用,呈剂量和时间依赖关系,48 h 半数抑制浓度(IC50)为 24.8 μg/ml,50 μg/ml 浓度下细胞生长几乎停滞[3] 2. 诱导 Eca109 细胞凋亡,呈剂量依赖关系,50 μg/ml 处理 48 h 后,亚 G1 期凋亡细胞比例从对照组的 3.26% 升高至 49.21%[3] 3. 下调 Eca109 细胞中 β-catenin、survivin 和 cyclin D1 的 mRNA 表达水平,呈剂量依赖关系[3] 4. 下调 Eca109 细胞中 β-catenin、survivin 和 cyclin D1 的蛋白表达水平,呈剂量依赖关系[3] |
| 体内研究 (In Vivo) |
在裸鼠中,baohuoside I (25 mg/kg) 降低生存素、细胞周期蛋白 D1 和 β-catenin 蛋白水平的表达[3]。
baohuoside I抑制人食管癌细胞异种移植瘤模型的体内肿瘤生长。采用人食管鳞状细胞癌异种移植模型研究保活苷1的体内抗癌活性。简单地说,将指数生长的萤火虫荧光素酶标记的Eca109细胞注射到Babl/c裸鼠的侧翼。癌细胞注射1周后,局部给药baohuoside I (25 mg/kg体重,每天1次)。小鼠在另外三周内每周接受一次Xenogen生物发光成像。如图5所示,baohuoside I治疗组与对照组相比,Xenogen成像信号明显降低。事实上,定量分析显示,在治疗后3周,即使肿瘤没有完全消除,baohuoside I介导的对异种移植肿瘤生长的抑制也具有统计学意义(p<0.01)(图5A和B)。组织学分析(H&E染色)表明,baohuoside I治疗组肿瘤肿块的细胞数量减少[3]。 1. 在人食管癌 Eca109-luc 裸鼠异种移植模型中,25 mg/kg 剂量 Baohuoside I 瘤内注射,每日一次,持续三周,可显著抑制肿瘤生长,生物发光成像信号强度显著降低(p<0.01)[3] 2. 组织学分析显示,用药组肿瘤组织细胞密度降低[3] 3. 肿瘤组织中 β-catenin、survivin 和 cyclin D1 蛋白表达水平分别下降 40%、41% 和 45%(均 p<0.01)[3] |
| 酶活实验 |
在这项工作中,研究人员研究了韩国淫羊藿(Epimedium koreanum)的一种成分保火苷I (baohuoside I)在宫颈癌和乳腺癌细胞中作为CXCR4表达和功能的调节因子。我们观察到保火苷I在HeLa细胞中以剂量和时间依赖的方式下调CXCR4的表达。用蛋白酶体和溶酶体抑制剂治疗对保火苷I抑制CXCR4表达的能力没有实质性影响。当我们研究其作用的分子机制时,我们发现CXCR4的表达抑制发生在mRNA水平。保火苷I引起的CXCR4表达水平下降与抑制cxcl12诱导的宫颈癌和乳腺癌细胞的侵袭有关。综上所述,我们的研究结果表明保火苷I是通过下调CXCR4的表达来发挥其抗转移作用的,因此具有抑制肿瘤转移的潜力[1]。
|
| 细胞实验 |
Western Blotting[1]< br >
为了检测CXCR4,用RIPA缓冲液[150 mM NaCl, 10 mM Tris (pH 7.2), 0.1%十二烷基硫酸钠(SDS), 1% Triton X-100, 1%脱氧胆酸盐,和5 mM乙二胺四乙酸(EDTA)],用完整的蛋白酶抑制剂鸡尾酒片富集,然后在冰上常规涡旋孵育30 min,然后在14000 rpm和4°C下离心15 min。使用比辛醌酸(BCA)蛋白测定试剂盒测定蛋白浓度。蛋白质样品在SDS样品缓冲液中煮沸5分钟,在10% SDS -聚丙烯酰胺凝胶上溶解。电泳后,将蛋白转移到聚二氟乙烯(PVDF)膜上,用5%脱脂干牛奶在含0.1% Tween 20 (TBST)的tris缓冲盐水中阻断,与一抗孵育至适当的终浓度,然后与辣根过氧化物酶偶联的抗兔或抗小鼠二抗杂交。每一步,用TBST洗涤膜3次,持续10分钟,根据制造商的说明,将转移的蛋白质与超信号微化学发光底物或硬膜发光底物孵育2分钟,并用成像仪LAS 4000进行可视化。 Invasion Assay[1]< br > 根据制造商的说明,使用Bio-Coat Matrigel入侵试验系统进行体外入侵试验。将癌细胞(5 × 104 /毫升)悬浮在培养基中,并将其植入孔径为8 μm的聚碳酸酯膜预涂覆的transwell腔室中。加保活苷I (25 μM)或不加保活苷I (25 μM)预孵育后,将传孔室置于24孔板中,分别加入基础培养基或含有100 ng/mL CXCL12的基础培养基。孵育后(HeLa和MDA-MB-231孵育24 h),用棉签擦拭transwell腔室上表面,固定入侵细胞并用Diff-Quick染色。在随机选择的5个显微镜视野(100倍)中计数入侵细胞的数量。 1. 细胞培养:人宫颈癌 HeLa 细胞采用添加 10% 胎牛血清(FBS)和 1% 抗生素的 RPMI1640 培养基培养;乳腺癌 MDA-MB-231 细胞、胰腺癌 HPAC 细胞、肝癌 HepG2 细胞采用添加 10% FBS 和 1% 抗生素的 Dulbecco 改良 Eagle 培养基(DMEM)培养。所有细胞均置于 37℃、5% CO₂ 和 95% 空气的环境中,当细胞汇合度达到 80% 时,用 0.25% 胰蛋白酶 - EDTA 消化 3-5 分钟进行传代[1] 2. Western Blot 实验:收集经 Baohuoside I 处理后的细胞,用含完整蛋白酶抑制剂混合物的 RIPA 缓冲液(150 mM NaCl、10 mM Tris(pH 7.2)、0.1% 十二烷基硫酸钠(SDS)、1% Triton X-100、1% 脱氧胆酸盐、5 mM 乙二胺四乙酸(EDTA))裂解细胞,冰上孵育 30 分钟并定期涡旋,随后在 4℃、14000 rpm 条件下离心 15 分钟。采用 BCA 蛋白测定试剂盒测定蛋白浓度,蛋白样品在 SDS 样品缓冲液中煮沸 5 分钟后,通过 10% SDS - 聚丙烯酰胺凝胶电泳分离,随后转移至聚偏氟乙烯(PVDF)膜。膜用含 5% 脱脂奶粉的 Tris 缓冲盐溶液(含 0.1% Tween 20,TBST)封闭,加入适当终浓度的一抗孵育后,再与辣根过氧化物酶偶联的二抗杂交。每步反应后用 TBST 洗涤膜 3 次,每次 10 分钟,最后用化学发光底物孵育 2 分钟,通过图像分析系统可视化蛋白条带[1] 3. RT - PCR 实验:采用 Trizol 试剂提取细胞总 RNA,按照试剂盒说明使用逆转录预混液合成 cDNA。以甘油醛 - 3 - 磷酸脱氢酶(GAPDH)为内参,通过定量 RT - PCR 分析 CXCR4 的相对表达。CXCR4 的引物序列为正义链(5′-CCG TGG CAA ACT GGT ACT TT-3′)和反义链(5′-TTT CAG CCA ACA GCT TCC TT-3′);GAPDH 的引物序列为正义链(5′-CAG CCT CAA GAT CAT CAG CA-3′)和反义链(5′-GTC TTC TGG GTG GCA GTG AT-3′)。PCR 反应体系包含 2.5 μL 10×Taq 反应缓冲液、0.5 μL 10 mM dNTP、1 μL 上下游引物和 2 μL 模板 DNA,总体积为 25 μL。扩增产物经 1.5% 琼脂糖凝胶电泳(含安全染料)分离后,通过图像分析系统拍照记录[1] 4. 实时定量 PCR 实验:以合成的 cDNA 为模板,使用 CXCR4 和 GAPDH 特异性引物,采用 SYBR Green 试剂盒在实时荧光定量 PCR 仪上进行反应。PCR 程序为 95℃ 预变性 10 分钟,随后进行 40 个循环(95℃ 10 秒、55℃ 30 秒),最后 40℃ 冷却 30 秒。以 GAPDH 的交叉点(Cp)值为对照,对 CXCR4 的 Cp 值进行归一化处理,用于相对定量分析[1] 5. 侵袭实验:采用基质胶包被的穿膜小室(聚碳酸酯膜孔径 8 μm)进行体外侵袭实验。将癌细胞(5×10⁴ 个/毫升)悬浮于培养基中并接种到上室,经 25 μM Baohuoside I 预处理或未预处理后,将穿膜小室置于 24 孔板中,下室加入基础培养基或含 100 ng/mL CXCL12 的基础培养基。HeLa 细胞和 MDA-MB-231 细胞孵育 24 小时后,用棉签擦拭上室表面,固定并染色侵袭到下室的细胞,在 100 倍显微镜下随机选取 5 个视野计数侵袭细胞数[1] 6. 电泳迁移率变动分析(EMSA):使用含 NF-κB 结合基序的寡核苷酸探针,用 DIG-ddUTP 进行末端标记。取 10 μg 样品蛋白与 DIG 标记的探针在室温下孵育 30 分钟进行结合反应,随后在 6% 非变性聚丙烯酰胺凝胶中(以 0.5×TBE 为电泳缓冲液)分离 DNA - 蛋白复合物。电泳后将凝胶转移至尼龙膜,通过化学发光法检测,并用图像分析仪定量信号强度[1] 1. 细胞培养:人非小细胞肺癌 A549 细胞采用添加 10% 热灭活胎牛血清(FBS)、100 单位/ml 青霉素和 100 μg/ml 链霉素的 RPMI-1640 培养基,在 37℃、5% CO₂ 湿润空气环境中培养,定期检测支原体感染呈阴性[2] 2. 细胞活力检测(MTT 法):将 1×10⁴ 个/孔细胞接种到 96 孔板,分别用 6.25、12.5、25 μM Baohuoside I 或 1 mM NAC 处理 24、48、72 h。去除含 MTT 的培养基后,每孔加入二甲基亚砜(DMSO)溶解形成的结晶,混合后用酶标仪在 540 nm 处检测吸光度[2] 3. 细胞周期分析:1×10⁶ 个/ml 细胞用 6.25、12.5、25 μM Baohuoside I 处理 24 h,用 PBS 洗涤后,胰蛋白酶-EDTA 收集细胞并计数,用 75% 乙醇固定后于 4℃ 保存。样品重悬于低渗碘化丙啶(PI)溶液(50 μg/ml PI、0.1% 柠檬酸钠、0.1% Triton X-100、0.1 mg/ml 核糖核酸酶 A),避光孵育 1 h 后,用流式细胞仪分析[2] 4. 凋亡分析(Annexin V/PI 双染法):1×10⁶ 个/ml A549 细胞先用 50 μM Z-VAD-FMK 或 1 mM NAC 预处理 1 h,再用 6.25、12.5、25 μM Baohuoside I 处理 24 h;或用 25 μM Baohuoside I 与 25 μM SB203580 或 25 μM SP600125 共孵育 24 h。洗涤后的细胞重悬于 Annexin-V 结合缓冲液,加入 FITC 标记的 Annexin-V 和 PI,室温避光孵育 15 min 后,添加结合缓冲液,用流式细胞仪检测凋亡细胞[2] 5. TUNEL 分析:2×10⁵ 个/ml A549 细胞用 6.25、12.5、25 μM Baohuoside I 处理后,用多聚甲醛固定,4℃ 下用 Triton-X100 通透 5 min。洗涤后,加入 TUNEL 反应混合物 37℃ 孵育 60 min,DNA 片段标记为绿色斑点;再用 DAPI(PBS 稀释至 1:20000)标记所有细胞核,洗涤后用荧光显微镜拍照[2] 6. 线粒体膜电位(DWM)检测:A549 细胞接种至汇合度 70-80%,用 6.25、12.5、25 μM Baohuoside I 处理 24 h,或用 1 mM NAC 或 5 μM FCCP 预处理 1 h。用 PBS 洗涤两次后,加入 JC-1 孵育 30 min,去除 JC-1 后,胰蛋白酶消化收集细胞,重悬于 PBS。用流式细胞仪检测每个样品 10000 个细胞在 530 nm(绿色荧光,FL-1)和 590 nm(红色荧光,FL-2)的荧光强度,通过绿色/红色荧光比率评估 DWM 变化[2] 7. 细胞内 ROS 生成检测:1×10⁶ 个/ml 细胞用 6.25、12.5、25 μM Baohuoside I 处理 12 h,或用 1 mM NAC 预处理 1 h,然后加入 10 μM DCF-DA 37℃ 孵育 15 min。细胞内 ROS 可将 DCF-DA 氧化为荧光化合物 2',7'-二氯荧光素(DCF),用流式细胞仪在激发波长 480 nm、发射波长 525 nm 处检测[2] 8. 细胞质和线粒体组分制备:2×10⁶ 个/ml 细胞用 PBS 洗涤后,重悬于等渗匀浆缓冲液,匀浆 80 次后,30g 离心 5 min 去除未破碎细胞。分别以 800g 离心 10 min 和 14000g 离心 30 min 分离线粒体组分[2] 9. Western blot 分析:2×10⁶ 个/ml A549 细胞用 6.25、12.5、25 μM Baohuoside I 处理 24 h 后,用冰预冷的 PBS 洗涤两次,用含 50 mM Tris–HCl、150 mM NaCl、0.02% 叠氮钠和 1% NP-40 的裂解液提取蛋白。取 50 μg 上清蛋白用 SDS 样品缓冲液煮沸变性,通过 10% SDS–PAGE 分离,半干转印至聚偏氟乙烯膜。膜用含 Tween 20 的 5% 脱脂牛奶封闭,加入针对 PARP、剪切型 PARP、Bcl-2、BAX、caspase 3、剪切型 caspase 3、caspase 9、剪切型 caspase 9 和 β-肌动蛋白的一抗孵育,用 TBS 洗涤三次后,加入辣根过氧化物酶结合的二抗室温孵育 1 h,化学发光试剂显影,用图像分析软件进行蛋白表达定量[2] 1. 细胞培养:人食管鳞状细胞癌 Eca109 细胞采用添加 10% 胎牛血清、100 U/ml 青霉素和 100 μg/ml 制霉菌素的 RPMI-1640 培养基,在 37℃、5% CO₂ 湿润环境中培养,汇合度达 80% 时用 0.25% 胰蛋白酶消化传代[3] 2. 细胞活力检测(MTT 法):将 1×10⁴ 个细胞/孔接种到 96 孔板,加入 3.125、6.25、12.5、25.0、50.0 μg/ml 浓度的 Baohuoside I,每个浓度设 10 个复孔,分别孵育 24、48、72 h。每孔加入 MTT 溶液(5 mg/ml 溶于 PBS)孵育 4 h,1500×g 离心 5 min 后去除培养基,加入 0.1 ml 二甲基亚砜(DMSO)溶解结晶,振荡后用酶标仪在 570 nm 波长处检测吸光度,以空白对照组细胞活力为 100% 计算药物对细胞活力的抑制率[3] 3. 凋亡分析(PI 染色法):Eca109 细胞用 0-50 μg/ml 浓度的 Baohuoside I 处理 48 h 后收集,重悬于含 50 μg/ml PI、0.1% Triton X-100、0.1 mmol/L EDTA(Na)₂ 和 50 μg/ml RNase 的 PBS 溶液中,避光孵育 30 min,用流式细胞仪(Ex=488 nm,Em=530 nm)分析,亚 G0 峰细胞视为凋亡细胞[3] 4. Western blot 分析:用细胞裂解缓冲液提取 Eca109 细胞总蛋白,超声破碎 20 sec 后 1500×g 离心 10 min 收集上清。取 20-100 μg 蛋白样品经 10% SDS-PAGE 凝胶(120 V 电泳 2 h)分离后,转移至硝酸纤维素膜(135 mA 转移 2 h)。膜用含 5% 牛奶的 TBST 缓冲液封闭过夜,洗涤三次后加入抗 β-catenin、抗 survivin、抗 cyclin D1 一抗室温孵育 2 h,再用 TBST 洗涤三次,加入荧光标记的二抗孵育 1 h,洗涤四次后用红外成像仪成像[3] 5. RT-PCR 分析:用 TRI 试剂提取细胞总 RNA,取 3-5 μg RNA 加入 oligo(dT)18、dNTP 和逆转录酶合成 cDNA。以 cDNA 为模板,采用特异性引物(cyclin D1 退火温度 55℃、35 个循环;survivin 退火温度 55℃、38 个循环;β-actin 退火温度 55℃、35 个循环)进行 PCR 扩增,扩增产物经 1.5% 琼脂糖凝胶电泳分离后,用图像分析系统分析[3] 6. 稳定标记 Eca109-luc 细胞系建立:通过脂质体转染法将含萤火虫荧光素酶基因的重组质粒转入 Eca109 细胞,用 1.0 μg/ml 嘌呤霉素筛选 7 天获得稳定细胞系,加入 150 μg/ml D-荧光素后用活体成像系统检测荧光素酶活性[3] |
| 动物实验 |
人食管鳞状细胞癌异种移植瘤模型。[3]
动物的使用和护理均遵循机构动物护理和使用委员会批准的指南。本研究使用4至6周龄的雌性Balb/c裸鼠。收集亚融合状态的Eca109-Luc细胞,并用PBS重悬至终浓度为2×10⁷个细胞/ml。注射前,将细胞重悬于PBS中,并通过0.4%台盼蓝排除法进行分析(活细胞率>90%)。皮下注射时,使用27G针头将约1×10⁶个Eca109-Luc细胞悬浮于200 µl PBS中,注射到每只小鼠的左侧腹部。肿瘤细胞注射后1周,每天一次对小鼠进行病灶内注射宝活苷I(25 mg/kg/只),而10只用于载体处理的小鼠则注射等体积的PBS。 Xenogen生物发光成像。[3] 小动物全身光学成像按所述方法进行。简而言之,小鼠用异氟烷麻醉,麻醉剂通过连接Xenogen IVIS成像系统的鼻罩进行,皮下注射后每周进行一次成像。成像时,小鼠腹腔注射0.1 ml无菌PBS,其中含有100 mg/kg体重的D-荧光素钠盐。通过将发射光叠加到动物的灰度照片上获得伪图像。定量分析使用Xenogen的Living Image V2.50.1软件进行,具体方法如前所述。 3周后处死动物,取出肿瘤样本进行组织学评估和蛋白质印迹分析。 1. 建立人食管癌裸鼠异种移植模型:选择4-6周龄的雌性Balb/c裸鼠。将 Eca109-luc 细胞重悬于 PBS 中,浓度为 2×10⁷ 个细胞/ml(台盼蓝染色显示活细胞率 >90%),取 200 μl 细胞悬液(含 1×10⁶ 个细胞)皮下注射至每只裸鼠左侧腹部[3] 2. 给药方案:肿瘤细胞注射一周后,治疗组裸鼠每日一次病灶内注射 25 mg/kg 的宝火苷 I,对照组注射等体积的 PBS,连续给药三周[3] 3. 体内成像检测:每周用异氟烷麻醉裸鼠,腹腔注射 100 mg/kg 体重的 D-荧光素钠盐水溶液。图像由体内光学成像系统采集,荧光信号强度使用图像分析软件进行定量分析[3] 4. 组织处理:给药三周后,处死裸鼠,解剖肿瘤组织。部分组织用10%福尔马林固定,石蜡包埋后进行苏木精-伊红(H&E)染色,部分组织用于蛋白质印迹分析[3] |
| 药代性质 (ADME/PK) |
1. 由于顶端外排转运蛋白的大量外排,宝菘苷I的生物利用度较低[2]
2. 宝菘苷I-磷脂复合物可提高其在Caco-2细胞单层模型中的吸收[2] 3. 维生素E生育酚聚乙二醇琥珀酸酯1000可增强宝菘苷I在四位点大鼠肠灌注模型中的肠道吸收[2] |
| 参考文献 |
|
| 其他信息 |
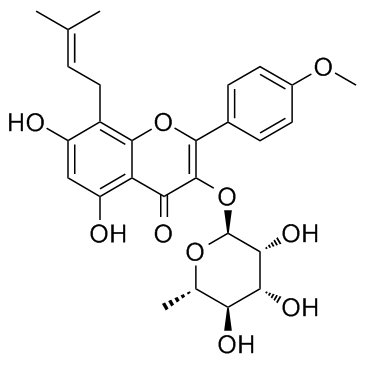
淫羊藿苷II是一种糖基氧基黄酮,其化学名称为3,5,7-三羟基-4'-甲氧基-8-异戊烯基黄酮,其中3位上的羟基已转化为α-L-鼠李糖苷。它具有植物代谢产物、抗炎剂、抗肿瘤剂和细胞凋亡诱导剂等多种活性。它在功能上与α-L-鼠李糖吡喃糖相关。
据报道,在有相关数据的淫羊藿(Epimedium pubescens)、尖叶淫羊藿(Epimedium acuminatum)和其他生物体中均发现了宝火苷I。 1. 宝火苷I,又名淫羊藿苷II,提取自朝鲜淫羊藿(Epimedium koreanum)的茎和叶,传统上用于中医治疗骨质疏松症、月经不调和关节疼痛[1]。 2. 先前的研究表明,宝火苷I对多种癌细胞具有抗癌活性,包括前列腺癌、骨髓瘤、骨肉瘤和皮肤癌。其作用机制包括降低人骨肉瘤细胞中缺氧诱导因子(HIF)1α蛋白水平,抑制前列腺癌PC3细胞中的环氧合酶(COX)2/前列腺素E2通路,阻断U266多发性骨髓瘤细胞中的信号转导和转录激活因子(STAT)3信号通路,以及通过内在和外在信号通路诱导乳腺癌MCF7细胞凋亡[1] 3. 宝火苷I通过下调CXCR4表达发挥抗转移作用,而CXCR4/CXCL12轴是肿瘤转移的关键介质。高表达 CXCR4 的肿瘤细胞倾向于转移至高分泌 CXCL12 的器官[1] 1. 菖蒲苷 I,又名淫羊藿苷 II,是从淫羊藿(Epimedium koreanum Nakai)中分离得到的一种黄酮类化合物,具有抗炎和抗癌活性[2] 2. 菖蒲苷 I 是淫羊藿苷在体内的主要生物活性代谢产物,在灌注大鼠肠道模型中,淫羊藿苷可快速水解为菖蒲苷 I[2] 3. 菖蒲苷 I 诱导 A549 细胞凋亡的机制涉及 ROS 介导的线粒体途径和 MAPK 途径。 ROS作为上游信号,可激活JNK和p38MAPK通路,从而触发线粒体功能障碍和凋亡相关分子的激活[2] 4. 宝菖蒲苷I诱导A549细胞凋亡涉及caspase依赖性和非caspase依赖性机制[2] 1. 宝菖蒲苷I是从黄菖蒲皮中提取的一种黄酮类化合物,分子式为C27H30O10,分子量为514,纯度>96%[3] 2. 宝菖蒲苷I通过抑制β-catenin依赖性信号通路并下调下游靶基因survivin和cyclin D1的表达,发挥抑制食管癌细胞增殖和诱导其凋亡的作用[3] 3. 宝火苷I对食管鳞状细胞癌具有潜在的治疗价值,为食管癌的新治疗方案提供了实验证据[3] |
| 分子式 |
C27H30O10
|
|---|---|
| 分子量 |
514.5211
|
| 精确质量 |
514.183
|
| CAS号 |
113558-15-9
|
| PubChem CID |
5488822
|
| 外观&性状 |
Light yellow to yellow solid powder
|
| 密度 |
1.5±0.1 g/cm3
|
| 沸点 |
759.4±60.0 °C at 760 mmHg
|
| 闪点 |
253.9±26.4 °C
|
| 蒸汽压 |
0.0±2.7 mmHg at 25°C
|
| 折射率 |
1.666
|
| LogP |
4.65
|
| tPSA |
159.05
|
| 氢键供体(HBD)数目 |
5
|
| 氢键受体(HBA)数目 |
10
|
| 可旋转键数目(RBC) |
6
|
| 重原子数目 |
37
|
| 分子复杂度/Complexity |
874
|
| 定义原子立体中心数目 |
5
|
| SMILES |
O1[C@]([H])([C@@]([H])([C@@]([H])([C@]([H])([C@]1([H])C([H])([H])[H])O[H])O[H])O[H])OC1C(C2=C(C([H])=C(C(C([H])([H])/C(/[H])=C(\C([H])([H])[H])/C([H])([H])[H])=C2OC=1C1C([H])=C([H])C(=C([H])C=1[H])OC([H])([H])[H])O[H])O[H])=O
|
| InChi Key |
NGMYNFJANBHLKA-LVKFHIPRSA-N
|
| InChi Code |
InChI=1S/C27H30O10/c1-12(2)5-10-16-17(28)11-18(29)19-21(31)26(37-27-23(33)22(32)20(30)13(3)35-27)24(36-25(16)19)14-6-8-15(34-4)9-7-14/h5-9,11,13,20,22-23,27-30,32-33H,10H2,1-4H3/t13-,20-,22+,23+,27-/m0/s1
|
| 化学名 |
5,7-dihydroxy-2-(4-methoxyphenyl)-8-(3-methylbut-2-enyl)-3-[(2S,3R,4R,5R,6S)-3,4,5-trihydroxy-6-methyloxan-2-yl]oxychromen-4-one
|
| 别名 |
Baohuoside I; 113558-15-9; Icariside II; BAOHUOSIDEI; CHEBI:82619; 5,7-dihydroxy-2-(4-methoxyphenyl)-8-(3-methylbut-2-enyl)-3-[(2S,3R,4R,5R,6S)-3,4,5-trihydroxy-6-methyloxan-2-yl]oxychromen-4-one; CHEMBL560116; 4H-1-Benzopyran-4-one, 3-[(6-deoxy-alpha-L-mannopyranosyl)oxy]-5,7-dihydroxy-2-(4-methoxyphenyl)-8-(3-methyl-2-buten-1-yl)-;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ≥ 32 mg/mL (~62.19 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (4.04 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.08 mg/mL (4.04 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.08 mg/mL (4.04 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: 20 mg/mL (38.87 mM) in 0.5% CMC/saline water (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.9436 mL | 9.7178 mL | 19.4356 mL | |
| 5 mM | 0.3887 mL | 1.9436 mL | 3.8871 mL | |
| 10 mM | 0.1944 mL | 0.9718 mL | 1.9436 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。