| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| Other Sizes |
|
| 靶点 |
Flt-1 (IC50 = 5 nM); KDR (IC50 = 1 nM); Flt-4 (IC50 = 3 nM); PDGFRα (IC50 = 36 nM); PDGFRβ (IC50 = 5 nM); c-Kit (IC50 = 2 nM)
Vascular Endothelial Growth Factor Receptor (VEGFR) 1/2/3, Platelet-Derived Growth Factor Receptor (PDGFR) α/β, and c-Kit, tyrosine kinases critical for angiogenesis and tumor growth. For Cediranib (NSC-732208; AZD-2171), literature [1] reported: VEGFR1 (IC50 = 1.5 nM), VEGFR2 (IC50 = 0.8 nM), VEGFR3 (IC50 = 3.0 nM), PDGFRβ (IC50 = 5.6 nM), c-Kit (IC50 = 16 nM) via HTRF kinase assay [1] |
|---|---|
| 体外研究 (In Vitro) |
Cediranib(也称为 AZD2171,一种吲哚醚喹唑啉衍生物)是一种高效 VEGFR (KDR) 抑制剂,IC50 <1nM,对 VEGFR 的选择性比 PDGFR-α、CSF-1R 和 Flt3 高 >1000 倍。 HUVEC 细胞。抑制血管内皮生长因子-A (VEGF) 信号传导是一种有前景的治疗方法,旨在通过消除肿瘤诱导的血管生成来稳定实体恶性肿瘤的进展。通过与三磷酸腺苷竞争,西地尼布结合并抑制所有三种血管内皮生长因子受体 (VEGF-1,-2,-3) 酪氨酸激酶,从而阻断 VEGF 信号传导、血管生成和肿瘤细胞生长。西地尼布正在临床开发中,作为治疗癌症的每日一次口服疗法。 Cediranib(也称为 AZD2171,一种吲哚醚喹唑啉衍生物)是一种高效 VEGFR (KDR) 抑制剂,IC50 为 <1 4= 5= it= 也= 抑制= with= ic50= of= nm= and= 显示= 相似=在 HUVEC 细胞中,对 VEGFR 的选择性比 PDGFR-α、CSF-1R 和 Flt3 高 110 倍=>1000 倍。抑制血管内皮生长因子-A (VEGF) 信号传导是一种有前景的治疗方法,旨在通过消除肿瘤诱导的血管生成来稳定实体恶性肿瘤的进展。通过与三磷酸腺苷竞争,西地尼布结合并抑制所有三种血管内皮生长因子受体 (VEGF-1,-2,-3) 酪氨酸激酶,从而阻断 VEGF 信号传导、血管生成和肿瘤细胞生长。西地尼布正在临床开发中,作为治疗癌症的每日一次口服疗法。激酶测定:将西地尼布以 10 mM 的浓度溶解在 DMSO 中。所有酶测定均在各自的 ATP Km(0.2 - 30 μM)下或略低于该值运行。西地尼布的抑制活性是针对一系列重组酪氨酸激酶 [KDR、Flt-1、Flt-4、c-Kit、PDGFRα、PDGFRβ、CSF-1R、Flt-3、FGFR1、Src、Abl、表皮生长因子] 确定的受体 (EGFR)、ErbB2、Aurora A 和 Aurora B] 使用 ELISA。使用视网膜母细胞瘤底物和 [γ-sup>33P]ATP 的闪烁邻近测定法检查相对于 CDK2 和 CDK4 丝氨酸/苏氨酸激酶的选择性。将西地尼布的活性与 MAPK 激酶 (MEK) 进行比较,显示出双重特异性。它是使用 MAPK 底物、[γ-33P]ATP 和纸捕获/闪烁计数来确定的。细胞测定:在存在和不存在生长因子的情况下,通过在4天的孵育期后测量3H-胸苷掺入来评估HUVEC细胞系的增殖。 MG63 骨肉瘤细胞的增殖是由 PDGF-AA 诱导的,PDGF-AA 选择性激活 PDGFRα 同二聚体的信号传导。 HUVEC 和 MG63 骨肉瘤细胞在不含酚红、含有 1% 炭脱 FCS、2 mM 谷氨酰胺和 1% 非必需氨基酸的 DMEM 中培养 24 小时。向西地尼布或载体中添加 PDGF-AA 配体 (50 ng/mL),并将板再孵育 72 小时。使用溴脱氧尿苷 ELISA 测定细胞增殖。
VEGFR依赖细胞与实体瘤细胞:在HUVECs(VEGFR2依赖)中,Cediranib(0.001 μM–1 μM)抑制VEGF诱导的增殖,MTT法(72小时)IC50=0.02 μM;0.1 μM处理24小时可阻断管腔形成90%。Western blot显示HUVECs经0.05 μM处理1小时后p-VEGFR2减少95% [1]。在HT-29(结直肠癌)和A549(肺癌)细胞中,其抑制增殖的MTT法(72小时)IC50分别为HT-29 0.15 μM、A549 0.2 μM;0.5 μM处理HT-29细胞48小时后,Annexin V-FITC染色显示凋亡率达45% [1] - 儿童神经母细胞瘤细胞:在SK-N-SH和IMR-32(神经母细胞瘤)细胞中,Cediranib(0.01 μM–10 μM)抑制增殖,CCK-8法(72小时)IC50分别为SK-N-SH 0.3 μM、IMR-32 0.4 μM。0.5 μM处理SK-N-SH细胞12小时后,Transwell实验显示迁移减少60% [2] |
| 体内研究 (In Vivo) |
西地尼布甚至可以在亚纳摩尔浓度下抑制肾小管萌芽,并抑制 VEGF 诱导的血管生成。西地尼布导致骨生长板肥大并阻止卵巢黄体发育。这些是依赖于血管生成的生理过程。西地尼布在人体肿瘤模型中以耐受性良好的剂量显示出广谱活性。此外,西地尼布会导致人肺肿瘤异种移植物中血管组织的消退。
结直肠癌与肺癌异种移植模型:6周龄雄性裸鼠接种HT-29细胞,用Cediranib 3 mg/kg或6 mg/kg(口服,每日一次)处理28天。肿瘤体积较溶媒组减少:3 mg/kg组65%、6 mg/kg组85%;肿瘤重量减少:3 mg/kg组60%、6 mg/kg组80% [1]。7周龄雌性裸鼠接种A549细胞,用5 mg/kg Cediranib(口服,每日一次)处理35天:肿瘤体积减少75%,微血管密度(CD31染色)减少70% [1] - 神经母细胞瘤异种移植模型:6周龄雌性裸鼠接种SK-N-SH细胞,用Cediranib 4 mg/kg(口服,每日一次)处理21天。肿瘤体积减少60%,血清神经母细胞瘤标志物NSE从350 ng/mL降至140 ng/mL [2] |
| 酶活实验 |
将西地尼布溶解在 DMSO 中,浓度为 10 mM。每个酶测试均在等于或略低于 ATP 相应 Km (0.2 - 30 μM) 的条件下进行。使用 ELISA 评估西地尼布对多种重组酪氨酸激酶的抑制活性,包括 KDR、Flt-1、Flt-4、c-Kit、PDGFRα、PDGFRβ、CSF-1R、Flt-3、FGFR1、Src、Abl 和表皮生长因子受体 (EGFR)、ErbB2、Aurora A 和 Aurora B。在闪烁邻近测定中,使用视网膜母细胞瘤底物和 [γ-sup>33P]ATP 研究对 CDK2 和 CDK4 丝氨酸/苏氨酸激酶的选择性。 Cediranib 的活性与 MAPK 激酶 (MEK) 的活性形成对比,表现出双重特异性。使用 MAPK 底物、[γ-33P]ATP 和纸捕获/闪烁计数来确定它。
VEGFR/PDGFR/c-Kit HTRF激酶实验:将重组人VEGFR1(791–1338位氨基酸)、VEGFR2(786–1356位氨基酸)、VEGFR3(803–1363位氨基酸)、PDGFRβ(562–1107位氨基酸)或c-Kit(544–976位氨基酸)与生物素化肽底物(Ac-EAIYAAPFAKKK-NH2,20 μM)、Eu标记抗磷酸酪氨酸抗体及ATP(10 μM)共同孵育于激酶缓冲液(25 mM Tris-HCl pH 7.5、10 mM MgCl₂、1 mM DTT)中。加入系列稀释的Cediranib(0.001 nM–100 nM),30°C孵育60分钟。检测时间分辨荧光(激发光340 nm,发射光620 nm),计算IC50 [1] |
| 细胞实验 |
孵育四天后,测量 3 H-胸苷掺入,以评估 HUVEC 细胞系在生长因子存在和不存在的情况下的增殖情况。 PDGF-AA 特异性刺激 PDGFRα 同二聚体的信号传导,导致 MG63 骨肉瘤细胞增殖。将 HUVEC 和 MG63 骨肉瘤细胞在不含酚红的 DMEM 中培养 24 小时,其中还含有 1% 木炭剥离的 FCS、2 mM 谷氨酰胺和 1% 非必需氨基酸。添加西地尼布或载体以及 50 ng/mL PDGF-AA 配体后,将板再孵育 72 小时。溴脱氧尿苷 ElISA 用于测量细胞增殖。
HUVEC与实体瘤细胞实验:HUVECs分别以5×10³个细胞/孔接种于96孔板(增殖实验)或1×10⁵个细胞/孔接种于Matrigel包被的24孔板(管腔形成实验),加入Cediranib(0.001 μM–1 μM)+VEGF(50 ng/mL),37°C、5% CO₂孵育。增殖实验72小时后MTT法检测;管腔形成实验24小时后定量。HT-29/A549细胞以5×10³个细胞/孔接种于96孔板,药物处理72小时后MTT法检测活力 [1] - 神经母细胞瘤细胞实验:SK-N-SH/IMR-32细胞以5×10³个细胞/孔接种于96孔板,用Cediranib(0.01 μM–10 μM)处理72小时;CCK-8法检测活力。迁移实验中,SK-N-SH细胞以5×10⁴个细胞/小室接种于Transwell小室,加入0.5 μM药物,12小时后计数迁移细胞 [2] |
| 动物实验 |
大鼠:将6周龄雌性Wistar衍生Alderley Park大鼠(n = 5)每日一次口服给予Cediranib(1.25–5 mg/kg/天)或赋形剂,持续28天。为研究停药的影响,每组另取5只大鼠,分别用赋形剂或Cediranib(5 mg/kg/天)治疗28天,然后停止治疗28天。采用苏木精-伊红(H&E)染色法对股胫关节和卵巢组织切片进行石蜡包埋。将每个关节股骨和胫骨的生长板区域合并,进行股胫关节切片的形态计量图像分析,从而分析化合物治疗的影响。形态计量分析也用于确定经苏木精-伊红染色(H&E染色)的卵巢切片中黄体的面积。
小鼠:选择携带人肺肿瘤异种移植瘤Calu-6(0.2±0.01 cm³)的小鼠,于第0天给予慢性剂量的西地尼布(6 mg/kg,每日口服)或载体。在最后一次给予西地尼布或载体后4小时,分别于第1、2、7、14和21天收集每组6至15个肿瘤。下一步是使用显色终点法或荧光免疫染色法检测切片中的CD31。 HT-29/A549异种移植瘤方案:将5×10⁶个HT-29细胞皮下植入6周龄雄性裸鼠体内。当肿瘤体积达到约 100 mm³ 时,将 Cediranib 溶解于 0.5% 甲基纤维素 + 0.1% Tween 80 溶液中,每日口服一次(3 mg/kg 或 6 mg/kg),持续 28 天。每 3 天测量一次肿瘤体积(长×宽²/2);于第 28 天处死小鼠,并称量肿瘤重量。携带 A549 异种移植瘤的 7 周龄雌性裸鼠每日口服一次 Cediranib(5 mg/kg,相同制剂),持续 35 天 [1] - SK-N-SH 神经母细胞瘤方案:将 4×10⁶ 个 SK-N-SH 细胞皮下植入 6 周龄雌性裸鼠体内。当肿瘤体积达到约 120 mm³ 时,每日口服一次 Cediranib(4 mg/kg,溶解于 0.5% 羟丙基甲基纤维素溶液中),持续 21 天。每3天测量一次肿瘤体积;安乐死后通过ELISA法定量血清NSE[2] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
口服给药后可利用。 生物半衰期 12 至 35 小时 大鼠药代动力学:雄性 Sprague-Dawley 大鼠(8 周龄)口服 Cediranib 10 mg/kg:口服生物利用度 = 62%,Cmax = 4.8 μM,Tmax = 1.2 小时,末端 t₁/₂ = 8.5 小时。静脉注射 2 mg/kg:清除率 (CL) = 7.8 mL/min/kg,稳态分布容积 (Vss) = 1.3 L/kg [1] - 人血浆蛋白结合率:99%(平衡透析 [1]) - 代谢:在人肝微粒体中,西地尼布主要通过 CYP3A4 (75%) 和 CYP2C9 (15%) 代谢;尿液中原形药物排泄量 < 5% [1] |
| 毒性/毒理 (Toxicokinetics/TK) |
体外细胞毒性:在正常人肝细胞 (NHH) 和儿科成纤维细胞中,Cediranib(浓度高达 10 μM,处理 72 小时)的细胞活力 > 80%,表明其非特异性毒性较低 [1][2]
- 体内急性毒性:大鼠经 Cediranib 10 mg/kg(口服,28 天)治疗后出现轻度高血压(12% 的动物,收缩压升高 < 25 mmHg),但未见肝肾损伤(ALT/AST/肌酐水平正常)[1] - 儿科模型毒性:小鼠经 Cediranib 4 mg/kg(口服,21 天)治疗后未出现体重减轻、嗜睡或神经毒性(脑组织病理学检查正常)[2] |
| 参考文献 | |
| 其他信息 |
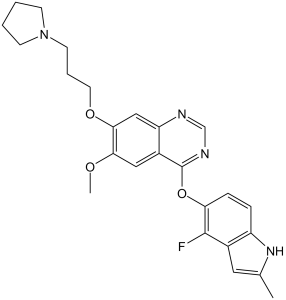
4-[(4-氟-2-甲基-1H-吲哚-5-基)氧基]-6-甲氧基-7-[3-(1-吡咯烷基)丙氧基]喹唑啉是一种芳香醚。
新型吲哚醚喹唑啉类化合物西地尼布(Cediranib)是一种高效的ATP竞争性抑制剂(IC50 < 1 nmol/L),体外可抑制重组KDR酪氨酸激酶。目前,西地尼布正作为一种每日一次的口服疗法进行临床开发,用于治疗癌症。 西地尼布是一种口服生物利用度高的吲哚醚喹唑啉衍生物,同时也是一种血管内皮生长因子受体(VEGFR)抑制剂,具有潜在的抗肿瘤活性。口服后,西地尼布可与三种血管内皮生长因子受体亚型 1 (VEGFR-1)、2 (VEGFR-2) 和 3 (VEGFR-3) 结合并抑制其活性,从而阻断 VEGF 信号传导、血管生成和肿瘤细胞生长。VEGFR 在多种肿瘤细胞类型中表达上调。 适应症 用于治疗肝癌、晚期非小细胞肺癌 (NSCLC)、晚期结直肠癌 (CRC) 和其他实体瘤。 作用机制 西地尼布抑制血管内皮生长因子 (VEGF) 受体酪氨酸激酶 (RTK)。通过阻断 VEGF 受体,西地尼布限制新生血管的生长,而新生血管对于支持肿瘤生长至关重要。因此,由于缺乏足够的血液供应,肿瘤细胞会因缺乏营养而生长缓慢或停止,并有可能提高其他疗法的疗效。临床前证据表明,该药物对这些位点具有高亲和力,并且在动物研究中耐受性良好且疗效显著。 Cediranib(NSC-732208;AZD-2171)是一种强效的多靶点酪氨酸激酶抑制剂,已开发用于治疗血管生成依赖性癌症(例如,结直肠癌、肺癌)和儿童实体瘤(例如,神经母细胞瘤)[1][2] - 其作用机制涉及与VEGFR、PDGFRβ和c-Kit的ATP结合口袋结合,抑制酪氨酸激酶的激活和下游信号传导(ERK/AKT),从而抑制血管生成、肿瘤生长和迁移[1][2] - 它在成人实体瘤和儿童神经母细胞瘤模型中均显示出临床前疗效,支持其用于跨年龄段癌症治疗的潜力[1][2] |
| 分子式 |
C25H27FN4O3
|
|---|---|
| 分子量 |
450.51
|
| 精确质量 |
450.206
|
| 元素分析 |
C, 66.65; H, 6.04; F, 4.22; N, 12.44; O, 10.65.
|
| CAS号 |
288383-20-0
|
| 相关CAS号 |
Cediranib maleate;857036-77-2
|
| PubChem CID |
9933475
|
| 外观&性状 |
white solid powder
|
| 密度 |
1.3±0.1 g/cm3
|
| 沸点 |
626.6±55.0 °C at 760 mmHg
|
| 闪点 |
332.7±31.5 °C
|
| 蒸汽压 |
0.0±1.8 mmHg at 25°C
|
| 折射率 |
1.642
|
| LogP |
4.8
|
| tPSA |
72.5
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
7
|
| 可旋转键数目(RBC) |
8
|
| 重原子数目 |
33
|
| 分子复杂度/Complexity |
625
|
| 定义原子立体中心数目 |
0
|
| SMILES |
FC1=C(C([H])=C([H])C2=C1C([H])=C(C([H])([H])[H])N2[H])OC1C2=C([H])C(=C(C([H])=C2N=C([H])N=1)OC([H])([H])C([H])([H])C([H])([H])N1C([H])([H])C([H])([H])C([H])([H])C1([H])[H])OC([H])([H])[H]
|
| InChi Key |
XXJWYDDUDKYVKI-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C25H27FN4O3/c1-16-12-17-19(29-16)6-7-21(24(17)26)33-25-18-13-22(31-2)23(14-20(18)27-15-28-25)32-11-5-10-30-8-3-4-9-30/h6-7,12-15,29H,3-5,8-11H2,1-2H3
|
| 化学名 |
4-[(4-fluoro-2-methyl-1H-indol-5-yl)oxy]-6-methoxy-7-(3-pyrrolidin-1-ylpropoxy)quinazoline
|
| 别名 |
AZD2171; NSC 732208; NSC732208; AZD 2171; NSC-732208; AZD-2171; Brand name: Recentin
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2 mg/mL (4.44 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.0 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2 mg/mL (4.44 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.0 mg/mL 澄清 DMSO 储备液添加到 900 μL 玉米油中并混合均匀。 View More
配方 3 中的溶解度: 5% DMSO+50% PEG 300+5% Tween+ddH2O: 5 mg/kg 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.2197 mL | 11.0985 mL | 22.1971 mL | |
| 5 mM | 0.4439 mL | 2.2197 mL | 4.4394 mL | |
| 10 mM | 0.2220 mL | 1.1099 mL | 2.2197 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT00750841 | Active Recruiting |
Drug: cediranib | Solid Tumors | AstraZeneca | September 9, 2008 | Phase 1 |
| NCT01391962 | Active Recruiting |
Drug: Cediranib Drug: Sunitinib |
Sarcoma, Alveolar Soft Part | National Cancer Institute (NCI) |
July 18, 2011 | Phase 2 |
| NCT03570437 | Active Recruiting |
Drug: Paclitaxel Drug: Cediranib |
Endometrial Neoplasms Carcinosarcoma |
University of Manchester | May 17, 2018 | Phase 2 |
| NCT02974621 | Active Recruiting |
Drug: Cediranib Drug: Cediranib Maleate |
Recurrent Glioblastoma | National Cancer Institute (NCI) |
December 7, 2017 | Phase 2 |
| NCT01364051 | Active Recruiting |
Drug: Cediranib Drug: Cediranib Maleate |
Refractory Malignant Solid Neoplasm Metastatic Melanoma |
National Cancer Institute (NCI) |
May 25, 2011 | Phase 1 |
AZD2171 inhibits VEGF-stimulated KDR phosphorylation in human endothelial cells.Cancer Res.2005 May 15;65(10):4389-400. |
AZD2171 inhibits tubule growthin vitro. HUVECs and human fibroblasts were obtained as commercial cocultures (AngioKit, TCS Cellworks).Cancer Res.2005 May 15;65(10):4389-400. |
AZD2171 inhibits VEGF-induced angiogenesisin vivo.Cancer Res.2005 May 15;65(10):4389-400. |
Consequences of inhibiting VEGF signaling and physiologic angiogenesisin vivo: effect of AZD2171 on bone morphogenesis and ovarian cycling in young female rats.Cancer Res.2005 May 15;65(10):4389-400. |
AZD2171 inhibits human tumor xenograft growth at doses that are well tolerated.Cancer Res.2005 May 15;65(10):4389-400. |
AZD2171 causes vascular regression in Calu-6 lung tumor xenografts.Cancer Res.2005 May 15;65(10):4389-400. |