| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| Other Sizes |
|
| 靶点 |
The extracellular signal-regulated kinase (ERK1/2) pathway is inhibited by CFM-2. CFM-2 upregulates tumor suppressor protein p21 and cell cycle regulatory factors while decreasing the phosphorylation of cAMP response element binding protein (CREB) and inhibiting the expression of cyclin D1. and p53 resulted in a drop in the proportion of lung adenocarcinoma cells in the G2 and S cell cycle stages.
|
|---|---|
| 体外研究 (In Vitro) |
CFM-2 抑制细胞外信号调节激酶 (ERK1/2) 通路。 CFM-2 上调抑癌蛋白 p21 和细胞周期调节因子,同时降低 cAMP 反应元件结合蛋白 (CREB) 的磷酸化并抑制细胞周期蛋白 D1 的表达。 p53导致处于G2和S细胞周期阶段的肺腺癌细胞比例下降。
|
| 体内研究 (In Vivo) |
当重复给予戊四唑时,CFM-2 预处理可减缓癫痫发作分级的进展。在 6 周重复戊四唑治疗期结束时,媒介物治疗对照中的平均癫痫评分为 0,用媒介物 + 戊四唑治疗的动物为 4.3(用 CFM-2(20 μmol/kg;腹膜 2.2)+ 治疗)长期治疗(静脉注射)的大鼠中戊四唑为 1.0,而用 CFM-2(50 μmol/kg;ip)+ 戊四唑)反复治疗的大鼠中为 1.0。在戊四唑点燃的动物中,CFM-2 同样可以抵消对 GABA 功能抑制剂的惊厥作用的敏感性的长期增加[1]。通过鞘内注射两种选择性非竞争性 AMPAR 拮抗剂 CFM-2(25 和 50 μg)和 GYKI 52466(50 μg),CFA 注射后 2 小时和 24 小时,同侧后爪的机械和热超敏性显着降低。超敏反应。当受到机械和热刺激时,对侧基础反应不受 GYKI 52466 或 CFM-2 的影响 [4]。
在P在Sprague-Dawley大鼠的戊四氮(PTZ)点燃模型中,CFM-2显示出抗惊厥活性。在重复给予PTZ(25 mg kg⁻¹,腹腔注射,每周三次,持续6周)期间,预先给予CFM-2(20或50 µmol kg⁻¹,腹腔注射,PTZ前30分钟)可延迟癫痫发作严重程度的进展。在6周结束时,载体+PTZ对照组的平均癫痫发作评分为4.3,CFM-2(20 µmol kg⁻¹)+ PTZ组大鼠为2.2,CFM-2(50 µmol kg⁻¹)+ PTZ组大鼠为1.0。[1] CFM-2可拮抗PTZ点燃动物对GABA功能抑制剂惊厥作用长期敏感性增加的现象。慢性治疗结束15天后,给予攻击剂量的PTZ(15 mg kg⁻¹,腹腔注射)在10只载体+PTZ点燃大鼠中的9只诱发了癫痫,但在CFM-2(20 µmol kg⁻¹)+ PTZ组的8只大鼠中仅2只发作,在CFM-2(50 µmol kg⁻¹)+ PTZ组的8只大鼠中仅1只发作。同样,治疗结束30天后给予印防己毒素(1.5 mg kg⁻¹,腹腔注射)攻击,在所有10只载体+PTZ点燃大鼠中都诱发了癫痫,但在长期用CFM-2(20或50 µmol kg⁻¹)治疗的大鼠中则未诱发。[1] TZ点燃模型中,重复给予CFM-2后未观察到其抗惊厥作用产生耐受性。[1] |
| 动物实验 |
在戊四唑 (PTZ) 点燃研究中,Sprague-Dawley 大鼠(250-280 g)在水合氯醛麻醉下植入额顶叶螺钉电极。经过至少 7 天的恢复期后,点燃阶段开始。每周三次(周一、周三、周五)腹腔注射 PTZ(25 mg kg⁻¹),持续长达 6 周。[1] 在慢性治疗期间,每次注射 PTZ 前 30 分钟,腹腔注射 CFM-2,剂量为 20 或 50 µmol kg⁻¹。对照组大鼠注射等体积的无菌生理盐水。根据预先设定的评分标准(0 = 无癫痫发作,5 = 伴有后肢伸展的全身强直性癫痫发作),对 PTZ 给药后 60 分钟内的癫痫发作严重程度进行评分。记录皮层电活动。 [1]
在挑战性实验中,慢性戊四唑(PTZ)治疗结束后15或30天,动物腹腔注射亚致惊厥剂量的PTZ(15 mg kg⁻¹)或苦味素(1.5 mg kg⁻¹),并观察1小时以记录癫痫发作情况。[1] 使用转棒试验评估运动功能。训练大鼠在旋转杆(直径4 cm,转速4.5 rpm)上保持5分钟。运动功能障碍定义为无法在测试时间内保持在旋转杆上。在急性CFM-2给药后30、60和90分钟,以及慢性治疗期间的第1、14和28天,于给药后30分钟评估运动功能。[1] 将CFM-2盐酸盐溶解于无菌生理盐水中进行给药。[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
在Sprague-Dawley大鼠中,通过转棒试验测定了CFM-2的TD₅₀值(导致50%动物出现运动功能障碍的剂量)。急性给药后,注射后30分钟、60分钟和90分钟的TD₅₀值分别为57.4 (48-68.7) µmol kg⁻¹、46.9 (39.1-56.4) µmol kg⁻¹和94.3 (76.2-116.7) µmol kg⁻¹。连续给药28天后,注射后30分钟和60分钟的TD₅₀值分别为58.8 (47.2-73.2) µmol kg⁻¹和48.6 (38.4-61.5) µmol kg⁻¹。 [1]
在慢性抗癫痫研究中使用的CFM-2剂量(20和50 µmol kg⁻¹)未引起可观察到的不良反应,例如共济失调、肌张力下降、运动活性降低或翻正反射消失。[1] 文中未明确计算CFM-2的治疗指数(TI = TD₅₀ / ED₅₀,针对阵挛性癫痫发作),但数据表明抗癫痫剂量和运动功能障碍剂量之间存在差异。[1] |
| 参考文献 |
|
| 其他信息 |
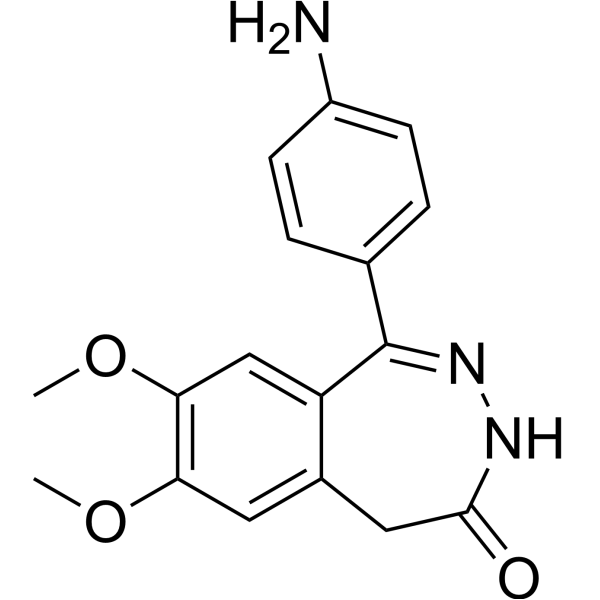
1-(4-氨基苯基)-7,8-二甲氧基-3,5-二氢-2,3-苯并二氮杂卓-4-酮是一种苯二氮卓类药物。
CFM-2(1-(4'-氨基苯基)-3,5-二氢-7,8-二甲氧基-4H-2,3-苯并二氮杂卓-4-酮盐酸盐)是一种新型的2,3-苯并二氮卓衍生物,可作为非选择性AMPA受体拮抗剂。[1] 该研究表明,像CFM-2这样的AMPA受体拮抗剂可能对某些类型的癫痫具有临床应用潜力,尤其因为与经典的苯二氮卓类药物不同,在所测试的模型中,重复给药后并未产生抗惊厥耐受性。 [1] 数据表明,AMPA受体的激活对于点燃癫痫发作的行为和电生理表现至关重要,而拮抗这些受体可以调节点燃过程和点燃后状态。[1] |
| 分子式 |
C17H17N3O3
|
|---|---|
| 分子量 |
311.33518
|
| 精确质量 |
311.127
|
| CAS号 |
178616-26-7
|
| PubChem CID |
4377504
|
| 外观&性状 |
Light yellow to khaki solid powder
|
| 密度 |
1.32g/cm3
|
| 折射率 |
1.637
|
| LogP |
2.056
|
| tPSA |
85.94
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
3
|
| 重原子数目 |
23
|
| 分子复杂度/Complexity |
460
|
| 定义原子立体中心数目 |
0
|
| InChi Key |
MJKADKZSYQWGLL-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C17H17N3O3/c1-22-14-7-11-8-16(21)19-20-17(13(11)9-15(14)23-2)10-3-5-12(18)6-4-10/h3-7,9H,8,18H2,1-2H3,(H,19,21)
|
| 化学名 |
1-(4-aminophenyl)-7,8-dimethoxy-3,5-dihydro-2,3-benzodiazepin-4-one
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ≥ 50 mg/mL (~160.60 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.75 mg/mL (8.83 mM) (饱和度未知) in 10% DMSO + 40% PEG300 +5% Tween-80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 27.5 mg/mL澄清的DMSO储备液加入到400 μL PEG300中,混匀;再向上述溶液中加入50 μL Tween-80 +,混匀;然后加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.2119 mL | 16.0596 mL | 32.1192 mL | |
| 5 mM | 0.6424 mL | 3.2119 mL | 6.4238 mL | |
| 10 mM | 0.3212 mL | 1.6060 mL | 3.2119 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。