| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| Other Sizes |
|

| 靶点 |
COX-1/cyclooxygenase-1 (IC50 = 3.2μM)
|
|---|---|
| 体外研究 (In Vitro) |
(-)-表儿茶素的 IC50 为 3.2 μM,在 70 μg/mL 浓度下对环加氧酶-1 (COX-1) 的抑制作用 > 95% [1]。 (-)-表儿茶素 NF-阻断 κB p65 亚基的核定位,从而阻止 IL-1β 诱导的 iNOS 产生。已证明,添加 IL-1β 会导致 (-)-表儿茶素爆发并限制 RINm5F 细胞中胰岛素的释放。此外,还证明(-)-表儿茶素具有溶胀性。它通过抑制 Jurkat T 细胞和霍奇金定位细胞的生长,增强 (-)-表儿茶素阻止 NF-κB 与这些细胞中的 DNA 结合的能力。将 20 μM 人参二醇与 150、200 或 250 μM (-)-表儿茶素组合可分别抑制人直肠癌 HCT-116 细胞的增殖 51%、97% 和 95%。膜联蛋白 V/PI 染色显示,交换后的细胞荧光水平分别增加了 11.9%、16.6% 和 25.8% [2]。
|
| 体内研究 (In Vivo) |
每天两次通过壁管饲法给动物喂水(媒介物)或1mg/kg的(-)-表儿茶素。在 15 天的过程中,锻炼组使用跑步机。使用 (-)-表儿茶素可以将原位访问期间的疲劳抵抗力提高约 30%,并将跑步机性能提高约 50% [3]。
|
| 酶活实验 |
肌肉代谢酶活性[3]
将腓肠肌分成10mg块,并在100体积(w:v)的柠檬酸合酶缓冲液(175 mm KCl,2 mm EDTA;pH 7.4)中均质化。在缓冲液中,用杵在冰上粉碎冷冻的肌肉切片60秒。匀浆在液氮中冷冻,并使用液氮进行三次冻融循环。使用前,将匀浆最后一次解冻,并在8000g下离心1分钟以去除颗粒物。 使用上清液,通过Srere(1969)的技术测量柠檬酸合酶活性。柠檬酸合酶的活性是通过巯基离子的产生速率来测量的,该速率基于乙酰辅酶A和草酰乙酸转化为柠檬酸合酶体和CoA-SH。在5,5′-二硫代双-2-硝基苯甲酸(DTNB)存在下,辅酶A SH产生巯基离子。样品在贝克曼DU 730分光光度计中以412nm进行分析。所有样品均进行了三次测试,并在37°C下进行了测量。 |
| 细胞实验 |
蛋白质印迹[3]
在500μl裂解缓冲液(1%Triton X-100、20 mm Tris、140 mm NaCl、2 mm EDTA和0.1%SDS)中,用聚铁酸盐将约50 mg的心脏和股四头肌肌肉均质化,并加入蛋白酶和磷酸酶抑制剂混合物,补充0.15 mm PMSF、5 mm Na3VO4和3 mm NaF。将匀浆通过胰岛素注射器五次,在4°C下超声处理30分钟,离心(12000 g)10分钟。使用Bradford法测量上清液中的总蛋白质含量。将总共40μg的蛋白质装载到4-15%的预制TGX聚丙烯酰胺凝胶(Bio-Rad)上,电转移(12V,50分钟),在封闭溶液(TBS中的5%脱脂奶粉加0.1%吐温20(TBS-T))中孵育1小时,然后在室温下用小鼠单克隆抗体MitoProfile(复合物I,20kDa;复合物II,30kDa;复合物III,46kDa;配合物V,55kDa;Timmers等人(2011)孵育3小时;氧化磷酸化,总OXPHOS)、Porin(35kDa;Huffman等人(2008))和Mitofilin(75kDa;Iyer等人(2009))。此外,我们使用了以下针对nNOS的兔多克隆抗体(约155 kDa(Hayashi等人,2009),抗磷酸化nNOS(约155 kDa(Chen等人,2000);Ser1417,Upstate Cat#07-544),抗Tfam(30 kDa(Franko等人,2008)),以研究线粒体生物合成的潜在机制。所有一抗均按1:1000和GAPDH(37kDa;Pansters等人(2011);兔多克隆第一抗体在TBS-T加5%脱脂奶粉中稀释1:2000。在TBS-T中洗涤膜(3×5分钟),并在室温下在HRP偶联的二抗(分别为抗小鼠IgG或抗兔IgG-HRP连接抗体)存在下孵育1小时,该二抗在封闭溶液中稀释1:10000。在TBS-T中再次洗涤膜3次,并使用ECL Plus检测试剂盒进行免疫印迹。使用ImageJ软件对条带强度进行数字量化(http://www.nih.gov). |
| 动物实验 |
实验设计与方法[2]
本研究采用组间设计,旨在探究(-)-表儿茶素对1岁小鼠后肢肌肉的影响。选择1岁小鼠是因为已有研究表明,与幼鼠(4-6月龄)相比,1岁小鼠的运动能力有所下降(Leick等,2010)。所有小鼠均进行递增负荷跑步机测试,随后随机分为四组:(1)水组,(2)水-运动组(W-Ex),(3)(-)-表儿茶素组((-)-Epi),以及(4)(-)-表儿茶素-运动组((-)-Epi-Ex)。第2组和第4组小鼠在研究期间的周一至周五进行啮齿动物跑步机训练。在最后一次训练后的第二天,所有小鼠均进行递增负荷跑步机测试。跑步机测试结束后48小时,处死小鼠。所有组别的股四头肌、趾长伸肌 (EDL) 和跖肌均被采集,用于形态计量学、生物化学、离体肌肉制备和分子分析。 (–)-表儿茶素给药[3] (–)-表儿茶素组 3 和 4 的小鼠连续 15 天,每天两次(早晚)给予 1.0 mg/kg 体重的 (–)-表儿茶素,而对照组 1 和 2 的小鼠则给予赋形剂(水)。(–)-表儿茶素和赋形剂均采用灌胃给药。 |
| 药代性质 (ADME/PK) |
代谢/代谢物
表儿茶素已知的人体代谢物包括5-(3',4'-二羟基苯基)-γ-戊内酯和间苯三酚。 一项小型定量临床研究,受试者食用80克富含原花青素的巧克力(其中含有137毫克(470微摩尔)(−)-表儿茶素),结果显示,2小时后,10名受试者中有8名血液中(−)-表儿茶素的浓度较基线水平升高12倍,达到257 ± 66 nmol/L,6小时后降至基线水平,而其余2名受试者的浓度则进一步升高[39]。这表明(−)-表儿茶素在人体内的半衰期和代谢存在很大的异质性。因此,天然(−)-表儿茶素的生物利用度低于维生素C和维生素E,分别约为维生素C和维生素E的1/200和1/150。鉴于摄入的(−)-表儿茶素大部分会发生化学修饰,除了天然化合物外,葡萄糖醛酸化和甲基化产物可能在生物效应中发挥关键作用。[2] |
| 参考文献 |
|
| 其他信息 |
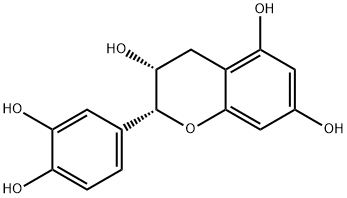
(-)-表儿茶素是一种具有(2R,3R)构型的儿茶素,具有抗氧化作用。它是一种多酚类化合物,也是一种儿茶素。它是(+)-表儿茶素的对映异构体。
表儿茶素已被用于糖尿病前期治疗的研究试验中。 据报道,(-)-表儿茶素存在于茶树(Camellia sinensis)、大叶菊(Cecropia hololeuca)以及其他有相关数据的生物体中。 它是一种抗氧化类黄酮,主要存在于木本植物中,以(+)-儿茶素和(-)-表儿茶素(顺式)两种形式存在。 另见:克罗菲勒默(单体);越橘(部分);猫爪草(部分)……查看更多…… 随着对心血管疾病、癌症、中风、神经退行性疾病和糖尿病等疾病机制的深入了解,目前正在评估更有效的治疗方法。传统医学,包括使用天然产物,在世界各地广泛应用,其基本假设是某些天然产物具有疗愈功效,甚至可能对许多困扰人类的疾病起到预防作用。本文综述了一类被称为多酚的天然化合物的生物学效应,包括芹菜素、表没食子儿茶素没食子酸酯、染料木素和(-)-表儿茶素,重点关注后者。(-)-表儿茶素具有多种独特的特性,使其发挥多种作用。其中之一是它能够与细胞内的活性氧(ROS)相互作用并将其清除。(-)-表儿茶素还能调节细胞信号传导,包括参与细胞增殖的MAP激酶通路。该通路中的突变通常与恶性肿瘤相关,因此,(-)-表儿茶素有望成为一种预防药物,并可作为化疗和放疗的辅助治疗手段,以改善治疗效果。本文探讨了一些酚类化合物在维持、保护和可能恢复健康方面的潜力。[2] 黄烷醇(-)-表儿茶素是可可豆的成分之一,已被证明对人类具有多种健康益处。我们使用1岁雄性小鼠,研究了连续15天给予(-)-表儿茶素治疗并进行规律运动对以下方面的影响:(1)运动能力,(2)肌肉疲劳,(3)毛细血管密度,以及(4)小鼠后肢和心肌线粒体生物合成。25只雄性小鼠(C57BL/6N)被随机分为四组:(1)水组,(2)水-运动组(W-Ex),(3)(-)-表儿茶素组((-)-Epi),以及(4)(-)-表儿茶素-运动组((-)-Epi-Ex)。动物经口灌胃(每日两次)分别接受1 mg/kg的(-)-表儿茶素或水(溶剂对照)。运动组进行为期15天的跑步机运动。(-)-表儿茶素组观察到跑步机运动能力显著提高(约50%),且肌肉抗疲劳能力增强(约30%)。与单独运动组相比,(-)-表儿茶素治疗组后肢和心肌中氧化磷酸化复合物的组成成分(包括线粒体丝氨酸蛋白酶、孔蛋白、nNOS、p-nNOS和Tfam)以及线粒体体积和嵴数量均显著增加。此外,骨骼肌毛细血管密度也显著增加。与单独使用(-)-表儿茶素相比,(-)-表儿茶素联合运动可进一步提高氧化磷酸化复合物蛋白、线粒体丝氨酸蛋白酶、孔蛋白和毛细血管密度。这些研究结果表明,(-)-表儿茶素单独使用或与运动结合使用,可诱导骨骼肌和心肌发生结构和代谢变化,从而提高耐力。因此,这些结果值得进一步评估(-)-表儿茶素的作用机制及其作为运动模拟剂的潜在临床应用。[3] |
| 分子式 |
C15H14O6
|
|---|---|
| 分子量 |
290.27
|
| 精确质量 |
290.079
|
| 元素分析 |
C, 62.07; H, 4.86; O, 33.07
|
| CAS号 |
490-46-0
|
| 相关CAS号 |
(-)-Epicatechin gallate;1257-08-5;(+)-Epicatechin;35323-91-2;(±)-Epicatechin-13C3;1217780-28-3; 490-46-0
|
| PubChem CID |
72276
|
| 外观&性状 |
White to light yellow solid powder
|
| 密度 |
1.6±0.1 g/cm3
|
| 沸点 |
630.4±55.0 °C at 760 mmHg
|
| 熔点 |
240 °C
|
| 闪点 |
335.0±31.5 °C
|
| 蒸汽压 |
0.0±1.9 mmHg at 25°C
|
| 折射率 |
1.742
|
| LogP |
0.49
|
| tPSA |
110.38
|
| 氢键供体(HBD)数目 |
5
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
1
|
| 重原子数目 |
21
|
| 分子复杂度/Complexity |
364
|
| 定义原子立体中心数目 |
2
|
| SMILES |
C1[C@H]([C@H](OC2=CC(=CC(=C21)O)O)C3=CC(=C(C=C3)O)O)O
|
| InChi Key |
PFTAWBLQPZVEMU-UKRRQHHQSA-N
|
| InChi Code |
InChI=1S/C15H14O6/c16-8-4-11(18)9-6-13(20)15(21-14(9)5-8)7-1-2-10(17)12(19)3-7/h1-5,13,15-20H,6H2/t13-,15-/m1/s1
|
| 化学名 |
(2R,3R)-2-(3,4-dihydroxyphenyl)-3,4-dihydro-2H-chromene-3,5,7-triol
|
| 别名 |
epi-Catechin; (-)-Epicatechin; (-)-Epicatechin; Epicatechin; 490-46-0; L-Epicatechin; Epicatechol; l-Acacatechin; (-)-Epicatechol; epi-Catechin; Epicatechin
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~344.51 mM)
H2O : ~2 mg/mL (~6.89 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (8.61 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (8.61 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (8.61 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.4451 mL | 17.2253 mL | 34.4507 mL | |
| 5 mM | 0.6890 mL | 3.4451 mL | 6.8901 mL | |
| 10 mM | 0.3445 mL | 1.7225 mL | 3.4451 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。