| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 500mg |
|
||
| 5g |
|
||
| 50g |
|
||
| Other Sizes |
|
| 靶点 |
Estragole acts on peripheral nerves to decrease neuronal excitability. The specific molecular target(s) (e.g., ion channels) are not identified in this study [1].
|
|---|---|
| 体外研究 (In Vitro) |
Estragole 在离体大鼠坐骨神经中诱导了剂量依赖性、可逆的复合动作电位(CAP)阻断作用。
在0.6 mM浓度下,Estragole 暴露180分钟后,对CAP峰峰值(PPA)或传导速度无显著影响[1]。 在2.0 mM浓度下,Estragole 在180分钟暴露结束时,将PPA显著降低至对照值的85.6 ± 3.96%。传导速度也降低[1]。 在4.0 mM浓度下,Estragole 在180分钟后,将PPA显著降低至对照值的49.3 ± 6.21%,将传导速度降低至77.7 ± 3.84%,将时值(两倍基强度下的脉冲宽度)增加至对照值的125.9 ± 10.43%,并将基强度(阈值刺激电压)增加至对照值的116.7 ± 4.59%[1]。 在6.0 mM浓度下,Estragole 在180分钟后,将PPA显著降低至对照值的13.04 ± 1.80%[1]。 所有效应均在数十分钟内缓慢发展,并在300分钟的洗脱期后完全可逆[1]。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
在非近交系雄性CD-1小鼠中,大约20%的雌激素剂量(一种天然存在的调味剂)以1'-羟基雌激素的结合物(推测为葡萄糖醛酸苷)的形式从尿液中排出。…… 代谢/代谢物 本研究探讨了雌激素的近端致癌代谢物1'-羟基雌激素在肝脏中的水平个体差异,这种差异是由于参与该代谢物形成和解毒的两个关键代谢反应(即雌激素的1'-羟基化和1'-羟基雌激素的氧化)的差异造成的。 1'-羟基雌激素的生成主要由P450 1A2、2A6和2E1催化,本研究结果支持1'-羟基雌激素的氧化是由17β-羟基类固醇脱氢酶2型(17β-HSD2)催化的。首先,本研究为14名受试者建立了基于生理的生物动力学(PBBK)模型,结果显示,该组受试者肝脏中1'-羟基雌激素浓度-时间曲线下面积(AUC)存在1.8倍的个体间差异。17β-HSD2对1'-羟基雌激素氧化作用的差异所造成的影响大于P450酶活性差异所造成的影响。其次,本研究采用蒙特卡罗模拟方法评估了1'-羟基雌激素肝脏水平在整个人群中可能出现的变异程度。该分析可用于推导化学物质特异性调整因子 (CSAF),其定义为肝脏中 1'-羟基雌激素 AUC 预测分布的第 99 百分位数除以第 50 百分位数。CSAF 的估计范围在 1.6 到 4.0 之间,具体取决于考虑的 1'-羟基雌激素氧化变异程度。将 CSAF 与用于解释人体生物动力学变异性的默认不确定性因子 3.16 进行比较,结果表明默认不确定性因子足以保护 99% 的人群。 草药成分雌激素生物活化为最终致癌代谢物 1'-磺酰氧基雌激素的程度取决于生物活化和解毒途径的相对水平。本研究在与相关组织组分孵育的条件下,考察了雌激素及其近端致癌代谢物1'-羟基雌激素在人体内的代谢动力学。基于获得的动力学数据,构建了雌激素在人体内的生理生物动力学(PBBK)模型,用于预测不同剂量雌激素的生物活化和解毒程度。随后,将该模型的预测结果与先前基于雄性大鼠雌激素PBBK模型的预测结果进行比较,以评估代谢活化是否存在物种差异。结果表明,1'-羟基雌激素在大鼠体内的次要代谢途径——1'-氧代雌激素的生成,是1'-羟基雌激素在人体内的主要解毒途径。由于人肝脏中1'-羟基雌激素氧化途径的活性较高,预测的1'-磺氧基雌激素生成量在不同物种间的差异仍然相对较小,尽管其前体1'-羟基雌激素的生成量在人体内预计是雄性大鼠的四倍,但预测人体内1'-磺氧基雌激素的生成量仍是雄性大鼠的两倍。总的来说,结论是,尽管人与雄性大鼠之间不同代谢途径的相对程度存在显著差异,但物种差异对雌激素最终生物活化为1'-磺氧基雌激素的影响很小。 1. 本研究使用[甲氧基-(14)C]标记化合物,在人体志愿者中研究了天然食品香料反式茴香脑和雌激素及其合成同系物对丙基茴香醚的代谢途径。所用剂量接近膳食中的摄入量,分别为1毫克、100微克和100微克。2. 在所有情况下,14C的主要消除途径均为尿液和呼出气体,以14CO2的形式排出。3. 采用溶剂萃取、薄层色谱和高效液相色谱分离尿液代谢物,并通过与标准品色谱迁移率比较和放射性同位素稀释法进行表征。反式茴香脑给药后检测到9种14C尿液代谢物,对丙基苯甲醚给药后检测到4种,雌激素给药后检测到5种。所有这些代谢物均为侧链氧化产物。4. 对丙基苯甲醚的主要代谢物为4-甲氧基马尿酸(12%)、1-(4'-甲氧基苯基)丙-1-醇(2%)和1-(4'-甲氧基苯基)丙-2-醇(8%)。 5. 反式茴香脑的主要代谢产物是4-甲氧基马尿酸(占剂量的56%),同时伴有少量1-(4'-甲氧基苯基)丙烷-1,2-二醇的两种异构体(共占3%)。6. 服用雌激素后,两名志愿者分别以1'-羟基雌激素的形式排出0.2%和0.4%的剂量。7. 本文讨论了人体代谢数据,并参考了这些化合物在小鼠和大鼠(常用于安全性评估的物种)中的代谢分布情况。 通过分析血浆和尿液中的代谢产物,研究了强致癌物雌激素在人体饮用茴香茶后的代谢情况。基于液相色谱-串联质谱(LC-MS/MS)检测的稳定同位素稀释分析表明,雌激素的1'-羟基化反应发生得非常迅速,尿液中结合型1'-羟基雌激素的浓度在1.5小时后达到峰值,而10小时后则检测不到。除了所给雌激素剂量中不足0.41%的结合型1'-羟基雌激素生成外,雌激素的进一步代谢产物对烯丙基苯酚的生成比例更高(17%)。饮用茴香茶后0.75-2.5小时内,血浆中也检测到了这两种代谢物。与之相反,这些样本中雌激素的浓度均未超过检测限。由此可见,过量的茴香主要香气成分反式茴香脑主要不干扰雌激素的代谢,但不能排除其对代谢物定量组成的影响。由于其高反应活性和不稳定性,无法确认雌激素硫酸结合物的存在。 有关 1-甲氧基-4-(2-丙烯基)苯(共 11 种)的更多代谢/代谢物(完整)数据,请访问 HSDB 记录页面。 |
| 参考文献 | |
| 其他信息 |
根据一个由科学和健康专家组成的独立委员会的说法,雌激素可能致癌。
雌激素是一种无色液体,具有茴香气味,不溶于水。它从鳄梨(Persea gratissima Grath.)的果皮和雌激素油中分离得到。此外,它还存在于俄罗斯茴香油、罗勒油、茴香松节油、龙蒿油和茴香树皮油中。(NTP, 1992) 雌激素是一种苯丙素类化合物,是胡椒酚(chavicol)中羟基被甲氧基取代的化合物。它具有多种用途,包括作为调味剂、昆虫引诱剂、植物代谢物、基因毒素和致癌物。它是一种烯基苯、单甲氧基苯和苯丙素类化合物。它在功能上与查维醇相关。 据报道,香茅、紫苏以及其他有相关数据的生物体中均含有雌激素。 另见:茴香油(部分);龙蒿(注释已移至)。 作用机制 蛋白磷酸酶2A (PP2A) 是一种丝氨酸/苏氨酸磷酸酶,可调节细胞信号通路。其失活与肿瘤恶性程度相关,这可能是由于其对细胞分化和恶性细胞转化的影响。因此,PP2A 被认为是一种有前景的癌症治疗靶点。在我们之前对肝致癌物雌激素 (ES) 的研究中,细胞增殖可能是将 ES 特异性 DNA 加合物转化为突变所必需的。为了探究细胞增殖的触发因素,我们采用灌胃法,以3、30和300 mg/kg/天的剂量,连续4周给予gpt delta大鼠ES。结果显示,仅在高剂量组观察到ES诱导的细胞增殖和基因突变,而ES特异性DNA加合物的产生呈剂量依赖性。Western blot分析表明,Akt和ERK通路被激活,但上游调控因子如c-Raf、PKC和PI3K未被激活。此外,我们还发现PP2A C亚基Tyr307位点的磷酸化以及Src的磷酸化。总体数据表明,高剂量ES可能通过激活Akt和ERK通路,导致PP2A失活,从而促进细胞周期进程。基于γ-H2AX免疫组化和Rad51蛋白的Western blot分析,我们发现突变谱中存在大片段缺失突变,这可能是由DNA双链断裂引起的。因此,PP2A 的失活很可能导致基因突变的加速和加剧。我们得出结论,PP2A 可能参与化学致癌的早期阶段,提示 PP2A 可能成为癌症一级预防的分子靶点。 雌激素(甲基胡椒酚)是一种挥发性萜类醚,是许多植物(例如罗勒、茴香、龙蒿)精油的主要成分,广泛用于民间医学和芳香疗法[1]。 该研究首次证明,雌激素作用于周围神经,可逆性地抑制与兴奋性相关的参数(复合动作电位振幅、传导速度、时值、阈值电流)。这种局部麻醉样活性在毫摩尔浓度范围内即可观察到[1]。 本研究并未探究兴奋性降低的机制,但提示可能与被动膜特性、电压依赖性钠电导或几何因素的改变有关[1]。 据称,Estragole 的神经阻滞有效浓度范围(2-6 mM)与普鲁卡因和利多卡因等经典局部麻醉剂相似。作者指出,在他们的实验条件下,Estragole 似乎能完全阻断所有复合动作电位 (CAP) 成分,其对某些感觉纤维成分的阻断效果与利多卡因相似,甚至可能更彻底[1]。 该研究引用了先前的研究,表明Estragole 具有镇静和抗惊厥活性,这与它对中枢神经系统的影响有关[1]。 |
| 分子式 |
C10H12O
|
|---|---|
| 分子量 |
148.2017
|
| 精确质量 |
148.088
|
| CAS号 |
140-67-0
|
| PubChem CID |
8815
|
| 外观&性状 |
Colorless to light yellow liquid
|
| 密度 |
0.9±0.1 g/cm3
|
| 沸点 |
216.0±0.0 °C at 760 mmHg
|
| 闪点 |
81.1±0.0 °C
|
| 蒸汽压 |
0.2±0.4 mmHg at 25°C
|
| 折射率 |
1.505
|
| LogP |
3.15
|
| tPSA |
9.23
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
1
|
| 可旋转键数目(RBC) |
3
|
| 重原子数目 |
11
|
| 分子复杂度/Complexity |
112
|
| 定义原子立体中心数目 |
0
|
| SMILES |
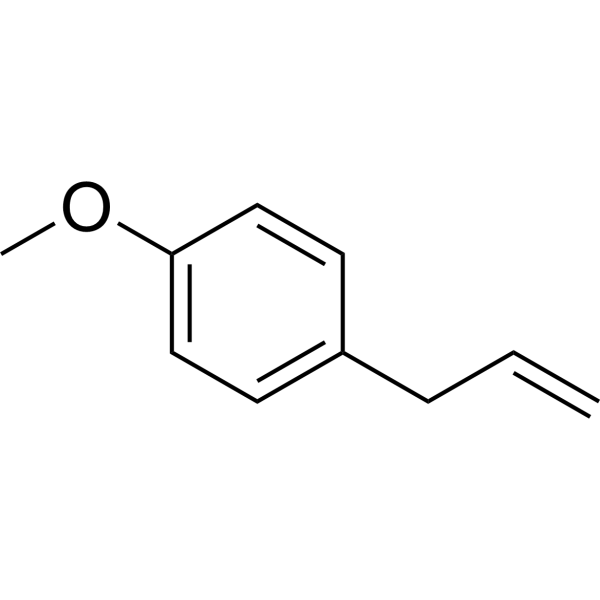
O(C([H])([H])[H])C1C([H])=C([H])C(=C([H])C=1[H])C([H])([H])C([H])=C([H])[H]
|
| InChi Key |
ZFMSMUAANRJZFM-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C10H12O/c1-3-4-9-5-7-10(11-2)8-6-9/h3,5-8H,1,4H2,2H3
|
| 化学名 |
1-methoxy-4-prop-2-enylbenzene
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~674.76 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (16.87 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (16.87 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (16.87 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 6.7476 mL | 33.7382 mL | 67.4764 mL | |
| 5 mM | 1.3495 mL | 6.7476 mL | 13.4953 mL | |
| 10 mM | 0.6748 mL | 3.3738 mL | 6.7476 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。