| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
exocytosis; Golgi; ARF-1
Exo1 modifies the GTPase activity of Golgi ARF1. Exo1 offers a separate method of interfering with Golgi activity because it blocks a portion of the membrane events that BFA blocks, although it appears to target a different protein target and likely has different side effects. Exo1 Disrupts Golgi structures to disrupt vesicular traffic from the ER to the Golgi apparatus. Exo1 has an IC50 of about 20 μM, which inhibits exocytosis. Exo1 inhibits newly synthesized proteins like VSVGts-GFP, transferrin, and MHC class I from acquiring endoglycosidase H resistance[1]. |
|---|---|
| 体外研究 (In Vitro) |
Exo1 修饰高尔基体 ARF1 的 GTP 酶活性。 Exo1 提供了一种干扰高尔基体活性的单独方法,因为它阻断了 BFA 阻断的部分膜事件,尽管它似乎针对不同的蛋白质靶点并且可能具有不同的副作用。 Exo1 破坏高尔基体结构,破坏从内质网到高尔基体的囊泡交通。 Exo1 的 IC50 约为 20 μM,可抑制胞吐作用。 Exo1 抑制新合成的蛋白质(如 VSVGts-GFP、转铁蛋白和 MHC I 类)获得内切糖苷酶 H 抗性[1]。
在BSC1细胞的VSVGts-GFP运输实验中,Exo1 抑制胞吐作用的IC₅₀约为20 µM [1] Exo1 (100 µM) 能像BFA一样,诱导高尔基体内容物(如GalT-GFP)迅速重新分布回内质网,延时荧光显微镜观察证实此点 [1] Exo1 处理导致ARF1-GFP和包被蛋白复合物I (COPI) 从高尔基体膜上快速解离,半衰期小于1分钟,与BFA类似 [1] 与BFA不同,Exo1 (100 µM) 在处理后2分钟内不诱导反式高尔基体网络相关包被蛋白(GGA3, AP-1, AP-3, 网格蛋白)的快速释放 [1] 与BFA不同,Exo1 不会使标记有内化转铁蛋白的内体膜形成管状结构 [1] 在体外交换实验中,Exo1 (100 µM) 不干扰几种ARF-GEF的鸟嘌呤核苷酸交换活性 [1] 用AlF₄ (AlCl₃ + NaF) 预处理会阻断 Exo1 (100 µM) 诱导野生型ARF1-GFP从高尔基体膜解离的能力 [1] 一个GTP酶缺陷的ARF1突变体 (ARF1[Q71L]-GFP) 对 Exo1 (100 µM) 的敏感性降低,仅表现出短暂且不完全的从高尔基体膜解离,并能阻止COPI的解离 [1] 表达ARF1[Q71L]可以挽救 Exo1 (100 µM) 存在下VSVGts-GFP从内质网的输出,并防止高尔基体塌陷 [1] Exo1 (100 µM) 不诱导CtBP/Bars50的ADP-核糖基化,而BFA会诱导 [1] Exo1 对高尔基体的影响是可逆的;化合物移除30分钟后,高尔基体标记物在核周区域重新出现 [1] |
| 酶活实验 |
色氨酸荧光法测定GDP/GTP交换。[1]
如上所述,进行了用于测量GTP与ARF1D17结合的荧光测定,该GTP结合由在F190Y、A191S、S198M和P208D位置突变的ARF核苷酸结合位点开放器(ARNO)的sec7结构域刺激。用100 mM的Exo1或10 mM的BFA测定具有100 nM重组ARNO sec7结构域的ARF1D17(5 mM)。 鸟嘌呤核苷酸交换试验[1] 整个膜。将含有5 mg蛋白质和不同量化合物的高尔基体膜与4 mM肉豆蔻酰化重组ARF1和100 mM GTP[g-35S]在30°C下孵育15分钟。通过闪烁计数测量与过滤器结合的放射性,并用在没有重组ARF的情况下结合的量对结果进行校正(背景<20%)。 重组GFB1、BFA抑制ARF-GEF 1和ARF[1] 如前所述,在30°C下,在50 mM Hepes(pH 7.5)、100 mM KCl、1 mM MgCl2、1 mM DTT、1.5 mg/ml唑连素囊泡和4 mM 5'-[g-硫代]-三磷酸(GTP[gS])的存在下进行反应,其中掺有[35S]GTP[gS](1250 Ci/mmol),最终比活度为3´105 cpm/pmol。反应中含有DMSO(终浓度2.5%)或溶解在DMSO中的指定浓度的BFA或Exo1。通过加入2mM牛ARF3/1或2mM重组肉豆蔻酰化人ARF5引发反应。通过稀释到2ml冰冷的洗涤缓冲液(50mM Hepes,pH 7.5/100mM KCl/10mM MgCl2)中终止反应(15ml)。通过0.45 mM硝化纤维膜过滤样品,然后用2 ml洗涤缓冲液冲洗四次,对结合的ARF-GTP[gS]进行定量。在LS 6500中分析了3毫升液体闪烁剂中的干燥过滤器。在减去仅含有唑连蛋白囊泡、仅M1和仅ARF-GEF的测定中测量的背景值后,计算ARF上负载的GEF依赖性GTP的量。[1] 如所述纯化牛ARF(ARF3和ARF1的混合物)和重组肉豆蔻酰化人ARF5。如所述纯化含有BFA抑制的ARF-GEF 1的Sec7结构域的六组氨酸标记片段。通过将编码全长GBF1的片段亚克隆到表达GST的pCEP4的修饰版本中,构建了GST标记的GBF1形式。在含有蛋白酶抑制剂混合物的裂解缓冲液(PBS/0.1%Triton X-100/1 mM PMSF)中提取表达GST-GBF1的HEK-293单层。按照制造商的说明,使用谷胱甘肽琼脂糖对GST-GFB1进行部分纯化。通过1500´g离心回收的珠子用2体积的裂解缓冲液洗涤两次,用不含洗涤剂的缓冲液洗涤一次。用含有10mM谷胱甘肽的洗涤缓冲液洗脱结合物质,并如前所述进行测定。 使用ARF-GEF的重组SEC7结构域进行了鸟嘌呤核苷酸交换实验。通过相对荧光强度的增加(例如使用mant-GTP)监测GTP加载到ARF1上。测试了 Exo1 (100 µM) 和 BFA (10 µM) 的效果。Exo1 对交换速率没有抑制作用,而BFA抑制了60% [1] 测试了 Exo1 对体外GTP酶激活蛋白刺激的ARF1-GTP水解的敏感性,发现不敏感 [1] |
| 细胞实验 |
内切糖苷酶H(Endo H)敏感性[1]
在6-cm培养皿中生长的细胞(106)在40°C下用VSVGts-GFP腺病毒转导过夜。之后,在40°C下用140 mCi 35S反式(ICN)脉冲标记细胞30分钟,然后在32°C下与或不与100 mMExo1或5 mM BFA一起孵育不同时间,并对新合成的蛋白质进行内切H敏感性处理。 延时荧光显微镜[1] 将细胞铺在25mm玻璃盖玻片上,并用适当的GFP融合蛋白转染。在37°C下16-24小时后,在METAMORPH的控制下,使用滨松ER电荷耦合器件相机,用尼康E300倒置显微镜(20´0.45数值孔径物镜)在活细胞中采集37°C的荧光图像。对于解离实验,在添加Exo1之前10分钟和之后30分钟收集图像。为了测量与膜相关的GFP信号量,我们首先对每张图像应用阈值,这样只有高于细胞质背景的信号才被认为可以确定积分强度。第一幅图像中的信号(100%)用于对剩余时间点的值进行归一化。没有对可能的光漂白进行校正,因为在此期间没有检测到明显的变化。在大多数情况下,我们给出了三个独立实验中4-6个细胞的平均值。 高通量表型筛选:将BSC1细胞与VSVGts-GFP腺病毒混合,接种于384孔板。通过针转移机器人加入化合物(来自化合物库)。细胞在40°C(VSVGts-GFP无法输出的非许可温度)培养,然后转移到32°C以允许同步输出。固定后,通过自动荧光显微镜获取图像,并目视评分对VSVGts-GFP运输的抑制情况 [1] 剂量反应实验:表达VSVGts-GFP的BSC1细胞在40°C与不同浓度的 Exo1 孵育,然后转移到32°C培养3小时。测量VSVGts-GFP递送到细胞表面的相对效率以确定IC₅₀ [1] 延时荧光显微镜:用 Exo1 (100 µM) 或 BFA (5 µM) 处理表达细胞器标记物(如ARF1-GFP, GalT-GFP, GGA3-GFP)的BSC1细胞。间隔拍摄图像以监测蛋白质解离和细胞器形态变化(如高尔基体管状化和塌陷)的动态过程 [1] 内切糖苷酶H抗性实验:对细胞进行脉冲标记,在存在或不存在 Exo1 (100 µM) 或 BFA (5 µM) 的情况下进行追踪,然后裂解。免疫沉淀VSVGts-GFP并用内切糖苷酶H处理,以评估其获得抗性的情况,抗性表明其通过了高尔基体 [1] 免疫荧光和细胞器标记物分析:用针对各种细胞器标记物的抗体(如转铁蛋白用于内体,组织蛋白酶D用于溶酶体,GM130用于高尔基体基质)染色固定细胞,以评估 Exo1 作用的特异性 [1] ARF1重装载实验:表达ARF1[Q71L]-GFP的细胞用BFA预处理以使其从高尔基体释放。BFA洗脱后,将细胞与对照培养基或 Exo1 (100 µM) 孵育,并随时间监测ARF1[Q71L]-GFP重新定位到高尔基体的情况 [1] |
| 参考文献 | |
| 其他信息 |
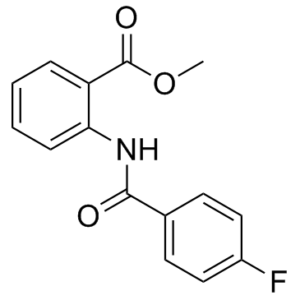
2-[[(4-氟苯基)-氧甲基]氨基]苯甲酸甲酯属于苯甲酰胺类化合物。
Exo1是从10,240个类药分子的表型筛选中鉴定出来的,这些分子是胞吐途径的抑制剂[1]。 其密切相关的类似物3-(4-氟苯甲酰氨基)-苯甲酸甲酯(m-Exo1)在该检测中没有明显作用,表明其具有构效特异性[1]。 一项包含234个相关化合物的小型构效关系(SAR)研究未能发现更有效的类似物[1]。 Exo1被提议作为BFA的补充研究工具,因为它影响一部分BFA敏感事件(内质网-高尔基体运输),但其作用机制不同,并且缺乏BFA的某些作用(例如,反式高尔基体网络/内体管状化、CtBP/Bars50 ADP核糖基化)。 [1] 提出的主要机制是Exo1干扰GTP加载下游的ARF1 GTPase循环,可能是通过增强GTP水解的无效循环,或通过阻止囊泡形成所需的有效ARF1-GTP-GAP-货物-COPI复合物的形成。[1] |
| 分子式 |
C15H12FNO3
|
|
|---|---|---|
| 分子量 |
273.26
|
|
| 精确质量 |
273.08
|
|
| 元素分析 |
C, 65.93; H, 4.43; F, 6.95; N, 5.13; O, 17.56
|
|
| CAS号 |
75541-83-2
|
|
| 相关CAS号 |
|
|
| PubChem CID |
310557
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| 密度 |
1.298 g/cm3
|
|
| 沸点 |
333.9ºC at 760 mmHg
|
|
| 闪点 |
155.8ºC
|
|
| LogP |
2.937
|
|
| tPSA |
55.4
|
|
| 氢键供体(HBD)数目 |
1
|
|
| 氢键受体(HBA)数目 |
4
|
|
| 可旋转键数目(RBC) |
4
|
|
| 重原子数目 |
20
|
|
| 分子复杂度/Complexity |
353
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
O=C(OC)C1=CC=CC=C1NC(C2=CC=C(F)C=C2)=O
|
|
| InChi Key |
KIAPWMKFHIKQOZ-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C15H12FNO3/c1-20-15(19)12-4-2-3-5-13(12)17-14(18)10-6-8-11(16)9-7-10/h2-9H,1H3,(H,17,18)
|
|
| 化学名 |
methyl 2-[(4-fluorobenzoyl)amino]benzoate
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (9.15 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL 澄清 DMSO 储备液加入900 μL 玉米油中,混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.6595 mL | 18.2976 mL | 36.5952 mL | |
| 5 mM | 0.7319 mL | 3.6595 mL | 7.3190 mL | |
| 10 mM | 0.3660 mL | 1.8298 mL | 3.6595 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT04491240 | Completed | Drug: EXO 1 inhalation Drug: EXO 2 inhalation |
Covid19 COVID-19 |
State-Financed Health Facility "Samara Regional Medical Center Dinasty" |
July 20, 2020 | Phase 1 Phase 2 |
Exit of VSVGts-GFP from the ER is inhibited by Exo1.
Exo1 does not induce the ADP-ribosylation of Bars50.Proc Natl Acad Sci U S A.2003 May 27;100(11):6469-74. |
Exo1 induces tubulation and collapse of the Golgi apparatus but not endosomes and TGN. |
Exo1 acts on ARF1-GTPase through a different mechanism compared with BFA.Proc Natl Acad Sci U S A.2003 May 27;100(11):6469-74. |