| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
HIV-1
Fostemsavir (BMS-663068): Prodrug of BMS-626529; the active component BMS-626529 targets HIV-1 envelope glycoprotein gp120 (binds to the CD4-binding site of gp120, EC50 for wild-type HIV-1 IIIB in TZM-bl cells = 0.035 μM; Ki for gp120-CD4 binding = 0.012 μM) [1] |
|---|---|
| 体外研究 (In Vitro) |
BMS-663068是小分子抑制剂BMS-626529的前药,通过与gp120结合并干扰病毒对CD4+ t细胞的附着来抑制人类免疫缺陷病毒1型(HIV-1)感染。由于gp120内的异质性,BMS-626529的活性依赖于病毒。为了更好地了解BMS-626529对HIV-1的抗谱,测定了其对多种实验室菌株和临床分离株的体外活性。BMS-626529对绝大多数病毒分离株的半数最大有效浓度(EC(50))值<10 nM;然而,对大多数易感病毒的敏感性变化大于6 log(10),在低pM范围内,对大多数易感病毒的有效浓度值达到最大值的一半。BMS-626529的体外抗病毒活性一般与嗜性或亚型无关,少数例外。测定BMS-626529对纯化gp120的结合亲和力表明,其抑制效力的一个因素可能是相对较长的解离半衰期。最后,在双药联合研究中,BMS-626529显示出与不同机制类别的抗逆转录病毒药物的加性或协同相互作用。这些结果表明BMS-626529应该对大多数HIV-1病毒有活性,并支持该化合物的持续临床开发。[1]
1. Fostemsavir (BMS-663068)本身在体外无抗HIV活性,其活性代谢产物BMS-626529在TZM-bl报告细胞中对多种野生型HIV-1毒株(IIIB、ADA、BaL、JR-FL)的复制具有强效抑制作用,EC50值范围为0.035 μM(IIIB)至0.089 μM(JR-FL)[1] 2. Fostemsavir的活性形式BMS-626529对HIV-1临床分离株具有广谱抑制活性,包括对逆转录酶抑制剂(RTIs)、蛋白酶抑制剂(PIs)和融合抑制剂(如T20)耐药的毒株;在TZM-bl细胞中,这些耐药株的EC50值为0.028 μM至0.105 μM[1] 3. 在人原代外周血单核细胞(PBMCs)中,BMS-626529对巨噬细胞嗜性(R5)和T细胞嗜性(X4)HIV-1毒株的EC50值分别为0.052 μM和0.041 μM[1] 4. BMS-626529通过抑制gp120与CD4受体的结合,阻断HIV-1病毒颗粒附着于宿主细胞(经流式细胞术和共聚焦显微镜验证);对病毒进入的附着后步骤(如融合、整合)无影响[1] 5. 联合用药研究中,BMS-626529与其他抗HIV药物(依非韦伦、恩曲他滨、替诺福韦、利托那韦)在体外表现出协同抗HIV活性,所有测试药物对的联合指数(CI)均<0.8[1] 6. BMS-626529在人细胞系(TZM-bl、CEM-SS)和原代PBMCs中的细胞毒性较低,CC50值>100 μM;对野生型HIV-1 IIIB的治疗指数(TI=CC50/EC50)>2800[1] |
| 体内研究 (In Vivo) |
BMS-663068,也称为 fostemsavir,对病毒感染的受试者表现出强大的抗病毒活性,IC50 值小于 100 nM[1]。
血浆HIV-1 RNA载量较基线的最大中位数下降范围为1.21至1.73 log(10)拷贝/mL。BMS-626529的血浆浓度与抗病毒反应无关,而低基线抑制浓度和最低和平均稳态BMS-626529血浆浓度,当通过基线蛋白结合调整的90%抑制浓度(抑制商)调整时,与抗病毒反应相关。BMS-663068总体耐受良好。结论:联合或不联合利托那韦给药BMS-663068 8天可显著降低血浆HIV-1 RNA水平,并且通常耐受性良好。BMS-663068作为联合抗逆转录病毒治疗的一部分进行长期临床试验是有必要的。临床试验注册,nct01009814。 [J Infect Dis . 2012 Oct 1;206(7):1002-11] |
| 酶活实验 |
Affinity and off-rates of attachment inhibitors from gp120.[1]
采用Micro BioSpin 6柱测定[3H]BMS-488043或[3H]BMS-626529与gp120的结合。结合溶液(30 μl)含有25 mM Tris-HCl (pH 7.5)、125 mM NaCl、50 nM gp120JRFL和连续稀释的[3H]BMS-488043或[3H]BMS-626529,使其达到平衡,然后吸附在MicroBioSpin 6柱上。将色谱柱离心(~ 14000 rpm) 5分钟,收集洗脱液,用闪烁计数器测定放射性。为了测量解离动力学,将150 nM [3H]BMS-626529或90 nM [3H]BMS-488043与60 nM gp120在室温下孵育1小时以达到平衡结合,然后加入大摩尔过量(14倍)可溶性CD4蛋白以驱动解离。在指定的时间间隔取等分,吸附到自旋柱上,离心,定量洗脱液中的放射性。通过比较有和没有可溶性CD4挑战的平行样品的氚信号,可以确定化合物结合的百分比。[1] 1. 基于SPR的gp120-CD4结合抑制实验[1]:将重组HIV-1 gp120蛋白固定在生物传感器芯片上,将系列浓度的Fostemsavir活性形式BMS-626529注射到芯片表面,随后加入重组可溶性CD4(sCD4)蛋白。实时检测表面等离子体共振(SPR)信号,定量sCD4与gp120的结合程度,计算抑制率并确定BMS-626529的Ki值。 2. 荧光偏振(FP)结合实验[1]:将荧光标记的CD4衍生肽与重组gp120蛋白及不同浓度的BMS-626529共同孵育,检测荧光偏振信号以衡量CD4肽与gp120的相互作用,计算抑制该相互作用的IC50,验证BMS-626529与gp120的CD4结合位点的结合特异性。 |
| 细胞实验 |
细胞毒性检测。[1]
在连续稀释的BMS-626529存在下进行细胞毒性实验长达6天,并使用XTT(2,3-双[2-甲氧基-4-硝基-5-巯基]- 2h -四氮唑-5-羧基苯胺)测定细胞活力。为了确定CC50值(杀死50%细胞所需的药物浓度),实验室适应细胞最初以0.1 × 106个细胞/ml的密度镀。在不含化合物的情况下,6天后细胞密度通常达到1.0 × 106 ~ 1.2 × 106/ml。 使用实验室病毒株进行药物敏感性试验。[1] MT-2(用于CXCR4或双向病毒)或PM1(用于ccr5向病毒)细胞以0.005的感染倍数感染,并在37°C的连续稀释药物中孵育4至6天。通过测定CXCR4病毒的逆转录酶(RT)活性或CCR5病毒的p24酶联免疫吸附试验来定量病毒产量。 用临床分离物进行药敏试验。[1] 临床分离菌感染pbmc微球,感染倍数为0.005,在0.5 ml体积中,37℃孵育3小时,然后在培养基中重悬,并添加到含有一系列稀释药物的板中。最终细胞密度为1 × 106个/ml。培养皿在37℃孵育,从感染后第5天开始使用p24酶联免疫吸附试验(ELISA)试剂盒监测病毒产量。当控制感染的上清液中p24水平在动态范围内(0.6 < A490 < 2.0)时,孵育终止。 用临床分离的包膜进行药敏试验。[1] 在百时美施贵宝赞助的试验中获得的血浆样本由Monogram生物科学公司进行测试,并与Monogram收集的其他样本一起进行测试。采用PhenoSense Entry法测定包膜的药物敏感性。通过逆转录酶PCR (RT-PCR)扩增包膜序列(gp160)并连接到pCXAS表达载体上。包膜表达载体制备成大的序列池(>200),以确保准确表示每个样本中存在的病毒准种的多样性。用包膜表达载体和在缺失包膜区域含有荧光素酶的复制缺陷HIV-1基因组载体共转染HEK293细胞,制备了重组HIV-1假病毒储备。利用重组假病毒颗粒感染表达CD4/CCR5/CXCR4的U87细胞系。通过比较BMS-626529存在和不存在时荧光素酶活性测定药物敏感性。药敏数据由Monogram Biosciences提供一半最大抑制浓度(IC50)值,并以此作为报告。 1. TZM-bl细胞中HIV-1复制抑制实验[1]:将TZM-bl细胞(经工程改造表达CD4、CCR5、CXCR4,且携带受HIV LTR启动子调控的荧光素酶报告基因)以1×10⁴个/孔的密度接种于96孔板,过夜培养。以0.01的感染复数(MOI)感染HIV-1病毒颗粒(如IIIB、ADA),随后加入系列浓度的Fostemsavir活性形式BMS-626529。孵育48小时后,使用发光底物检测荧光素酶活性,根据与感染未处理对照组相比的荧光素酶信号降低程度,计算病毒抑制的EC50。 2. 原代PBMCs中HIV-1复制实验[1]:从健康供体分离人PBMCs,经植物血凝素(PHA)活化3天。将活化的PBMCs以1×10⁶个/孔接种于24孔板,以0.05的MOI感染R5或X4型HIV-1毒株,加入不同浓度的BMS-626529。感染后第7天收集培养上清,通过ELISA定量病毒p24抗原水平,确定在原代细胞中抑制病毒复制的EC50。 3. 细胞毒性实验(MTT法)[1]:将TZM-bl细胞、CEM-SS细胞和原代PBMCs接种于96孔板,加入系列浓度的BMS-626529处理72小时。加入MTT溶液,孵育4小时后用二甲基亚砜溶解甲臜结晶,检测570 nm处吸光度以计算细胞活力,确定半数细胞毒性浓度(CC50)。 4. 药物联合协同实验[1]:将TZM-bl细胞感染HIV-1 IIIB,加入固定比例的BMS-626529与其他抗HIV药物(依非韦伦、恩曲他滨、替诺福韦)。48小时后检测荧光素酶活性,采用周-泰莱法计算联合指数(CI),判断协同作用(CI<1)、相加作用(CI=1)或拮抗作用(CI>1)。 5. 病毒附着实验[1]:将HIV-1病毒颗粒与BMS-626529在37℃预孵育1小时,随后加入TZM-bl细胞并在冰上孵育2小时(仅允许病毒附着,不发生进入)。洗去未结合的病毒后培养细胞48小时,检测荧光素酶活性以评估BMS-626529对病毒附着的影响;同时设置附着后加药的平行实验,验证其对病毒进入/融合无作用。 |
| 动物实验 |
本研究为一项开放标签、多剂量、平行研究,共纳入50名HIV-1感染者,随机分配至5个治疗方案组(每12小时服用600 mg BMS-663068加100 mg利托那韦[Q12H]、睡前服用1200 mg BMS-663068加100 mg利托那韦、每12小时服用1200 mg BMS-663068加100 mg利托那韦、每12小时服用1200 mg BMS-663068加100 mg利托那韦、或每12小时服用1200 mg BMS-663068),疗程8天。研究旨在评估BMS-663068的药效学、药代动力学和安全性。[J Infect Dis.] 2012年10月1日;206(7):1002-11。
|
| 药代性质 (ADME/PK) |
吸收、分布和排泄
替姆沙韦的吸收主要受限于口服给药后溶解度和溶解度欠佳。替姆沙韦的膦酰氧甲基前药福斯特沙韦与母体药物相比,在酸性条件下具有更高的水溶性和稳定性。口服福斯特沙韦后,其绝对生物利用度约为26.9%。每日两次口服600mg福斯特沙韦后,其Cmax和AUCtau分别为1770 ng/mL和12900 ng·h/L,Tmax约为2小时。与标准餐同服福司沙韦可使其 AUC 增加约 10%,而与高脂餐同服可使其 AUC 增加约 81%。 替姆沙韦代谢迅速,之后以无活性代谢物的形式经尿液和粪便排出体外。给药后,约 51% 的药物经尿液排出,其中不足 2% 为原药;33% 经粪便排出,其中 1.1% 为原药。 静脉注射替姆沙韦后,其稳态分布容积约为 29.5 L。 替姆沙韦(福斯特沙韦的活性代谢物)的平均清除率和表观清除率分别为 17.9 L/h 和 66.4 L/h。 代谢/代谢物 福斯特沙韦在肠腔刷状缘膜上的碱性磷酸酶的作用下迅速水解为活性代谢物替姆沙韦。替姆沙韦进一步生物转化生成两种主要的无活性代谢物:酯酶水解产物BMS-646915和CYP3A4氧化生成的N-去烷基化代谢物BMS-930644。口服给药后,约36.1%经酯酶代谢,21.2%经CYP3A4代谢,不足1%经UDP-葡萄糖醛酸转移酶(UGT)结合后被清除。已知替姆沙韦及其两种主要代谢物均能抑制BCRP。 生物半衰期 替姆沙韦的半衰期约为11小时。口服福斯特沙韦后,血浆中通常检测不到福斯特沙韦。 1. 福斯特沙韦 (BMS-663068) 是一种前药,在体外和体内均可快速水解为其活性代谢物 BMS-626529;该水解反应由细胞磷酸酶催化,在人血浆和外周血单核细胞 (PBMC) 培养物中,1 小时内即可完全转化 [1] |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
在注册临床试验中,福斯特沙韦与高达25%的患者出现丙氨酸氨基转移酶(ALT)升高相关,但仅有4%的受试者ALT水平超过正常值上限(ULN)5倍。大多数ALT升高是短暂的、无症状的,无需调整剂量或停药。更显著的ALT升高通常归因于其他疾病或HIV感染并发症。在注册前试验中,未观察到福斯特沙韦引起的肝损伤的明确病例。自福斯特沙韦获准用于HIV多药联合治疗以来,尚未有已发表的病例报告显示其使用会导致临床上明显的肝损伤。 值得注意的是,在福斯特沙韦的大型预注册试验中,合并乙型肝炎病毒(HBV)或丙型肝炎病毒(HCV)感染的患者血清转氨酶水平显著升高。该试验中因肝病死亡的病例似乎是由于治疗期间合并感染加重所致。显然,合并HBV或HCV感染的患者应在接受福斯特沙韦抗逆转录病毒治疗之前或同时接受这些病毒感染的治疗。 可能性评分:E(未经证实但怀疑是导致临床上明显的肝损伤的原因)。 妊娠和哺乳期影响 ◉ 哺乳期用药概述 目前尚无关于哺乳期使用福斯特沙韦的信息。由于该药物及其活性代谢物替姆沙韦的蛋白结合率超过80%,因此其在乳汁中的含量可能很低。通过抗逆转录病毒疗法实现并维持病毒抑制可将母乳喂养传播的风险降低至1%以下,但并非为零。对于接受抗逆转录病毒疗法且病毒载量持续低于检测限的HIV感染者,如果她们选择母乳喂养,应予以支持。如果病毒载量未被抑制,建议使用巴氏消毒的捐赠母乳或配方奶。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对泌乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白结合 替姆沙韦在血浆中的蛋白结合率约为 88.4%,主要与血清白蛋白结合。 1. 体外细胞毒性:BMS-626529(福斯特沙韦的活性形式)在人细胞系(TZM-bl CC50 > 100 μM,CEM-SS CC50 > 100 μM)和原代外周血单核细胞(PBMC)(CC50 > 100 μM)中具有较低的细胞毒性,因此具有较高的治疗指数(野生型 HIV-1 的 TI > 2800)。 IIIB) [1] 2. 血浆蛋白结合率:BMS-626529 在人血浆中表现出中等的血浆蛋白结合率 (78%),体外未观察到对其他蛋白结合药物的显著置换作用 [1] 3. 药物相互作用:在浓度高达 10 μM 时,BMS-626529 不会抑制或诱导人肝微粒体中的主要细胞色素 P450 (CYP) 同工酶(CYP1A2、CYP2C9、CYP2C19、CYP2D6、CYP3A4)[1] |
| 参考文献 | |
| 其他信息 |
福斯特沙韦(商品名:Rukobia)是一种处方药,已获得美国食品药品监督管理局 (FDA) 批准,用于治疗符合特定条件的既往接受过治疗的成人 HIV 感染者,具体条件由医疗保健提供者确定。福斯特沙韦必须与其他 HIV 药物联合使用。
福斯特沙韦是替姆沙韦的膦酰氧甲基前药,替姆沙韦是一种新型 HIV-1 附着抑制剂。它与 gp120 结合并抑制其活性,gp120 是 HIV-1 gp160 包膜糖蛋白的一个亚基,可促进 HIV-1 与宿主细胞 CD4 受体的附着——通过这种方式,替姆沙韦阻止了 HIV-1 病毒生命周期的第一步。gp120 作为 HIV-1 感染治疗的潜在靶点的发现相对较新,其源于人们希望为耐药 HIV-1 感染患者寻找替代靶蛋白(即机制正交的疗法)。福斯特马韦是首个获得FDA批准的病毒附着抑制剂,于2020年7月获批,用于与其他抗逆转录病毒药物联合治疗既往接受过多种治疗且目前治疗无效的多重耐药HIV-1感染患者。靶向gp120亚基是治疗HIV-1感染的一种全新策略,而像替姆沙韦这样的病毒附着抑制剂的加入,为那些几乎没有有效治疗方案的患者填补了治疗选择上的空白。 福斯特马韦是一种独特的抗逆转录病毒药物,它能与人类免疫缺陷病毒(HIV)的包膜抗原结合,抑制其与CD4+淋巴细胞表面受体的结合。它用于治疗尽管接受了优化的背景治疗,但仍存在多重耐药感染且病毒抑制不足的患者。福斯特沙韦与治疗期间血清转氨酶升高发生率较低相关,但尚未有确凿证据表明其与临床上明显的肝损伤事件相关。 药物适应症 福斯特沙韦与其他抗逆转录病毒药物联合使用,适用于治疗因耐药、不耐受或安全性问题而导致当前抗逆转录病毒治疗失败的、经多次治疗的成人多重耐药HIV-1感染患者。 鲁科比亚与其他抗逆转录病毒药物联合使用,适用于治疗无法构建抑制性抗病毒方案的成人多重耐药HIV-1感染患者。 作用机制 HIV-1 gp160包膜糖蛋白中的gp120亚基是治疗HIV-1感染的一个新靶点。这些亚基负责促进病毒生命周期的第一步——病毒附着,它们介导病毒与宿主细胞 CD4 受体之间的相互作用。附着后,HIV-1 在宿主细胞内进行组装、出芽和成熟,之后成熟的病毒颗粒被释放,继续其生命周期。福斯特沙韦的活性代谢物替姆沙韦是一种 HIV-1 附着抑制剂。它直接与 gp120 亚基结合,抑制病毒与宿主 CD4 受体的相互作用,从而阻止病毒复制所需的初始附着。研究还表明,它能够抑制病毒进入细胞所需的其他 gp120 依赖性附着后步骤。 药效学 替姆沙韦抑制 HIV-1 病毒生命周期的第一阶段:病毒附着。其作用持续时间中等,因此需要每日两次给药。研究发现,以大约 4 倍于推荐人剂量的福斯特沙韦给药时,会显著延长 QTc 间期。有QTc间期延长病史的患者、正在服用其他可延长QTc间期药物的患者和/或患有既往心脏疾病的患者应谨慎使用福斯特沙韦,并在基线和整个治疗期间监测提示QTc间期延长的体征或症状。福斯特沙韦也应谨慎用于合并乙型或丙型肝炎病毒感染的患者,因为临床试验中观察到这些人群中肝转氨酶升高的比例更高。 1. 福斯特沙韦 (BMS-663068) 是一种首创的HIV-1附着抑制剂前药;其活性代谢物BMS-626529是一种小分子,可与HIV-1包膜糖蛋白gp120的CD4结合位点结合,从而阻止病毒与表达CD4的宿主细胞(T细胞、巨噬细胞)的初始附着[1] 2.与其他抗HIV药物(例如,逆转录酶抑制剂、蛋白酶抑制剂、融合抑制剂)不同,福斯特沙韦作用于病毒生命周期的早期阶段(附着),并且对其他抗逆转录病毒药物耐药的HIV-1毒株有效[1]。 3. 福斯特沙韦与现有抗逆转录病毒药物具有协同抗HIV活性,使其成为多重耐药HIV-1感染患者联合治疗的潜在候选药物[1]。 |
| 分子式 |
C25H26N7O8P
|
|---|---|
| 分子量 |
583.48984
|
| 精确质量 |
583.158
|
| 元素分析 |
C, 51.46; H, 4.49; N, 16.80; O, 21.94; P, 5.31
|
| CAS号 |
864953-29-7
|
| 相关CAS号 |
Temsavir;701213-36-7;Fostemsavir Tris;864953-39-9; Temsavir;701213-36-7; 864953-29-7(free base); 864953-39-9 (tromethamine) ; 864953-31-1 (disodium); 942117-71-7 (dihydrate)
|
| PubChem CID |
11319217
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.6±0.1 g/cm3
|
| 沸点 |
904.1±75.0 °C at 760 mmHg
|
| 闪点 |
500.6±37.1 °C
|
| 蒸汽压 |
0.0±0.3 mmHg at 25°C
|
| 折射率 |
1.723
|
| LogP |
-2.98
|
| tPSA |
192.02
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
11
|
| 可旋转键数目(RBC) |
8
|
| 重原子数目 |
41
|
| 分子复杂度/Complexity |
1020
|
| 定义原子立体中心数目 |
0
|
| SMILES |
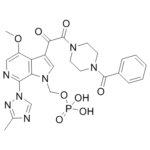
O=C(C1C2C(=C(N3C=NC(C)=N3)N=CC=2OC)N(COP(O)(O)=O)C=1)C(N1CCN(C(C2C=CC=CC=2)=O)CC1)=O
|
| InChi Key |
SWMDAPWAQQTBOG-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C25H26N7O8P/c1-16-27-14-32(28-16)23-21-20(19(39-2)12-26-23)18(13-31(21)15-40-41(36,37)38)22(33)25(35)30-10-8-29(9-11-30)24(34)17-6-4-3-5-7-17/h3-7,12-14H,8-11,15H2,1-2H3,(H2,36,37,38)
|
| 化学名 |
(3-(2-(4-benzoylpiperazin-1-yl)-2-oxoacetyl)-4-methoxy-7-(3-methyl-1H-1,2,4-triazol-1-yl)-1H-pyrrolo[2,3-c]pyridin-1-yl)methyl dihydrogen phosphate
|
| 别名 |
BMS-663068; BMS663068; BMS-663068 dihydrate; BMS 663068; Fostemsavir; 864953-29-7; BMS-663068 free acid; Fostemsavir [USAN]; Fostemsavir(BMS-663068); 97IQ273H4L;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL ( ~171.38 mM )
H2O : ~20 mg/mL (~34.28 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 8.33 mg/mL (14.28 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶。 (<60°C).
请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.7138 mL | 8.5691 mL | 17.1383 mL | |
| 5 mM | 0.3428 mL | 1.7138 mL | 3.4277 mL | |
| 10 mM | 0.1714 mL | 0.8569 mL | 1.7138 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
 (A) Distribution of EC50s for BMS-626529 against HIV-1 subtype B clinical isolates in the PBMC assay.Antimicrob Agents Chemother.2012 Jul;56(7):3498-507. |
|---|
 Distribution of EC50s for BMS-626529 against HIV-1 non-subtype B clinical isolates in the PBMC assay.Antimicrob Agents Chemother.2012 Jul;56(7):3498-507. |
 Distribution of EC50s for BMS-626529 against HIV-1 clinical isolates according to tropism in the PBMC assay.Antimicrob Agents Chemother.2012 Jul;56(7):3498-507. |