| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| Other Sizes |
|
| 靶点 |
Histone acetyltransferases (HATs), specifically p300/CBP and PCAF. Garcinol is a cell-permeable natural HAT inhibitor that also modulates multiple signaling pathways including NF-κB, STAT3, PI3K/AKT, MAPK, and Wnt/β-catenin. It also regulates microRNA expression and reverses epithelial-mesenchymal transition (EMT). [1, 2]
In leishmanicidal assays, garcinol (as guttiferone A) showed an IC₅₀ of 0.16 μM against L. donovani amastigotes. [1] For anticholinesterase activity, garcinol (as garcinol) showed an IC₅₀ of 0.66 μM against AChE and 7.39 μM against BChE. [1] |
|---|---|
| 体外研究 (In Vitro) |
Garcinol(作为 guttiferone A 和 guttiferone F)对杜氏利什曼原虫无鞭毛体表现出显著的抗利什曼原虫活性,IC₅₀ 值分别为 0.16 μM 和 0.20 μM,强于参考化合物米替福新(0.47 μM)。 [1]
Garcinol 表现出强效的乙酰胆碱酯酶抑制活性,IC₅₀ 为 0.66 μM,与加兰他敏(0.50 μM)相当。它还表现出丁酰胆碱酯酶抑制活性,IC₅₀ 为 7.39 μM。Guttiferone A 和 guttiferone F 对 BChE 的活性高于加兰他敏(IC₅₀ 分别为 2.77 和 3.50 μM)。 [1] 作为 HAT 抑制剂,Garcinol 在 HeLa 细胞中抑制了超过 70% 的被评估基因的表达,其中许多基因控制细胞分裂、程序性死亡和致癌过程。 [2] Garcinol 在多种癌细胞系中诱导 S 期细胞周期阻滞并促进凋亡,包括卵巢癌、胃癌、结肠癌、口腔鳞癌、胶质母细胞瘤、肝细胞癌、黑色素瘤、乳腺癌、胰腺癌和子宫内膜癌。 [2] Garcinol 下调 cyclin D1 和 cyclin D3,抑制 CDK2 和 CDK4,并抑制 PI3K/AKT 信号通路。它激活 p53 和硫氧还蛋白还原酶,导致 ROS 积累增加、JNK 激活和 DNA 损伤信号传导。在 MCF-7 乳腺癌细胞中,它通过 ROS/JNK/ATF-2/Bcl-2 轴激活线粒体凋亡。 [2] Garcinol 通过干扰 IκBα 磷酸化和 p65 核转位来抑制 NF-κB 信号通路,减少促炎细胞因子、抗凋亡因子和细胞周期调节因子的表达。 [2] Garcinol 上调肿瘤抑制性 miRNA,下调致癌性 miRNA。 [2] Garcinol 通过增加 E-cadherin 和减少 vimentin、ZEB1/2 和 Snail 表达来逆转上皮-间充质转化。 [2] Garcinol 通过抑制 NF-κB、STAT3 和 HIF-1α 通路来抑制 VEGF 表达和血管生成。 [2] 对两种 HNSCC 细胞系(CAL27 和 UMSCC1)进行了评估,这些细胞系的生长受到 garcinol(10-50 μM;24-72 小时)以时间和剂量依赖性方式的抑制 [3]。在 HNSCC 细胞中,garcinol(10-50 μM;24-72 小时)会导致细胞凋亡 [3]。 garcinol(50 μM;1-6 小时)以时间依赖性方式抑制组成型 IκBα 的磷酸化和降解 [3]。 |
| 体内研究 (In Vivo) |
在原发性渗出性淋巴瘤模型中,NOD/SCID 小鼠接种 BCBL1-Luc 细胞后,隔日腹腔注射 garcinol(2.5 和 25 mg/kg),连续三周,以剂量依赖性方式抑制肿瘤生长。 [2]
在前列腺癌异种移植模型中,腹腔注射或口服 garcinol(50 mg/kg/天,每周 5 天)使肿瘤质量减少 >80%,增加 NK 细胞活性,增加 caspase-3 和 -9 活性,降低 Bcl-2 和 Bcl-xL,增加 Bax 和 Bad。 [2] 在乳腺癌异种移植模型中,口服 garcinol(5 mg/只/天,每周 6 天,持续 4 周)抑制 NF-κB、vimentin、核 β-catenin 和 EMT 标志物,同时上调 miR-200 和 let-7 家族。在 4T1 乳腺癌模型中,garcinol(1 mg/kg)与低剂量紫杉醇(5 mg/kg)联用增强了治疗效果。 [2] 在胰腺癌 KPC 转基因小鼠模型中,饮食中添加 garcinol(0.05%)延迟了胰腺上皮内瘤变进展,增强了 NK 细胞活性,并与吉西他滨联用提高了生存率。 [2] 在结肠癌发生模型中,饮食中添加 garcinol(250 或 500 ppm)减少了肿瘤大小和发生率,通过抑制 ERK1/2、PI3K/Akt 和 Wnt/β-catenin 通路降低了 COX-2、cyclin D1 和 VEGF。 [2] 在头颈部鳞状细胞癌异种移植模型中,garcinol 减少了肿瘤生长,降低了 NF-κB、STAT3、MAPKs、p65、Ki-67 和 CD31,并诱导了凋亡,且无毒性。garcinol 与顺铂联用显示出增强的疗效。 [2] 在胶质母细胞瘤异种移植模型中,garcinol(1 mg/kg 腹腔注射)减少了肿瘤大小,实现了 100% 的生存率,降低了 STAT3、pSTAT3、STAT5A、pSTAT5A、Ki-67 和 Bcl-xL,并增加了 Bax 和 miR-181d 表达。 [2] 在皮肤癌模型中,局部或口服 garcinol 减少了耳部炎症,抑制了 TPA 诱导的皮肤肿瘤发展,降低了 iNOS 和 COX-2 表达,并阻断了 NF-κB 核转位。 [2] 在肺癌异种移植模型中,garcinol(15 mg/kg 腹腔注射,持续 40 天)使肿瘤大小减少约 50%,并通过 DDIT3 激活下调 ALDH1A1。 [2] 在体外抗利什曼原虫实验中,guttiferone A 和 F 对杜氏利什曼原虫的 IC₅₀ 分别为 0.16 和 0.20 μM,强于米替福新(0.47 μM)。但这些化合物对 L6 细胞表现出细胞毒性,IC₅₀ 分别为 7.34 和 5.4 μM,选择性指数分别为 46 和 27。 [1] Garcinol(腹膜内注射;1 和 2 mg/kg;每周 5 次,持续 4 周)可有效减缓肿瘤发展 [3]。 |
| 酶活实验 |
乙酰胆碱酯酶和丁酰胆碱酯酶抑制实验: 使用稍加修改的分光光度法进行实验。乙酰硫代胆碱碘化物和丁酰硫代胆碱氯化物分别用作 AChE 和 BChE 的底物。DTNB 用于测量胆碱酯酶活性。将 100 mM 磷酸钠缓冲液(pH 8.0, 140 μL)、DTNB(10 μL)、待测化合物溶液(20 μL)和酶溶液(20 μL)混合,在 25°C 下孵育 15 分钟。加入 10 μL 底物启动反应。通过在 412 nm 处监测黄色 5-硫代-2-硝基苯甲酸阴离子的形成来跟踪水解反应,持续 15 分钟。所有反应均在 96 孔板中一式三份进行。使用 EZ-Fit Enzyme Kinetics 软件计算 IC₅₀ 值。 [1]
|
| 细胞实验 |
抗利什曼原虫活性实验: 杜氏利什曼原虫无鞭毛体在含 10% 热灭活 FBS 的 SM 和 SDM-79 培养基(1:1, pH 5.4)中培养。在 96 孔板中制备化合物的系列稀释液。每孔加入 10⁵ 个无鞭毛体,在 37°C、5% CO₂ 下孵育 72 小时。加入刃天青溶液,继续孵育 2-4 小时。在 536 nm 激发和 588 nm 发射波长下测量荧光。使用米替福新作为阳性对照。从 sigmoidal 抑制曲线计算 IC₅₀ 值。 [1]
细胞毒性实验: 将大鼠骨骼肌成肌细胞接种于 96 孔板中,在含 10% 热灭活 FBS 的 MEM 中培养。加入提取物的三倍系列稀释液。在 37°C、5% CO₂ 下孵育 72 小时。加入刃天青作为活力指示剂,测量荧光。使用鬼臼毒素作为阳性对照。使用 Softmax Pro 软件计算 IC₅₀ 值。 [1] 一般基于细胞的实验: Garcinol 已在多种癌细胞系中进行了测试,包括 HeLa、MCF-7、MDA-MB-231、PC-3、A549、U87MG、CAL27、PANC-1 等。实验包括用于活力的 MTT、用于细胞周期和凋亡的流式细胞术、用于蛋白表达的 Western blotting、用于基因表达的 qPCR 和 miRNA 阵列。Garcinol 处理通常诱导 S 期阻滞,增加 ROS,激活 caspase,改变 Bcl-2 家族蛋白表达,并调节信号通路。 [2] 细胞增殖测定[3] 细胞类型: CAL27 和 UMSCC1 细胞 测试浓度: 10、25、50 µM 孵育时间:24、48和72小时 实验结果:以时间和剂量依赖性方式抑制两种HNSCC细胞系的增殖。 细胞凋亡分析[3] 细胞类型: CAL27 和 UMSCC1 细胞 测试浓度: 10、25、50 µM 孵育持续时间:24、48和72小时 实验结果:诱导HNSCC细胞凋亡。 蛋白质印迹分析[3] 细胞类型: CAL27 细胞 测试浓度: 50 µM 孵育时间:1、2、4、6小时 实验结果:以时间依赖性方式抑制组成型IκBα磷酸化和降解。 |
| 动物实验 |
动物/疾病模型: 五周龄无胸腺nu/nu雄性小鼠,皮下接种CAL27肿瘤[3]
剂量: 1和2 mg/kg 给药途径: 腹腔注射(ip);每周五次,持续4周 实验结果: 显著抑制肿瘤生长。 |
| 药代性质 (ADME/PK) |
计算机 ADMET 分析预测 Garcinol 具有类药特性且口服生物可利用。然而,天然 garcinol 水溶性差、代谢快、生物利用度有限。 [2]
已开发纳米制剂以改善溶解度、稳定性和肿瘤靶向性。在 B16F10 黑色素瘤荷瘤小鼠中,⁹⁹ᵐTc 标记的 garcinol 负载 PLGA 纳米粒在肿瘤区域显示出中度积累。 [2] |
| 毒性/毒理 (Toxicokinetics/TK) |
在抗利什曼原虫研究中,Garcinol 对大鼠骨骼肌成肌细胞 L6 细胞显示出细胞毒性,IC₅₀ 为 7.34 μM,选择性指数为 46。Guttiferone F 的 IC₅₀ 为 5.4 μM,SI 为 27。 [1]
在动物研究中,garcinol 耐受性良好,在所用剂量下未见明显毒性效应,包括对肝脏、肾脏、肺、心脏或食道未见组织学或病理学变化。 [2] 在 Wistar 大鼠的急性安全性研究中,40% garcinol 制剂在 2000 mg/kg 高单次剂量下未产生任何不良效应,可归类为 GHS 第 5 类。在 28 天和 90 天重复剂量口服毒性研究以及生殖和发育毒性评估中,最高测试剂量 100 mg/kg/天未见治疗相关变化。 [2] 在一项针对非酒精性脂肪性肝炎患者的临床试验中,garcinol、姜黄素类化合物和胡椒碱的组合在 90 天期间未见不良毒性效应,血液学和临床实验室参数无明显变化。 [2] |
| 参考文献 |
|
| 其他信息 |
Garcinol 是一种多异戊二烯基化二苯甲酮,主要来源于藤黄果和印度藤黄的果皮和叶子。约占果皮含量的 2-3%。 [2]
Garcinol 于 2004 年首次被鉴定为一种细胞可渗透的组蛋白乙酰转移酶抑制剂,靶向 p300/CBP 和 PCAF。这一发现为其抗癌活性提供了分子解释。 [2] Garcinol 与姜黄素在结构和功能上有相似之处,包括 C3 酮基、羟基化酚环和促进凋亡诱导的 α,β-不饱和酮部分。 [2] Garcinol 已在多种恶性肿瘤中显示出抗癌效果,包括卵巢癌、胃癌、结肠癌、口腔鳞癌、胶质母细胞瘤、肝细胞癌、黑色素瘤、乳腺癌、胰腺癌、子宫内膜癌、淋巴瘤、前列腺癌、肺癌、头颈癌和皮肤癌。 [2] Garcinol 通过抑制 NF-κB 和 STAT3 信号通路、减少促炎细胞因子产生以及下调 COX-2 和 iNOS 来发挥抗炎特性。 [2] Garcinol 通过抑制 STAT3 信号、减少 NOTCH1 和 Wnt/β-catenin 信号以及诱导间充质-上皮转化来靶向癌症干细胞。 [2] 已开发 garcinol 的纳米制剂以克服溶解度和生物利用度问题,在临床前模型中显示出改善的肿瘤积累和治疗效果。 [2] Garcinol 的类似物,包括 isogarcinol、epigarcinol 和 cambogin,也显示出抗癌活性。 [2] |
| 分子式 |
C38H50O6
|
|---|---|
| 分子量 |
602.8
|
| 精确质量 |
602.36
|
| 元素分析 |
C, 75.71; H, 8.36; O, 15.92
|
| CAS号 |
78824-30-3
|
| PubChem CID |
5490884
|
| 外观&性状 |
Light yellow to yellow solid powder
|
| 密度 |
1.1±0.1 g/cm3
|
| 沸点 |
710.8±60.0 °C at 760 mmHg
|
| 熔点 |
235-236ºC
|
| 闪点 |
397.6±29.4 °C
|
| 蒸汽压 |
0.0±2.4 mmHg at 25°C
|
| 折射率 |
1.563
|
| LogP |
11.26
|
| tPSA |
111.9
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
10
|
| 重原子数目 |
44
|
| 分子复杂度/Complexity |
1300
|
| 定义原子立体中心数目 |
4
|
| SMILES |
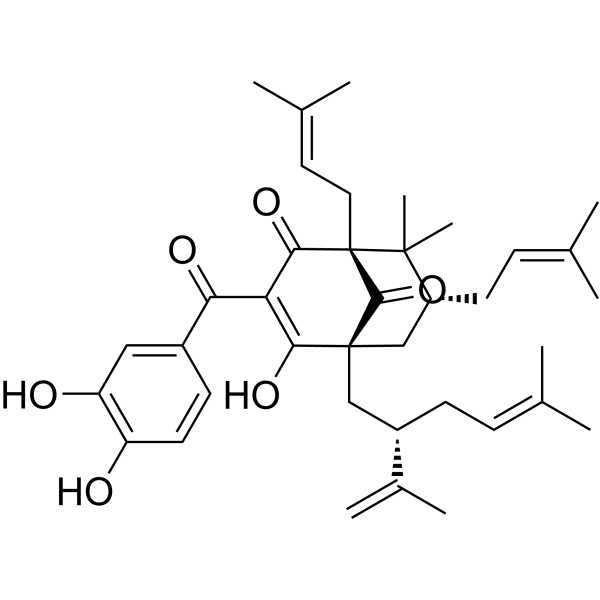
CC(=CC[C@@H]1C[C@@]2(C(=O)/C(=C(/C3=CC(=C(C=C3)O)O)\O)/C(=O)[C@@](C2=O)(C1(C)C)CC=C(C)C)C[C@H](CC=C(C)C)C(=C)C)C
|
| InChi Key |
DTTONLKLWRTCAB-UDFURZHRSA-N
|
| InChi Code |
InChI=1S/C38H50O6/c1-22(2)11-13-27(25(7)8)20-37-21-28(15-12-23(3)4)36(9,10)38(35(37)44,18-17-24(5)6)34(43)31(33(37)42)32(41)26-14-16-29(39)30(40)19-26/h11-12,14,16-17,19,27-28,39-41H,7,13,15,18,20-21H2,1-6,8-10H3/b32-31+/t27-,28+,37+,38-/m0/s1
|
| 化学名 |
(1S,3E,5R,7R)-3-[(3,4-dihydroxyphenyl)-hydroxymethylidene]-6,6-dimethyl-5,7-bis(3-methylbut-2-enyl)-1-[(2S)-5-methyl-2-prop-1-en-2-ylhex-4-enyl]bicyclo[3.3.1]nonane-2,4,9-trione
|
| 别名 |
Garcinol; Camboginol; SCHEMBL19565392; 78824-30-3; CID 5281560
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~50 mg/mL (~82.95 mM)
Ethanol : ~20 mg/mL (~33.18 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 2.5 mg/mL (4.15 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浮液;超声助溶。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.6589 mL | 8.2946 mL | 16.5893 mL | |
| 5 mM | 0.3318 mL | 1.6589 mL | 3.3179 mL | |
| 10 mM | 0.1659 mL | 0.8295 mL | 1.6589 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。