| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 体外研究 (In Vitro) |
通过占据脯氨酰-tRNA 合成酶的脯氨酸和 tRNA 结合位点,卤常酮竞争性抑制脯氨酰-tRNA 合成酶 [1]。在 KYSE70 和 A549 细胞中,卤常酮(1、10、100、1000 和 10,000 nM;48 小时)的 IC50 分别为 114.6 和 58.9 nM。在KYSE70和A549细胞中,卤常酮(1、10、100和1000 nM;24小时)针对NRF2蛋白的IC50分别为22.3和37.2 nM。在 KYSE70 和 A549 细胞中,halofuginone 对总蛋白合成的 IC50 值分别为 22.6 和 45.7 nM [1]。 Halofuginone 通过 KCNA5 通道在转染 KCNA5 基因的 HEK 细胞中提高 K+ 电流,并在肺动脉平滑肌细胞 (PASMC) 中提高电压门控 K+ (Kv) 电流。在转染钙敏感受体基因的 HEK 细胞中,卤常酮 (0.03-1μM) 抑制受体操纵的 Ca2+ 内流 (ROCE),而在 PASMC 中,它减弱钙池操纵的 Ca2+ 内流 (SOCE) [5]。
|
|---|---|
| 体内研究 (In Vivo) |
在前交叉韧带横断 (ACLT) 的小鼠中,卤常酮(0.2、0.5、1 或 2.5 mg/kg;每隔一天腹膜内注射一次,持续一个月)可减缓骨关节炎 (OA) 的进展。较低浓度(0.2 或 0.5 mg/kg)对软骨下骨的影响最小,较高浓度(2.5 mg/kg)会导致关节软骨中蛋白多糖的损失[3]。 Halofuginone(0.25 mg/kg;腹腔注射;每日;16 天)可降低肿瘤中的 NRF2 蛋白水平;然而,用赋形剂、卤酮(0.25 mg/kg,每日腹腔注射)或单独顺铂治疗之间的肿瘤体积没有显着差异。与单独使用氟戊酮或顺铂相比,氟戊酮和顺铂联合治疗可显着抑制肿瘤体积[1]。每两周腹腔内给予氟喷肽(0.3 mg/kg)。
|
| 细胞实验 |
细胞活力测定[1]
细胞类型:来自携带NRF2基因突变的人食管癌KYSE70细胞和携带KEAP1基因突变的A549细胞 测试浓度:1 , 10, 100, 1000, 10000 nM 孵育时间: 48 小时 实验结果: IC50 KYSE70 和 A549 中的浓度细胞大小分别为 114.6 和 58.9 nM。 Western Blot分析[1] 细胞类型:源自人食管癌的KYSE70细胞含有NRF2基因突变; A549 细胞含有 KEAP1 基因突变。 测试浓度:1、10、100、1000 nM 孵育持续时间:24 小时 实验结果:NRF2蛋白在KYSE70和A549细胞中的IC50分别为22.3和37.2 nM。 |
| 动物实验 |
动物/疾病模型:雄性裸鼠(BALB/c nu/nu(裸鼠))(6-8周龄)[1]
剂量:0.25 mg/kg 给药途径:腹腔注射(ip);每日一次;持续16天 实验结果:与顺铂联合治疗显著抑制了肿瘤体积。肿瘤中NRF2蛋白水平确实降低。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
口服后生物利用度高,吸收迅速。 生物半衰期 23.8 至 72.1 小时 |
| 参考文献 |
[1]. Tsuchida K, et al. Halofuginone enhances the chemo-sensitivity of cancer cells by suppressing NRF2 accumulation. Free Radic Biol Med. 2017 Feb;103:236-247.
[2]. Keller TL, et al. Halofuginone and other Febrifugine derivatives inhibit prolyl-tRNA synthetase. Nat Chem Biol. 2012 Feb 12;8(3):311-7. [3]. Cui Z, et al. Halofuginone attenuates osteoarthritis by inhibition of TGF-β activity and H-type vessel formation in subchondral bone. Ann Rheum Dis. 2016 Sep;75(9):1714-21. [4]. Tracy L McGaha, et al. Halofuginone, an inhibitor of type-I collagen synthesis and skin sclerosis, blocks transforming-growth-factor-beta-mediated Smad3 activation in fibroblasts. J Invest Dermatol. 2002 Mar;118(3):461-70. [5]. Pritesh P Jain, et al. Halofuginone, a Promising Drug for Treatment of Pulmonary Hypertension. Br J Pharmacol. 2021 Mar 10. |
| 其他信息 |
哈洛夫吉酮是一种低分子量喹唑啉酮生物碱,是胶原蛋白α1(I)和基质金属蛋白酶2 (MMP-2)基因表达的强效抑制剂。哈洛夫吉酮还能有效抑制小鼠的肿瘤进展和转移。Collgard Biopharmaceuticals公司正在开发哈洛夫吉酮用于治疗硬皮病,并于2000年3月获得美国食品药品监督管理局(FDA)授予的孤儿药资格认定。
据报道,绣球花(Hydrangea febrifuga)中也含有哈洛夫吉酮,并有相关数据。 哈洛夫吉酮是一种口服有效的喹唑啉酮生物碱,具有潜在的抗肿瘤活性。哈洛夫吉酮干扰转化生长因子β (TGF-β) 的信号通路,抑制基质金属蛋白酶2的表达,从而抑制I型胶原蛋白的合成并诱导细胞外基质降解,最终抑制血管生成、肿瘤生长或转移。 药物适应症 用于治疗硬皮病、癌症和再狭窄。 新生犊牛:- 预防由已确诊的隐孢子虫引起的腹泻,适用于有隐孢子虫病史的农场。应在出生后24至48小时内开始给药。- 减轻由已确诊的隐孢子虫引起的腹泻。应在腹泻发生后24小时内开始给药。两种情况下均已证实可减少卵囊排出。 新生犊牛:预防已确诊的隐孢子虫感染引起的腹泻,适用于有隐孢子虫病史的农场。应在出生后24至48小时内开始给药。减少已确诊的隐孢子虫感染引起的腹泻。应在腹泻发生后24小时内开始给药。两种情况下均已证实可减少卵囊排出。 新生犊牛:预防已确诊的隐孢子虫感染引起的腹泻,适用于有隐孢子虫病史的农场。应在出生后24至48小时内开始给药。减少已确诊的隐孢子虫感染引起的腹泻。应在腹泻发生后24小时内开始给药。两种情况下均已证实卵囊排出量减少。 作用机制 哈洛夫吉酮是胶原蛋白α1(I)和基质金属蛋白酶2 (MMP-2)基因表达的强效抑制剂。哈洛夫吉酮还能抑制细胞外基质沉积和细胞增殖。哈洛夫吉酮显著的抗肿瘤作用归因于其对肿瘤基质支持、血管生成、侵袭性和细胞增殖的综合抑制作用。 药效学 哈洛夫吉酮是一种完全合成的小分子,是基质细胞活化、细胞迁移和I型胶原蛋白合成的强效且选择性的调节剂,而I型胶原蛋白合成已被认为是人体组织修复过程中的“主开关”。 |
| 精确质量 |
413.014
|
|---|---|
| CAS号 |
55837-20-2
|
| 相关CAS号 |
Halofuginone hydrobromide;64924-67-0
|
| PubChem CID |
456390
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.7±0.1 g/cm3
|
| 沸点 |
595.8±60.0 °C at 760 mmHg
|
| 熔点 |
>150ºC dec.
|
| 闪点 |
314.1±32.9 °C
|
| 蒸汽压 |
0.0±1.8 mmHg at 25°C
|
| 折射率 |
1.712
|
| LogP |
1.24
|
| tPSA |
84.22
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
4
|
| 重原子数目 |
24
|
| 分子复杂度/Complexity |
533
|
| 定义原子立体中心数目 |
2
|
| SMILES |
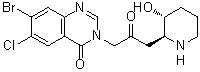
C1C[C@@H]([C@H](NC1)CC(=O)CN2C=NC3=CC(=C(C=C3C2=O)Cl)Br)O
|
| InChi Key |
LVASCWIMLIKXLA-CABCVRRESA-N
|
| InChi Code |
InChI=1S/C16H17BrClN3O3/c17-11-6-13-10(5-12(11)18)16(24)21(8-20-13)7-9(22)4-14-15(23)2-1-3-19-14/h5-6,8,14-15,19,23H,1-4,7H2/t14-,15+/m1/s1
|
| 化学名 |
7-bromo-6-chloro-3-[3-[(2R,3S)-3-hydroxypiperidin-2-yl]-2-oxopropyl]quinazolin-4-one
|
| 别名 |
RU 19110 Halofuginone TempostatinRU19110 RU-19110
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~20 mg/mL (~48.23 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2 mg/mL (4.82 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.0 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2 mg/mL (4.82 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.0mg/mL澄清的DMSO储备液加入到900μL 20%SBE-β-CD生理盐水中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 0.67 mg/mL (1.62 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT00064142 | COMPLETED | Drug: halofuginone hydrobromide Other: placebo Other: laboratory biomarker analysis Other: pharmacological study |
AIDS-related Kaposi Sarcoma Recurrent Kaposi Sarcoma |
National Cancer Institute (NCI) | 2003-05 | Phase 2 |
| NCT00027677 | COMPLETED | Drug: halofuginone hydrobromide | Unspecified Adult Solid Tumor, Protocol Specific |
European Organisation for Research and Treatment of Cancer - EORTC |
2001-08 | Phase 1 |
| NCT02525302 | TERMINATED | Drug: HT-100 | Duchenne Muscular Dystrophy | Akashi Therapeutics | 2015-05 | Phase 2 |
| NCT01847573 | TERMINATED | Drug: HT-100 | Duchenne Muscular Dystrophy | Processa Pharmaceuticals | 2013-05 | Phase 1 Phase 2 |
| NCT01978366 | TERMINATED | Drug: HT-100 | Duchenne Muscular Dystrophy | Processa Pharmaceuticals | 2013-10 | Phase 2 |
|
|