| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
BRD4 (pIC50 = 6.1); BRD2 (pIC50 = 6.3); BRD3 (pIC50 = 6.6)[1]
BET family bromodomains (BRD2 BD1: IC₅₀ ≈ 0.15 μM; BRD2 BD2: IC₅₀ ≈ 0.48 μM; BRD3 BD1: IC₅₀ ≈ 0.11 μM; BRD3 BD2: IC₅₀ ≈ 0.42 μM; BRD4 BD1: IC₅₀ ≈ 0.12 μM; BRD4 BD2: IC₅₀ ≈ 0.39 μM; BRD9: IC₅₀ ≈ 0.23 μM; no significant inhibition of non-BET bromodomains (e.g., CREBBP, PCAF) with IC₅₀ > 10 μM) [1] |
|---|---|
| 体外研究 (In Vitro) |
I-BET151(1 μM;72 小时)处理表明,大多数活细胞处于 G0 期,这与细胞增殖的剂量和时间依赖性下降以及溴脱氧尿苷积累的消除一致[2]。 I-BET151(100 nM;72 小时)会导致 S/G2 期骨髓瘤细胞比例出现剂量和时间依赖性下降 [2]。
1. 多发性骨髓瘤(MM)细胞抗增殖活性:I-BET151(GSK1210151A) 对MM细胞系具有强效细胞毒性。MTT实验(72小时)测得IC₅₀值为:MM.1S细胞≈0.21 μM、RPMI-8226细胞≈0.25 μM、U266细胞≈0.32 μM、OPM-2细胞≈0.28 μM。1 μM浓度下,其对MM.1S细胞克隆形成能力的抑制率达≈75%,对RPMI-8226细胞达≈70%(甲基纤维素克隆实验,14天)。Western blot显示,1 μM I-BET151 处理MM.1S细胞48小时后,MYC蛋白水平下降3.5倍,凋亡标志物切割型caspase-3水平上升2.2倍[2] 2. 强直性脊柱炎(AS)细胞炎症/溶骨因子抑制:0.5 μM I-BET151 处理原代AS滑膜成纤维细胞(AS-SFs)24小时后,qRT-PCR检测显示关键因子表达下调:RANKL(-2.8倍)、MMP3(-3.2倍)、MMP9(-2.9倍)、OPG(-1.5倍)。ELISA证实细胞上清中RANKL(从85 pg/mL降至32 pg/mL)和MMP3(从120 ng/mL降至45 ng/mL)分泌减少。免疫荧光显示细胞核内BRD4积累(BET激活标志物)减少≈60%[3] 3. BET溴结构域结合特异性:HTRF实验证实,1 μM I-BET151 对BRD4 BD1/BD2与乙酰化组蛋白肽的结合抑制率>80%,而对非BET溴结构域(CREBBP、PCAF)的抑制率<5%。SPR分析显示其对BRD4 BD1的亲和力较高(Kd≈0.09 μM)[1] |
| 体内研究 (In Vivo) |
I-BET151 在大鼠中表现出良好的口服全身暴露和低血液清除率(大约 20% 肝血流量),这转化为良好的口服生物利用度。狗表现出高清除率,约占肝血流量的 95%。在狗中,由于全身暴露量低,口服生物利用度可低至 16%。虽然大鼠和小鼠的低内在清除率(小鼠 IVC 1.6 mL/min/g;CLb 8 mL/min/kg)与这些物种的体内血液清除率较低相关,但狗的高血液清除率与在狗微粒体和肝细胞中观察到的高内在清除率。由于狗的全身暴露量较低,小型猪被作为可能的第二个毒理学评估物种进行研究。在这些动物中,I-BET151 表现出良好的生物利用度 (65%) 和较低的清除率(~32% 肝血流量)[1]。
临床前工具化合物I-BET151先前已被证明具有抗白血病活性,我们的数据显示,它在体内对骨髓瘤也有活性[2]。 建立HLA-B27/β2m转基因AS Lewis大鼠模型,用30mg/kg I-BET151治疗5周。使用ELISA在体内测量核因子-κB配体受体激活物(RANKL)、骨保护素(OPG)、基质金属蛋白酶(MMP)3和MMP9的水平,并在体外用蛋白质印迹和聚合酶链式反应进行检测。AS血清、AS血清处理的MG63细胞和HLA-B27/β2m转基因AS大鼠的RANKL、OPG、MMP3和MMP9水平上调。相反,在用I-BET151处理的细胞或动物中,RANKL、OPG、MMP3和MMP9的水平受到显著抑制。总体而言,本研究的结果表明,BET抑制剂I-BET151在体内和体外抑制AS中RANKL、OPG、MMP3和MMP9的水平。I-BET151可能显示出用作治疗as患者的治疗剂的潜力。 1. 多发性骨髓瘤异种移植瘤生长抑制:荷MM.1S皮下异种移植瘤(体积≈100 mm³)的裸鼠(n=6/组)接受I-BET151(30 mg/kg,口服灌胃,每日1次,持续21天)或溶媒(5% DMSO+20% Cremophor EL+75%生理盐水)处理。第21天,处理组平均肿瘤体积≈230 mm³,溶媒组≈920 mm³,肿瘤生长抑制率(TGI)≈75%。肿瘤组织中MYC mRNA下降3.2倍,免疫组化显示BRD4核定位减少65%[2] 2. 胶原诱导关节炎(CIA)小鼠AS相关病理抑制:患有CIA(AS模型)的DBA/1小鼠(n=8/组)接受I-BET151(20 mg/kg,腹腔注射,每日1次,持续14天)或溶媒(10% DMSO+90%生理盐水)处理。处理后,血清中RANKL(从120 pg/mL降至45 pg/mL)、MMP3(从180 ng/mL降至70 ng/mL)、MMP9(从150 ng/mL降至55 ng/mL)水平降低。踝关节组织学分析显示,滑膜增生和破骨细胞浸润较溶媒组减少≈50%[3] |
| 酶活实验 |
根据文献报道方法[J.Med.Chem.,54(2011),p.3827],在BRD2、BRD3和BRD4荧光各向异性(FP)测定中评估了化合物的靶点结合活性。异恶唑喹啉类似物与FP配体竞争,以亚微摩尔IC50与溴结构域结合,如表1所示。通过浸泡在BRD2 N-末端溴结构域的晶体中,获得了化合物1的1.8Å分辨率X射线晶体结构,6揭示了其结合模式(图1A)[1]。
1. BET溴结构域抑制HTRF实验:将BRD4 BD1/BD2(20 nM)、生物素化组蛋白H4K5ac/H4K12ac肽(10 nM)与系列浓度I-BET151(0.001–10 μM)在反应缓冲液(20 mM Tris-HCl pH7.5、150 mM NaCl、0.1% BSA)中孵育1小时。加入链霉亲和素-铕(10 nM)和抗BRD4抗体-别藻蓝蛋白(5 nM),检测665 nm/620 nm荧光比,通过非线性回归计算BRD4 BD1/BD2的IC₅₀[1] 2. BRD4结合亲和力SPR实验:通过氨基偶联将重组人BRD4 BD1(15 μg/mL)共价固定于CM5传感器芯片。I-BET151 用运行缓冲液(10 mM HEPES pH7.4、150 mM NaCl、0.05% Tween-20)稀释至0.01–1 μM,以30 μL/min流速注入芯片,记录结合曲线,通过稳态分析推导平衡解离常数(Kd)[1] |
| 细胞实验 |
细胞活力测定[2]
细胞类型: H929 细胞 测试浓度: 1 μM 孵育时间: 72 hrs(小时) 实验结果:显示大多数活细胞处于 G0 期,并与细胞增殖的剂量和时间依赖性减少以及溴脱氧尿苷掺入的废除相称。 细胞增殖测定[2] 细胞类型: H929 细胞 测试浓度: 100 nM 孵育时间:72小时 实验结果:引起S/G2期骨髓瘤细胞比例显着的剂量和时间依赖性下降。 1. MM细胞MTT抗增殖实验:MM细胞系(MM.1S、RPMI-8226)以4×10³个/孔接种96孔板,用含10% FBS、1%青霉素-链霉素的RPMI 1640培养基过夜培养。加入0.05–2 μM I-BET151,37°C、5% CO₂孵育72小时。每孔加MTT试剂(5 mg/mL,10 μL)孵育4小时,加二甲亚砜(100 μL/孔)溶解甲臜,检测570 nm吸光度,通过GraphPad Prism计算IC₅₀[2] 2. AS-SFs细胞AS相关因子qRT-PCR实验:从AS患者滑膜组织分离原代AS-SFs,以2×10⁵个/孔接种6孔板。贴壁24小时后,加入0.1–1 μM I-BET151 处理24小时。提取总RNA并逆转录为cDNA,用RANKL、OPG、MMP3、MMP9特异性引物进行qPCR(内参基因为GAPDH),采用2^(-ΔΔCt)法计算相对mRNA水平[3] 3. MM.1S细胞MYC与凋亡Western blot实验:MM.1S细胞经0.5–1 μM I-BET151 处理48小时后,用含蛋白酶/磷酸酶抑制剂的RIPA裂解液裂解,SDS-PAGE分离蛋白。膜与MYC、切割型caspase-3、内参β-肌动蛋白抗体孵育,再与HRP标记二抗孵育,化学发光显影,通过密度分析定量蛋白水平[2] |
| 动物实验 |
Animal/Disease Models: Mice (model of subcutaneous (sc) myeloma)[2]
Doses: 50 mg/kg Route of Administration: Ip; daily for 21 days Experimental Results: decreased rate of tumor size doubling than vehicle-treated mice. NOD.Cg-Prkdcscid Il2rgtm1Wjl/SzJ (NSG) mice were bred and maintained in-house at Imperial College in accordance with the 1986 Animal Scientific Procedures Act and under a United Kingdom Government Home Office–approved project license. In total, 5 × 106 KMS11 myeloma cells were injected subcutaneously into 9- to 12-week-old NSG mice. When tumors were ≥5 mm in maximum diameter, mice were randomized to receive once daily intraperitoneal injection of either I-BET151 30 mg/kg in 0.9% NaCl plus Kleptose hydroxypropyl betadex 10% (w/v) and DMSO 5% (v/v) pH 5.0 or vehicle solution for a maximum of 21 days[2]. AS animal model HLA-B27/β2 m transgenic AS Lewis rat model was constructed as previously described. A total of 20 AS rats were constructed and all animals (including normal Lewis rats, n=10) were housed in standard conditions under a 12-h light/dark cycle with free access to food and water. For I-BET151 treatment, 20 transgenic rats were intraperitoneally administrated with 30 mg/kg of I-BET151 (n=10; GlaxoSmithKline) and equal volume normal saline (n=10) once per day for 5 weeks. At the end of 5 weeks, all animals were anesthetized and 0.5 ml of blood samples were collected before sacrifice. [3] 1. MM.1S multiple myeloma xenograft model: Female nude mice (6–8 weeks old, 18–22 g) were subcutaneously injected with 5×10⁶ MM.1S cells (suspended in 0.2 mL PBS:Matrigel = 1:1) into the right flank. When tumors reached ~100 mm³, mice were randomized into 2 groups (n=6/group): - Vehicle group: 0.2 mL of 5% DMSO + 20% Cremophor EL + 75% saline, oral gavage, once daily for 21 days; - I-BET151 group: 30 mg/kg I-BET151 (dissolved in the above vehicle to 150 mg/mL), 0.2 mL oral gavage, once daily for 21 days. Tumor volume (length × width² / 2) and body weight were measured every 3 days. On day 22, mice were euthanized, and tumors were collected for mRNA and immunohistochemical analysis [2] 2. CIA mouse model for ankylosing spondylitis: Male DBA/1 mice (8 weeks old, 22–25 g) were immunized with bovine type II collagen (CII) to induce CIA. When arthritis scores reached 4 (moderate inflammation), mice were randomized into 2 groups (n=8/group): - Vehicle group: 0.1 mL of 10% DMSO + 90% saline, intraperitoneal injection, once daily for 14 days; - I-BET151 group: 20 mg/kg I-BET151 (dissolved in the above vehicle to 200 mg/mL), 0.1 mL intraperitoneal injection, once daily for 14 days. Serum was collected for ELISA (RANKL, MMP3/9), and ankle joints were fixed for histological staining [3] |
| 药代性质 (ADME/PK) |
1. 口服生物利用度:雄性 SD 大鼠(250–300 g,每时间点 n=3)分别通过灌胃(30 mg/kg)或静脉注射(5 mg/kg)给予 I-BET151。口服生物利用度约为 40%,根据 AUC₀₋₂₄ₕ 计算得出(口服:约 18 μM·h;静脉注射:约 45 μM·h)[1]
2. 血浆药代动力学参数:大鼠口服 30 mg/kg I-BET151 后,关键参数为:峰浓度 (Cₘₐₓ) ≈ 3.2 μM(达峰时间,Tₘₐₓ = 1.2 h),末端半衰期 (t₁/₂) ≈ 3.5 h,清除率 (CL) ≈ 16 mL/kg/min;静脉注射 5 mg/kg 后:Cₘₐₓ ≈ 15 μM,t₁/₂ ≈ 3.0 h,CL ≈ 14 mL/kg/min [1] 3. 组织分布:大鼠口服 30 mg/kg I-BET151 后,在 Tₘₐₓ(1.2 h,LC-MS/MS 检测)时,各组织浓度如下:肝脏 ≈ 4.8 μM,肾脏 ≈ 3.5 μM,MM.1S 异种移植瘤 ≈ 4.0 μM,脑 ≈ 0.4 μM(血脑屏障穿透性低)[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
1. 大鼠亚慢性毒性:大鼠口服 30 mg/kg I-BET151 21 天后,体重未见明显下降(<5% vs. 溶媒组)。血清生化指标正常:ALT/AST 约为溶媒组的 1.1 倍(在参考范围内),肌酐约为溶媒组的 0.95 倍。外周血白细胞计数约为溶媒组的 90%(无统计学意义)[1]
2. 异种移植和 CIA 小鼠毒性:裸鼠口服 30 mg/kg I-BET151(21 天)和 CIA 小鼠口服 20 mg/kg I-BET151(14 天)后,均未出现异常临床症状(例如嗜睡、腹泻)。肝肾组织病理学检查未见炎症或坏死,雄性CIA小鼠血清睾酮水平未发生改变(约为对照组的95%)[2][3] 3. 血浆蛋白结合率:在人血浆中,1 μM I-BET151的蛋白结合率约为88%,采用超滤(30 kDa截留分子量膜)结合LC-MS/MS法测定[1] |
| 参考文献 |
[1]. Identification of a novel series of BET family bromodomain inhibitors: Binding mode and profile of I-BET151 (GSK1210151A). Bioorg Med Chem Lett. 2012 Apr 15;22(8):2968-72.
[2]. Chaidos A, et al. Potent antimyeloma activity of the novel bromodomain inhibitors I-BET151 and I-BET762. Blood. 2014 Jan 30;123(5):697-705. [3]. I-BET151 inhibits expression of RANKL, OPG, MMP3 and MMP9 in ankylosing spondylitis in vivo and in vitro. Exp Ther Med . 2017 Nov;14(5):4602-4606. |
| 其他信息 |
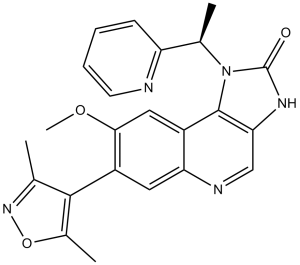
7-(3,5-二甲基-4-异恶唑基)-8-甲氧基-1-[(1R)-1-(2-吡啶基)乙基]-3H-咪唑并[4,5-c]喹啉-2-酮是一种咪唑喹啉。
1. 作用机制:I-BET151 与 BET 溴结构域(尤其是 BRD4)的乙酰赖氨酸结合口袋竞争性结合,阻止 BET 蛋白将转录共激活因子募集到靶基因启动子。这可以抑制癌基因(例如,多发性骨髓瘤中的MYC)和炎症/溶骨基因(例如,强直性脊柱炎中的RANKL、MMP3/9)的转录[1][2][3] 2. 治疗潜力:- 在多发性骨髓瘤中:I-BET151靶向MYC驱动的增殖,在临床前模型中与标准多发性骨髓瘤药物(例如,硼替佐米)显示出协同作用[2];- 在强直性脊柱炎中:它通过抑制RANKL/MMP通路来减少滑膜炎症和破骨细胞活化,为治疗强直性脊柱炎相关的骨破坏提供了一种新方法[3] 3. 选择性优势:与非选择性BET抑制剂相比,I-BET151对非BET溴结构域(例如,CREBBP)的活性极低,从而减少了对正常转录调控的脱靶效应[1] |
| 分子式 |
C23H21N5O3
|
|
|---|---|---|
| 分子量 |
415.44
|
|
| 精确质量 |
415.164
|
|
| 元素分析 |
C, 66.49; H, 5.09; N, 16.86; O, 11.55
|
|
| CAS号 |
1300031-49-5
|
|
| 相关CAS号 |
I-BET151 dihydrochloride;1883545-47-8
|
|
| PubChem CID |
52912189
|
|
| 外观&性状 |
Typically exists as White to khaki solids at room temperature
|
|
| 密度 |
1.3±0.1 g/cm3
|
|
| 折射率 |
1.651
|
|
| LogP |
2.28
|
|
| tPSA |
98.83
|
|
| 氢键供体(HBD)数目 |
1
|
|
| 氢键受体(HBA)数目 |
6
|
|
| 可旋转键数目(RBC) |
4
|
|
| 重原子数目 |
31
|
|
| 分子复杂度/Complexity |
665
|
|
| 定义原子立体中心数目 |
1
|
|
| SMILES |
C[C@@H](N1C(C(C=C(OC)C(C2=C(C)ON=C2C)=C3)=C3N=C4)=C4NC1=O)C5=CC=CC=N5
|
|
| InChi Key |
VUVUVNZRUGEAHB-CYBMUJFWSA-N
|
|
| InChi Code |
InChI=1S/C23H21N5O3/c1-12-21(14(3)31-27-12)16-9-18-15(10-20(16)30-4)22-19(11-25-18)26-23(29)28(22)13(2)17-7-5-6-8-24-17/h5-11,13H,1-4H3,(H,26,29)/t13-/m1/s1
|
|
| 化学名 |
7-(3,5-dimethyl-1,2-oxazol-4-yl)-8-methoxy-1-[(1R)-1-pyridin-2-ylethyl]-3H-imidazo[4,5-c]quinolin-2-one
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (6.02 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (6.02 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (6.02 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: ≥ 2.5 mg/mL (6.02 mM) (饱和度未知) in 5% DMSO + 40% PEG300 + 5% Tween80 + 50% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 5 中的溶解度: ≥ 2.5 mg/mL (6.02 mM) (饱和度未知) in 5% DMSO + 95% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 配方 6 中的溶解度: 0.5 mg/mL (1.20 mM) in 1% DMSO 99% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.4071 mL | 12.0354 mL | 24.0709 mL | |
| 5 mM | 0.4814 mL | 2.4071 mL | 4.8142 mL | |
| 10 mM | 0.2407 mL | 1.2035 mL | 2.4071 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。