| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| 2g |
|
||
| Other Sizes |
|
| 靶点 |
Icariin inhibits phosphodiesterase-5 (PDE5) with IC₅₀ = 0.432 μM and phosphodiesterase-4 (PDE4) with IC₅₀ = 73.50 μM. [1]
Icariin activates peroxisome proliferator-activated receptor alpha (PPARα). [2] |
|---|---|
| 体外研究 (In Vitro) |
淫羊藿苷是一种 cGMP 特异性 PDE5 抑制剂。使用 3 H-cGMP 和 3 H-cAMP 的两步放射性同位素方法检查淫羊藿苷对 PDE5 和 PDE4 活性的抑制作用。淫羊藿苷对PDE5的选择性功效是其167.67倍(PDE4/PDE5的IC50)[1]。在这项工作中,评估了细胞活力,以确定淫羊藿苷是否可以保护内皮 HUVEC 免受氧化低密度脂蛋白 (ox-LDL) 造成的损伤。与对照组相比,暴露于ox-LDL 24小时后,细胞的活力显着降低(P<0.05)。另一方面,与ox-LDL模拟组相比,淫羊藿苷能够以浓度依赖性方式显着(P<0.05)减少ox-LDL引起的细胞损伤[3]。淫羊藿苷通过 MAPK 信号通路抑制 ER 介导的(ER 应激)自噬,从而保护 BMSC 免受 OGD 诱导的细胞凋亡[4]。
PDE5 和 PDE4 酶活性:淫羊藿苷在体外对 cGMP 特异性 PDE5 和 cAMP 特异性 PDE4 活性有抑制作用,这可能与其调节环核苷酸水平的潜在作用有关。然而,给定文献中未报道如 IC50 等具体的抑制动力学参数。[1] 脂质代谢基因表达:在细胞模型中,淫羊藿苷激活 PPARα,导致脂质代谢基因表达上调。这一激活作用通过脂质代谢途径中相关基因 mRNA 水平的升高得以证明,表明其在脂质代谢调节中的作用。[2] 动脉粥样硬化相关效应:体外研究表明,淫羊藿苷可影响与动脉粥样硬化相关的过程。在动脉粥样硬化发展的背景下,它可能作用于与炎症、脂质代谢和细胞黏附相关的细胞功能,尽管所提供文献中未充分阐述确切的分子机制和详细的细胞反应。[3] 生殖功能相关细胞效应:在与雄性生殖功能相关的细胞中对淫羊藿苷进行了研究。它可能对诸如精子相关的细胞功能有影响,潜在地影响如精子发生和精子功能等过程,但给定文献中未详细说明具体的细胞和分子变化。[4] 细胞凋亡保护:在氧糖剥夺(OGD)条件下的兔骨髓间充质干细胞(BMSCs)中,淫羊藿苷保护细胞免受凋亡。它通过 MAPK 信号通路抑制内质网(ER)介导的自噬。可能通过蛋白质免疫印迹(Western blot)分析检测自噬相关蛋白(如 LC3 - II/I 比值)以及 MAPK 信号通路相关蛋白(磷酸化和总形式的 MAPK 蛋白)的水平,通过聚合酶链式反应(PCR)检测相关基因的 mRNA 水平。[5] |
| 体内研究 (In Vivo) |
Icariin 是一种 PPARα 激活剂,还可促进 Cyp4a10 和 Cyp4a14。它还调节参与脂质代谢的蛋白质和酶的 mRNA 水平,例如过氧化物酶体和线粒体中的脂肪酸结合蛋白和脂肪酸氧化。淫羊藿苷是治疗高脂血症的有用药物。研究淫羊藿苷对 PPARα 及其靶基因的影响有助于了解它如何影响脂质代谢。连续五天,给小鼠口服安妥明 (500 mg/kg) 或淫羊藿苷 (100、200、400 和 mg/kg)。提取肝脏总RNA后,分析脂质代谢相关基因和PPARα的表达。淫羊藿苷和氯贝特分别诱导 PPARα 及其标记基因 Cyp4a10 和 Cyp4a14 2-4 倍和 4-8 倍。脂肪酸 (FA) 结合蛋白和共激活蛋白 Fabp1、Fabp4 和 Acsl1 增加了两倍。线粒体 FA β-氧化酶(Cpt1a、Acat1、Acad1 和 Hmgcs2)的 mRNA 增加了 2-3 倍。淫羊藿苷和氯贝丁酯还可提高近端 β-氧化酶(Acox1、Ech1 和 Ehhadh)的 mRNA。淫羊藿苷对 FA 合成酶 (Fasn) 或甾醇调节元件结合因子 1 (Srebf1) 的 mRNA 表达没有影响。淫羊藿苷和氯贝丁酯刺激脂质裂解基因 Lipe 和 Pnpla2[2]。成年大鼠以 0(对照)、50、100 或 200 mg/kg 体重的剂量连续 35 天口服淫羊藿苷。研究结果表明,淫羊藿苷对睾丸或附睾的体重或器官系数基本上没有影响。另一方面,100 mg/kg 淫羊藿苷可显着增加附睾精子数量。此外,剂量为 50 和 100 mg/kg 的淫羊藿苷可显着提高睾酮水平。此外,给予 100 mg/kg 淫羊藿苷会影响支持细胞中的卵泡刺激素受体 (FSHR) 和claudin-11 mRNA 表达。该测试评估丙二醛 (MDA) 水平和超氧化物歧化酶 (SOD) 活性;用 50 和 100 mg/kg 淫羊藿苷处理可增加抗氧化能力,但用 200 mg/kg 淫羊藿苷处理会增加氧化应激[4]。
脂质代谢基因表达:在小鼠体内,淫羊藿苷激活 PPARα,诱导脂质代谢基因表达。通过分析用淫羊藿苷处理的小鼠肝脏或脂肪组织中相关基因的 mRNA 水平得以证实。PPARα 的激活及随后的基因表达变化可能有助于体内脂质代谢的调节。[2] 动脉粥样硬化相关效应:在与动脉粥样硬化相关的动物模型中,淫羊藿苷在减少动脉粥样硬化病变方面有效果。它可能通过如抗炎、改善血脂谱和调节血管细胞功能等机制发挥作用。然而,给定文献中未完整描述关于病变大小、血脂水平和细胞功能变化的具体深入机制和详细实验数据。[3] 雄性大鼠生殖功能:在雄性大鼠中,淫羊藿苷对生殖功能有影响。它可能影响诸如精子质量(数量、活力、形态)以及与雄性生殖相关的激素水平等参数。但所提供文献中未全面报道确切的实验数据和详细机制。[4] |
| 酶活实验 |
PDE5 和 PDE4 活性测定:为测量淫羊藿苷对 cGMP 特异性 PDE5 和 cAMP 特异性 PDE4 活性的影响,可能进行了体外酶活性实验。反应体系包含纯化的 PDE5 或 PDE4 酶、它们各自的底物(PDE5 的 cGMP 和 PDE4 的 cAMP)以及不同浓度的淫羊藿苷。孵育适当时间后,使用如高效液相色谱(HPLC)或比色法等方法检测剩余底物水平或产物生成量(如 PDE5 水解 cGMP 产生的 GMP 或 PDE4 水解 cAMP 产生的 AMP),以评估淫羊藿苷对酶活性的抑制作用。[1]
|
| 细胞实验 |
PPARα 激活实验:转染 PPARα 响应荧光素酶报告基因的 HepG2 细胞经淫羊藿苷 (0.1-100 μM) 处理 24 小时。检测荧光素酶活性评估转录激活作用。通过 qRT-PCR 分析 CPT1A/ACOX1 的 mRNA 表达。 [2]
BMSC 凋亡/自噬实验:兔 BMSCs 在氧糖剥夺 (OGD) 条件下处理 6 小时(含/不含 0.1-10 μM 淫羊藿苷)。通过 Annexin V-FITC/PI 流式细胞术检测凋亡。通过 Western blot 分析自噬标志物 (LC3-II, Beclin-1, p62) 及 MAPK 磷酸化水平。 [5] |
| 动物实验 |
Mice: Adult 8-week old male C57BL/6 mice are acclimated for 1-week in a temperature- and humidity-controlled facility with a standard 12-h light schedule. Mice have free access to SPF-grade rodent chow and purified drinking water. Mice are treated with Icariin (100, 200, and 400 mg/kg) for 5 days. Clofibrate (CLO, 500 mg/kg, po for 5 days) is used as a positive control, for negative controls, mice are given 2% CMC (10 mL/kg). 24 h after the last dose, livers are collected for analysis.
Rats: Forty adult male SD rats weighing 200-290 g (12-16 weeks old) are randomly assigned to groups (n=10 per group) according to their body weight. The rats receive daily intragastric administration of Icariin at 0 (control), 50, 100, or 200 mg/kg per day for 35 consecutive days. The animals are weighed weekly, and the treatments are adjusted accordingly. At the end of the Icariin treatment period, all rats are sacrificed; blood samples are subsequently collected for further analyses of testosterone levels. Lipid metabolism study in mice: Mice were randomly divided into different groups, including a control group and Icariin - treated groups. Icariin was dissolved in an appropriate vehicle (such as dimethyl sulfoxide - saline solution). The mice in the treatment groups were administered Icariin via oral gavage at specific doses (e.g., 10 - 50 mg/kg body weight) once a day for a certain period (e.g., 4 - 8 weeks). At the end of the treatment, the mice were sacrificed, and liver and adipose tissues were collected for further analysis of lipid metabolic gene expression. [2] Atherosclerosis - related animal study: Animal models of atherosclerosis (such as ApoE - knockout mice or rabbits fed a high - fat diet) were used. The animals were randomly divided into groups. Icariin was formulated into a suitable dosage form (such as a suspension in carboxymethylcellulose sodium solution). The treatment groups received Icariin via oral gavage or intraperitoneal injection at appropriate doses (e.g., 20 - 100 mg/kg body weight) for a specific duration (e.g., 8 - 12 weeks). The control groups received the vehicle only. At the end of the experiment, atherosclerotic lesions in the aorta or other relevant blood vessels were examined by histological staining, and blood lipid profiles were measured. [3] Male reproductive function study in rats: Male rats were randomly grouped. Icariin was dissolved in a proper solvent (such as ethanol - saline mixture). The treatment groups were given Icariin via oral gavage at different doses (e.g., 10 - 30 mg/kg body weight) once a day for a specific period (e.g., 6 - 10 weeks). At the end of the treatment, the rats were sacrificed, and reproductive organs (such as testes and epididymis) were collected. Sperm parameters (count, motility, morphology) were analyzed, and hormonal levels (such as testosterone) in the blood were measured. [4] |
| 毒性/毒理 (Toxicokinetics/TK) |
雄性大鼠连续28天灌胃给予淫羊藿苷(剂量分别为50、100或200 mg/kg/天)后,未观察到毒性反应。[4]
|
| 参考文献 | |
| 其他信息 |
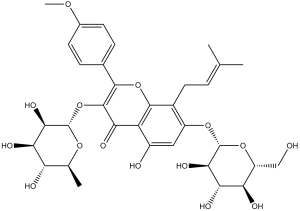
高脂血症模型:喂食高脂饮食的小鼠每日灌胃给予溶于生理盐水的淫羊藿苷(50 mg/kg),持续4周。收集血清和肝组织进行分析。[2]动脉粥样硬化模型:喂食1%胆固醇饮食的兔子每日灌胃给予溶于生理盐水的淫羊藿苷(30 mg/kg),持续12周。对主动脉病变进行组织学分析;测定血脂。[3]生殖功能模型:雄性大鼠每日灌胃给予溶于生理盐水的淫羊藿苷(50/100/200 mg/kg),持续28天。分析附睾精子参数和血清睾酮水平。 [4]淫羊藿苷属于黄酮醇类化合物,其结构为山奈酚,在8位被3-甲基丁-2-烯-1-基取代,3、4'和7位的羟基分别转化为相应的6-脱氧-α-L-甘露吡喃糖苷、甲基醚和β-D-葡萄糖吡喃糖苷。淫羊藿苷是一种磷酸二酯酶-5抑制剂,提取自淫羊藿属的多种植物,被认为是中药淫羊藿的主要活性成分。它具有维持骨密度、作为植物雌激素、EC 3.1.4.35(3',5'-环磷酸鸟苷磷酸二酯酶)抑制剂和抗氧化剂的作用。它是一种糖基氧基黄酮,属于黄酮醇类化合物。
淫羊藿苷已被用于研究其在人体内的药代动力学特征。 据报道,淫羊藿苷存在于短角淫羊藿、截形淫羊藿以及其他有相关数据的生物体中。 |
| 分子式 |
C33H40O15
|
|
|---|---|---|
| 分子量 |
676.66
|
|
| 精确质量 |
676.236
|
|
| 元素分析 |
C, 58.58; H, 5.96; O, 35.47
|
|
| CAS号 |
489-32-7
|
|
| 相关CAS号 |
|
|
| PubChem CID |
5318997
|
|
| 外观&性状 |
Light yellow to yellow solid powder
|
|
| 密度 |
1.6±0.1 g/cm3
|
|
| 沸点 |
948.5±65.0 °C at 760 mmHg
|
|
| 熔点 |
223-225ºC
|
|
| 闪点 |
300.9±27.8 °C
|
|
| 蒸汽压 |
0.0±0.3 mmHg at 25°C
|
|
| 折射率 |
1.679
|
|
| LogP |
2.48
|
|
| tPSA |
238.2
|
|
| 氢键供体(HBD)数目 |
8
|
|
| 氢键受体(HBA)数目 |
15
|
|
| 可旋转键数目(RBC) |
9
|
|
| 重原子数目 |
48
|
|
| 分子复杂度/Complexity |
1170
|
|
| 定义原子立体中心数目 |
10
|
|
| SMILES |
C[C@H]1[C@@H]([C@H]([C@H]([C@@H](O1)OC2=C(OC3=C(C2=O)C(=CC(=C3CC=C(C)C)O[C@H]4[C@@H]([C@H]([C@@H]([C@H](O4)CO)O)O)O)O)C5=CC=C(C=C5)OC)O)O)O
|
|
| InChi Key |
TZJALUIVHRYQQB-XLRXWWTNSA-N
|
|
| InChi Code |
InChI=1S/C33H40O15/c1-13(2)5-10-17-19(45-33-28(42)26(40)23(37)20(12-34)46-33)11-18(35)21-24(38)31(48-32-27(41)25(39)22(36)14(3)44-32)29(47-30(17)21)15-6-8-16(43-4)9-7-15/h5-9,11,14,20,22-23,25-28,32-37,39-42H,10,12H2,1-4H3/t14-,20+,22-,23+,25+,26-,27+,28+,32-,33+/m0/s1
|
|
| 化学名 |
5-hydroxy-2-(4-methoxyphenyl)-8-(3-methylbut-2-en-1-yl)-7-(((2S,3R,4S,5S,6R)-3,4,5-trihydroxy-6-(hydroxymethyl)tetrahydro-2H-pyran-2-yl)oxy)-3-(((2S,3R,4R,5R,6S)-3,4,5-trihydroxy-6-methyltetrahydro-2H-pyran-2-yl)oxy)-4H-chromen-4-one
|
|
| 别名 |
Icariin; 489-32-7; Ieariline; CHEBI:78420; VNM47R2QSQ; Epimedii herba icariin; 5-hydroxy-2-(4-methoxyphenyl)-8-(3-methylbut-2-enyl)-7-[(2S,3R,4S,5S,6R)-3,4,5-trihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-3-[(2S,3R,4R,5R,6S)-3,4,5-trihydroxy-6-methyloxan-2-yl]oxychromen-4-one; 3-((6-Deoxymannopyranosyl)oxy)-7-(glucopyranosyloxy)-5-hydroxy-2-(4-methoxyphenyl)-8-(3-methyl-2-butenyl)-4H-1-benzopyran-4-one;
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (3.69 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL 澄清 DMSO 储备液加入900 μL 玉米油中,混合均匀。 配方 2 中的溶解度: ≥ 2.08 mg/mL (3.07 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL澄清的DMSO储备液加入到400 μL PEG300中,混匀;再向上述溶液中加入50 μL Tween-80,混匀;然后加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 View More
配方 3 中的溶解度: 2.08 mg/mL (3.07 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 配方 4 中的溶解度: 10 mg/mL (14.78 mM) in 50% PEG300 50% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 5 中的溶解度: 10 mg/mL (14.78 mM) in 0.5% CMC/saline water (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.4778 mL | 7.3892 mL | 14.7785 mL | |
| 5 mM | 0.2956 mL | 1.4778 mL | 2.9557 mL | |
| 10 mM | 0.1478 mL | 0.7389 mL | 1.4778 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT02112123 | Completed | Drug: Icariin Dietary Supplement: Matching placebo |
the Pharmacokinetic Profile of Icariin in Humans |
University of Texas Southwestern Medical Center |
April 2014 | Phase 1 |
| NCT01979133 | Completed Has Results | Drug: Icariin | Bipolar Disorder Substance Use Disorder |
University of Texas Southwestern Medical Center |
October 2013 | Phase 3 |
| NCT05903456 | Not yet recruiting | Procedure: TACE(transcatheter arterial chemoembolization) |
Hepatocellular Carcinoma | Zhejiang Cancer Hospital | July 2023 | Phase 2 |
|
|
|