| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
FGFR1 (IC50 = 0.9 nM); FGFR2 (IC50 = 1.4 nM); FGFR3 (IC50 = 1 nM); FGFR4 (IC50 = 60 nM)
Infigratinib phosphate suppresses FGFR1, FGFR2, and FGFR3 at IC50 values of ~1 nM, FGFR3K650E at IC50 values of 4.9 nM, and FGFR4 at IC50 values of 60 nM. With the exception of VEGFR2, KIT, and LYN, which are inhibited at submicromolar concentrations (IC50=0.18, 0.75, and 0.3 μM, respectively), the IC50 values for all other kinases fall within the μM range (FYN, LCK, YES, and ABL, IC50=1.9, 2.5, 1.1, and 2.3 μM, respectively). With IC50 values in the low nanomolar range, infigratinib inhibits the proliferation of the FGFR1-, FGFR2-, and FGFR3-dependent BaF3 cells in a manner similar to that seen in the enzymatic assay for the inhibition of receptor kinase activity. Except for VEGFR2 (IC50 1449 and 938 nM), which has at least a 400-fold selectivity versus FGFR1, FGFR2, and FGFR3, all IC50 values for the remaining cells are greater than 1.5 μM[1]. The growth of FGFR2-mutant endometrial cancer cells is effectively inhibited by infigratinib (at concentrations between 1 nM and 10 μM)[2]. |
|---|---|
| 体外研究 (In Vitro) |
体外活性:BGJ398 还可以抑制 VEGFR2,但效力较低。 BGJ398 抑制 VEGFR2 的 IC50 为 0.18 μM。 BGJ398 抑制其他激酶,包括 ABL、FYN、KIT、LCK、LYN 和 YES,IC50 分别为 2.3 μM、1.9 μM、0.75 μM、2.5 μM、0.3 μM 和 1.1 μM。在细胞水平上,BGJ398 抑制 FGFR1-、FGFR2-Q 和 FGFR3 依赖性 BaF3 细胞的增殖,IC50 分别为 2.9 μM、2.0 μM 和 2 μM。 BGJ398 干扰特定酪氨酸残基的自磷酸化,包括 FGFR-WT、FGFR2-WT、FGFR3-K650E、FGFR3-S249C 和 FGFR4-WT,IC50 分别为 4.6 nM、4.9 nM、5 nM、5 nM 和 168 nM。 BGJ398 抑制野生型 (WT) FGFR3 过表达的癌细胞(例如 RT112、RT4、SW780 和 JMSU1)的增殖,IC50 分别为 5 nM、30 nM、32 nM 和 15 nM。激酶测定:在放射性标记的 ATP 存在下,通过测量纯化的 GST 融合 FGFR3-K650E 激酶结构域对合成底物的磷酸化来评估酶促激酶活性。通过将 10 μL 3 倍浓缩的 BGJ398 溶液或对照与 10 μL 相应底物混合物(肽底物、ATP 和 [γ33P]ATP)混合来测量酶活性。通过添加 10 μL 3 倍浓缩的酶溶液(在测定缓冲液中)来启动反应。测定组分的最终浓度如下:10 ng GST-FGFR3-K650E、20 mM Tris-HCl、pH 7.5、3 mM MnCl2、3 mM MgCl2、1 mM DTT、250 μg/mL PEG 20000、2 μg /mL 聚 (EY) 4:1、1% DMSO 和 0.5 μM ATP (γ-[33P]-ATP 0.1 μCi)。根据过滤结合 (FB) 方法,在 96 孔板中在室温下进行 10 分钟,最终体积为 30 μL,包括 BGJ398。通过添加 20 μL 125 mM EDTA 来终止酶反应,并按如下方式对 33P 掺入多肽底物进行定量:将 30 μL 停止的反应混合物转移到之前用 125 mM EDTA 浸泡 5 分钟的 Immobilon-PVDF 膜上。甲醇,用水冲洗,用 0.5% H3PO4 浸泡 5 分钟,然后安装在断开真空源的真空歧管上。点样后,连接真空,并用 0.5% H3PO4 (200 μL) 冲洗每个孔。除去游离膜并在摇床上用 1% H3PO4 抛光四次,用乙醇抛光一次。将膜干燥并添加 10 μL/孔的闪烁液覆盖。最终将板密封并在微板闪烁计数器中计数。 IC50值通过BGJ398的抑制百分比的线性回归分析来计算。细胞测定:鼠 BaF3 细胞系在补充有 10% FBS 的 RPMI-1640 培养基中培养,通过使用通过突变或与二聚化伙伴融合激活的酪氨酸激酶进行稳定转导,使其增殖和存活不依赖于 IL-3。 4.5 g/L 葡萄糖、1.5 g/L 碳酸氢钠和青霉素/链球菌。细胞每周传代两次。使用荧光素酶生物发光测定评估 BGJ398 介导的 BaF3 细胞增殖和活力的抑制。使用 μFill 液体分配器将指数生长的 BaF3 或 BaF3 Tel-TK 细胞以 50 μL/孔接种到 384 孔板(4250 个细胞/孔)中。 BGJ398 在 DMSO 中连续稀释并排列在聚丙烯 384 孔板中。然后使用 pintool 转移装置将 50 nL BGJ398 转移至含有细胞的板中,并将板在 37 °C (5% CO2) 下孵育 48 小时。然后添加 25 μL Bright-Glo,并使用 Analyst-GT 定量发光。使用定制曲线拟合软件来生成细胞活力百分比与抑制剂浓度对数函数的逻辑拟合。 IC50 值确定为将细胞活力降低至 DMSO 对照的 50% 所需的 BGJ398 浓度。
选择性FGFR抑制剂 NVP-BGJ398 以浓度依赖性的方式抑制所有20个测试子宫内膜癌细胞系的增殖,IC50值范围从FGFR2突变细胞系AN3CA的1.0 µmol/L到KRAS突变细胞系HEC1A的10.0 µmol/L。具有激活型FGFR2突变(S252W, N550K)的细胞系,其平均IC50值显著低于FGFR2野生型细胞系(平均IC50 2.96 vs. 5.55, P = 0.021)。同时存在BRAF突变的MFE319细胞系(也含有FGFR2 S252W突变)是FGFR2突变细胞系中对药物最不敏感的。[2] 在临床可达到的浓度1 µmol/L下,NVP-BGJ398 在4个FGFR2突变细胞系中的3个抑制了锚定非依赖性生长(≥50%生长抑制),但在11个FGFR2野生型细胞系中仅对3个(27%)有效,表明其活性与FGFR2突变状态相关性更强。[2] NVP-BGJ398 在FGFR2突变细胞中抑制FGFR2通路信号传导。它在携带FGFR2 N550K突变的细胞(AN3CA, MFE296)中以时间依赖性方式阻断FRS2α和ERK的磷酸化,并在具有S252W突变的细胞(MFE280)中阻断了基础和FGF7刺激的磷酸化。然而,在24至72小时内观察到ERK信号传导的恢复。该抑制剂对AKT磷酸化的影响较弱或可变。在FGFR2野生型细胞(SNGM, HEC1A)中,NVP-BGJ398 处理不改变ERK或AKT信号。[2] 用 NVP-BGJ398 处理可诱导FGFR2突变细胞系(AN3CA, MFE296, MFE280)中G0–G1期细胞比例显著增加和凋亡显著增加,但对FGFR2野生型细胞系(SNGM, HEC1A)的细胞周期或凋亡影响极小或无影响。[2] |
| 体内研究 (In Vivo) |
在该原位异种移植膀胱癌模型中,连续 12 天口服 10 和 30 mg/kg 剂量的 BGJ398 后可诱导肿瘤生长抑制和停滞。有趣的是,接受 BGJ398 的动物要么没有体重减轻(10 毫克/公斤),要么体重增加 10%(30 毫克/公斤),这进一步表明了疗效。 RT112荷瘤雌性Rowett大鼠接受单次口服BGJ398单磷酸盐,剂量为4.25和8.51 mg/kg。 BGJ398 以剂量依赖性方式显着降低 pFRS2 和 pMAPK 的水平。 BGJ398 以剂量依赖性方式显着抑制 bFGF 刺激的血管生成。然而,BGJ398 不会损害 VEGF 诱导的血管形成。
在来源于FGFR2突变子宫内膜癌细胞(AN3CA, MFE296)的小鼠异种移植模型中,每日口服30 mg/kg的 NVP-BGJ398 显著延迟了肿瘤生长。[2] 在使用FGFR2野生型SNGM异种移植模型的长期研究中,NVP-BGJ398 未显示抑制作用。然而,在FGFR2野生型HEC1A异种移植模型中,NVP-BGJ398 治疗确实延迟了肿瘤生长,尽管在这些细胞的体外实验中未显示效力。[2] |
| 酶活实验 |
纯化的 GST 融合 FGFR3-K650E 激酶结构域在放射性标记 ATP 存在的情况下磷酸化合成底物,以测量酶激酶活性。通过将 10 μL 相应底物混合物(肽底物、ATP 和 [γ33P]ATP)与 10 μL 3 倍浓缩的 Infigratinib 溶液或对照混合来测定酶活性。将测定缓冲液与 10 μL 浓缩酶溶液混合 3 次以启动反应。以下是检测成分的最终浓度:0.5 μM ATP (γ-[33P]-ATP 0.1 μCi)、3 mM MnCl2、3 mM MgCl
|
| 细胞实验 |
添加有 10% FBS、4.5 g/L 葡萄糖、1.5 g/L 碳酸氢钠和 Pen/Strep 的 RPMI-1640 培养基用于培养小鼠 BaF3 细胞系。每周两次细胞通过。荧光素酶生物发光测定用于评估化合物介导的 BaF3 细胞增殖和活力的抑制。使用 μFill 液体分配器,将指数生长的 BaF3 或 BaF3 Tel-TK 细胞以 50 μL/孔接种到新鲜培养基中的 384 孔板(4250 个细胞/孔)中。在 DMSO 中连续稀释后,将 infigratinib 置于 384 孔聚丙烯板中。使用 pintool 转移装置将 50 nL 化合物转移至板中后,将板在 37°C (5% CO 2 ) 下孵育 48 小时。接下来,添加 25 μL Bright-Glo,并使用 Analyst-GT 测量发光。使用专门的曲线拟合软件生成细胞活力百分比与抑制剂浓度对数函数的逻辑拟合。将细胞活力降低至 DMSO 对照的 50% 所需的化合物浓度称为 IC50 值[1]。
细胞以2×10^5至5×10^5的密度铺于24孔板中,并用浓度递增的 NVP-BGJ398(0.001 至 10 µmol/L)处理。7天后,通过胰蛋白酶消化收集细胞并计数。计算生长抑制率,并从剂量反应曲线中插值计算IC50值。[2] 软琼脂克隆形成实验: 在24孔板中铺0.5%琼脂底层。将细胞(5×10^3)与含有或不含1 µmol/L NVP-BGJ398 的0.3%琼脂顶层混合,一式四份铺板。培养板孵育长达5周。染色菌落后进行视觉计数。计算相对于未处理对照的抑制百分比。[2] 蛋白质印迹分析: 用 NVP-BGJ398 处理细胞,洗涤并裂解。测定蛋白质浓度。通过SDS-PAGE分离蛋白质,转印至膜,并用抗磷酸化FRS2α、磷酸化AKT、磷酸化ERK和α-Tubulin的抗体进行检测。对于MFE280细胞,在抑制剂处理前用FGF7(30 ng/mL,30分钟)进行刺激。使用化学荧光法进行检测。[2] 细胞周期分析: 对数生长期的细胞用 NVP-BGJ398 处理72小时。对细胞进行染色并通过流式细胞术分析,以确定处于不同细胞周期阶段的细胞比例。[2] 细胞凋亡实验(膜联蛋白V/PI): 细胞用 NVP-BGJ398 处理72小时。使用膜联蛋白V-FITC和碘化丙啶染色,然后进行流式细胞术检测细胞凋亡。[2] |
| 动物实验 |
小鼠:采用 HsdNpa 雌性无胸腺裸鼠(Nude-nu)。Infigratinib 以 10 和 30 mg/kg/天的剂量连续口服 12 天。Infigratinib 配制成 PEG300/D5W (2:1, v/v) 混悬液。采用 ANOVA 分析肿瘤和体重数据,并使用 Dunnett 检验进行事后比较,以比较治疗组和对照组。组内比较采用 Tukey 事后检验。统计分析使用 GraphPad Prism 4.02 软件。计算 T/C (%) 值作为疗效指标。
大鼠:采用 6 至 9 周龄的 Rowett 裸鼠(Woman in the nude rats)。荷瘤大鼠(n=8)每日一次腹腔灌注(灌胃)infigratinib,连续20天,剂量分别为5、10和15 mg/kg/qd(游离碱当量)。该药物配制成pH 4.6的乙酸-醋酸盐缓冲液/PEG300(1:1,v/v)溶液,用量为每公斤体重5毫升。肿瘤体积的计算公式为长×宽×高×π/6,可用游标卡尺测量。抗肿瘤活性以T/C(%)表示,计算公式为(治疗组肿瘤体积平均变化量/对照组肿瘤体积平均变化量)×100。计算肿瘤消退率(%)。 将子宫内膜癌细胞(每只小鼠2×10^7个细胞)皮下注射到4-6周龄的雌性无胸腺小鼠的侧腹部。当肿瘤平均体积达到约 105 mm³(7 天)后,根据肿瘤体积和重量将小鼠分为不同的治疗组。每组 10 只小鼠,每日通过灌胃给予以下两种治疗:(i)溶剂对照组,或(ii)NVP-BGJ398,剂量为 30 mg/kg(配制方法为:6 mg 溶于 0.5 mL PEG300 和 0.5 mL pH 4.68 的乙酸/醋酸盐缓冲液中)。连续测量肿瘤体积。[2] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
吸收 infigratinib 的平均(%CV)Cmax 为 282.5 ng/mL (54%),AUC0-24h 为 3780 ng·h/mL (59%)。在 5 至 150 mg 的剂量范围内,infigratinib 的 Cmax 和 AUC 呈非比例性增加,并在 15 天内达到稳态。达到稳态后,infigratinib 血浆峰浓度的中位时间 (Tmax) 为 6 小时,范围为 2 至 7 小时。BHS697 的平均(%CV)Cmax 为 42.1 ng/mL (65%),CQM157 的平均(%CV)Cmax 为 15.7 ng/mL (92%)。 BHS697 和 CQM157 的平均 AUC0-24h (%CV) 分别为 717 ng·h/mL (55%) 和 428 ng·h/mL (72%)。在健康受试者中,高脂高热量膳食使 infigratinib 的 AUCinf 增加 80%-120%,Cmax 增加 60%-80%。Tmax 中位数也从 4 小时延长至 6 小时。低脂低热量膳食使 infigratinib 的平均 AUCinf 增加 70%,Cmax 增加 90%。 消除途径 在健康受试者中单次口服放射性标记的 infigratinib 后,约 77% 的剂量从粪便中回收,其中 3.4% 的剂量为未改变的母体形式。约 7.2% 的剂量从尿液中回收,其中 1.9% 的剂量为未改变的形式。 分布容积 在稳态下,infigratinib 的几何平均值(CV%)表观分布容积为 1600 L (33%)。在单次口服给药的大鼠中,infigratinib 的脑血浆浓度比(基于 AUC0-inf)为 0.682。 清除率 在稳态下,infigratinib 的几何平均值(CV%)总表观清除率 (CL/F) 为 33.1 L/h (59%)。 代谢/代谢物 根据体外研究结果,约 94% 的 infigratinib 由 CYP3A4 代谢,约 6% 的药物由含黄素单加氧酶 3 (FMO3) 代谢。约38%的剂量以母体药物的形式存在于血浆中,BHS697和CQM157是infigratinib的两种主要代谢产物,各自的浓度均超过剂量的10%。它们具有药理活性,其中BHS697约占infigratinib总药理活性的16%至33%,CQM157约占9%至12%。BHS697经CYP3A4进一步代谢,而CQM157则通过I期和II期生物转化途径代谢。BHS697和CQM157的确切代谢途径和结构尚未完全阐明。 生物半衰期 在稳态下,infigratinib的几何平均值(CV%)末端半衰期为33.5小时(39%)。 |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
在英菲格替尼治疗晚期或转移性胆管癌的开放标签临床试验中,不良事件较为常见,导致64%的患者中断用药,60%的患者减少用药,15%的患者永久停药,主要原因是高磷血症、感染和脓毒症,而非肝损伤。在108例患者的预注册试验中,51%的患者出现ALT升高,其中6%的患者ALT升高至正常值上限的5倍以上。这些升高通常具有自限性,无论是否调整剂量,均可迅速恢复正常。没有患者出现临床上明显的肝损伤或黄疸。自英菲格替尼获批以来,尚未有临床上明显的肝损伤病例报告。然而,其临床应用经验总体有限,且治疗期间血清转氨酶升高频率较高,提示可能发生具有临床意义的肝损伤。 可能性评分:E(未经证实但可能,罕见,是导致临床明显肝损伤的原因)。 妊娠和哺乳期影响 ◉ 哺乳期用药概述 Infigratinib 已停止在美国销售。目前尚无关于哺乳期使用 infigratinib 的临床信息。由于 infigratinib 与血浆蛋白的结合率为 96.8%,因此其在乳汁中的含量可能很低。然而,由于该药对母乳喂养的婴儿可能具有毒性,且半衰期为 33.5 小时,因此生产商建议在接受 infigratinib 治疗期间以及末次给药后 1 个月内停止母乳喂养。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对哺乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白结合 Infigratinib 与血浆蛋白的结合率约为 96.8%,主要与脂蛋白结合。蛋白结合率与浓度相关。 |
| 参考文献 |
|
| 其他信息 |
磷酸英菲替尼是英菲替尼的磷酸盐形式,英菲替尼是一种口服生物利用度高的泛抑制剂,可抑制人成纤维细胞生长因子受体(FGFR),具有潜在的抗血管生成和抗肿瘤活性。给药后,英菲替尼选择性地结合并抑制FGFR的活性,从而抑制血管生成和细胞增殖,并诱导具有激活型FGFR扩增、突变或融合的肿瘤细胞死亡。FGFR是一类受体酪氨酸激酶,参与肿瘤细胞分化和增殖、肿瘤血管生成以及肿瘤细胞存活。激活型FGFR扩增、突变或融合发生在多种癌细胞类型中。
另见:Infigratinib(具有活性部分)。 通过合理设计芳环的取代模式,我们优化了一系列新型N-芳基-N'-嘧啶-4-基脲,以获得强效且选择性的成纤维细胞生长因子受体酪氨酸激酶1、2和3抑制剂。基于其体外活性,我们选择化合物1h(NVP-BGJ398)进行体内评估,并在过表达野生型FGFR3的RT112膀胱癌异种移植模型中显示出显著的抗肿瘤活性。这些结果支持化合物1h作为一种新型抗癌药物的潜在治疗用途。[1] 近期在子宫内膜癌中发现的激活型成纤维细胞生长因子受体2(FGFR2)突变为新型靶向治疗提供了契机。本研究探讨了两种FGFR抑制剂——多激酶抑制剂多维替尼(TKI258)和选择性更高的FGFR抑制剂NVP-BGJ398——在子宫内膜癌治疗中的应用潜力。我们利用20株经分子鉴定的人类子宫内膜癌细胞系,检测了这两种抑制剂对肿瘤细胞生长、FGFR2信号通路、细胞周期和细胞凋亡的影响。采用软琼脂克隆形成实验研究了细胞的非锚定依赖性生长。体内研究则采用子宫内膜癌异种移植模型进行。结果显示,与FGFR2野生型细胞系相比,携带FGFR2激活突变(S252W、N550K)的细胞系对多维替尼和NVP-BGJ398更为敏感(P值分别为0.073和0.021)。两种药物均能抑制FGFR2信号通路,诱导细胞周期阻滞,并显著增加FGFR2突变细胞系的凋亡。体外实验表明,多维替尼和NVP-BGJ398均能有效抑制FGFR2突变子宫内膜癌细胞的生长,但与NVP-BGJ398相比,多维替尼的活性对FGFR2突变细胞系的限制性更小。体内实验表明,多维替尼和NVP-BGJ398均能显著抑制FGFR2突变子宫内膜癌异种移植模型的生长。此外,在长期体内研究中,多维替尼在FGFR2野生型子宫内膜癌异种移植模型中也显示出显著的抗肿瘤活性,包括肿瘤的完全消退。多维替尼和NVP-BGJ398值得在FGFR2突变子宫内膜癌患者中进行进一步的临床评估。多维替尼可能对FGFR2突变以外的子宫内膜癌也具有抗肿瘤活性,并可能使患者选择更加灵活。[2] NVP-BGJ398是一种高选择性的泛FGFR激酶抑制剂,通过合理的药物设计进行了优化。其选择性表明,与非选择性多激酶抑制剂相比,其毒性特征可能更佳。[2] 部分子宫内膜癌存在激活型FGFR2突变(例如,配体结合域中的S252W突变,激酶域中的N550K突变),这些突变赋予肿瘤对FGFR抑制剂的敏感性。与原发肿瘤相比,这些突变在复发/转移性疾病中的频率可能更高。[2] 本研究的临床前数据支持了在携带FGFR2突变的复发性子宫内膜癌患者中开展NVP-BGJ398临床试验的合理性。[2] |
| 分子式 |
C26H34CL2N7O7P
|
|
|---|---|---|
| 分子量 |
658.47
|
|
| 精确质量 |
657.163
|
|
| 元素分析 |
C, 47.43; H, 5.20; Cl, 10.77; N, 14.89; O, 17.01; P, 4.70
|
|
| CAS号 |
1310746-10-1
|
|
| 相关CAS号 |
Infigratinib;872511-34-7
|
|
| PubChem CID |
56669626
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| LogP |
4.574
|
|
| tPSA |
182.66
|
|
| 氢键供体(HBD)数目 |
5
|
|
| 氢键受体(HBA)数目 |
12
|
|
| 可旋转键数目(RBC) |
8
|
|
| 重原子数目 |
43
|
|
| 分子复杂度/Complexity |
773
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
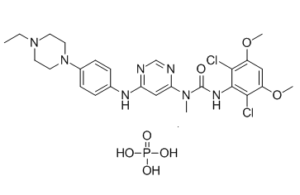
ClC1C(=C([H])C(=C(C=1N([H])C(N(C([H])([H])[H])C1C([H])=C(N=C([H])N=1)N([H])C1C([H])=C([H])C(=C([H])C=1[H])N1C([H])([H])C([H])([H])N(C([H])([H])C([H])([H])[H])C([H])([H])C1([H])[H])=O)Cl)OC([H])([H])[H])OC([H])([H])[H].P(=O)(O[H])(O[H])O[H]
|
|
| InChi Key |
GUQNHCGYHLSITB-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C26H31Cl2N7O3.H3O4P/c1-5-34-10-12-35(13-11-34)18-8-6-17(7-9-18)31-21-15-22(30-16-29-21)33(2)26(36)32-25-23(27)19(37-3)14-20(38-4)24(25)28;1-5(2,3)4/h6-9,14-16H,5,10-13H2,1-4H3,(H,32,36)(H,29,30,31);(H3,1,2,3,4)
|
|
| 化学名 |
3-(2,6-dichloro-3,5-dimethoxyphenyl)-1-[6-[4-(4-ethylpiperazin-1-yl)anilino]pyrimidin-4-yl]-1-methylurea;phosphoric acid
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|---|
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.5187 mL | 7.5934 mL | 15.1867 mL | |
| 5 mM | 0.3037 mL | 1.5187 mL | 3.0373 mL | |
| 10 mM | 0.1519 mL | 0.7593 mL | 1.5187 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT05514912 | Not yet recruiting | Drug: Cisplatin Drug: Infigratinib Phosphate |
Stage 0 Intrahepatic Cholangiocarcinoma AJCC v8 Resectable Intrahepatic Cholangiocarcinoma |
Emory University | November 1, 2023 | Phase 2 |
| NCT04197986 | Terminated | Drug: Infigratinib Drug: Placebo |
Upper Tract Urothelial Carcinomas Urothelial Bladder Cancer |
QED Therapeutics, Inc. | March 11, 2020 | Phase 3 |
Targeting Fgfr2-fusion containing tumors with the FGFR-inhibitor BGJ398 results in complete response.Cancer Discov.2018 Mar;8(3):354-369. |
Multiple, different genetic aberrations lead to common elevated MAPK and/or PI3K pathway activation in human breast cancer patients.Cancer Discov.2018 Mar;8(3):354-369. |
Targeting Dhx9-Raf1 and cMet with MEK- and MET-inhibitor, respectively, result in tumor regression or delayed progression.
|