| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
- Isoviolanthin targets the TGF-β/Smad signaling pathway (key proteins: TGF-βRII, p-Smad2, p-Smad3) and PI3K/Akt/mTOR signaling pathway (key proteins: p-PI3K, p-Akt, p-mTOR)[1]
|
|---|---|
| 体外研究 (In Vitro) |
- 逆转TGF-β1介导的肝癌(HCC)细胞上皮-间质转化(EMT):在经TGF-β1(5 ng/mL)处理的HepG2和Huh7细胞中,异紫黄质(5、10、20 μM)呈浓度依赖作用。20 μM时,上皮标志物E-钙黏蛋白较仅TGF-β1组升高2.8倍(western blot)和2.5倍(mRNA,qPCR),间质标志物N-钙黏蛋白降低65%(western blot)和60%(mRNA),波形蛋白降低62%(western blot)和58%(mRNA)[1]
- 抑制通路激活:在TGF-β1刺激的HepG2细胞中,异紫黄质(20 μM)使Smad2磷酸化降低70%、Smad3降低68%、PI3K降低65%、Akt降低72%、mTOR降低66%(western blot),这些靶标的总蛋白水平无变化[1] - 抑制迁移和侵袭:Transwell实验中,异紫黄质(20 μM)使TGF-β1刺激的HepG2细胞迁移率降低68%、侵袭率降低72%(vs仅TGF-β1组);划痕愈合实验中,20 μM使伤口愈合时间延长2.3倍[1] - 抑制克隆形成:异紫黄质(20 μM)使TGF-β1刺激的HepG2细胞克隆数减少65%(结晶紫染色),10 μM减少40%,5 μM无显著效果[1] |
| 细胞实验 |
- 细胞活力实验:HepG2/Huh7细胞(5×10³个/孔)用异紫黄质(0–40 μM)单独或联合TGF-β1(5 ng/mL)处理48小时,加入MTT试剂后测570 nm吸光度;≤20 μM 异紫黄质对肝癌细胞活力无影响[1]
- Western blot实验:处理后的肝癌细胞裂解,蛋白经SDS-PAGE分离后,用EMT标志物(E-钙黏蛋白、N-钙黏蛋白、波形蛋白)和通路蛋白(p-Smad2、p-Smad3、p-PI3K、p-Akt、p-mTOR)抗体孵育,以GAPDH为内参[1] - qPCR实验:提取处理后细胞总RNA并逆转录为cDNA,用EMT标志物引物进行qPCR,通过2⁻ΔΔCt法计算相对mRNA表达量[1] - Transwell实验:迁移实验将处理后细胞(1×10⁵个/孔)接种于无Matrigel的Transwell上室;侵袭实验用上室包被Matrigel(2×10⁵个/孔),24小时后染色计数下室细胞[1] - 克隆形成实验:处理后细胞(500个/孔)孵育14天,固定后用结晶紫染色,计数>50个细胞的克隆[1] |
| 参考文献 | |
| 其他信息 |
已有报道称,异紫罗兰素存在于西番莲(Passiflora sexflora)和紫菀(Angiopteris evecta)中,并有相关数据报道。
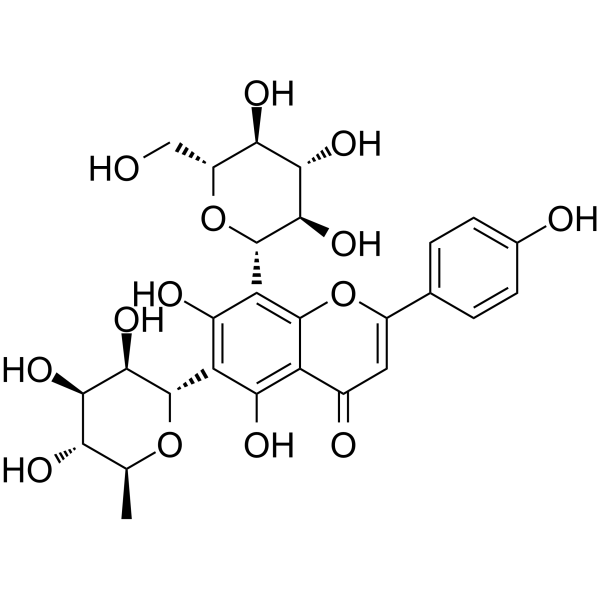
- 异紫罗兰素是一种从石斛(Dendrobium officinale,一种传统中药植物)茎中提取的天然化合物[1] - 其在肝细胞癌(HCC)细胞中的抗上皮间质转化(EMT)作用是通过抑制TGF-β/Smad和PI3K/Akt/mTOR通路介导的,这些通路调控EMT和HCC的进展[1] |
| 分子式 |
C27H30O14
|
|---|---|
| 分子量 |
578.518709659576
|
| 精确质量 |
578.164
|
| CAS号 |
40788-84-9
|
| PubChem CID |
101422758
|
| 外观&性状 |
Light yellow to yellow solid powder
|
| tPSA |
250.97
|
| 氢键供体(HBD)数目 |
10
|
| 氢键受体(HBA)数目 |
14
|
| 可旋转键数目(RBC) |
4
|
| 重原子数目 |
41
|
| 分子复杂度/Complexity |
970
|
| 定义原子立体中心数目 |
10
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 本产品在运输和储存过程中需避光。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~250 mg/mL (~432.14 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (3.60 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.08 mg/mL (3.60 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.7285 mL | 8.6427 mL | 17.2855 mL | |
| 5 mM | 0.3457 mL | 1.7285 mL | 3.4571 mL | |
| 10 mM | 0.1729 mL | 0.8643 mL | 1.7285 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。