| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| Other Sizes |
|
| 靶点 |
Incubating tumor cells with 10 mM L-2,4-diaminobutyric acid for 24 hours at 37°C causes irreversible and total destruction. L-DABA's cell-damaging actions could be attributed to osmotic lysis caused by non-saturated intracellular buildup of the compound. L-DABA's deleterious effects can be removed by incubating it with L-alanine and L-methionine at the same time [1]. Kinetic investigations show that L-DABA is a non-linear, non-competitive inhibitor of GABA transaminase activity. The rise in GABA levels induced by L-DABA is consistent with the suppression of GABA transaminase activity [2]. L-2,4-diaminobutyric acid is an amino acid analog that has cytotoxic effects on the human glioma cell line SKMG-1 and normal human fibroblasts. The L-DABA concentration needed to reduce cell counts to 50% of control after 24 hours of incubation at 37°C is 12.5 mM for human fibroblasts and 20 mM for glioma cell lines [3].
|
|---|---|
| 体外研究 (In Vitro) |
将肿瘤细胞与 10 mM L-2,4-二氨基丁酸在 37°C 下孵育 24 小时会导致不可逆的完全破坏。 L-DABA 的细胞损伤作用可能是由于该化合物在细胞内不饱和积累引起的渗透裂解所致。 L-DABA 的有害作用可通过将其与 L-丙氨酸和 L-蛋氨酸同时孵育来消除[1]。动力学研究表明,L-DABA 是 GABA 转氨酶活性的非线性、非竞争性抑制剂。 L-DABA 诱导的 GABA 水平升高与 GABA 转氨酶活性的抑制一致 [2]。 L-2,4-二氨基丁酸是一种氨基酸类似物,对人胶质瘤细胞系 SKMG-1 和正常人成纤维细胞具有细胞毒性作用。 37°C 孵育 24 小时后,将细胞计数减少至对照的 50% 所需的 L-DABA 浓度对于人成纤维细胞为 12.5 mM,对于神经胶质瘤细胞系为 20 mM [3]。
L-DABA 对小鼠纤维肉瘤细胞表现出强效且不可逆的细胞溶解活性。在37°C下用10 mM L-DABA 孵育24小时,通过乳酸脱氢酶释放测定,导致100%的肿瘤细胞裂解。达到50%裂解所需的时间约为7-8小时。[1] 细胞溶解效应具有浓度依赖性。5 mM的 L-DABA 即使孵育48小时也只能引起有限的细胞损伤,表明裂解效应在5至10 mM之间存在一个尖锐的阈值。[1] 10 mM L-DABA 的细胞毒性作用可被同时加入的10 mM L-丙氨酸和10 mM L-蛋氨酸完全消除,这两种氨基酸通过系统A转运与 L-DABA 竞争。丙氨酸和蛋氨酸的D型异构体以及肌氨酸(N-甲基甘氨酸)的保护作用则弱得多。[1] 推测的作用机制是细胞渗透性裂解,可能同时伴随细胞内腺苷酸电荷的降低,这是由于 L-DABA 通过系统A转运进行能量依赖性的、不可饱和的细胞内积累所致。[1] |
| 体内研究 (In Vivo) |
L-DABA 治疗可以阻止肿瘤生长 43.4%[1]。在体内,L-DABA 比体外更有效地抑制 GABA 转氨酶 [2]。
在皮下移植了小鼠纤维肉瘤细胞的小鼠中,腹腔注射等渗的0.1 M (100 mM) L-DABA 溶液能显著抑制肿瘤生长。[1] 在总共涉及90只小鼠的六个实验系列中,42只可评估的 L-DABA 治疗组小鼠的平均肿瘤重量为1.16克(±0.77克),而27只未治疗的对照组小鼠为2.05克(±1.22克)。这代表平均肿瘤重量减少了43.4%。减少的程度因治疗方案不同而在各系列间有所差异(8.3% 至 61.5%)。[1] 治疗并未导致肿瘤完全消退,并且在经 L-DABA 治疗后手术切除肿瘤的7只动物中,有5只出现了局部复发。[1] |
| 细胞实验 |
细胞培养: 小鼠纤维肉瘤细胞常规在添加了10%胎牛血清和抗生素(青霉素和链霉素)的Eagle极限必需培养基中,于37°C、5% CO₂的湿润环境中培养。[1]
细胞溶解实验: 用于实验的细胞接种于培养皿中生长24小时。随后将培养液更换为简化的无血清MEM。将 L-DABA 以1至20 mM(通常为10 mM)的终浓度加入此培养基中,可单独加入或与其他氨基酸(如L-丙氨酸、L-蛋氨酸、它们的D型异构体或肌氨酸)各10 mM同时加入。孵育培养基的渗透压经过调整。细胞与化合物在37°C下孵育4至48小时(通常为24小时)。[1] 活力评估: 孵育结束后,通过光学显微镜评估细胞活力。收集培养上清液,通过测量释放到培养基中的乳酸脱氢酶活性来定量细胞裂解程度。总细胞LD活性通过对单独的细胞样品进行低渗休克结合冻融裂解来测定。细胞裂解百分比通过比较测试上清液中的LD活性(经对照细胞背景校正后)与总细胞LD活性来计算。[1] |
| 动物实验 |
动物和肿瘤模型:使用成年雄性NMR1小鼠(体重约35 g)。将小鼠纤维肉瘤细胞(5 × 10⁷ 个细胞)通过小切口皮下移植到麻醉小鼠的右侧腹部。[1]
药物配制和给药:将L-DABA(二盐酸盐形式)溶于水,配制成0.1 M(100 mM)溶液。用氢氧化钠调节pH至7.4,得到等渗溶液(渗透压约300-310 mOsm)。[1] 治疗方案:肿瘤移植后1至4天开始治疗。小鼠每日腹腔注射0.1 M L-DABA溶液。注射体积(剂量)通常为每次注射0.50 ml至0.90 ml(50-90 µmol DAB),大多数系列研究中每日单次给药。不同实验系列的总治疗周期为8至23天。[1] 剂量调整:根据动物的临床状况和体重变化进行个体化剂量调整。如果动物24小时内体重下降超过0.5-2.0 g,则暂停治疗或减少剂量,待体重恢复后方可恢复治疗。[1] 终点:在最后一次治疗后2-12天,当对照组小鼠的肿瘤达到总体重的约10%时,对动物实施安乐死。切除实体瘤并称重。[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
治疗相关死亡率:体内注射L-DABA会导致显著的毒性。在所有系列的61只接受治疗的小鼠中,有17只(27.9%)在治疗期间死亡。死亡率因给药方案的不同而有所差异。[1]
体重减轻:L-DABA治疗持续导致动物体重减轻,这至少部分归因于食欲不振。[1] 神经毒性:一些接受治疗的动物出现了特定的神经系统症状,包括程度不一的强直-痉挛、尾部和四肢僵硬、身体动作不协调和抽搐,以及触觉敏感性增强。嗜睡也是常见的症状。停用L-DABA 1-3天后,这些症状通常可逆转。 [1] 毒性机制推测:神经毒性症状可能由L-DABA脱氨导致的氨中毒引起,也可能由L-DABA抑制GABA转氨酶导致脑内GABA水平升高引起。然而,本研究并未通过实验证实这些机制。[1] |
| 参考文献 | |
| 其他信息 |
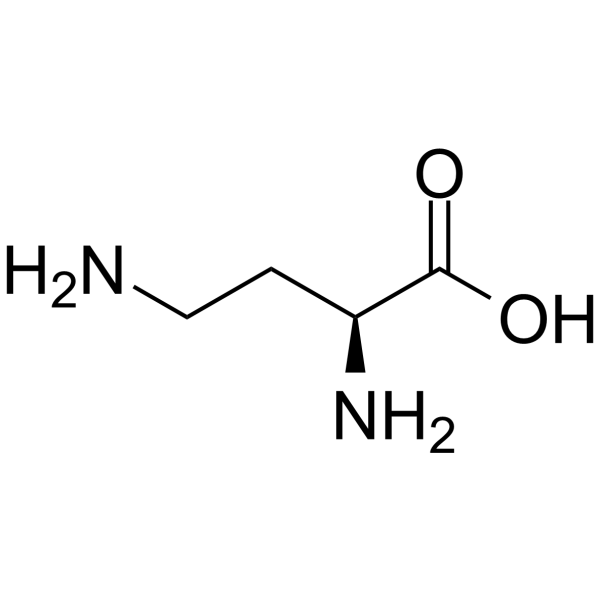
L-2,4-二氨基丁酸是一种具有S构型的2,4-二氨基丁酸。它是一种植物代谢产物,在功能上与丁酸相关。它是L-2,4-二氮杂丁酸酯的共轭碱,也是L-2,4-二氨基丁酸酯的共轭酸,还是D-2,4-二氨基丁酸的对映异构体。
据报道,L-2,4-二氨基丁酸存在于阔叶野豌豆(Lathyrus latifolius)、白黄链霉菌(Streptomyces albidoflavus)以及其他有相关数据的生物体中。 L-DABA是一种不可代谢的二氨基酸类似物。 [1] 其抗肿瘤作用在化疗药物中被认为是独一无二的,因为它主要靶向质膜转运系统(A系统),导致渗透性溶解,而不是干扰DNA合成或其他细胞内过程。[1] 由于本研究观察到其显著的全身毒性(体重减轻、神经毒性、致死性),作者得出结论,L-DABA单独作为抗肿瘤药物的局限性在于其疗效有限。然而,他们认为其独特的作用机制可能为与其他作用于不同亚细胞靶点的药物联合治疗提供新的可能性。[1] 该研究还假设,正常细胞和恶性细胞之间A系统转运蛋白的潜在质性差异(例如,对巯基反应物的敏感性)可能被用于未来的治疗策略中,以实现对肿瘤细胞的选择性毒性。[1] |
| 分子式 |
C4H10N2O2.HBR
|
|---|---|
| 分子量 |
199.04634
|
| 精确质量 |
118.074
|
| CAS号 |
1758-80-1
|
| 相关CAS号 |
(S)-L-DABA dihydrochloride;1883-09-6
|
| PubChem CID |
134490
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.218 g/cm3
|
| 沸点 |
321ºC at 760 mmHg
|
| 闪点 |
147.9ºC
|
| 蒸汽压 |
6.36E-05mmHg at 25°C
|
| 折射率 |
1.513
|
| LogP |
1.105
|
| tPSA |
89.34
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
4
|
| 可旋转键数目(RBC) |
3
|
| 重原子数目 |
8
|
| 分子复杂度/Complexity |
84.1
|
| 定义原子立体中心数目 |
1
|
| SMILES |
C(CN)[C@@H](C(=O)O)N
|
| InChi Key |
OGNSCSPNOLGXSM-VKHMYHEASA-N
|
| InChi Code |
InChI=1S/C4H10N2O2/c5-2-1-3(6)4(7)8/h3H,1-2,5-6H2,(H,7,8)/t3-/m0/s1
|
| 化学名 |
(2S)-2,4-diaminobutanoic acid
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
H2O : ~1 mg/mL (~8.47 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 100 mg/mL (846.53 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶。
请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 5.0239 mL | 25.1193 mL | 50.2386 mL | |
| 5 mM | 1.0048 mL | 5.0239 mL | 10.0477 mL | |
| 10 mM | 0.5024 mL | 2.5119 mL | 5.0239 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。