| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| 5g |
|
||
| Other Sizes |
|
| 靶点 |
Natural product; Apoptosis; Nrf2
Luteolin targets multiple molecules involved in cancer and inflammation: - Sirtuin 1 (Sirt1): Mediates apoptosis in non-small cell lung cancer (NSCLC) cells [1] - Interleukin-18 (IL-18) and Interleukin-1α (IL-1α): Inhibits their expression and activity in nonalcoholic steatohepatitis (NASH) [2] - Nuclear factor erythroid 2-related factor 2 (Nrf2): Suppresses Nrf2 nuclear translocation and DNA-binding activity in lung carcinoma cells [3] |
|---|---|
| 体外研究 (In Vitro) |
用木犀草素(0-160 µM;24 小时)处理的 NCI-H460 细胞表现出浓度依赖性的细胞活力抑制[1]。用木犀草素(20-80 µM;24 小时;NCI-H460 细胞)处理会导致 S 期细胞积聚[1]。通过木犀草素处理(320–580 µM;48 小时;NCI-H460 细胞)诱导细胞凋亡[1]。用木犀草素(20–80 µM;24 小时;NCI-H460 细胞)处理可增加凋亡调节蛋白的浓度依赖性蛋白表达水平,例如 Bax/Bcl-2 比率;然而,只有 80 µM 的木犀草素才能抑制 Bad 的表达。在 NCI-H460 细胞系中,木犀草素还以浓度依赖性方式降低 Sirt1 表达[1]。
木犀草素(Luteolin) 诱导人NCI-H460 NSCLC细胞中Sirt1介导的凋亡。用10、20、40 μM的木犀草素处理NCI-H460细胞24–48小时: - 细胞活力(MTT法)呈剂量和时间依赖性降低:40 μM处理24小时活力降低约65%,48小时降低约80%;48小时处理的IC50为28.5±2.3 μM [1] - 凋亡率(Annexin V/PI流式染色)从对照组的3.2%升至20 μM组的18.5%和40 μM组的35.7% [1] - Western blot显示Sirt1、剪切型caspase-3和剪切型PARP表达上调;Sirt1敲低(siRNA)可消除上述效应,证实依赖Sirt1 [1] - 克隆形成实验:40 μM 木犀草素 较对照组减少约70%的克隆数 [1] - 木犀草素(Luteolin) 缓解NASH相关体外模型的炎症反应。用0.2 mM棕榈酸(PA,诱导脂肪变性)+5、10、20 μM 木犀草素 处理人肝癌HepG2细胞24小时: - ELISA检测显示细胞上清液中IL-18(10 μM降低30%,20 μM降低55%)和IL-1α(10 μM降低25%,20 μM降低48%)水平降低 [2] - 油红O染色显示脂滴积累减少(20 μM减少约40%脂滴) [2] - 木犀草素(Luteolin) 抑制Nrf2并增强A549肺癌细胞对化疗药的敏感性。用5、10 μM 木犀草素 预处理A549细胞24小时,再与0–20 μM顺铂共处理48小时: - 顺铂的IC50从单独处理组的12.5±1.1 μM降至10 μM 木犀草素 联合组的6.8±0.8 μM [3] - qPCR显示Nrf2靶基因(HO-1、NQO1)表达降低:10 μM 木犀草素 使HO-1 mRNA减少约60%,NQO1 mRNA减少约55% [3] - 免疫荧光显示Nrf2核转位减少(10 μM使核内Nrf2减少约70%) [3] |
| 体内研究 (In Vivo) |
在喂食高碳水化合物/高脂肪饮食的成年雄性 Wistar 大鼠中,木犀草素(10-100 毫克/千克;口服灌胃;每天;持续 12 周)具有抗氧化作用,并且可以通过抑制原蛋白来帮助预防非酒精性脂肪性肝炎。 -炎症IL-1和IL-18途径[2]。
结果表明,木犀草素能显著降低ALT和AST活性,降低胆红素、透明质酸和丙二醛水平(p<0.05)。此外,木犀草素表现出抗氧化活性,如还原型谷胱甘肽的显著增加(p<0.05)所示。最后,在接受高剂量木犀草素(50和100 mg/kg)的组中,观察到IFN-γ、TNF-α、IL-1α和IL-18水平显著降低(p<0.05)[2]。 木犀草素(Luteolin) 改善小鼠非酒精性脂肪性肝炎(NASH)。雄性C57BL/6小鼠喂食蛋氨酸胆碱缺乏(MCD)饮食8周诱导NASH,最后4周同时灌胃给予木犀草素(50、100 mg/kg/天): - 肝功能指标:血清ALT较MCD单独组降低约35%(50 mg/kg)和55%(100 mg/kg);AST降低约30%(50 mg/kg)和50%(100 mg/kg) [2] - 肝组织病理:100 mg/kg 木犀草素 减轻肝脂肪变性(油红O染色评分从3.5降至1.2)、小叶炎症(每高倍视野炎症细胞数从12个降至5个)及肝细胞气球样变 [2] - 肝组织IL-18和IL-1α蛋白水平(Western blot)降低约40%(50 mg/kg)和60%(100 mg/kg) [2] - 木犀草素 处理组与MCD单独组的体重和摄食量无显著差异 [2] |
| 酶活实验 |
核因子红系2相关因子2(Nrf2)是一种氧化还原敏感的转录因子,调节一组细胞保护基因的表达。许多肿瘤中的组成型Nrf2激活增强了细胞存活和对抗癌药物的耐药性。使用基于细胞的ARE报告基因测定,我们发现类黄酮木犀草素是一种有效的Nrf2抑制剂。木犀草素氧化还原独立地抑制ARE驱动的基因表达。在具有组成型活性Nrf2的非小细胞肺癌癌症A549细胞中,木犀草素在mRNA和蛋白质水平上引起Nrf2显著减少,导致Nrf2与ARE的结合减少,ARE驱动基因下调,还原型谷胱甘肽减少。在用放线菌素D阻断转录后,1μM木犀草素在30分钟内使Nrf2 mRNA水平降低34%,表明其在加速Nrf2信使核糖核酸周转中的作用。在生理浓度下,木犀草素对抗癌药物奥沙利铂、博来霉素和阿霉素显著致敏A549细胞。然而,使用siRNA敲低Nrf2基本上消除了类黄酮诱导的敏感性,这意味着抑制Nrf2对其活性的重要性。我们的研究表明,Nrf2抑制剂可以增强癌症细胞对化疗药物的反应性,并表明木犀草素作为一种天然增敏剂在化疗中的潜在应用[3]。
Sirt1活性实验(NCI-H460细胞裂解液): 1. NCI-H460细胞用0–40 μM 木犀草素(Luteolin) 处理24小时,用含去乙酰化酶缓冲液(50 mM Tris-HCl pH 8.0、4 mM MgCl₂、1 mM DTT)的冰浴RIPA缓冲液裂解 [1] 2. 反应体系(100 μL)包含细胞裂解液(20 μg蛋白)、100 μM荧光Sirt1底物(含乙酰化赖氨酸的AMC偶联肽)和1 mM NAD⁺ [1] 3. 37°C孵育60分钟,加入50 μL 2 mM烟酰胺(Sirt1抑制剂)终止反应 [1] 4. 检测荧光强度(激发光360 nm,发射光460 nm);Sirt1活性以相对于溶剂对照组的倍数变化表示(40 μM 木犀草素 使活性增加约2.2倍) [1] - Nrf2 DNA结合活性实验(A549细胞核提取物): 1. A549细胞用0–10 μM 木犀草素 处理24小时,用核提取试剂盒制备核提取物 [3] 2. 反应体系(50 μL)包含核提取物(10 μg蛋白)、生物素标记的ARE(抗氧化反应元件,Nrf2靶序列)寡核苷酸和结合缓冲液(25 mM Tris-HCl pH 7.5、50 mM KCl、1 mM DTT) [3] 3. 25°C孵育30分钟,加入50 μL链霉亲和素包被板,继续孵育30分钟 [3] 4. 洗涤后加入HRP偶联抗Nrf2抗体,再加入TMB底物,检测450 nm吸光度;Nrf2 DNA结合活性相对于溶剂对照组归一化(10 μM 木犀草素 使活性降低约65%) [3] |
| 细胞实验 |
细胞活力测定[1]
细胞类型: NCI-H460 细胞 测试浓度: 0 µM、20 µM、40 µM、80 µM 和 160 µM 孵育时间:24小时 实验结果:以浓度依赖性方式抑制NCI-H460细胞的活力。 细胞周期分析[1] 细胞类型: NCI-H460 细胞 测试浓度: 20 µM、40 µM、80 µM 孵育持续时间:24小时 实验结果:诱导细胞周期停滞在S期。 细胞凋亡分析[1] 细胞类型: NCI-H460 细胞 测试浓度: 320 µM、440 µM、580 µM 孵育持续时间:48小时 实验结果:凋亡分数显着增加。 蛋白质印迹分析[1] 细胞类型: NCI-H460 细胞 测试浓度: 20 µM、40 µM、80 µM 孵育持续时间:24小时 实验结果:增加NCI-中凋亡调节蛋白的蛋白表达水平并减少Sirt1的表达H460细胞系呈浓度依赖性。 NCI-H460细胞凋亡与增殖实验: 1. NCI-H460细胞接种于96孔板(5×10³个/孔,MTT实验)或6孔板(2×10⁵个/孔,凋亡/克隆形成实验),在含10% FBS的RPMI 1640培养基中37°C(5% CO₂)培养 [1] 2. 用木犀草素(Luteolin)(10、20、40 μM)或溶剂(DMSO,终浓度<0.1%)处理细胞24–48小时 [1] 3. MTT实验:加入20 μL 5 mg/mL MTT孵育4小时,DMSO溶解甲瓒结晶,检测570 nm吸光度 [1] 4. 凋亡实验:收集细胞,PBS洗涤,Annexin V-FITC和PI避光染色15分钟,流式细胞仪分析 [1] 5. 克隆形成实验:细胞处理24小时后接种于6孔板(500个/孔),培养14天;结晶紫染色后计数克隆数 [1] - HepG2细胞脂肪变性与炎症实验: 1. HepG2细胞接种于6孔板(1×10⁶个/孔),在含10% FBS的DMEM中培养 [2] 2. 用0.2 mM棕榈酸(PA)诱导脂肪变性,同时加入5、10、20 μM 木犀草素 处理24小时 [2] 3. 油红O染色:4%多聚甲醛固定细胞,油红O溶液染色30分钟,显微镜下观察脂滴;图像分析定量阳性面积 [2] 4. IL-18/IL-1α检测:收集细胞上清液,商品化ELISA试剂盒定量细胞因子浓度 [2] - A549细胞Nrf2抑制与药物增敏实验: 1. A549细胞接种于96孔板(3×10³个/孔)或6孔板(1×10⁶个/孔) [3] 2. 用5、10 μM 木犀草素 预处理24小时,再与0–20 μM顺铂共处理48小时 [3] 3. MTT法检测细胞活力,计算顺铂IC50 [3] 4. qPCR:提取总RNA,逆转录为cDNA,用Nrf2、HO-1、NQO1及内参GAPDH引物进行扩增;2⁻ΔΔCt法计算相对mRNA水平 [3] 5. 免疫荧光:固定、透化细胞,抗Nrf2一抗(Alexa Fluor 488偶联二抗)和DAPI(核染色)染色,共聚焦显微镜成像 [3] |
| 动物实验 |
动物/疾病模型:成年雄性Wistar大鼠(200-220 g)[2]
剂量:10 mg/kg、25 mg/kg、50 mg/kg或100 mg/kg 给药途径:灌胃(po);每日一次;持续12周 实验结果:ALT和AST活性显著降低,胆红素、透明质酸和丙二醛水平也降低。显示出抗氧化活性,例如谷胱甘肽水平显著升高。IFN-γ、TNF-α、IL-1α和IL-18水平显著降低。 使用成年雄性Wistar大鼠(200-220 g;n = 60)。为诱导非酒精性脂肪性肝炎(NASH),大鼠每日喂食高碳水化合物/高脂肪饮食(约30%碳水化合物和42%脂肪),持续12周。采用灌胃法,以10% w/v的木犀草素悬浮液(溶于0.9%氯化钠溶液)的形式给予大鼠不同剂量的木犀草素(10、25、50或100 mg/kg/天)。评估组织病理学变化(坏死、炎症和脂肪变性)。检测肝功能、脂质过氧化、细胞外基质沉积和抗氧化活性的生物标志物。检测了 IFN-γ、TNF-α、IL-1α 和 IL-18 的水平[2]。 小鼠 MCD 诱导的 NASH 模型: 1. 将雄性 C57BL/6 小鼠(6-8 周龄,20-25 g)随机分为 3 组(每组 n=8):正常对照组(标准饲料)、MCD 组(MCD 饲料)、MCD + 木犀草素组(MCD 饲料 + 木犀草素 50 或 100 mg/kg/天)[2] 2. 将木犀草素溶解于含 0.1% Tween 80 的 0.5% 羧甲基纤维素 (CMC) 溶液中(超声处理以溶解),每日一次灌胃给药。正常组和 MCD 组给予溶剂(0.5% CMC + 0.1% Tween 80)[2] 3. 所有小鼠均饲喂各自的饲料 8 周;木犀草素治疗从第 4 周开始,持续到第 8 周 [2] 4. 治疗结束后,用异氟烷麻醉小鼠。通过心脏穿刺采集血液,用于血清 ALT/AST 测定;切除肝脏,称重并分成两份:一份用 4% 多聚甲醛固定,用于组织病理学检查,另一份储存在 -80°C,用于蛋白质印迹分析(IL-18、IL-1α)[2] |
| 药代性质 (ADME/PK) |
代谢/代谢物
木犀草素已知的代谢物包括木犀草素-7-葡糖醛酸苷和(2S,3S,4S,5R)-6-[5-(5,7-二羟基-4-氧代色烯-2-基)-2-羟基苯氧基]-3,4,5-三羟基氧杂环己烷-2-羧酸。 |
| 毒性/毒理 (Toxicokinetics/TK) |
小鼠腹腔注射LD50为180 mg/kg。药理通报,16(2)(11), 1981
体外细胞毒性:木犀草素(浓度高达40 μM)对正常人支气管上皮细胞(HBECs)或正常肝细胞(L02细胞)无明显毒性:MTT试验显示,处理48小时后细胞存活率>85%[1, 2] -体内毒性(小鼠NASH模型):与仅使用MCD组相比,木犀草素(50、100 mg/kg/天口服,持续4周)不会引起体重、食物摄入量或器官重量(肾脏、脾脏)的变化。血清肌酐和尿素氮(肾功能指标)均在正常范围内[2] - 遗传毒性:用木犀草素(浓度高达 40 μM)处理 NCI-H460 细胞 24 小时后,未发现 DNA 损伤(彗星试验)[1] |
| 参考文献 |
[1]. Ma L, et al. Luteolin exerts an anticancer effect on NCI-H460 human non-small cell lung cancer cells through the induction of Sirt1-mediated apoptosis. Mol Med Rep. 2015 Sep;12(3):4196-4202.
[2]. Abu-Elsaad N, et al. Protection against nonalcoholic steatohepatitis through targeting IL-18 and IL-1alpha by luteolin. Pharmacol Rep. 2019 Aug;71(4):688-694. [3]. Xiuwen Tang, et al. Luteolin inhibits Nrf2 leading to negative regulation of the Nrf2/ARE pathway and sensitization of human lung carcinoma A549 cells to therapeutic drugs. Free Radic Biol Med. 2011 Jun 1;50(11):1599-609. |
| 其他信息 |
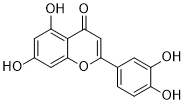
木犀草素是一种四羟基黄酮,其四个羟基分别位于3'、4'、5和7位。它被认为在人体内发挥着重要作用,具有抗氧化、清除自由基、抗炎和调节免疫系统的功能,并且对多种癌症具有活性。它还具有多种功能,包括作为EC 2.3.1.85(脂肪酸合成酶)抑制剂、抗肿瘤剂、血管内皮生长因子受体拮抗剂、植物代谢产物、肾脏保护剂、血管生成抑制剂、c-Jun N端激酶抑制剂、抗炎剂、细胞凋亡诱导剂、自由基清除剂和免疫调节剂。它是一种3'-羟基黄酮和四羟基黄酮。它是木犀草素-7-醇盐的共轭酸。
据报道,木犀草素存在于茶树(Camellia sinensis)、党参(Codonopsis lanceolata)和其他有相关数据的生物体中。 木犀草素是一种天然存在的黄酮类化合物,具有潜在的抗氧化、抗炎、诱导细胞凋亡和化学预防活性。给药后,木犀草素可清除自由基,保护细胞免受活性氧(ROS)引起的损伤,并直接诱导肿瘤细胞的细胞周期阻滞和凋亡。这可以抑制肿瘤细胞增殖并抑制转移。 铋矿是一种矿物,其化学式为Bi3+2O3或Bi2O3。国际矿物学协会(IMA)的符号为Bis。 5,7,3',4'-四羟基黄酮,属于黄酮类化合物。 另见:黄酮(亚类);洋甘菊(成分之一)。胡芦巴籽(部分)... 查看更多... 作用机制: - 抗癌(非小细胞肺癌):木犀草素上调 Sirt1,使 p53 去乙酰化并激活 caspase 依赖性凋亡途径,抑制细胞增殖并诱导细胞凋亡 [1] - 抗非酒精性脂肪性肝炎:木犀草素抑制肝脏 IL-18/IL-1α 表达,减少炎症细胞浸润和肝细胞损伤;它还能通过调节脂肪酸代谢来减少脂质积累[2] - 化疗增敏(肺癌):木犀草素抑制Nrf2核转位及其下游抗氧化基因(HO-1、NQO1),逆转Nrf2介导的化疗耐药性并增强顺铂诱导的细胞死亡[3] - 治疗潜力:木犀草素是一种天然黄酮类化合物(存在于蔬菜、水果和草药中),具有以下潜在应用:(1)通过诱导细胞凋亡治疗非小细胞肺癌;(2)通过抗炎和抗脂肪变性作用治疗非酒精性脂肪性肝炎; (3) 增强耐药肺癌的化疗敏感性 [1, 2, 3] - 与合成药物相比的优势:木犀草素对正常细胞/组织的毒性较低,与合成化疗药物或抗炎药物相比,是长期抗炎或抗癌治疗更安全的选择 [1, 2] - 局限性:木犀草素水溶性差,这可能限制其口服生物利用度;需要采用制剂策略(例如纳米载体)来改善其递送 [3] |
| 分子式 |
C15H10O6
|
|
|---|---|---|
| 分子量 |
286.24
|
|
| 精确质量 |
286.047
|
|
| 元素分析 |
C, 62.94; H, 3.52; O, 33.54
|
|
| CAS号 |
491-70-3
|
|
| 相关CAS号 |
Luteolin (Standard);491-70-3; 6113-16-2 (hydrate)
|
|
| PubChem CID |
5280445
|
|
| 外观&性状 |
Light yellow to yellow solid powder
|
|
| 密度 |
1.7±0.1 g/cm3
|
|
| 沸点 |
616.1±55.0 °C at 760 mmHg
|
|
| 熔点 |
~330 °C(lit.)
|
|
| 闪点 |
239.5±25.0 °C
|
|
| 蒸汽压 |
0.0±1.8 mmHg at 25°C
|
|
| 折射率 |
1.768
|
|
| 来源 |
Camellia sinensis, Codonopsis lanceolata, and other organisms; Escherichia coli
|
|
| LogP |
2.4
|
|
| tPSA |
111.13
|
|
| 氢键供体(HBD)数目 |
4
|
|
| 氢键受体(HBA)数目 |
6
|
|
| 可旋转键数目(RBC) |
1
|
|
| 重原子数目 |
21
|
|
| 分子复杂度/Complexity |
447
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
O1C(=C([H])C(C2=C(C([H])=C(C([H])=C12)O[H])O[H])=O)C1C([H])=C([H])C(=C(C=1[H])O[H])O[H]
|
|
| InChi Key |
InChI=1S/C15H10O6/c16-8-4-11(19)15-12(20)6-13(21-14(15)5-8)7-1-2-9(17)10(18)3-7/h1-6,16-19H
|
|
| InChi Code |
InChI=1S/C15H10O6/c16-8-4-11(19)15-12(20)6-13(21-14(15)5-8)7-1-2-9(17)10(18)3-7/h1-6,16-19H
|
|
| 化学名 |
2-(3,4-Dihydroxyphenyl)-5,7-dihydroxy-4-benzopyroneInChi Key:IQPNAANSBPBGFQ-UHFFFAOYSA-N
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (7.27 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 配方 2 中的溶解度: 20 mg/mL (69.87 mM) in 50% PEG300 50% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶. *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.4936 mL | 17.4679 mL | 34.9357 mL | |
| 5 mM | 0.6987 mL | 3.4936 mL | 6.9871 mL | |
| 10 mM | 0.3494 mL | 1.7468 mL | 3.4936 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT05204407 | Recruiting | Dietary Supplement: Luteolin Dietary Supplement: Placebo |
Schizophrenia Schizoaffective Disorder |
University of Maryland, Baltimore | June 13, 2022 | Not Applicable |
| NCT06047899 | Not yet recruiting | Dietary Supplement: Luteolin Other: Placebo |
Memory | Prof. Dominique de Quervain, MD | November 28, 2023 | Not Applicable |
| NCT04468854 | Terminated | Dietary Supplement: Luteolin Other: Placebo |
Memory | University of Basel | January 1, 2020 | Not Applicable |
| NCT03444558 | Completed | Dietary Supplement: Natural supplement containing chlorogenic acid and luteolin |
Metabolic Syndrome | University of Palermo | June 1, 2017 | Not Applicable |
|
|---|
|
|