| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
NK1/neurokinin receptor
|
|---|---|
| 体内研究 (In Vivo) |
以1 mg/kg剂量枸橼酸马罗匹坦治疗的小鼠,其溃疡性皮炎病变显著减小。静脉注射马罗匹坦可使最低肺泡浓度降低16%。相比之下,硬膜外注射生理盐水或马罗匹坦后,最低肺泡浓度(分别为2.17%和1.92%)保持不变。S组的所有犬只均出现了呕吐(6/9)、干呕(1/9)或恶心症状(2/9)。M组中则没有犬只出现呕吐、干呕或恶心症状。与S组相比,M组犬只的呕吐发生率(p=0.0090)、呕吐和干呕发生率(p=0.0023)以及呕吐、干呕和恶心的综合发生率(p<0.0001)均显著降低。
结论与临床相关性:马罗匹坦能够预防犬只因肌肉注射氢吗啡酮所引起的呕吐、干呕和恶心。[1] 在比格犬中评估了马罗匹坦的药代动力学特性,试验犬每日一次口服赛瑞宁®片剂(辉瑞动物保健),剂量分别为2 mg/kg体重或8 mg/kg体重,连续给药14天。对血浆浓度数据进行非房室模型药代动力学分析,以测定AUC(0-24)(首次和末次给药后)、Ct(谷浓度,每次给药后24小时测定)、Cmax(首次和末次给药后)、tmax(首次和末次给药后)、λz(终末处置速率常数;末次给药后)、t(1/2)(末次给药后)和CL/F(口服清除率;末次给药后)。每日给予8 mg/kg剂量连续十四天后,马罗匹坦在血浆中的蓄积程度显著高于每日给予2 mg/kg剂量连续十四天,这反映在AUC(0-24)的蓄积比率上,8 mg/kg剂量组为4.81,而2 mg/kg剂量组为2.46。这很可能是由于先前已证实的马罗匹坦非线性药代动力学特性所致,即高剂量(8 mg/kg)会使其代谢清除机制饱和,从而延缓药物消除。为确定达到稳态马罗匹坦血浆浓度所需的时间,对各治疗组马罗匹坦Ct值的最小二乘均值拟合了非线性模型。基于此模型,每日口服2 mg/kg剂量组达到90%稳态约需四次给药,而每日口服8 mg/kg剂量组则需要八次给药。[2] |
| 动物实验 |
纳入研究的犬只需满足以下条件:年龄大于1岁、健康且计划接受择期骨科手术。犬只被随机分配接受两种皮下注射治疗方案之一。M组在麻醉前1小时接受1.0 mg/kg的马罗匹坦,S组接受0.1 mL/kg的生理盐水。所有犬只均接受0.1 mg/kg的氢吗啡酮肌注作为术前用药。一位不知晓分组情况的观察者记录了术前用药后30分钟内犬只是否出现呕吐、干呕和/或恶心症状。[1]
分析阶段[2] 采用改进的HPLC-MS/MS方法(结合UPLC技术)测定血浆样本中的马罗匹坦及其主要羟基化叔丁基代谢物(CJ-18,518)。结果表明,根据辉瑞动物保健标准操作规程(SOP),该方法具有可接受的准确度和精密度(±15%,定量下限(LLOQ)处可接受±20%)。在该检测中,将400 μL含有内标(分子量为454.66的马罗匹坦类似物,浓度为5 ng/mL)的乙腈溶液加入到100 μL犬血浆样品中以沉淀蛋白质。样品涡旋混匀后离心,取10 μL上清液转移至含有790 μL稀释液(50/50乙腈/水,含0.1%甲酸)的洁净96孔聚丙烯板中。每个样品取6 μL注入配备Waters ACQUITY BEH C18色谱柱(1.7 μm,2.1 × 50 mm)的Waters ACQUITY UPLC®系统进行分析。流动相为90% 5 mM甲酸铵(含0.3%甲酸)和10%(B)乙腈(含0.3%甲酸),保持0.2 min,然后梯度洗脱至99.9% B(历时1.8 min),保持2 min,再洗脱至10% B(历时0.1 min),保持0.9 min。整个运行过程中流速为0.6 mL/min。检测采用API 4000 MS/MS系统(Applied Biosystems,美国加利福尼亚州福斯特城),在正离子电喷雾模式下进行,监测马罗匹坦的母离子→子离子跃迁469→177、主要代谢物的母离子→子离子跃迁485→193和内标物的母离子→子离子跃迁455→163。峰色谱图的积分在 Analyst 软件(v1.4.2,Applied Biosystems)中进行,原始数据导入 Watson LIMS(v7.2.0.03,Thermo Electron Corp.,美国宾夕法尼亚州费城)。线性回归采用 1/浓度² 的加权因子。所有计算均在 Watson 中完成。在前两次分析运行中,马罗匹坦及其主要代谢物的分析范围均为 1.00 ng/mL 至 1000 ng/mL,在最后一次运行中为 1.00 ng/mL 至 100 ng/mL。在前两次分析运行中,质控样品(添加已知量各分析物的基质样品)的浓度分别为 3 ng/mL、30 ng/mL 和 800 ng/mL,在最后一次运行中为 3 ng/mL 和 30 ng/mL。由于最高浓度的两个标准品和高浓度质控品未达到可接受的限度,分析运行 3 的标准曲线被截断至定量上限 (ULOQ) 100 ng/mL。这并未影响样本结果,因为分析运行 3 仅包含一个复测样本,其值接近标准曲线的下限。预计 8 mg/kg 治疗组的样本浓度将达到或接近 ULOQ,因此在用空白血浆稀释五倍后进行检测。分析运行中包含了适当的稀释度质控品,所有样本均进行了三次分析。马罗匹坦的批间质控偏差范围为 -5.0% 至 -2.7%,最大变异系数为 5.2%;代谢物的批间质控偏差范围为 -7.0% 至 -5.0%,最大变异系数为 6.2%。在犬血浆中,马罗匹坦及其代谢物在-20°C下储存时分别稳定182天和181天,在室温下储存时至少稳定24小时(内部数据)。药代动力学阶段[2] 使用Watson(v7.2.0.03)软件,采用非房室模型,以标称采样时间和剂量估算药代动力学参数。血浆浓度-时间曲线下面积(AUC)的估算采用梯形求和法。对于每只动物,在指定剂量下测定了以下马罗匹坦及其代谢物的药代动力学参数:[2] 首次和末次给药后24小时的Ct;[2] [2] 末次给药后测定λz(末端处置速率常数)、CL/F(口服清除率——仅适用于马罗匹坦)和t1/2(消除半衰期)。λz和t1/2通过对数转换数据进行线性回归,并根据浓度-时间曲线末端部分的斜率估算得出。CL/F通过将实际剂量除以实际AUC0-24来确定。[2] |
| 参考文献 |
|
| 其他信息 |
马罗匹坦(以柠檬酸马罗匹坦的形式使用)是一种神经激肽受体拮抗剂,由硕腾公司专门为治疗犬的晕动病和呕吐而开发。它于2007年获得美国食品药品监督管理局(FDA)批准用于犬,最近也获准用于猫。
另见:柠檬酸马罗匹坦(有盐形式)无水柠檬酸马罗匹坦(是其活性成分)。 适应症 犬:用于治疗和预防化疗引起的恶心;用于预防除晕动病引起的呕吐;用于治疗呕吐,并与其他辅助治疗措施联合使用;用于预防围手术期恶心和呕吐,并改善使用α-阿片受体激动剂吗啡后全身麻醉的恢复。猫:用于预防呕吐和减轻恶心,但晕动病引起的恶心除外;用于治疗呕吐,并与其他辅助治疗措施联合使用。 片剂 犬:用于预防化疗引起的恶心;用于预防晕动病引起的呕吐;用于预防和治疗呕吐,并与其他辅助治疗措施联合使用,以及与注射用塞瑞尼亚溶液联合使用。注射液 犬:用于治疗和预防化疗引起的恶心。用于预防呕吐(晕动病引起的呕吐除外)。用于治疗呕吐,需与其他辅助治疗措施联合使用。用于预防围手术期恶心和呕吐,并改善使用α-阿片受体激动剂吗啡后全身麻醉的恢复。猫:用于预防呕吐和减轻恶心(晕动病引起的恶心除外)。用于治疗呕吐,需与其他辅助治疗措施联合使用。 |
| 分子式 |
C32H40N2O
|
|---|---|
| 分子量 |
468.6728
|
| 精确质量 |
468.314
|
| 元素分析 |
C, 82.01; H, 8.60; N, 5.98; O, 3.41
|
| CAS号 |
147116-67-4
|
| 相关CAS号 |
Maropitant-13C,d3; 359875-09-5 (citrate hydrate); 862543-54-2 (citrate)
|
| PubChem CID |
204108
|
| 外观&性状 |
White solid powder
|
| LogP |
6.706
|
| tPSA |
24.5
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
8
|
| 重原子数目 |
35
|
| 分子复杂度/Complexity |
620
|
| 定义原子立体中心数目 |
2
|
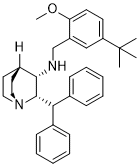
| SMILES |
CC(C)(C)C1=CC=C(OC)C(CN[C@@H]2[C@H](C(C3=CC=CC=C3)C4=CC=CC=C4)N5CCC2CC5)=C1
|
| InChi Key |
OMPCVMLFFSQFIX-CONSDPRKSA-N
|
| InChi Code |
InChI=1S/C32H40N2O/c1-32(2,3)27-15-16-28(35-4)26(21-27)22-33-30-25-17-19-34(20-18-25)31(30)29(23-11-7-5-8-12-23)24-13-9-6-10-14-24/h5-16,21,25,29-31,33H,17-20,22H2,1-4H3/t30-,31-/m0/s1
|
| 化学名 |
(2S,3S)-2-benzhydryl-N-[(5-tert-butyl-2-methoxyphenyl)methyl]-1-azabicyclo[2.2.2]octan-3-amine
|
| 别名 |
Maropitant; CJ-11972; CJ 11972; CJ11972; CJ-11,972; CJ 11,972; CJ11,972; brand name: Cerenia
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: ~25 mg/mL (~53.3 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (5.33 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL 澄清 DMSO 储备液加入900 μL 玉米油中,混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.1337 mL | 10.6685 mL | 21.3370 mL | |
| 5 mM | 0.4267 mL | 2.1337 mL | 4.2674 mL | |
| 10 mM | 0.2134 mL | 1.0668 mL | 2.1337 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
|
|