| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|

| 靶点 |
Methoxatin (Pyrroloquinolinequinone, PQQ) is identified as the tightly bound, likely covalent, organic cofactor in copper-containing amine oxidases (EC 1.4.3.6). [1]
Methoxatin (Pyrroloquinolinequinone, PQQ) is suggested to be a component, possibly a free agent, involved in the NADPH oxidase system that drives superoxide (O₂⁻) production in phagocytes (e.g., neutrophils). Its exact role within the multicomponent oxidase complex is not fully stipulated. [2] |
|---|---|
| 体外研究 (In Vitro) |
吡咯喹啉醌二钠盐会促进出生幼鼠和母鼠坚果的免疫反应恶化、脱发、驼背姿势和主动脉瘤易感性[2]。
Methoxatin (PQQ) 在体外可以催化氧化还原循环。在过量还原剂(如甘氨酸盐)存在下,于生理 pH 和有氧条件下,PQQ 能将 NADPH 氧化为 NADP⁺,自身被还原为其半醌形式 (PQQH⁻),随后将氧气还原为超氧化物 (O₂⁻)。这表明 PQQ 可能作为一种 NADPH 氧化酶,直接将电子传递给氧气。[2] 有机阳离子二亚苯基碘𬭩 (DPI) 和二苯基碘𬭩 (BPI),以及芳香邻二胺 4,5-二甲基苯二胺 (DIMPDA),在模型硝基蓝四唑 (NBT) 测定中被证明可以隔离合成的 PQQ 并抑制其氧化还原循环活性。抑制 33 nM PQQ 溶液氧化还原循环能力 50% 所需的 DIMPDA 浓度为 100 µM。碘𬭩化合物达到 50% 抑制所需的浓度分别为:BPI 10 µM,DPI 1.5 µM。[2] |
| 酶活实验 |
本研究采用共振拉曼光谱法探测牛血浆胺氧化酶中有机辅因子的结构。使用 2,4-二硝基苯肼对酶进行衍生化:将过量 10% 摩尔的 DNPH(溶解在无水乙醇中)加入到溶解于 0.1 M 磷酸钾缓冲液(pH 7.2)中的酶溶液中,在室温下孵育 16 小时。蛋白浓度范围为 0.07 至 0.11 mM。随后测量所得 BPAO-DNPH 加合物的共振拉曼光谱,并与模型化合物(包括纯品 methoxatin (PQQ)、吡哆醛、1,10-菲咯啉-5,6-二酮、1,7-菲咯啉-5,6-二酮和 2-吡啶甲醛)的 DNPH 衍生物光谱进行详细比较。BPAO-DNPH 与 PQQ-DNPH 光谱的振动频率高度吻合,尤其是在指纹区(300-600 cm⁻¹,660-800 cm⁻¹ 和 1300-1700 cm⁻¹),这为“该辅因子是 PQQ 或极其相似的衍生物”的结论提供了有力证据。[1]
采用甘氨酸-硝基蓝四唑 (NBT) 测定法测量 PQQ 水平并评估其氧化还原循环活性。测定混合物包含待分析样品、还原牛血清白蛋白以及溶于 2 M 甘氨酸溶液 (pH 10) 中的 NBT。总反应体积为 1.5 ml。混合物在 25°C 下避光孵育 1 小时。在此系统中,PQQ 氧化甘氨酸,还原态的 PQQ 将氧气还原为超氧化物,后者再将 NBT 还原为紫色二甲臜。通过测量 550 nm 处生成的甲臜量,并对照标准曲线进行定量,可以放大信号,从而检测到皮摩尔水平的 PQQ。该测定法也用于证明 DPI、BPI 和 DIMPDA 对 PQQ 氧化还原循环的抑制作用。[2] |
| 细胞实验 |
采用标准的铁细胞色素 c 测定法测量佛波醇肉豆蔻酸乙酸酯 (PMA) 刺激的豚鼠中性粒细胞产生的超氧化物 (O₂⁻)。简言之,将 900 µl 含有葡萄糖、钙和镁的磷酸盐缓冲盐水加入 100 µl 细胞悬液 (3 x 10⁷ 个细胞) 中。向对照管中加入超氧化物歧化酶 (SOD, 2 µg/ml)。加入抑制剂 (DPI、BPI、DIMPDA) 和/或 PQQ,混合物在 37°C 下孵育 5 分钟。然后加入细胞色素 c 溶液,随后用 PMA (5 µl,1 mg/ml DMSO 溶液) 刺激 5 分钟。超氧化物产量通过铁细胞色素 c 的 SOD 敏感性还原来测量。[2]
为了研究细胞中 PQQ 的存在,将豚鼠中性粒细胞与氚标记的抑制剂 ([³H]DIMPDA 或 [³H]DPI) 一起孵育。将悬浮于含有钙、镁和葡萄糖的 PBS 中的细胞 (1 x 10⁸) 与 1 mM [³H]DIMPDA 或 5-10 µM [³H]DPI 在 37°C 下孵育 5 分钟,然后用 PMA 刺激 90 秒。随后将细胞冷却、洗涤并处理以分离加合物。[2] 为了从细胞中分离 PQQ-抑制剂加合物,将处理并洗涤后的细胞进行超声破碎。将超声破碎物进行超速离心。上清液通过超滤器,超滤液用水饱和的乙酸乙酯萃取。含有水溶性加合物的水相被保留用于 HPLC 分析。[2] |
| 动物实验 |
从豚鼠腹膜中收集中性粒细胞。简而言之,将30 ml 12%酪蛋白酸钠溶液腹腔注射到500 g Hartley豚鼠体内。打开腹膜,收集诱导产生的中性粒细胞,用冷生理盐水冲洗,用尼龙纱布过滤,并通过离心沉淀。将沉淀物短暂悬浮于水中以裂解红细胞,然后立即用9%生理盐水恢复至等渗状态。洗涤中性粒细胞,重悬于磷酸盐缓冲液(PBS)中,并调整浓度至3 x 10⁷个细胞/5 ml。细胞制备物中中性粒细胞含量>90%,台盼蓝染色排除法检测细胞活力>90%。[2]
|
| 药代性质 (ADME/PK) |
文中指出,先前的研究(本研究未详细阐述)表明,给大鼠服用[¹⁴C]-PQQ后,药物会被小肠吸收并经尿液排出,剩余部分则浓缩于红细胞和白细胞中。[2]
|
| 毒性/毒理 (Toxicokinetics/TK) |
文中提到,缺乏PQQ的母鼠所产幼鼠,以及哺乳期幼鼠,均表现出免疫反应受损、脱发、弓背姿势以及易患主动脉瘤等症状,表明膳食缺乏会导致这些后果。本研究未提供关于PQQ的急性毒性、LD₅₀、器官毒性或药物相互作用的数据。[2]
|
| 参考文献 | |
| 其他信息 |
甲氧沙汀 (PQQ) 含有亲电羰基,并表现出单电子和双电子氧化还原化学性质,这与胺氧化酶的催化机制相关,其中连续的单电子步骤可能参与 O₂ 的再氧化。[1] 甲氧沙汀 (PQQ) 作为哺乳动物酶的辅因子被鉴定出来,这提示它可能是一种此前未被发现的维生素。[1] 本文所述的共振拉曼光谱方法展示了一种强大的结构研究方法,可在接近天然的条件下研究蛋白质结合的生色团(如甲氧沙汀 (PQQ))的结构,而无需分离辅因子。[1] 本研究从豚鼠中性粒细胞中分离出了甲氧沙汀 (PQQ)。 [2]
PQQ 被描述为一种阴离子型、水溶性、可进行氧化还原循环的邻醌。在哺乳动物系统中,它似乎以游离形式存在且可透析,已在细胞裂解液、生物体液和鸡蛋中检测到。[2] PQQ 被认为是哺乳动物的必需营养素,对免疫功能至关重要。[2] 在动物实验中,PQQ 已被证实能够保护大鼠免受氧化损伤、毒性损伤以及缺血再灌注损伤(在中风大鼠模型中)。[2] 抑制剂 DPI、BPI 和 DIMPDA 可阻断 PMA 刺激的豚鼠中性粒细胞释放 O₂⁻。向细胞悬液中添加外源性 PQQ 可以解除(逆转)这种阻断作用。 [2] 1 µM 的 DPI 可抑制中性粒细胞超氧化物生成 74%,50 µM 的 BPI 可抑制 64%,200 µM 的 DIMPDA 可抑制 50%。DIMPDA 和 DPI 的抑制作用可通过洗涤细胞逆转,且可逆程度与抑制剂-PQQ 键的性质相关(DPI 为非共价键)。[2] 从豚鼠中性粒细胞中分离出 [³H]DPI-PQQ 加合物和 [³H]DIMPDA-PQQ 加合物,并用高效液相色谱法与标准品进行共色谱分析。用螯合剂 Tiron 处理分离出的 [³H]DPI-PQQ 加合物可破坏该加合物并释放游离的 PQQ。 [2] 根据从加合物中回收的放射性,计算得出中性粒细胞中PQQ的浓度约为每10⁸个细胞30 nmol。[2] |
| 分子式 |
C14H4N2NA2O8
|
|---|---|
| 分子量 |
374.1697
|
| 精确质量 |
373.976
|
| CAS号 |
122628-50-6
|
| 相关CAS号 |
Pyrroloquinoline quinone;72909-34-3
|
| PubChem CID |
3078772
|
| 外观&性状 |
Pink to red solid powder
|
| 沸点 |
1018.6ºC at 760mmHg
|
| 闪点 |
569.8ºC
|
| 蒸汽压 |
0mmHg at 25°C
|
| tPSA |
180.38
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
9
|
| 可旋转键数目(RBC) |
1
|
| 重原子数目 |
26
|
| 分子复杂度/Complexity |
636
|
| 定义原子立体中心数目 |
0
|
| SMILES |
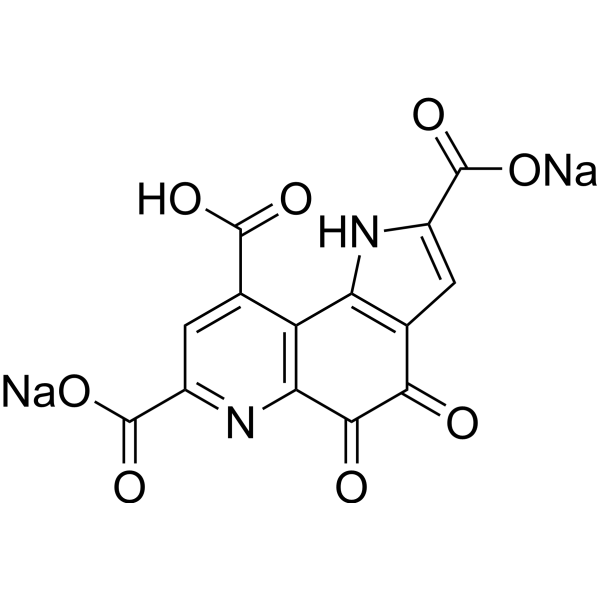
[Na+].[Na+].O=C1C(C2=C(C(C(=O)[O-])=C([H])C(C(=O)[O-])=N2)C2=C1C([H])=C(C(=O)O[H])N2[H])=O
|
| InChi Key |
UFVBOGYDCJNLPM-UHFFFAOYSA-L
|
| InChi Code |
InChI=1S/C14H6N2O8.2Na/c17-10-4-2-6(14(23)24)15-8(4)7-3(12(19)20)1-5(13(21)22)16-9(7)11(10)18;;/h1-2,15H,(H,19,20)(H,21,22)(H,23,24);;/q;2*+1/p-2
|
| 化学名 |
disodium;2-carboxy-4,5-dioxo-1H-pyrrolo[2,3-f]quinoline-7,9-dicarboxylate
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
H2O : ~1.25 mg/mL (~3.34 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 2 mg/mL (5.35 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶。 (<60°C).
配方 2 中的溶解度: 5 mg/mL (13.36 mM) in 0.5% CMC-Na/saline water (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.6726 mL | 13.3629 mL | 26.7258 mL | |
| 5 mM | 0.5345 mL | 2.6726 mL | 5.3452 mL | |
| 10 mM | 0.2673 mL | 1.3363 mL | 2.6726 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。