| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
GPR55
|
|---|---|
| 体外研究 (In Vitro) |
O-1602在体外引起非cb1 / cb2介导的血管扩张。介导O-1602作用的作用机制仍在争论中。多篇报道发现O-1602可激活七跨膜G蛋白偶联受体GPR55,提示GPR55可能是一种新型大麻素受体。然而,GPR55的药理学经常提供相互矛盾的结果,可能是因为GPR55配体的活性受到所采用的功能测定的影响。[2]
与对照相比,O‐1602显著提高了hNSCs的增殖率。[3] |
| 体内研究 (In Vivo) |
中枢和外周给药O-1602会剧烈刺激食物摄入,并长期增加肥胖。O-1602的贪食作用是由可卡因和安非他明调控的厌氧性神经肽转录物的mRNA和蛋白水平下调介导的。对脂肪量的影响与食物摄入无关,涉及到白色脂肪组织中脂溶酶(如激素敏感脂肪酶和脂肪甘油三酯脂肪酶)表达的减少。与此一致的是,体外数据显示O-1602增加了脂肪细胞内钙和脂质积累的水平。最后,我们将O-1602注射到GPR55−/−小鼠中,发现O-1602能够诱导GPR55缺失小鼠的摄食行为。
结论:这些发现表明O-1602独立于GPR55受体调节食物摄入和肥胖。因此,非典型大麻素可能代表了一类参与能量平衡的新分子。[2]
GPR55激动剂O-1602抑制冰毒诱导的焦虑和抑郁样行为;O-1602激活GPR55可预防海马神经发生损伤;O-1602激活GPR55可抑制小胶质细胞的激活,减轻神经炎症。腹腔注射O-1602可预防慢性社交失败引起的焦虑和抑郁。与以往研究一致,我们的研究抑制了GPR55, O-1602激活GPR55可以缓解冰毒引起的焦虑和抑郁样行为;这些发现表明,内源性大麻素系统参与了冰毒诱导的负面情绪。[1] 通过连接渗透泵的导管将O‐1602持续注入海马,导致齿状回内Ki67+细胞增加。通过DCX+和BrdU+细胞的评估,O‐1602增加了未成熟神经元的生成,与载药处理的动物相比。与对照相比,GPR55−/−动物海马内的增殖和神经发生率降低,而O‐1602没有影响。[3] |
| 细胞实验 |
O‐1602对3T3-L1脂肪细胞内钙[(Ca2+)i]动员和分化的影响[2]
如前所述,3T3-L1细胞分化为脂肪细胞[28]。简单地说,将3T3-L1细胞培养在0.1 mg/ml聚赖氨酸包被的25 mM圆形盖片上,在Dulbecco's Modified Eagle培养基(DMEM)中添加10%胎牛血清(FBS)、4 mM谷氨酰胺和1%抗生素-抗菌溶液。在100%汇合(第0天),细胞在含有10% FBS、0.5 mM异丁基甲基黄嘌呤、0.25µM地塞米松和10µg/ml胰岛素的DMEM中孵育72小时(第3天)。之后,用含有10% FBS和10µg/ml胰岛素的DMEM替换培养基72小时(第6天),然后用不含胰岛素的DMEM交换,直到第10 - 12天,此时细胞被处理用于(Ca2+)i测量。分化后的3T3-L1细胞在含20 mM NaHCO3 (pH 7.4)的无酚红DMEM中加载2.5µM Fura-2AM和0.02% Pluronic F127,在37°C下加载30 min。然后用不含酚红的DMEM清洗细胞的盖片,安装在赛克斯-摩尔室中,放置在配有plano - fluor 40×油浸物镜的尼康Eclipse TE2000-E荧光显微镜的温控台上。细胞依次在340和380 nm处外照,每5秒照射100 ms,持续8-10分钟。使用metaflupc软件控制图像采集,在加入100µM O-1602之前(基线)和之后在505/510 nm处捕获荧光发射,使用后端薄电荷耦合装置冷却数码相机运行在一比特模式。(Ca2+)i的变化记录为相应激发波长的比值(F340/F380)。 O‐1602对3T3-L1细胞脂肪细胞分化的影响[2] 3T3-L1脂肪细胞分化过程在O-1602(10µM)存在或不存在的情况下进行,持续10天。在此期间,每2天更新一次治疗。第10天,细胞在多聚甲醛(4%)中固定15分钟,在60%异丙醇中彻底洗涤,并在Oil Red O溶液(Sigma, St. Louis, MO, USA)中培养30分钟。用H2O2洗掉多余的染料后,将板置于明场显微镜下,使用10倍物镜捕获随机场的照片。然后,用100%异丙醇孵育细胞10分钟洗脱油红O,在500 nm处测量光密度以估计染料掺入情况。在另一组分化的3T3-L1细胞中,我们分离RNA并测量脂肪细胞分化主要调控因子的基因表达,如下所述。 为了研究GPR55激活对hNSC增殖的影响,将细胞镀在层粘连蛋白包被的6孔板上。细胞粘附过夜,然后用LPI (1 μM), GPR55的内源性配体,或合成激动剂,O‐1602 (1 μM)或ML184 (1 μM),在降低生长因子培养基(5%生长因子)中处理。减少生长因子培养基被用来更好地模拟低增殖表型,同时仍然保持“干性”状态。流式细胞术分析显示,48小时后巢蛋白+或Sox2+群体没有显著减少(数据未显示)。用GPR55选择性拮抗剂ML193 (5 μM)处理的细胞在加入激动剂之前预处理30分钟。载体处理的细胞在5%的生长因子培养基中接受0.1%的DMSO。在分化研究中,细胞在不含生长因子的ReNcell培养基中分别用ML184 (1 μM)、ML193 (5 μM)或ML184 (1 μM)和ML193 (5 μM)的组合处理。[3] |
| 动物实验 |
研究人员通过系统性注射GPR55激动剂O-1602,观察GPR55激活的效果。剂量和给药途径参考既往文献。小鼠被随机分为载体组、甲基苯丙胺(METH)组和O-1602+METH组。经过7天的适应期后,METH组和O-1602+METH组的小鼠连续14天每天腹腔注射一次10 mg/kg的METH,而对照组小鼠则注射等体积的生理盐水。在14天的METH治疗期间,O-1602+METH组的小鼠在每次METH注射前30分钟额外腹腔注射10 mg/kg的O-1602,而载体组和METH组的小鼠则注射等体积的生理盐水。METH治疗结束后,进行为期2天的停药期。次日,在光照周期内连续4天进行行为学测试。[1]
\n\n急性O-1602注射的代谢效应[2] \n为研究急性外周效应,大鼠单次腹腔注射赋形剂[5%二甲基亚砜(DMSO)]或O-1602,剂量分别为2、20和200 µg/kg体重。为研究急性中枢效应,大鼠单次脑室内(icv)注射赋形剂(5% DMSO)或O-1602,剂量分别为0.02、0.1、0.5、1、5和10 µg/只。在两项实验中,分别于注射O-1602后1、2、4、6和24小时测量食物摄入量。为了准确了解每只大鼠的食物摄入量,我们按照给大鼠注射载体或 O-1602 的顺序称量了食物。此外,我们还称量了食物的洒落量。 \n\n亚慢性 O-1602 输注的代谢效应[2] \n为了评估 O-1602 的代谢效应,我们在外周和中枢水平进行了为期 1 周的亚慢性输注。在外周水平,我们连续 7 天每天腹腔注射 O-1602,剂量分别为 0.1、0.5 和 1 mg/kg 体重。对于亚慢性中枢输注 O-1602 的实验,将大鼠麻醉后,采用立体定位技术,在侧脑室植入慢性脑室内插管,坐标如下:前囟后方 1.3 mm,中矢状缝外侧 1.9 mm,深度 3.5 mm(如前所述)。将导管从脑内输注插管连接至渗透泵流量调节器(型号 2001D 或 2ML2)。采用钝性分离法在大鼠背部皮下形成一个囊袋,并将渗透泵插入其中。缝合切口,并保持大鼠体温直至完全恢复。随后,分别向大鼠输注载体或 O-1602(1、10 和 100 µg/天),持续 7 天。在给予外周和中枢 O-1602 后,评估了食物摄入量、体重、身体成分和脂肪细胞代谢。使用核磁共振 (NMR) 成像技术测量了输注 O-1602 的大鼠的身体成分。测量在手术前和治疗期结束后处死前进行。 \n\n急性注射 O-1602 对 GPR55 缺陷小鼠的代谢影响[2] \n为了检验 O-1602 的促食作用是否特异性地由 GPR55 介导,对缺乏 GPR55 的小鼠分别腹腔注射载体(50% DMSO)或 O-1602,剂量分别为 200 µg/kg 体重和 2 µg/kg 体重。在注射 O-1602 后 1、2、4、6 和 24 小时测量食物摄入量。 \n\n海马内注射[3] \n动物用异氟烷麻醉,并固定在立体定位仪上。异氟烷以蒸汽吸入,诱导浓度为 4-5%,维持浓度为 1.5-2%。立体定位坐标以 Bregma 为参考点(单位:毫米)计算,前后方向 -2.0,内外方向 +1.5,背腹方向 -1.5。将载体[人工脑脊液(ACSF,Tocris Bioscience),0.05%乙醇]或O-1602(O-1602先用100%乙醇稀释,再用ACSF进一步稀释,最终乙醇浓度不超过0.05%)通过不锈钢套管(Alzet Durect,美国加利福尼亚州库比蒂诺;脑灌注套件3)注入体内。该套管通过聚乙烯管连接至渗透泵(Alzet Durect,型号1002)。为确保植入后立即开始灌注,泵在37℃下用无菌生理盐水预充过夜。灌注期为连续14天。灌注剂量设定为4 μg·kg⁻¹·day⁻¹。选择 O-1602 进行体内治疗的原因是 ML184 是一种哌嗪类化合物,其结构与葛兰素史克公司生产的另一种苯甲酰哌嗪类 GPR55 激动剂 (GSK494581A) 相似,后者对人 GPR55 有活性,但对啮齿动物 GPR55 无活性 (Brown et al., 2011)。 \n体内实验中,O-1602 的母液用 100% 乙醇 (EtOH) 配制。所有母液均分装后储存于 -20°C。 |
| 参考文献 |
|
| 其他信息 |
甲基苯丙胺是一种强效且高度成瘾的神经毒性精神兴奋剂,戒断期间会引发一系列不良情绪反应。G蛋白偶联受体55 (GPR55) 是一种新型内源性大麻素受体,与情绪调节密切相关。本文构建了甲基苯丙胺诱导的小鼠戒断期焦虑和抑郁样行为模型,结果显示海马中GPR55表达降低。激活GPR55可减轻这些行为症状,同时改善海马神经发生受损并减少神经炎症。这些发现强调了GPR55在介导甲基苯丙胺戒断的神经心理后果中的关键作用,其机制可能涉及调节海马神经发生和炎症。[1] 目的:已知大麻素可控制能量稳态。非典型大麻素通过未知的靶点产生药理作用。我们旨在研究非典型大麻素 O-1602 是否调控食物摄入和体重。方法:对大鼠进行急性或亚慢性 O-1602 注射,并通过实时聚合酶链式反应 (RT-PCR) 检测脂肪细胞代谢相关因子的表达。体内实验结果与体外实验结果相符,体外实验中,将 3T3-L1 脂肪细胞与 O-1602 孵育,并测量细胞内钙离子和脂质的积累。最后,由于一些报道表明 O-1602 是假定的大麻素受体 GPR55 的激动剂,我们在 GPR55 基因敲除小鼠中进行了测试。[2]
背景和目的:大麻素系统对神经干细胞 (NSC) 增殖和成年神经发生具有功能性调控作用,但并非所有观察到的类大麻素化合物的作用都可归因于大麻素 1 (CB1) 或 CB2 受体。最近被重新鉴定的GPR55受体已被证实可被多种大麻素配体激活,这表明GPR55是第三种大麻素受体。本研究探讨了GPR55激活在神经干细胞(NSC)增殖和早期成年神经发生中的作用。实验方法:采用流式细胞术评估GPR55激动剂(LPI、O-1602、ML184)对体外培养的人(h)NSC增殖的影响。采用流式细胞术、qPCR和免疫组织化学方法检测人NSC的分化。采用免疫组织化学方法评估C57BL/6和GPR55-/-小鼠海马中未成熟神经元的形成。[3] |
| 分子式 |
C17H22O2
|
|---|---|
| 分子量 |
258.35538
|
| 精确质量 |
258.161
|
| 元素分析 |
C, 79.03; H, 8.58; O, 12.38
|
| CAS号 |
317321-41-8
|
| PubChem CID |
45073499
|
| 外观&性状 |
White to light yellow ointment
|
| 密度 |
1.1±0.1 g/cm3
|
| 沸点 |
401.6±45.0 °C at 760 mmHg
|
| 闪点 |
185.2±23.3 °C
|
| 蒸汽压 |
0.0±1.0 mmHg at 25°C
|
| 折射率 |
1.565
|
| LogP |
4.91
|
| tPSA |
40.46
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
2
|
| 可旋转键数目(RBC) |
2
|
| 重原子数目 |
19
|
| 分子复杂度/Complexity |
372
|
| 定义原子立体中心数目 |
2
|
| SMILES |
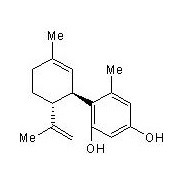
CC1=C[C@H]([C@@H](CC1)C(=C)C)C2=C(C=C(C=C2C)O)O
|
| InChi Key |
KDZOUSULXZNDJH-LSDHHAIUSA-N
|
| InChi Code |
InChI=1S/C17H22O2/c1-10(2)14-6-5-11(3)7-15(14)17-12(4)8-13(18)9-16(17)19/h7-9,14-15,18-19H,1,5-6H2,2-4H3/t14-,15+/m0/s1
|
| 化学名 |
5-methyl-4-[(1R,6R)-3-methyl-6-prop-1-en-2-ylcyclohex-2-en-1-yl]benzene-1,3-diol
|
| 别名 |
O-1602; 317321-41-8; 5-METHYL-4-[(1R,6R)-3-METHYL-6-(1-METHYLETHENYL)-2-CYCLOHEXEN-1-YL]-1,3-BENZENEDIOL; O 1602; 5-methyl-4-[(1R,6R)-3-methyl-6-prop-1-en-2-ylcyclohex-2-en-1-yl]benzene-1,3-diol; CHEMBL3402654; O1602; 59F4R2N5N5;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~387.06 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (9.68 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (9.68 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (9.68 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.8706 mL | 19.3528 mL | 38.7057 mL | |
| 5 mM | 0.7741 mL | 3.8706 mL | 7.7411 mL | |
| 10 mM | 0.3871 mL | 1.9353 mL | 3.8706 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。