| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
Metal remover
|
|---|---|
| 体外研究 (In Vitro) |
各种吸附剂可用于去除重金属和有毒金属,硅基材料最受欢迎。最近,人们对有机部分和介观结构材料的改性产生了相当大的兴趣,使其能够用作去除金属的有效吸附剂。在这项研究中,我们报告了通过后合成方法将四(4-羧基苯基)卟啉(TCPP)成功掺入介孔二氧化硅中。由于卟啉桥联基团的螯合性质,TCPP-SBA-15已被发现是从水溶液中去除Cu(II)的有效材料。对NH2-SBA-15二氧化硅和TCPP-SBA-15对铜(II)离子的吸附进行了比较研究。结果表明,TCPP-SBA-15材料的吸附容量高于NH2-SBA-15二氧化硅,在13 mmol g−1左右达到吸附最大值。[1]
NH2-SBA-15和TCPP-SBA-15的粉末低角度X射线衍射图如图1a所示。所有样品均显示出三个分辨率很高的衍射峰,其中一个非常强烈的峰位于0.9-1.18°的2θ处,两个峰位于1.4-1.8°的2°处。这些峰可以被标记为(1 0 0)、(1 1 0)和(2 0 0)平面,它们对应于六边形空间群对称p6mm的介观结构。TCPP-SBA-15的XRD图谱显示出强烈的(100)峰,这表明当TCPP在NH2-SBA-15上官能化时,介孔材料的骨架稳定性得到了很好的保持。TCPP-SBA-15图案中的(1 1 0)和(2 0 0)峰的相对强度低于NH2-SBA-15中的峰,从而表明卟啉分散在介孔通道中。发现所有材料的氮吸附-解吸等温线均为IV型曲线,具有明确的毛细管冷凝步骤,具有均匀介孔材料的特征(图1b)。通过使用BET方程从氮吸附等温线评估表面积。孔径是通过Barrett–Joyner–Halenda(BJH)方法使用吸附-解吸等温线的解吸分支计算的。NH2-SBA-15和TCPP-SBA-15的比表面积和中孔直径如表1所示。通过表面积和总孔体积的变化,可以看出掺入TCPP后中孔收缩的趋势,这表明TCPP组的加载会使中孔结构特征变差。[1] 傅里叶变换红外光谱(FT-IR)证实了TCPP掺入介孔二氧化硅中(图3)。在NH2-SBA-15的傅里叶变换红外光谱中,1628 cm-1附近的峰被归因于不对称NH2拉伸(νasNH2)和NH2变形(δNH2)[27],3300 cm-1处的宽峰可归因于仲胺(NH)拉伸(ɁNH)和对称NH2拉伸(?sNH2)之间的重叠。TCPP-SBA-15的FT-IR光谱在1713和1527 cm-1处显示峰值。这些峰分别归因于TCPP的C双键O伸缩振动和酰胺基的NH2变形(δNH2)。当TCPP的羧基与SBA-15上的氨基反应时,形成酰胺基。在该光谱中还观察到TCPP羧基的OH伸缩(3645 cm-1)、Si-O-Si晶格振动的泛音(1984和1850 cm-1)和CH2伸缩(2863和2929 cm-1)。[1] 紫外-可见光谱也证实了SBA-15上存在TCPP(图4)。TCPP光谱显示Soret带(417nm)和四个弱Q带。TCPP-SBA-15在414 nm(Soret带)和514、548、591和647 nm处显示吸收带。这一结果表明,在制备过程中,TCPP被官能化到SBA-15上(其特征是与大量TCPP相关的Soret带的蓝移)。当TCPP在SBA-15上官能化时,TCPP附近的极性增加,吸收带向更高能量的移动证明了这一点。[1] 脱金属反应后,分离并洗涤TCPP-SBA-15。洗涤后,进行紫外-可见光谱研究。含有吸附Cu(II)离子的TCPP-SBA-15的紫外-可见光谱与Cu-TCPP相似,在417nm处显示Soret带,在540和583nm处显示两个Q带。因此,观察到铜分子在TCPP中与中心氮配体螯合。 通过吸附实验研究了不同Cu(II)离子浓度(65至1065 mg L−1)下TCPP对介孔二氧化硅的影响。在相同条件下对不含TCPP的介孔二氧化硅进行了比较实验。吸附速率已使用方程式(1)进行分析,并绘制在图5中。Cu(II)浓度从65增加到1065 mg L−1,以达到代表活性点饱和的平台值,这些活性点可用于与TCPP-SBA-15上的金属离子相互作用;换言之增加Cu(II)浓度以获得对感兴趣的金属离子的最大去除能力。TCPP-SBA-15样品对Cu(II)的最大吸附量为每克吸附剂13mmol Cu(II,见表2)。此外,在实验开始时观察到高去除率,之后在60分钟内逐渐达到平衡值。脱金属实验通常在1小时内完成,这表明结合过程相当快。这种高吸附容量是通过将卟啉基团掺入二氧化硅结构中实现的(图5)。如前所述,卟啉桥联基团的螯合性能会影响水中金属的去除过程。卟啉基团对Cu(II)离子的高亲和力导致了非常高的吸附容量。高吸附速率也可归因于材料的均匀多孔结构,其特征是存在规则的中通道。[1] 还研究了TCPP-SBA-15对汽车涂料行业收集的废水样本的效率,最初,在15分钟的短时间内,废水样本中含有32 mg L-1的Cu2+离子,Cu2+的浓度已降低到一半(15 mg L-1)。发现200分钟后,如ICP-MS研究所示,在流出物样品中没有观察到Cu2+。因此,它可以被认为是去除铜的有效系统。 分配系数(Kd)用于评估吸附剂对Cu(II)离子的亲和力。表2总结了分布系数。在TCPP-SBA-15的情况下,Kd增加,表明对Cu(II)离子的亲和力随着TCPP基团的负载而增加。从环境角度来看,TCPP基团对Cu(II)物种的相当大的亲和力导致了高分布系数,这一事实很重要。表2中还列出了由方程式(3)计算的不同初始浓度下Cu(II)离子的去除能力。[1] 3. 铜(II)的回收和吸附剂的再生是关键过程。为了进行这两个过程并测量吸附剂的实际效用,通过在1小时内用50毫升0.2 M HCl溶液处理0.1克含有吸附Cu2+离子的TCPP-SBA-15进行了解吸实验。由于使用了0.2 M HCl水溶液,h+可以替代被TCPP-SBA-15吸附的金属离子。图6显示了TCPP-SBA-15金属离子络合物的解吸速率随时间的变化。解吸过程在60分钟时达到平衡,Cu(II)的解吸率为65.1%(图6a)。[1] 使用与吸附实验相同的程序对TCPP-SBA-15进行了可重复使用性实验。使用相同的材料重复吸附-解吸循环3次(图6b)。第一次循环后的吸附容量约为11.906 mmol g−1,第二次循环后为11.760 mmol g−于1,第三次循环后则为11.630 mmol g−着1。通过紫外-可见光谱监测铜络合物在TCPP-SBA-15上的解吸(图7a)。无铜TCPP-SBA-15的紫外-可见光谱包括两个主要特征:一系列可见带(Q带)和一个极其强烈的带(Soret带)。与大多数游离碱四(4-羧基苯基)卟啉的光谱类似,无铜TCPP-SBA-15的光谱显示出明确的Q带,这些Q带被分配给0→ 0 和0→ 1 最低π不同x和y分量的振动跃迁→ π*跃迁。这证明在解吸过程中回收了Cu(II)。重复使用的吸附剂的光谱显示出与四(4-羧基苯基)卟啉铜光谱相似的谱带,该卟啉在417 nm处也有Soret谱带,在540和583 nm处有Q谱带(图7a)。为了确认TCPP-SBA-15内是否存在Cu(II)离子,我们对含有吸附Cu(Ⅱ)离子的TCPP-SBA-15样品进行了EPR研究(图7b)。含有吸附的Cu(II)离子的TCPP-SBA-15样品的EPR光谱可以用参数g||=2.20和g⊥=2.06的轴向自旋哈密顿量来解释,这表明TCPP中与氮配体连接的Cu(Ⅱ)离子具有方形平面对称性(图7b)[1]。 |
| 酶活实验 |
吸附试验[1]
脱金属实验是通过在25°C下搅拌250 mL金属溶液中的100 mgTCPP-SBA-15进行的。进行了两种不同的Cu2+浓度,即1065和65 mg L−1。NH2-SBA-15也进行了相同的吸附试验。在不同时间间隔后,分析每个小瓶的溶液中的Cu2+浓度,并使用方程式(1)计算Cu2+的去除率。 其中Qe是平衡时吸附在TCPP-SBA-15上的Cu2+量(mg/g),C0是CuSO4·5H2O水溶液中Cu2+的初始浓度(mg L−1),Ce是平衡时CuSO4•5H2O水中Cu2+的最终浓度(mg L-1),V是溶液的总体积(L);m吸附剂质量(g)。用于评估吸附剂对水溶液中吸附质亲和力的分布系数Kd可以使用方程式(2)计算 通过后合成方法成功地将四(4-羧基苯基)卟啉(TCPP)作为有机部分掺入介孔二氧化硅中。TCPP的螯合特性使这种吸附剂具有从水溶液中去除Cu(II)离子的吸引力。研究了铜(II)在TCPP-SBA-15上的吸附,并与在NH2-SBA-15二氧化硅上的吸附进行了比较。结果表明,吸附量在13 mmol g−1左右达到最大值,TCPP-SBA-15材料的吸附容量高于NH2-SBA-15二氧化硅。[1] 研究了四(4-羧基苯基)卟啉(TCPP)官能化NH2-SBA-15对Cu(II)离子的吸附。使用不同初始浓度的Cu(II)在TCPP-SBA-15上进行金属吸附。铜(II)在TCPP-SBA-15样品上的最大吸附量为每克吸附剂12.96毫摩尔铜(Ⅱ)。解吸过程在60分钟时达到平衡,Cu(II)的解吸率为65.1%。对含有吸附Cu(II)离子的TCPP-SBA-15进行的再生实验表明,在连续三个吸附-解吸循环后,吸附容量分别为11.906、11.760和11.630 mmol g−1。因此,我们可以得出结论,TCPP配体使这些材料能够作为吸附剂去除Cu(II)离子[1]。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
为了实现药物靶向和延长递送至受影响组织,应优化粒径。本文描述了平均粒径对介孔四(羧基苯基)卟啉 (TCPP) 的药代动力学和光血栓活性的影响,TCPP 被封装在基于聚(D,L-乳酸)的可生物降解纳米颗粒中。采用乳化扩散法制备了四批平均粒径分别为 121 至 343 nm 的纳米颗粒。测量了每种 TCPP 纳米颗粒制剂从血管中的渗出情况以及光化学诱导的血管阻塞程度。这些临床前试验在鸡胚绒毛尿囊膜 (CAM) 中进行。荧光显微镜显示,TCPP从CAM血管中的有效渗漏及其光血栓形成效率均取决于纳米颗粒药物载体的尺寸。事实上,在实验条件下,当颗粒尺寸减小时,血管与周围组织之间的TCPP荧光对比度增加。这表明较大的纳米颗粒能更快地从血液中清除。此外,在注射1 mg/kg体重的药物剂量,并间隔1分钟进行药物-光照处理后,以10 J/cm²的光照剂量照射,结果表明,随着颗粒尺寸的增大,血管损伤程度逐渐降低。当使用平均直径为121 nm的TCPP负载纳米颗粒时,观察到最高的光血栓形成效率。因此,在所应用的条件下,例如治疗与年龄相关性黄斑变性 (AMD) 相关的脉络膜新生血管 (CNV) 等疾病时,这些实验表明,最小的纳米颗粒可被视为最佳制剂,因为它们表现出最大的血管血栓形成程度以及最低的外渗。/TCPP 纳米颗粒/ 我们研究了 SW480 细胞对介孔四(羧基苯基)卟啉 (TCPP) 纳米颗粒的摄取,并系统地研究了 TCPP 纳米颗粒的细胞内化机制,同时还研究了 TCPP 纳米颗粒的光细胞毒性。首先,我们采用混合溶剂法制备了介孔四(羧基苯基)卟啉 (TCPP) 纳米颗粒。采用荧光分光光度法分析了SW480细胞对光敏剂(TCPP纳米颗粒、TCPP负载的聚乳酸-羟基乙酸共聚物(PLGA)纳米颗粒和游离TCPP)的摄取情况。通过将SW480细胞在4℃下预孵育,以及分别用蔗糖、无钾缓冲液和菲利平预孵育,研究了内吞作用机制。采用Western blot和RT-PCR方法分析了SW480细胞与这三种光敏剂孵育后网格蛋白重链(Clathrin HC)的表达。最后,我们分析了SW480细胞与光敏剂孵育并接受照射后的光细胞毒性。结果显示,SW480细胞在孵育1小时后即可快速摄取TCPP纳米颗粒(0.0083 fmol TCPP/细胞)。我们还证实,SW480细胞对TCPP纳米颗粒的摄取是通过网格蛋白介导的内吞途径实现的。由于SW480细胞能够快速内化TCPP纳米颗粒,这种特殊的光敏剂在体外对SW480细胞表现出极高的光细胞毒性。这种无基质包覆的纳米级光敏剂——TCPP纳米颗粒,比其他光敏剂(TCPP负载的PLGA纳米颗粒和游离TCPP)具有更高的光细胞毒性。体内肿瘤生长抑制实验表明,在所有TCPP治疗组中,TCPP纳米颗粒联合光动力疗法(PDT)的肿瘤抑制效果最为显著。本研究结果表明,TCPP纳米颗粒是一种潜在且高效的光动力疗法药物。 /TCPP纳米颗粒/ 皮下移植异种尿路上皮癌的无胸腺裸鼠接受了合成光敏剂介孔四(4-羧基苯基)卟啉的静脉注射。使用Kr+激光器(407 nm)激发肿瘤和皮肤的荧光,并在注射光敏剂后不同时间点,使用光纤传感器结合光学多通道分析仪在652 nm处检测荧光。采用Ar+激光器泵浦染料激光器(650 nm;100 mW/cm²;100 J/cm²)进行光动力治疗。在四周的随访期内测定肿瘤生长延迟情况,并将其与体内荧光测量结果进行关联。 介孔四(4-羧基苯基)卟啉 (mTCPP) 是一种市售的小分子荧光团和光敏剂,具有四个游离羧酸基团。 mTCPP 易于与胺类化合物偶联,从而方便地连接功能基团。本研究合成并评估了四价赖氨酸偶联的 mTCPP,以探索其在靶向成像和光动力疗法中的潜在应用。我们首先通过酰胺偶联反应,将 Fmoc 保护的 D-赖氨酸或 L-赖氨酸与 mTCPP 的 ε-氨基偶联,然后进行 Fmoc 脱保护。所得化合物在水溶液中的溶解性较差,但可通过表面活性剂(例如胆酸)的辅助溶解。L-氨基酸转运蛋白 (LAT1) 可以摄取多种中性 L-氨基酸。体外 U87 细胞研究表明,疏水性的 Fmoc 保护的赖氨酸偶联的 mTCPP 前体可被非特异性摄取,而 D-赖氨酸或 L-赖氨酸偶联的 mTCPP 则不被摄取。同样,只有Fmoc保护的化合物在经蓝光照射和孵育后,才在细胞中诱导了显著的光毒性。这些实验结果并未提供证据表明赖氨酸-mTCPP能够特异性靶向癌细胞。然而,它们确实突显了mTCPP作为一种便捷易用的框架,可用于评估光敏剂的分子靶向性。/赖氨酸偶联的mTCPP/ |
| 毒性/毒理 (Toxicokinetics/TK) |
毒性概述
鉴定和用途:四羧基苯基卟啉 (TCPP) 是一种深蓝色至紫色至黑色的粉末。TCPP 是一种强效的光敏剂,可被可见光激活。它曾被用作研究化学品、化学中间体和卟啉染料。它已在动物细胞模型中用于癌症的光动力疗法测试,并作为肺癌患者的非侵入性诊断检测方法。人体研究:尚无相关数据。动物研究:使用琼脂糖凝胶电泳研究了 TCPP 对 ColE1 超螺旋 DNA 的光敏作用。在中性条件下观察到光诱导的单链和双链断裂的形成。 相互作用 使用一系列肿瘤定位卟啉和 L1210 肿瘤系统,研究了肿瘤细胞在卟啉定位和光化学治疗反应中的作用。对携带L1210实体瘤的DBA/2Ha小鼠进行体内光照射,这些小鼠此前已注射过内消旋-四-(4-磺酸苯基)卟啉、内消旋-四-(4-羧基苯基)卟啉或血卟啉衍生物(Hpd)。结果表明,这三种化学物质均能诱发光动力反应,导致暴露组织坏死。采用温和的机械方法和生理条件从注射过卟啉的小鼠中分离出肿瘤细胞,然后在体外光照射条件下,在已建立的优化快速细胞毒性效应的条件下,未观察到明显的细胞死亡。使用注射过Hpd的小鼠的脾细胞也观察到了类似的情况,这些脾细胞可能含有大量的卟啉。荧光显微镜观察以及对细胞内卟啉的化学提取和定量分析均表明,体外光照无法迅速产生细胞毒性效应是由于卟啉的缺失或含量极低所致。这些结果表明,在该特定肿瘤系统中,肿瘤细胞本身在卟啉定位中仅起次要作用,因此在光照下不易被杀死。这提示在体内光照过程中,仅由细胞内卟啉引起的快速细胞毒性效应可能不会在大多数实质细胞中发生。 解毒剂和急救措施 /SRP:/ 立即采取急救措施:确保已进行充分的去污处理。如果患者停止呼吸,应立即开始人工呼吸,最好使用按需呼吸机、球囊面罩或简易呼吸面罩(如已接受过相关培训)。必要时进行心肺复苏。立即用流动清水冲洗受污染的眼睛。不要催吐。如果发生呕吐,将患者身体前倾或置于左侧卧位(如果可能,头部向下),以保持呼吸道通畅并防止误吸。保持患者安静并维持正常体温。立即就医。/A类和B类毒物/ /SRP:/ 基本治疗:建立通畅的呼吸道(必要时使用口咽或鼻咽通气道)。必要时进行吸痰。观察呼吸功能不全的迹象,必要时辅助通气。使用无创呼吸面罩以10至15升/分钟的流量给予氧气。监测肺水肿,必要时进行治疗……。监测休克,必要时进行治疗……。预判癫痫发作,必要时进行治疗……。如果眼睛受到污染,立即用水冲洗眼睛。在转运过程中,持续用0.9%生理盐水冲洗每只眼睛……。不要使用催吐剂。误服时,漱口并给予5 mL/kg至200 mL的水稀释,前提是患者能够吞咽、有强烈的咽反射且不流涎……。皮肤烧伤经去污后,用干燥的无菌敷料覆盖……。/A类和B类毒物/ /SRP:/ 高级治疗:对于意识不清、严重肺水肿或严重呼吸窘迫的患者,考虑进行口咽或鼻咽气管插管以控制气道。使用球囊面罩进行正压通气可能有效。考虑药物治疗肺水肿……。考虑使用β受体激动剂(如沙丁胺醇)治疗严重支气管痉挛……。监测心律,必要时治疗心律失常……。开始静脉输注5%葡萄糖溶液(D5W TKO)/SRP:“保持通畅”,最小流速/。如果出现低血容量的迹象,请使用0.9%生理盐水(NS)或乳酸林格氏液(LR)。对于伴有低血容量迹象的低血压,应谨慎输液。注意液体过量的迹象……。使用地西泮(安定)或劳拉西泮(阿提凡)治疗癫痫发作……。使用盐酸丙美卡因辅助眼部冲洗……。 /毒物A和B/ 非人类毒性摘录 /替代和体外试验/ 在pH 8.3的Tris-硼酸-EDTA (TBE)缓冲溶液中,通过测量紫外-可见吸收光谱、稳态荧光光谱、稳态荧光各向异性光谱、时间分辨荧光光谱、共振光散射(RLS)、傅里叶变换红外光谱(FT-IR)和圆二色谱(CD),并借助原子力显微镜(AFM),研究了内消旋-四(4-羧基苯基)卟啉(TCPP)阴离子形式与小牛胸腺脱氧核糖核酸(CT DNA)之间的相互作用。小牛胸腺脱氧核糖核酸对卟啉的静态荧光猝灭表明形成了基态复合物。基态复合物的形成是一个自发的分子相互作用过程,其中通过氢键或范德华力进行的外侧沟槽结合起主要作用。对于生物医学应用而言,这项研究非常重要,因为阴离子卟啉TCPP不会改变CT DNA的原始结构,从而选择性地切割核酸以破坏癌细胞或肿瘤细胞,而阳离子卟啉在同一过程中会显著改变蛋白质结构。PMID:20655240 /替代和体外试验/ 本研究采用琼脂糖凝胶电泳法研究了血卟啉衍生物,即内消旋-四(对磺酸苯基)卟啉、内消旋-四(对羧基苯基)卟啉和内消旋-四(4-N-甲基吡啶基)卟啉对ColE1超螺旋DNA的光敏化作用。在中性条件下观察到了光诱导的单链和双链断裂。单线态氧在血卟啉衍生物,如间位四(对磺酸苯基)卟啉和间位四(对羧基苯基)卟啉的致癌机制中占主导地位,并在间位四(4-N-甲基吡啶基)卟啉的致癌机制中发挥重要作用。这些结果提示,使用卟啉光敏剂的光化学疗法和荧光内镜检查可能存在光动力致癌的风险。PMID:7020932 |
| 参考文献 | |
| 其他信息 |
治疗用途
/EXPL THER/ 应优化粒径以实现靶向和延长药物递送至受影响组织。本文描述了平均粒径对介孔四(羧基苯基)卟啉 (TCPP) 的药代动力学和光血栓活性的影响,TCPP 被封装在基于聚(D,L-乳酸)的可生物降解纳米颗粒中。采用乳化扩散法制备了四批平均粒径分别为 121 至 343 nm 的纳米颗粒。测量了每种 TCPP 纳米颗粒制剂从血管中的渗出情况以及光化学诱导的血管阻塞程度。这些临床前试验在鸡胚绒毛尿囊膜 (CAM) 中进行。荧光显微镜显示,TCPP从CAM血管中的有效渗漏及其光血栓形成效率均取决于纳米颗粒药物载体的尺寸。事实上,在实验条件下,当颗粒尺寸减小时,血管与周围组织之间的TCPP荧光对比度增加。这表明较大的纳米颗粒能更快地从血液中清除。此外,在注射1 mg/kg体重的药物剂量,并间隔1分钟进行药物-光照处理后,以10 J/cm²的光照剂量照射,结果表明,随着颗粒尺寸的增大,血管损伤程度逐渐降低。当使用平均直径为121 nm的TCPP负载纳米颗粒时,观察到最高的光血栓形成效率。因此,在这一应用范围内,例如治疗与年龄相关性黄斑变性 (AMD) 相关的脉络膜新生血管 (CNV) 等疾病时,这些实验表明,最小的纳米颗粒可被视为最佳制剂,因为它们表现出最大的血管血栓形成程度以及最低的外渗。/TCPP 纳米颗粒/ /EXPL THER/ 本研究利用一系列肿瘤定位卟啉和 L1210 肿瘤系统,探讨了肿瘤细胞在卟啉定位和光化学治疗反应中的作用。对携带L1210实体瘤的DBA/2Ha小鼠进行体内光照射,这些小鼠此前已注射过内消旋-四-(4-磺酸苯基)卟啉、内消旋-四-(4-羧基苯基)卟啉或血卟啉衍生物(Hpd)。结果表明,这三种化学物质均能诱发光动力反应,导致暴露组织坏死。采用温和的机械方法和生理条件从注射过卟啉的小鼠中分离出肿瘤细胞,然后在体外光照射条件下,在已建立的优化快速细胞毒性效应的条件下,未观察到明显的细胞死亡。使用注射过Hpd的小鼠的脾细胞也观察到了类似的情况,这些脾细胞可能含有大量的卟啉。荧光显微镜观察以及对细胞内卟啉的化学提取和定量分析均表明,体外光照无法迅速诱导细胞死亡效应的原因在于细胞内卟啉含量极低或完全缺失。这些结果表明,在该特定肿瘤系统中,肿瘤细胞本身在卟啉定位中仅起次要作用,因此在光照下不易被杀死。这提示在体内光照过程中,仅由细胞内卟啉引起的快速细胞死亡效应可能不会在大多数实质细胞中发生。 /EXPL THER/ 我们研究了SW480细胞对介孔四(羧基苯基)卟啉(TCPP)纳米颗粒的摄取,并系统地研究了TCPP纳米颗粒的细胞内化机制,同时还研究了TCPP纳米颗粒的光细胞毒性。首先,采用混合溶剂法制备了介孔四(羧基苯基)卟啉(TCPP)纳米颗粒。采用荧光分光光度法分析了SW480细胞对光敏剂(TCPP纳米颗粒、负载TCPP的聚乳酸-羟基乙酸共聚物(PLGA)纳米颗粒和游离TCPP)的摄取情况。通过将SW480细胞在4℃下预孵育,以及分别用蔗糖、无钾缓冲液和菲利平预孵育SW480细胞,研究了内吞作用机制。采用Western blot和RT-PCR方法分析了SW480细胞与这三种光敏剂孵育后网格蛋白重链(Clathrin HC)的表达。最后,我们分析了SW480细胞与光敏剂孵育并接受光照后的光细胞毒性。 SW480细胞在孵育1小时后迅速摄取TCPP纳米颗粒(0.0083 fmol TCPP/细胞)。我们还证实,SW480细胞对TCPP纳米颗粒的摄取是通过网格蛋白介导的内吞途径实现的。由于SW480细胞对TCPP纳米颗粒的快速内化,这种特殊的光敏剂在体外对SW480细胞表现出极高的光细胞毒性。这种无基质包覆的纳米级光敏剂——TCPP纳米颗粒,比其他光敏剂(TCPP负载的PLGA纳米颗粒和游离TCPP)具有更高的光细胞毒性。体内肿瘤生长抑制实验表明,在所有TCPP治疗组中,TCPP纳米颗粒联合光动力疗法(PDT)治疗组的肿瘤抑制效果最为显著。本研究结果表明,TCPP纳米颗粒是一种潜在且有效的光动力疗法药物。 /TCPP纳米颗粒/ /EXPL THER/ 引言:早期发现高危人群的肺癌可降低死亡率。低剂量螺旋CT(LDCT)是目前的标准检查方法,但其假阳性率极高(>96%),导致不必要的、甚至可能存在危险的检查。因此,我们着手开发一种简便、无创且定量的肺癌检测方法。方法:本概念验证研究评估了CyPath早期肺癌检测方法对LDCT确诊的高危对照组(n = 102)和癌症组(n = 26)受试者的敏感性和特异性。我们采用多变量logistic回归分析评估了四(4-羧基苯基)卟啉(TCPP)标记的肺痰样本中红色荧光细胞(RFC)的荧光强度参数以及受试者的基线特征的预测能力。此外,我们还绘制了受试者工作特征曲线(ROC曲线)以评估CyPath检测方法的敏感性和特异性。结果:在癌症患者中检测到放射性荧光细胞(RFC)的频率高于高危人群(p = 0.015),且两组人群的RFC特征存在差异。癌症的两个独立预测因子分别是每位受试者RFC平均荧光强度/面积的平均值(p < 0.001)和吸烟年限(p = 0.003)。基于CyPath的分类器在测试人群中的总体准确率为81%,假阳性率为40%,阴性预测值为83%。结论:基于四(4-羧基苯基)卟啉的CyPath检测方法能够以相当高的准确率将研究参与者正确分类为癌症患者或高危人群。优化痰液采集、样本判读以及改进分类器有望提高检测的灵敏度和特异性。因此,CyPath 检测方法有望与低剂量CT筛查互补,或作为早期肺癌检测的独立方法。 /EXPL THER/ 将皮下移植异种尿路上皮癌的无胸腺裸鼠静脉注射合成敏化剂间位四(4-羧基苯基)卟啉。使用Kr+激光器(407 nm)激发肿瘤和皮肤的荧光,并在注射敏化剂后不同时间点,使用光纤传感器结合光学多通道分析仪在652 nm处检测荧光。使用Ar+激光器泵浦染料激光器(650 nm;100 mW/cm²;100 J/cm²)进行光动力治疗。在为期四周的随访期内测定肿瘤生长延迟情况,并将其与体内荧光测量结果进行关联。 |
| 分子式 |
C48H30N4O8
|
|---|---|
| 分子量 |
790.79
|
| 精确质量 |
790.206
|
| 元素分析 |
C, 72.91; H, 3.82; N, 7.09; O, 16.19
|
| CAS号 |
14609-54-2
|
| PubChem CID |
86278368
|
| 外观&性状 |
Dark blue to purple to black powder
|
| 密度 |
1.5±0.1 g/cm3
|
| 熔点 |
> 300 °C
|
| 折射率 |
1.734
|
| LogP |
11.46
|
| tPSA |
205.5
|
| 氢键供体(HBD)数目 |
6
|
| 氢键受体(HBA)数目 |
10
|
| 可旋转键数目(RBC) |
8
|
| 重原子数目 |
60
|
| 分子复杂度/Complexity |
1310
|
| 定义原子立体中心数目 |
0
|
| SMILES |
O([H])C(C1C([H])=C([H])C(=C([H])C=1[H])C1C2C([H])=C([H])C(=C(C3C([H])=C([H])C(C(=O)O[H])=C([H])C=3[H])C3=C([H])C([H])=C(C(C4C([H])=C([H])C(C(=O)O[H])=C([H])C=4[H])=C4C([H])=C([H])C(C(C5C([H])=C([H])C(C(=O)O[H])=C([H])C=5[H])=C5C([H])=C([H])C=1N5[H])=N4)N3[H])N=2)=O |c:20,86,t:58,80|
|
| InChi Key |
HHDUMDVQUCBCEY-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C48H30N4O8/c53-45(54)29-9-1-25(2-10-29)41-33-17-19-35(49-33)42(26-3-11-30(12-4-26)46(55)56)37-21-23-39(51-37)44(28-7-15-32(16-8-28)48(59)60)40-24-22-38(52-40)43(36-20-18-34(41)50-36)27-5-13-31(14-6-27)47(57)58/h1-24,49,52H,(H,53,54)(H,55,56)(H,57,58)(H,59,60)
|
| 化学名 |
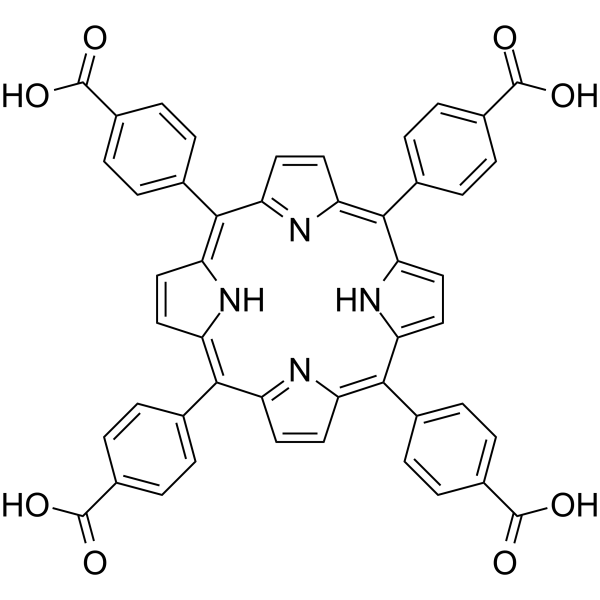
4-[10,15,20-tris(4-carboxyphenyl)-21,23-dihydroporphyrin-5-yl]benzoic acid
|
| 别名 |
14609-54-2; Tetracarboxyphenylporphine; CCRIS 8701; HSDB 8470; meso-Tetra-(4-carboxyphenyl)porphine; Benzoic acid, 4,4',4'',4'''-(21H,23H-porphine-5,10,15,20-tetrayl)tetrakis-; 4,4',4'',4'''-(Porphine-5,10,15,20-tetrayl) tetrakis (benzoic acid); meso-Tetra(4-carboxyphenyl)porphine;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: (1). 本产品在运输和储存过程中需避光。 (2). 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: 4 mg/mL (5.06 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 2.5 mg/mL (3.16 mM) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浮液;超声助溶。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: 2.5 mg/mL (3.16 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.2646 mL | 6.3228 mL | 12.6456 mL | |
| 5 mM | 0.2529 mL | 1.2646 mL | 2.5291 mL | |
| 10 mM | 0.1265 mL | 0.6323 mL | 1.2646 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。