| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| Other Sizes |
|
| 靶点 |
Metabolite of mycophenolic acid
|
|---|---|
| 体外研究 (In Vitro) |
麦考酚酸葡萄糖苷酸的 IC50 为 3.3 mg/L,对 IMP 脱氢酶 (IMPDH) 表现出适度的 II 型抑制作用[3]。
MPA和MPAG/霉酚酸7-O-葡糖苷酸对hNaDC3[1] 的影响 在表达hNaDC3的卵母细胞中,添加0.1 与单独的ORI-2相比,mM MPA诱导了较小的内向电流(图1A)。当钠被N-甲基-D-葡糖胺替代时,MPA相关的内向电流被消除,表明MPA的钠依赖性易位(图1A)。图1还显示了0.1 mM MPA(B,空心圆)和0.1 hNaDC3卵母细胞中的mMMPAG(C,开环)是膜电位的函数,与1 同一卵母细胞中的mM琥珀酸盐(闭合圆圈)。在所有测试的电位下,琥珀酸依赖性内向电流的幅度均大于MPA或MPAG诱导的电流。当添加琥珀酸、MPA或MPAG时,在H 2 O注射的卵母细胞中没有观察到内向电流(数据未显示)。与1一起使用时 mM琥珀酸、MPA在0.1和1时分别使内向电流衰减了16±10%和28±8% mM。MPAG的作用更强,在0.1时,电流已经下降了32±19% mM(图2)。这些数据表明MPA和MPAG与人类NaDC3相互作用并由其运输。 MPAG和AcMPAG对hOAT1-和hOAT3-介导的转运的影响[1] 在肾脏清除方面,MPA的葡萄糖醛酸代谢产物,特别是MPAG,通常从肝脏输送到肾脏[1],具有特别重要的意义。与MPA相比,葡糖苷酸MPAG和AcMPAG在临床相关浓度下没有显著减弱表达hOAT1的卵母细胞对PAH的摄取(图5)。然而,hOAT3卵母细胞对ES的摄取受到100μg/ml的显著抑制 μM AcMPAG(80.9±6.5%,P<0.01),以及10 µM和100 μM MPAG(分别为53.7±5.2%,P<0.01和69.2±12.7%,P<0.05)(图5)。在这些实验中,抑制10 µM AcMPAG略低于10 µM MPAG(46.8±14.5%),由于其高度可变性,没有统计学意义。然而,剂量反应曲线表明,AcMPAG是一种更有效的hOAT3抑制剂(IC 50 2.88±0.42 µM)比MPAG(IC 50 15.2±18.5 µM)(图6)。 使用纯化的重组人II型肌苷酸单磷酸脱氢酶(IMPDH)评估霉酚酸葡糖苷酸(MPAG)抑制动力学。发现MPAG抑制浓度(IC50)比MPA高532至1022倍。正如预期的那样,根据紧密结合抑制剂动力学,霉酚酸(MPA)的IC50值随着IMPDH浓度的增加而增加,而黄嘌呤单磷酸(用作对照的竞争性IMPDH抑制剂)的IC50值更不依赖于酶浓度。尽管MPAG对IMPDH活性的抑制作用较弱,但与MPA相比,IC50值随着酶浓度的增加而增加。高效液相色谱分析检测到MPAG制剂中存在痕量MPA(0.2%摩尔),这可以解释这一观察结果。这些数据支持MPAG是MPA的药理学非活性代谢产物的说法。[2] 结果:MPA和AcMPAG对rhIMPDH II有抑制作用(IC(50)分别为25.6微克/升和301.7微克/升;MPA对NAD和IMP的K(i)分别为50.8和57.7nmol/L;AcMPAG对NAD和IMP的敏感性分别为382.0和511.0 nmol/L。MPAG对酶没有显著影响。AcMPAG显然通过与MPA相同的非竞争性抑制机制起作用,IC(50)高12倍,K(i)高8-10倍。当与MPA共孵育时,AcMPAG在药理学浓度下的活性可以忽略不计。此外,在各自的最大浓度(C(max))下孵育6小时后,Jurkat细胞中MPA的浓度是AcMPAG的10倍。 结论:AcMPAG是一种比MPA弱的rhIMPDH II抑制剂,在体外淋巴细胞中的浓度较低,这表明它在体内没有药理活性,可能不需要在MPA治疗的患者中进行监测[3]。 |
| 体内研究 (In Vivo) |
在艾利希小鼠自发性腺癌模型中,霉酚酸葡萄糖醛酸(腹膜内注射;6 mg/小鼠;两天一次;6 天)治疗可抑制肿瘤生长[2]。
|
| 酶活实验 |
IMPDH活性测定[2]
如前所述测定IMPDH活性。简而言之,测定混合物(最终体积,1ml)含有400 nmol NAD、200 nmol IMP、0.1 mol pH 7.8的磷酸钾、0.5 mol氯化钾、3 mmol EDTA、适当浓度的IMPDH,以及一系列浓度的酶抑制剂MPA、MPAG或XMP。在贝克曼DU 640分光光度计上,在37°C下在340 nm处监测NADH形成20分钟。使用PS-Plot计算机程序统计计算中位抑制浓度(IC50)(最小二乘拟合)。 RHimpdh ii酶测定[3] rhIMPDH II测定在100 mmol/L Tris-HCl缓冲液(pH 8,37°C)中进行,该缓冲液含有100 mmol/L KCl、2 mmol/L EDTA和1 mmol/L二硫苏糖醇。我们将100μL rhIMPDH II(4%vol/vol)加入850μL酶缓冲液中,并将其与20μL IMP(0.01-10mmol/L)充分涡旋混合。使用培养箱块将反应介质预热至37°C。我们向培养混合物中加入10μL的潜在抑制剂(MPA、AcMPAG或MPAG),用乙腈稀释(最终百分比为1%vol/vol)。对照培养物中加入了相同量的乙腈。然后,我们通过加入20μL NAD+(0.25-20mmol/L)开始反应。立即将混合物充分混合,转移到1-mL紫外微孔中,并放置在调温分光光度计中。由于rhIMPDH II催化的反应是等摩尔的,NADH的形成与IMP和NAD+的用量直接相关。反应监测包括NAD+还原的分光光度测量(λ=340nm处的摩尔吸光系数6220)。每秒进行两次测量,持续5分钟。我们使用内部程序计算结果,该程序使用线性回归模型计算每个反应的初始速度。 为了在测定过程中测试AcMPAG和MPAG的稳定性,将这两种分子在37°C下以2种不同浓度(10μg/L和10 mg/L)在1 mL反应混合物中分别孵育30分钟。每5分钟取样100μL,与100μL乙腈/甲酸(97%/3%vol/vol)混合,并立即在冰上冷却以避免进一步降解。通过在37°C的水中以相同浓度孵育AcMPAG和MPAG,进行了三次阴性对照。然后使用经过验证的HPLC-MS/MS方法在每个样品中测定MPA、AcMPAG和MPAG。 抑制实验[3] 如上所述,将rhIMPDH II与饱和浓度的两种共底物(IMP 200μmol/L;NAD+400μmol/L)和10种浓度递增的3种潜在抑制剂(MPA(1μg/L至1 mg/L)、AcMPAG(10μg/L至10 mg/L)和MPAG(200μg/L至20 mg/L))孵育三次。我们使用Hill模型和Winreg 3.1计算了每种潜在抑制剂的半最大抑制浓度(IC50)。 为了计算IMPDH II共底物NAD+和IMP的抑制常数(Ki),每种抑制剂在5个递增的浓度下孵育(AcMPAG为50μg/L至3.0 mg/L,MPA为1μg/L至1.0 mg/L)。我们首先在固定饱和浓度(200μmol/L)的IMP和增加浓度的NAD+(5-400μmol/L)下进行实验,然后在饱和NAD+浓度(400μmol/L)和6个增加浓度的IMP(2μmol/L至200μol/L)下进行。我们使用名为Inhib 1.1的内部软件通过非线性回归计算了每种共基质的每种抑制剂的Ki。 为了比较AcMPAG单独或在MPA存在下对rhIMPDH II的影响,将AcMPAG与rhIMPDHⅡ以MPA IC50值的0.05至10倍的浓度孵育,MPA或AcMPAG的IC50约为IC50(分别为25μg/L和300μg/L)。对于没有任何抑制剂的阳性对照计算抑制率。 |
| 细胞实验 |
aCmpag和mpa穿过细胞膜的能力[3]
我们在一个75平方厘米的培养瓶中,以2×106个细胞/mL的浓度,在RPMI 1640培养基中培养来自淋巴瘤人细胞系的Jurkat细胞,该培养基补充了10%FBS、2 mmol/L谷氨酰胺、1%氨基酸、1%维生素、1%丙酮酸盐、100 U/mL青霉素和100 mg/L链霉素。在37°C和5%CO2下与MPA(终浓度20 mg/L)、AcMPAG和MPAG(此处作为AcMPAG的化学稳定对照;终浓度2 mg/L)一起孵育6小时。然后对培养基进行离心;取样并分析上清液以测量细胞外浓度,通过加入200μL 50/50(vol/vol)低渗水/甲酸溶液并在-20°C下孵育48小时,使用细胞沉淀来测量裂解后的细胞内浓度。我们使用已发表的LC-MS/MS技术定量MPA、MPAG和AcMPAG。该技术的定量限为10μg/L。在10mg/L范围内,线性关系得到验证(r=0.999)。在该线性范围内,批内CV<10%,批间CV<15%。回收率良好,线性范围内的平均相对误差<15%。 我们无法计算实际的细胞内浓度,因为无法精确测量细胞内培养基的体积,甚至细胞的体积或质量。因此,我们计算了孵育6小时后细胞中发现的药物量(μg)与时间0时孵育培养基中存在的化合物总量(例如加标量)的比率,以比较AcMPAG与MPAG和MPAG的细胞传代。 |
| 动物实验 |
动物/疾病模型:植入艾氏腹水瘤细胞的瑞士白化品系小鼠[2]
剂量:6 mg/只小鼠 给药途径:腹腔注射(ip);6 mg/只小鼠;每两天一次;6 天 实验结果:与未治疗的对照组相比,肿瘤抑制率为 76.8%。 |
| 药代性质 (ADME/PK) |
代谢/代谢物
霉酚酸葡萄糖醛酸苷是已知的霉酚酸的人体代谢物。 |
| 参考文献 |
|
| 其他信息 |
总之,霉酚酸酯与人OAT1和OAT3均具有高亲和力,并抑制底物转运。代谢产物MPAG和AcMPAG被发现与hOAT3相互作用,但不与hOAT1相互作用。其强效抑制作用(IC50值远低于霉酚酸酯治疗期间的血浆浓度范围)使得hOAT1和hOAT3成为干扰合用hOAT1/hOAT3药物底物(如抗病毒药、皮质类固醇或利尿剂)肾脏清除的敏感靶点。[1]
背景:霉酚酸(MPA)是前药霉酚酸酯吗替麦考酚酯的活性成分,广泛用于肾脏、肝脏或心脏移植后的免疫抑制方案。MPA主要代谢为无活性的7-O-葡萄糖醛酸苷(MPAG)。少量MPA转化为具有药理活性的酰基葡糖醛酸苷(AcMPAG)。所有化合物最终均经肾脏排泄。由于其结构特性,MPA及其代谢物是人有机阴离子转运蛋白1(OAT1)和3(OAT3)以及钠-二羧酸盐共转运蛋白3(NaDC3)的候选底物。方法:利用体外合成的cRNA,在经胶原酶去除卵泡的非洲爪蟾卵母细胞中表达人(h)OAT1、hOAT3和hNaDC3。注射后第3天,测量了以下指标:(i)使用MPA和MPAG(仅在表达hNaDC3的卵母细胞中)测定的底物相关电流;(ii)在有或无MPA、MPAG或AcMPAG存在的情况下,测定[3H]对氨基马尿酸(hOAT1)或[3H]硫酸雌酮(hOAT3)的摄取。结果:在-60 mV的膜电位下,表达hNaDC3的卵母细胞中,MPA(0.1 mM)和MPAG(0.1 mM)均诱导了内向电流,其强度分别为琥珀酸(1 mM)诱导电流的17%和25%。反之,琥珀酸(1 mM)诱导的电流被MPA和MPAG部分抑制。人OAT1和HOAT3均被MPA强效抑制(IC50分别为1.24和0.52 μM)。MPA的两种葡萄糖醛酸苷代谢物也以浓度依赖的方式抑制人OAT3(MPAG的IC50为15.2 μM,AcMPAG的IC50为2.88 μM),而对HOAT1无抑制作用,这与HOAT3相比HOAT1更倾向于转运体积较大的底物相一致。结论:MPA及其代谢物与肾脏有机阴离子转运蛋白HOAT1和HOAT3强效相互作用,从而可能干扰抗病毒药物、皮质醇和其他有机阴离子的肾脏分泌。[1]这些数据支持MPAG几乎没有或完全没有直接药理活性的假设。由于 MPAG 对 IMPDH 的抑制作用明显较弱,因此观察到的 IC50 值随 IMPDH 浓度升高而增加的现象并非由 MPAG 本身引起,因为只有高亲和力抑制剂才能产生这种效应。另一种解释是,这种看似较弱的抑制作用是由少量高亲和力抑制剂 MPA 的存在造成的。HPLC 分析在 MPAG 中检测到少量 MPA 的结果支持了这一假设。此外,当计算 MPAG 制剂中痕量污染物 MPA 的浓度并将其代入 IC50 测定中时,IC50(MPAcontam) 值与 IC50 MPA 结果非常接近(表 1),进一步支持了上述假设。这些数据支持以下假设:与 MPA 相比,MPAG 对药理靶点的直接作用很小。然而,对于血浆中MPA代谢物浓度较高的患者(例如,肾移植后移植物功能延迟恢复的患者),需要探讨葡萄糖醛酸酶的作用对活性药物浓度的潜在贡献。[2] 背景:霉酚酸(MPA)的免疫抑制作用主要归因于其对IMPDH II的抑制,从而导致淋巴细胞增殖减少。我们研究了MPA代谢物MPA-苯基-葡萄糖醛酸苷(MPAG)和MPA-酰基-葡萄糖醛酸苷(AcMPAG)对重组人IMPDH II(rhIMPDH II)的作用,以及它们在体外进入淋巴细胞的情况。方法:我们通过分光光度法测定NADH生成的初始速率来测量rhIMPDH II的活性,从而计算动力学参数K(m)、IC(50)和K(i)(米氏常数、半数抑制浓度和抑制常数)。我们分别用每种化合物孵育 Jurkat 淋巴瘤细胞后,采用液相色谱-串联质谱法测量了 MPA、MPAG 和 AcMPAG 的细胞内和细胞外浓度。[3] |
| 分子式 |
C23H28O12
|
|---|---|
| 分子量 |
496.46
|
| 精确质量 |
496.158
|
| 元素分析 |
C, 55.64; H, 5.68; O, 38.67
|
| CAS号 |
31528-44-6
|
| 相关CAS号 |
Mycophenolic acid glucuronide-d3
|
| PubChem CID |
6442661
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.502g/cm3
|
| 沸点 |
875.7ºC at 760mmHg
|
| 熔点 |
98-100ºC
|
| 闪点 |
299.6ºC
|
| 折射率 |
1.624
|
| LogP |
0.298
|
| tPSA |
189.28
|
| 氢键供体(HBD)数目 |
5
|
| 氢键受体(HBA)数目 |
12
|
| 可旋转键数目(RBC) |
9
|
| 重原子数目 |
35
|
| 分子复杂度/Complexity |
827
|
| 定义原子立体中心数目 |
5
|
| SMILES |
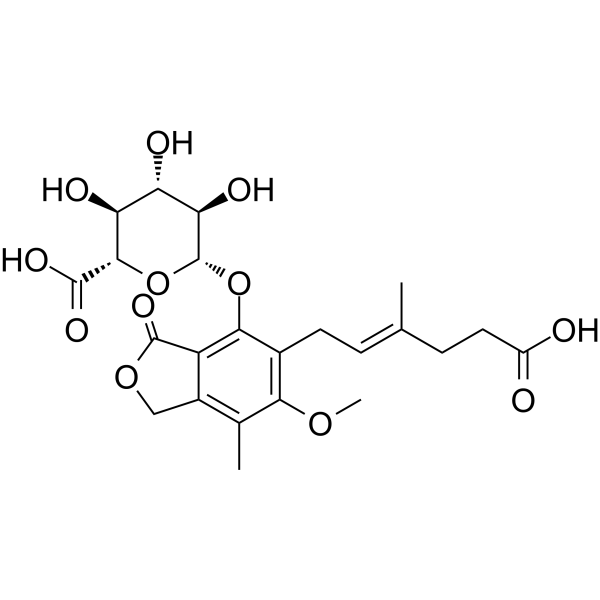
CC1=C2COC(=O)C2=C(C(=C1OC)C/C=C(\C)/CCC(=O)O)O[C@H]3[C@@H]([C@H]([C@@H]([C@H](O3)C(=O)O)O)O)O
|
| InChi Key |
BYFGTSAYQQIUCN-HGIHDBQLSA-N
|
| InChi Code |
InChI=1S/C23H28O12/c1-9(5-7-13(24)25)4-6-11-18(32-3)10(2)12-8-33-22(31)14(12)19(11)34-23-17(28)15(26)16(27)20(35-23)21(29)30/h4,15-17,20,23,26-28H,5-8H2,1-3H3,(H,24,25)(H,29,30)/b9-4+/t15-,16-,17+,20-,23+/m0/s1
|
| 化学名 |
(2S,3S,4S,5R,6S)-6-[[5-[(E)-5-carboxy-3-methylpent-2-enyl]-6-methoxy-7-methyl-3-oxo-1H-2-benzofuran-4-yl]oxy]-3,4,5-trihydroxyoxane-2-carboxylic acid
|
| 别名 |
mycophenolic acid glucuronide; 31528-44-6; Mycophenolic acid glucosiduronate; Mycophenolic acid 7-O-glucuronide; 54TS5J9T0K; UNII-54TS5J9T0K; MPAG cpd; .BETA.-D-GLUCOPYRANOSIDURONIC ACID, 5-((2E)-5-CARBOXY-3-METHYL-2-PENTEN-1-YL)-1,3-DIHYDRO-6-METHOXY-7-METHYL-3-OXO-4-ISOBENZOFURANYL;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: 33.33 mg/mL (67.14 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (5.04 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (5.04 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (5.04 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.0143 mL | 10.0713 mL | 20.1426 mL | |
| 5 mM | 0.4029 mL | 2.0143 mL | 4.0285 mL | |
| 10 mM | 0.2014 mL | 1.0071 mL | 2.0143 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。