| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| Other Sizes |
|
| 靶点 |
CFTR/cystic fibrosis transmembrane conductance regulator
|
|---|---|
| 体内研究 (In Vivo) |
Olacaftor(VX-440)是一种下一代校正器,在一项2期试验中进行了评估,该试验是随机、双盲、安慰剂和活性对照研究,旨在评估VX-440与特扎卡福和伊伐卡福三联使用在CF患者中的安全性和耐受性,这些CF患者是F508del突变和MF CFTR突变的杂合子,不太可能对特扎卡佛和/或伊伐卡佛治疗(F508del MF)有反应,或者是F508del突变的纯合子(ClinicalTrials.gov标识符:NCT02951195)[https://pmc.ncbi.nlm.nih.gov/articles/PMC7088950/].
|
| 参考文献 | |
| 其他信息 |
背景:囊性纤维化(CF)是一种常见的遗传性疾病,会缩短患者的寿命,其病因是囊性纤维化跨膜传导调节因子(CFTR)蛋白的变异。II类CFTR变异F508del是最常见的致病变异(在高达90%的CF患者中发现)。F508del变异导致CFTR蛋白功能缺失——缺陷蛋白在到达细胞膜之前就被降解,而细胞膜是CFTR蛋白发挥跨上皮盐转运功能所必需的部位。纠正性治疗有望使许多CF患者受益。本综述评估了单一矫正剂(单药治疗)以及矫正剂(最常用的是lumacaftor、tezacaftor、elexacaftor、VX-659、Olacaftor (VX-440) 或 VX-152)与增强剂(例如ivacaftor)的任意组合(双联和三联疗法)。
目标:评估CFTR矫正剂(无论是否联合增强剂)对携带II类CFTR突变(最常见的是F508del)的任何年龄段囊性纤维化患者(pwCF)的临床获益和危害的影响。 检索方法:我们检索了Cochrane囊性纤维化试验注册库(2022年11月28日)、相关文章的参考文献列表和在线试验注册库(2022年12月3日)。 纳入标准:比较携带II类CFTR突变的囊性纤维化患者使用CFTR矫正剂与对照组的随机对照试验(RCT)(平行设计)。 数据收集和分析:两位作者独立提取数据,评估偏倚风险并判断证据确定性(GRADE);我们联系了研究人员以获取更多数据。 主要结果:我们纳入了 34 项 RCT(4781 名参与者),持续时间从 1 天到 48 周不等;两项 lumacaftor-ivacaftor 研究的扩展提供了额外的 96 周安全性数据(1029 名参与者)。我们评估了 8 项单药治疗 RCT(344 名参与者)(4PBA、CPX、lumacaftor、cavosonstat 和 FDL169)、16 项双药治疗 RCT(2627 名参与者)(lumacaftor-ivacaftor 或 tezacaftor-ivacaftor)和 11 项三药治疗 RCT(1804 名参与者)(elexacaftor-tezacaftor-ivacaftor/deutivacaftor;VX-659-tezacaftor-ivacaftor/deutivacaftor;Olacaftor (VX-440)-tezacaftor-ivacaftor;VX-152-tezacaftor-ivacaftor)。 21项随机对照试验(RCT)的参与者基因型为F508del/F508del,7项RCT的参与者基因型为F508del/最小功能(MF),1项RCT的参与者基因型为F508del/门控基因型,1项RCT的参与者基因型为F508del/F508del或F508del/残余功能基因型,1项RCT的参与者基因型为F508del/门控基因型或F508del/残余功能基因型,3项RCT的参与者基因型为F508del/F508del或F508del/MF。不同比较的偏倚风险评估结果有所不同。由于年龄限制(例如仅限成人)或非标准设计(例如从单药治疗转换为联合治疗),16项RCT的结果可能不适用于所有囊性纤维化患者。单药治疗研究者报告未出现死亡病例,也未观察到具有临床意义的生活质量 (QoL) 改善。尚无充分证据确定其对肺功能的影响。没有安慰剂对照的单药治疗随机对照试验 (RCT) 显示轻度、中度或重度不良反应 (AE) 存在差异;由于不良反应种类繁多且受试者人数较少(均为 F508del/F508del 突变体),因此难以评估这些事件的临床意义。双药治疗方面,在 tezacaftor-ivacaftor 组中出现 1 例死亡(被认为与研究药物无关)。在所有时间点,与安慰剂相比,lumacaftor-ivacaftor 和 tezacaftor-ivacaftor 治疗组的生活质量评分(呼吸领域)均更优(中等确定性证据)。6 个月时,与安慰剂相比,所有双药联合治疗组的一秒用力呼气容积 (FEV1) 占预计值的百分比均有所改善(高至中等确定性证据)。更多囊性纤维化患者在使用lumacaftor-ivacaftor后报告出现早期短暂性呼吸困难(比值比 (OR) 2.05,99% 置信区间 (CI) 1.10 至 3.83;I² = 0%;2 项研究,739 名参与者;高质量证据)。在 120 周(初始研究期和随访期)内,每日两次服用 400 mg lumacaftor-ivacaftor 的患者(80 名参与者)收缩压升高 5.1 mmHg,舒张压升高 4.1 mmHg。tezacaftor-ivacaftor 的随机对照试验未报告这些不良反应。与安慰剂组相比,接受伊伐卡托联合其他疗法的囊性纤维化患者肺部急性加重率降低(所有证据均为中等确定性):卢马卡托 600 mg(风险比 (HR) 0.70,95% 置信区间 0.57 至 0.87;I² = 0%;2 项研究,739 名参与者);卢马卡托 400 mg(HR 0.61,95% 置信区间 0.49 至 0.76;I² = 0%;2 项研究,740 名参与者);以及特扎卡托(HR 0.64,95% 置信区间 0.46 至 0.89;1 项研究,506 名参与者)。三联疗法:无研究报告死亡病例(高确定性证据)。所有其他证据的确定性均为低至中等。与对照组相比,三联疗法组患者在六个月时的生活质量呼吸领域评分可能有所改善(6 项研究)。三联疗法可能使FEV1占预计值的相对变化和绝对变化更大(所有组合均有四项研究)。对于接受elexacaftor-tezacaftor-ivacaftor治疗的F508del/MF患者,其FEV1占预计值的绝对变化可能比安慰剂组更大(平均差异14.30,95% CI 12.76至15.84;1项研究,403名参与者;中等确定性证据),其他药物组合和基因型也得到了类似的结果。三联疗法组和对照组的不良事件发生率几乎没有差异(10项研究)。没有研究报告下次肺部急性加重的时间,但在接受 elexacaftor-tezacaftor-ivacaftor 治疗的 F508del/F508del 患者中,4 周时发生肺部急性加重的比例较低(OR 0.17,99% CI 0.06 至 0.45;1 项研究,175 名参与者),24 周时发生肺部急性加重的比例也较低(OR 0.29,95% CI 0.14 至 0.60;1 项研究,405 名参与者);其他三联疗法和基因型组合也观察到了类似的结果。 作者结论:对于 F508del/F508del 囊性纤维化患者,尚无充分证据表明矫正药物单药治疗具有临床意义的疗效。本综述中的其他数据降低了双联疗法的疗效证据;这些药物不再被视为标准疗法。在特殊情况下(例如,患者无法耐受三联疗法或因年龄原因),使用这些药物可能是合适的。两种双联疗法(lumacaftor-ivacaftor 和 tezacaftor-ivacaftor)均能带来类似的轻微改善,改善生活质量和呼吸功能,并降低肺部急性加重率。虽然生活质量和 FEV1 的疗效仍然优于双联疗法,但与我们之前的研究结果相比有所降低。Lumacaftor-ivacaftor 与早期短暂性呼吸困难和长期血压升高相关(tezacaftor-ivacaftor 未观察到此现象)。Tezacaftor-ivacaftor 的安全性更高,但缺乏 12 岁以下儿童的数据。在 12 岁以下儿童中,lumacaftor-ivacaftor 对呼吸功能有显著改善,且未发现明显的近期安全性问题,但在考虑使用 lumacaftor-ivacaftor 时,应权衡其在长期成人数据中观察到的血压升高和呼吸困难。三联疗法试验的数据表明,包括 FEV1 和生活质量在内的多个关键指标均有所改善。对于携带一个或两个F508del变异的12岁及以上囊性纤维化患者(pwCF),三联疗法(elexacaftor-tezacaftor-ivacaftor/deutivacaftor;VX-659-tezacaftor-ivacaftor/deutivacaftor;Olacaftor (VX-440)-tezacaftor-ivacaftor;VX-152-tezacaftor-ivacaftor)的不良事件发生率可能差异很小或没有差异(中等确定性证据)。需要对12岁以下儿童和肺部疾病更严重的患者进行进一步的随机对照试验。参考文献:Cochrane Database Syst Rev. 2023 Nov 20;11(11):CD010966. https://pubmed.ncbi.nlm.nih.gov/37983082/ |
| 分子式 |
C29H34FN3O4S
|
|---|---|
| 分子量 |
539.661369800568
|
| 精确质量 |
539.225
|
| 元素分析 |
C, 64.54; H, 6.35; F, 3.52; N, 7.79; O, 11.86; S, 5.94
|
| CAS号 |
1899111-41-1
|
| 相关CAS号 |
Olacaftor;1897384-89-2
|
| PubChem CID |
130203218
|
| 外观&性状 |
White to light yellow solid powder
|
| LogP |
6.3
|
| tPSA |
97
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
7
|
| 可旋转键数目(RBC) |
8
|
| 重原子数目 |
38
|
| 分子复杂度/Complexity |
902
|
| 定义原子立体中心数目 |
1
|
| SMILES |
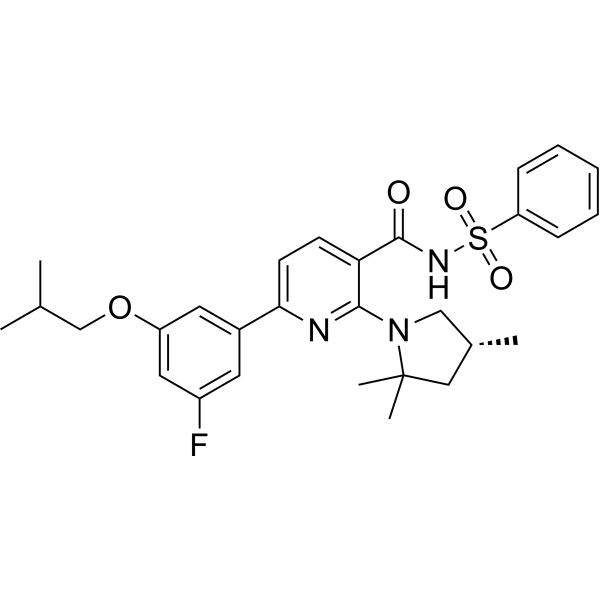
S(C1C=CC=CC=1)(NC(C1=CC=C(C2C=C(C=C(C=2)OCC(C)C)F)N=C1N1C[C@H](C)CC1(C)C)=O)(=O)=O
|
| InChi Key |
NHOUNZMCSIHKHJ-HXUWFJFHSA-N
|
| InChi Code |
InChI=1S/C29H34FN3O4S/c1-19(2)18-37-23-14-21(13-22(30)15-23)26-12-11-25(27(31-26)33-17-20(3)16-29(33,4)5)28(34)32-38(35,36)24-9-7-6-8-10-24/h6-15,19-20H,16-18H2,1-5H3,(H,32,34)/t20-/m1/s1
|
| 化学名 |
N-(benzenesulfonyl)-6-[3-fluoro-5-(2-methylpropoxy)phenyl]-2-[(4R)-2,2,4-trimethylpyrrolidin-1-yl]pyridine-3-carboxamide
|
| 别名 |
(R)-Olacaftor; 1899111-41-1; SCHEMBL19097503; (R)-VX-440;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: 250 mg/mL (463.25 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (3.85 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.08 mg/mL (3.85 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL 澄清 DMSO 储备液加入到 900 μL 玉米油中并混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.8530 mL | 9.2651 mL | 18.5302 mL | |
| 5 mM | 0.3706 mL | 1.8530 mL | 3.7060 mL | |
| 10 mM | 0.1853 mL | 0.9265 mL | 1.8530 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。