| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| Other Sizes |
|
| 靶点 |
Receptor-interacting protein kinase 1 (RIP1), receptor-interacting protein kinase 3 (RIP3), and mixed lineage kinase domain-like protein (MLKL) [1]
|
|---|---|
| 体外研究 (In Vitro) |
化合物6i 对人胶质瘤U251细胞表现出强效的抗增殖活性,IC50值为0.94 μM,比雷公藤红素(IC50 = 4.43 μM)强约4.7倍。对A172(IC50 = 3.03 μM)、LN229(IC50 = 1.78 μM)和U87(IC50 = 1.22 μM)细胞系也显示出活性。 [1]
在正常人肝L02细胞中,化合物6i 的IC50值为2.14 μM,而雷公藤红素为0.83 μM。 [1] 化合物6i 以时间和浓度依赖性方式抑制U251细胞生长。在0.5 μM处理72小时时,抑制率约为49%。 [1] 在克隆形成实验中,化合物6i(0.5和1.0 μM,24-72小时)显著减少了U251细胞集落数量,0.5 μM处理48小时后无集落形成。 [1] 在划痕愈合实验中,化合物6i(0.5和1.0 μM)以浓度依赖性方式降低U251细胞的迁移率。 [1] Hoechst 33342染色显示,化合物6i(1.0 μM,48小时)与对照组相比,未增加凋亡细胞的比例(染色质凝集和核碎片)。 [1] Annexin V-FITC/PI流式细胞术分析显示,化合物6i(0.5、1.0和2.0 μM,48小时)未增加早期凋亡细胞(AV+/PI-)的百分比。 [1] 用泛caspase抑制剂z-VAD-FMK(20、40、80 μM)预处理不能阻止化合物6i诱导的细胞死亡,表明其抗增殖活性并非主要通过凋亡介导。 [1] 透射电子显微镜观察化合物6i处理的U251细胞,显示坏死性凋亡的形态学特征:质膜完整性丧失、线粒体肿胀、细胞质空泡化和自噬体形成。未观察到凋亡特征(凋亡小体、膜起泡、染色质凝集)。 [1] 化合物6i(0.5、1.0和2.0 μM,48小时)以浓度依赖性方式增加细胞膜通透性,通过PI染色和流式细胞术测量。 [1] 用RIP1抑制剂Nec-1(10 μM)预处理可显著阻止化合物6i诱导的U251细胞活力降低。 [1] 化合物6i(0.5、1.0和2.0 μM,48小时)以浓度依赖性方式诱导线粒体去极化,通过JC-1染色和流式细胞术测量。线粒体膜去极化细胞的百分比从对照组的164.5%降至2 μM时的1.6%。 [1] 用RIP1抑制剂GSK2982772(2.5 μM)、RIP3抑制剂GSK872(2.5 μM)和MLKL抑制剂necro sulfonamide(1.0 μM)预处理可有效挽救化合物6i(1.0 μM)触发的U251细胞死亡。 [1] Western blot分析显示,化合物6i(0.5、1.0、2.0和4.0 μM,24或48小时)在U251细胞中以浓度依赖性方式上调p-RIP1、RIP1、p-RIP3、RIP3、p-MLKL和MLKL的表达。 [1] 与雷公藤红素相比,化合物6i 诱导U251细胞坏死性凋亡的能力更强,表现为坏死性凋亡抑制剂(Nec-1、GSK872、necro sulfonamide)在化合物6i处理的细胞中比在雷公藤红素处理的细胞中具有更强的活力挽救效果。 [1] 在人胶质瘤细胞系中,RIP1/RIP3/MLKL 激活剂 1(化合物 6i)(96 小时)表现出抗增殖作用 [1]。在 U251 细胞上,RIP1/RIP3/MLKL 激活剂 1(0–4 µM,0-72 小时)以浓度和时间依赖性方式表现出强大的抗增殖活性 [1]。 RIP1/RIP3/MLKL 激活剂 1(10 µM,0-72 小时)证明了可接受的稳定性 [1]。据观察,RIP1/RIP3/MLKL 激活剂 1(0–2 µM,24 小时)可有效阻止 U251 细胞迁移 [1]。在 U251 细胞中,RIP1/RIP3/MLKL 激活剂 1 通过 RIP1/RIP3/MLKL 途径引起线粒体去极化和坏死性凋亡 [1]。在 U251 细胞中,RIP1/RIP3/MLKL 激活剂 1 无法引起细胞凋亡 [1]。 |
| 体内研究 (In Vivo) |
在斑马鱼异种移植模型中,化合物6i(2.50 ng/尾,静脉循环显微注射)与对照组相比,显著降低了U251异种移植物的荧光强度,表明其在体内抑制U251细胞增殖。阳性对照5-FU使用50.0 ng/尾。 [1]
在昆明小鼠中的血脑屏障通透性研究:化合物6i 通过尾静脉注射给药,剂量为1.0、3.0和9.0 mg/kg。注射后0.5和1.0小时的脑组织分析显示,化合物6i能够穿过血脑屏障,且脑组织中的浓度以浓度依赖性方式增加。 [1] 化合物 6i,RIP1/RIP3/MLKL 激活剂 1(2.50 ng/尾;静脉注射;48 小时),表现出可接受的 BBB 通透性,同时抑制体内 U251 细胞增殖 [1]。 |
| 细胞实验 |
细胞活力测定(MTT):将细胞接种于96孔板中,密度为2000个/孔,培养12小时。加入不同浓度的化合物6i,孵育96小时。加入MTT(5 mg/mL,20 μL),在37°C孵育3-4小时。弃去上清液,加入DMSO(150 μL/孔),在490 nm处读取吸光度。计算IC50值。 [1]
克隆形成实验:将U251细胞(800个/孔)接种于6孔板中,用化合物6i(0、0.5、1.0 μM)处理24-72小时,然后在无药培养基中培养11天。用4%多聚甲醛固定集落,用0.1%结晶紫染色30分钟,计数>50个细胞的集落。 [1] 划痕愈合实验:将U251细胞(1 × 10⁵/孔)培养至>90%融合。用200 μL移液管尖端制造划痕。用化合物6i(0.5和1.0 μM)处理细胞。在0和24小时拍摄图像,计算迁移率。 [1] Hoechst 33342染色:用化合物6i(1.0 μM)或雷公藤红素(1.0 μM)处理U251细胞48小时。加入Hoechst 33342缓冲液,避光孵育20分钟,用荧光显微镜观察凋亡细胞。 [1] 凋亡分析(Annexin V-FITC/PI):用不同浓度的化合物6i处理U251细胞48小时。收集细胞,用Annexin V-FITC和PI孵育,通过流式细胞术分析。 [1] 线粒体膜电位测量(JC-1):用化合物6i处理U251细胞48小时,用JC-1染色30分钟,通过流式细胞术分析。 [1] Western blot分析:用化合物6i(0.5、1.0、2.0、4.0 μM)处理U251细胞24或48小时。裂解细胞,用BCA试剂盒测定蛋白浓度。通过SDS-PAGE分离蛋白,转移至PVDF膜,用5% BSA封闭,与抗GAPDH、p-RIP1、RIP1、p-RIP3、RIP3、p-MLKL和MLKL的一抗在4°C孵育12小时,然后与HRP标记的二抗孵育2小时。使用ImageLab软件检测蛋白条带。 [1] 膜通透性PI染色:用化合物6i(0.5、1.0、2.0 μM)处理U251细胞48小时,用PI染色,通过流式细胞术分析。 [1] 透射电子显微镜:用化合物6i处理U251细胞,固定,在透射电子显微镜下观察形态变化。 [1] 细胞增殖测定[1] 细胞类型: A172、LN229、U87、U251 和 L02 细胞系 测试浓度: U251 细胞为 0-4 µM 孵化持续时间:96小时; U251 细胞 24、48 和 72 小时 实验结果:对于 A172、LN229、U87、U251 和 L02 表现出抗增殖活性,IC50 值为 3.03 ± 0.70、1.78分别为 ± 0.79、1.22 ± 0.89、0.94 ± 0.45 和 0.99 ± 0.46 µM 细胞。以时间和浓度依赖性方式抑制 U251 细胞的生长。 蛋白质印迹分析[1] 细胞类型: U251 测试浓度: 0、0.5、1、2 和 4 µM 孵育持续时间:24 或 48 小时 实验结果:p-RIP1、RIP1、p 表达的浓度依赖性上调-RIP3、RIP3、p-MLKL 和 MLKL 在 24 或 48 小时。 |
| 动物实验 |
血脑屏障通透性研究:将雄性昆明小鼠(6-8周龄,每组n=4)随机分为六组。将化合物6i溶于含6.0%乙醇和6.0%聚氧乙烯蓖麻油的生理盐水中,分别以1.0、3.0和9.0 mg/kg的剂量经尾静脉注射给药。注射后0.5或1.0 h处死小鼠。取出脑组织,称重,与无菌生理盐水(1:5 w/v)混合,匀浆,用2倍体积的甲醇/乙腈(1:9)混合液提取,过滤后进行LC-MS分析。 [1]
斑马鱼异种移植模型:将CM-Dil标记的U251细胞显微注射到受精后2天(dpf)的野生型AB品系斑马鱼胚胎的卵黄囊中。将胚胎置于35℃培养至3 dpf。将斑马鱼胚胎随机分配到6孔板中(每孔30个胚胎)。通过静脉循环显微注射给予化合物6i(2.50 ng/尾)和5-FU(50 ng/尾,阳性对照),并孵育48小时。从每个孔中随机选取10个胚胎,并在荧光显微镜下拍照。使用图像分析软件分析荧光强度。[1] 动物/疾病模型:斑马鱼广谱AB品系;将 200 个 CM-DiI 标记的 U251 细胞移植到每条野生型斑马鱼胚胎的卵黄囊中(受精后 2 天)[1] 剂量: 2.50 ng/尾 给药途径: 显微注射;48 小时 实验结果: U251 异种移植的荧光强度显著降低。 |
| 参考文献 |
| 分子式 |
C43H56N4O3
|
|---|---|
| 分子量 |
676.929751396179
|
| 精确质量 |
676.435
|
| CAS号 |
2682850-41-3
|
| PubChem CID |
163322291
|
| 外观&性状 |
Orange to red solid powder
|
| 密度 |
1.19±0.1 g/cm3(Predicted)
|
| LogP |
8.3
|
| tPSA |
97.1
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
6
|
| 重原子数目 |
50
|
| 分子复杂度/Complexity |
1560
|
| 定义原子立体中心数目 |
5
|
| SMILES |
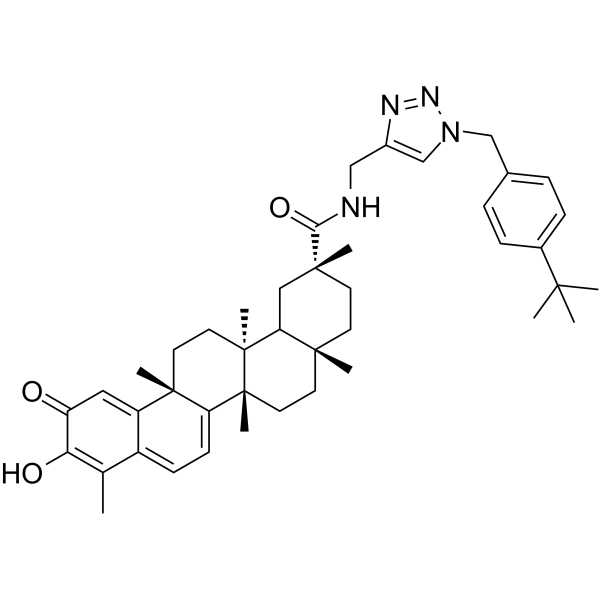
CC1=C(C(=O)C=C2C1=CC=C3[C@]2(CC[C@@]4([C@@]3(CC[C@@]5(C4C[C@](CC5)(C)C(=O)NCC6=CN(N=N6)CC7=CC=C(C=C7)C(C)(C)C)C)C)C)C)O
|
| InChi Key |
QLFCJGYFBTYJGC-RSWNTZNOSA-N
|
| InChi Code |
InChI=1S/C43H56N4O3/c1-27-31-14-15-34-41(7,32(31)22-33(48)36(27)49)19-21-43(9)35-23-40(6,17-16-39(35,5)18-20-42(34,43)8)37(50)44-24-30-26-47(46-45-30)25-28-10-12-29(13-11-28)38(2,3)4/h10-15,22,26,35,49H,16-21,23-25H2,1-9H3,(H,44,50)/t35?,39-,40-,41+,42-,43+/m1/s1
|
| 化学名 |
(2R,4aS,6aR,6aS,14aS)-N-[[1-[(4-tert-butylphenyl)methyl]triazol-4-yl]methyl]-10-hydroxy-2,4a,6a,6a,9,14a-hexamethyl-11-oxo-1,3,4,5,6,13,14,14b-octahydropicene-2-carboxamide
|
| 别名 |
RIP1/RIP3/MLKL activator 1; 2682850-41-3; RIP1/RIP3/MLKL activator-1;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~147.73 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (3.69 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浮液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 配方 2 中的溶解度: 2.5 mg/mL (3.69 mM) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL 澄清 DMSO 储备液添加到 900 μL 玉米油中并混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.4773 mL | 7.3863 mL | 14.7726 mL | |
| 5 mM | 0.2955 mL | 1.4773 mL | 2.9545 mL | |
| 10 mM | 0.1477 mL | 0.7386 mL | 1.4773 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。