| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| Other Sizes |
|
| 靶点 |
KDM1/lysine-specific demethylase 1 (LSD1)
|
|---|---|
| 体外研究 (In Vitro) |
S2101 是赖氨酸特异性脱甲基酶 1 (LSD1) 的抑制剂,IC50 为 0.99 μM,Ki 为 0.61 μM,Kinact/Ki 为 4560 M/s。此外,S2101 对 MAO-A (Ki=110 µM,Kinact/Ki=60 M/s) 和 MAO-B (Ki=17 µM,Kinact/Ki=18 M/s) 的抑制活性显着降低。在 HEK293T 细胞中用 S2101 处理 H3K4me2,这种处理会导致 H3K4me2 呈剂量依赖性升高,这肯定是由于 LSD1 失活而积累的。在 S2101 治疗期间,核提取物中 LSD1 和组蛋白 H3 的水平没有显着变化。由于用 1 μM S2101 处理时,50 μM 2-PCPA 会引发相似量的 H3K4me2,因此推测 S2101 在人体细胞中的 LSD1 抑制作用比 2-PCPA 大约高 50 倍[1]。
|
| 酶活实验 |
LSD1抑制实验[1]
采用过氧化物酶偶联反应法获得了LSD1去甲基酶抑制的动力学抑制参数。将LSD1蛋白(3.0 pmol)与40μM H3K4me2肽在含有10 mM HEPES Na(pH 7.5)、200μM 4-氨基安替比林、改良Trinder试剂TOOS[N-乙基-N-(2-羟基-3-磺基丙基)-3-甲基苯胺,钠盐,二水合物]和0.01 mg/mL辣根过氧化物酶的缓冲液中孵育10分钟。该系统产生7.61±0.56 min−1的kcat和16±5μM的Km。辣根过氧化物酶利用LSD1去甲基化产生的过氧化物酶副产物将TOOS和4-氨基安替比林转化为粉红色/紫色化合物,λmax为555 nm(http://www.dojindo.co.jp/protocol/protocol/trinder.pdf). 在黑暗中制备反应混合物以抑制Trinder试剂的反应性。用微孔板读取器(Ultrospec Visible Plate reader II 96,GE Healthcare)每10秒在562nm处测量反应混合物的吸收。尽管TOOS的λmax为555 nm,但在562 nm处测量波长足以提供准确的抑制结果,因为用于计算KI的方程取决于活性的差异,而不是绝对值。将结果转化为LSD1的去甲基化肽的量和MAOs的氧化酪胺的量,使用TOOS的ε值3.92×104。对结果进行分析,并与慢结合抑制剂方程(方程1)拟合以产生kobs,并根据Kitz−Wilson分析进一步转换以计算kinact和KIapp,或者当y截距明显为非零时,使用偏移值koffset(方程2)(26-31)。将KIapp转化为KI,以排除底物浓度的偏差(等式3)(26)。使用GraFit拟合数据(http://www.erithacus.com/grafit/)和KyPlot(http://www.kyenslab.com/jp/). MAO抑制试验[1] 使用过氧化物酶偶联反应法进行MAO抑制测定,基本上与LSD1相同,但分别以40或50μM酪胺为底物和9.0和4.5μg MAO-A和MAO-B。以与LSD1相同的方式分析和计算结果。每个结果都是从至少三个单独的实验中计算出来的。在时间过程测定上绘制的符号是实验的平均值,并且使用KyPlot通过慢结合抑制剂方程计算和拟合最佳拟合线。 |
| 细胞实验 |
化合物处理的细胞的蛋白质印迹分析[1]
HEK293T细胞在Dulbecco改良的Eagle培养基中的100 mm培养皿中生长,该培养基含有10%FBS和100单位/mL青霉素、100μg/mL链霉素抗生素溶液,在37°C的5%CO2气氛下。用LSD1抑制剂处理约70%融合度的细胞24小时,分离,并用冰冷的PBS冲洗数次。根据制造商的说明,使用CelLytic Nuclear提取试剂盒制备核提取物。将每个核提取物在10%至20%的SDS−聚丙烯酰胺凝胶上进行电泳,然后转移到硝化纤维膜上。用第一抗体(抗H3,Abcam ab1791;抗H3K4me2,Upstate 07-030;和抗LSD1)探测膜上的蛋白质,然后用第二抗体(山羊抗兔IgG−辣根过氧化物酶偶联物)探测,并用化学发光系统Immobilion Western检测。 |
| 参考文献 | |
| 其他信息 |
赖氨酸特异性去甲基化酶1 (LSD1/KDM1) 可使组蛋白H3去甲基化,此外,抑癌基因p53和DNA甲基转移酶1 (Dnmt1) 也参与此过程,从而通过改变染色质结构来调控真核生物基因表达。由于LSD1异常与多种癌症相关,且LSD1抑制可恢复癌细胞中异常沉默基因的表达,因此LSD1特异性抑制剂被认为是理想的抗癌药物。本研究基于LSD1和单胺氧化酶B (MAO-B) 与抗抑郁药反苯环丙胺 (2-PCPA) 衍生物的复合物结构,设计并合成了几种LSD1抑制剂候选化合物。在LSD1去甲基化实验中,化合物S2101表现出比反式环丙胺和已知的LSD1小分子抑制剂更强的LSD1抑制活性,其ak(inact)/K(I)值为4560 M⁻¹ s⁻¹。与反式环丙胺相比,该化合物对单胺氧化酶的抑制作用较弱。通过测定抑制剂与LSD1结合的结构,确定了两种2-PCPA衍生物2-PFPA和S1201的抑制模式,结果表明抑制剂-FAD加合物与周围LSD1残基的相互作用增强了其稳定性。这些分子有望成为治疗癌症或潜伏病毒感染的候选药物,也可作为LSD1相关生物学研究的工具[1]。
|
| 精确质量 |
311.09
|
|---|---|
| 元素分析 |
C, 61.64; H, 5.17; Cl, 11.37; F, 12.19; N, 4.49; O, 5.13
|
| CAS号 |
1239262-36-2
|
| PubChem CID |
121513887
|
| 外观&性状 |
White to off-white solid powder
|
| tPSA |
35.2Ų
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
4
|
| 可旋转键数目(RBC) |
4
|
| 重原子数目 |
21
|
| 分子复杂度/Complexity |
322
|
| 定义原子立体中心数目 |
2
|
| SMILES |
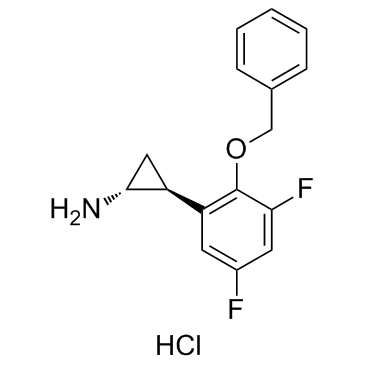
C1[C@H]([C@@H]1N)C2=C(C(=CC(=C2)F)F)OCC3=CC=CC=C3.Cl
|
| InChi Key |
CTSUZAFTJVLOIX-SBKWZQTDSA-N
|
| InChi Code |
InChI=1S/C16H15F2NO.ClH/c17-11-6-13(12-8-15(12)19)16(14(18)7-11)20-9-10-4-2-1-3-5-10;/h1-7,12,15H,8-9,19H2;1H/t12-,15+;/m0./s1
|
| 化学名 |
(1R,2S)-2-(3,5-difluoro-2-phenylmethoxyphenyl)cyclopropan-1-amine;hydrochloride
|
| 别名 |
S2101; S-2101; S 2101
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~320.77 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 5 mg/mL (16.04 mM) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浮液;超声助溶。
例如,若需制备1 mL的工作液,可将100 μL 50.0 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 5 mg/mL (16.04 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 50.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 5 mg/mL (16.04 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。