| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
VEGFR2 (IC50 = 30 nM); c-Met (IC50 = 32 nM)
Pamufetinib mesylate significantly inhibits the proliferation of MET-amplified cancer cells (GI50=0.032-0.362 μM) and strongly suppresses the VEGF-dependent proliferation of HUVECs (IC50=0.019 μM) as a MET-targeted inhibitor. In comparison to other VEGFR-targeted kinase inhibitors, pamufetinib mesylate is significantly less toxic in a variety of normal cell lines[1]. In PC-9 and HCC827 cells, erlotinib resistance, Met phosphorylation, and VEGF production induced by HGF are all inhibited by crizotinib and Pamufetinib mesylate[2]. |
|---|---|
| 体外研究 (In Vitro) |
体外活性:Pamufetinib/TAS-115 是一种新型、有效的 VEGFR 和肝细胞生长因子受体 (MET) 靶向激酶抑制剂,具有改进的安全性,对 rVEGFR2 和 rMET 的 IC50 分别为 30 和 32 nM。 VEGF 受体 (VEGFR) 信号在肿瘤血管生成中发挥关键作用。尽管一些 VEGFR 信号靶向药物已被批准用于临床,但其实用性受到相关毒性或对此类疗法的耐药性的限制。为了克服这些限制,开发了 TAS-115 来抑制 VEGFR2 和 MET 的激酶活性及其信号依赖性细胞生长,其抑制效果与其他已知的 VEGFR 或 MET 抑制剂一样强。 TAS-115 的激酶选择性比舒尼替尼更具特异性,并且 TAS-115 对 VEGFR 信号或 MET 信号独立的细胞产生相对较弱的生长抑制 (GI50 > 10 μmol/L)。此外,与其他 VEGFR 抑制剂相比,TAS-115 对各种正常细胞造成的损伤较小。这些数据表明 TAS-115 具有极高的选择性和特异性,至少在体外是如此。在体内研究中,TAS-115 通过阻断血管生成来完全抑制 MET 灭活肿瘤的进展,连续 6 周每天给药,即使是 TAS-115 的血清饱和剂量,也没有毒性。 TAS-115 对激酶和靶细胞的显着选择性与耐受性的改善相关,并有助于在不减少剂量或洗脱期的情况下维持治疗的能力。此外,TAS-115 还可诱导 MET 扩增的人类荷瘤小鼠的肿瘤显着缩小并延长生存期。这些数据表明TAS-115是一种独特的VEGFR/MET靶向抑制剂,具有提高的抗肿瘤功效和降低的毒性。此外,据报道,通过三联临床药物或TAS-115联合厄洛替尼对EGFR、HGF/Met和VEGF/VEGF受体2进行三重抑制,可能有助于控制EGFR突变的进展。通过逆转 EGFR-TKI 耐药性和抑制血管生成来治疗肺癌。激酶测定:使用迁移率变动测定进行酶抑制研究。简而言之,0.3 μg/mL 重组 MET(rMET,N 端谷胱甘肽 S-转移酶 (GST) 标签;Carna Biosciences)和 1.5 μmol/L FL-肽 2 (Caliper Life Sciences) 或 2 μg/mL 重组 VEGFR2将(rVEGFR2,氨基酸 790 末端,N 末端 6His 标记;Upstate)和 1.5 μmol/L FL-Peptide 22(Caliper Life Sciences)添加到含有 1/2 米氏常数 (Km) 水平的 25 μL 混合物中ATP、100 mmol/L HEPES (pH 7.2)、0.003% (w/v) Brij35、0.04% (v/v) Tween 20、10 mmol/L MgCl2、1 mmol/L 二硫苏糖醇,完整迷你不含 EDTA 的蛋白酶抑制剂混合物片剂(Roche Diagnostics,KK)和 PhosSTOP 磷酸酶抑制剂混合物片剂(Roche Diagnostics,KK),仅在 rVEGFR2 的情况下添加 0.05% (w/v) CHAPSO。将反应混合物在 28°C 下孵育 90 分钟,并通过添加 15 mmol/L EDTA 终止反应。使用 LabChip EZ Reader 版本 2.1.82.0(UCC 版本:1.96,CCD 版本:102)计算磷酸化肽。根据对照孔和药物处理孔中形成的磷酸化肽的量,使用逻辑回归分析计算50%抑制浓度(IC50)。使用 ProfilerPro Kit 1-8 (Caliper Life Sciences) 进行了总共 192 项激酶面板测定,并使用迁移率变动测定进行了分析。细胞测定:将MKN45细胞接种于6孔板中。第二天,将 TAS-115 以所需的最终浓度添加到孔中,并将细胞孵育 30 分钟。洗涤后,使用细胞提取缓冲液(Invitrogen Corporation)裂解细胞。使用试剂和抗体部分中提到的抗体进行免疫印迹分析细胞裂解物。为了研究细胞 VEGFR2 磷酸化,将 HUVEC 铺在胶原蛋白包被的培养皿中 (BD Biosciences, Inc.)。第二天,在过夜孵育期间进行血清饥饿。然后,以所需的最终浓度添加 TAS-115 和 VEGF。孵育 5 分钟后,用哺乳动物蛋白提取试剂(M-PER;Pierce Thermo Scientific)制备细胞裂解液,并使用免疫印迹检测 VEGFR2 磷酸化。使用 LAS1000 plus 和 Multi Gauge Ver. 来分析印迹图像。 3.0(富士胶片)。使用 GAPDH 的信号强度计算图像的相对信号值。
TAS-115 在 PC-9/HGF 和 HCC827 肺癌细胞中抑制 MET 磷酸化。在浓度低于 10 μmol/L 时,TAS-115 不影响 PC-9 或 HCC827 细胞的生长。然而,当与厄洛替尼(0.3 μmol/L)联合使用时,它能以浓度依赖的方式逆转肝细胞生长因子(HGF)在这些细胞系中诱导的厄洛替尼耐药性。[2] TAS-115 抑制由外源性或内源性 HGF 刺激的 PC-9 癌细胞中 VEGF 的产生。[2] TAS-115 以剂量依赖的方式抑制 VEGF 刺激的人真皮微血管内皮细胞(HMVECs)的活力,效果与贝伐珠单抗类似。克唑替尼未显示此效果。[2] 蛋白质印迹分析表明,TAS-115 和贝伐珠单抗能抑制 VEGF 在 HMVECs 中诱导的 VEGFR-2 磷酸化。[2] |
| 体内研究 (In Vivo) |
AS-115(50 mg/kg/d)在治疗期间完全阻止肿瘤生长。在 MET 扩增的人类癌症移植模型中,TAS-115(200 mg/kg/d)可诱导初始肿瘤体积缩小 48%。该模型中 TAS-115 的估计 50% 有效剂量 (ED50) 为 8 mg/kg/d。当以 50 或 200 mg/kg/天的剂量施用 TAS-115 时,TAS-115 显着延长了这些小鼠的存活时间。 TAS-115 在体内抑制 PC-9/HGF 肿瘤的血管生成。此外,厄洛替尼和 TAS-115 的双药组合成功抑制 PC-9/HGF 肿瘤生长,并延缓与持续肿瘤脉管系统抑制相关的肿瘤再生,即使在停止治疗后也是如此。
在携带 PC-9/HGF 肿瘤(过表达 HGF)的裸鼠中,每日口服 TAS-115(75 mg/kg)单药可适度抑制肿瘤生长(第39天抑制率为76.6%)。[2] TAS-115(每日口服75 mg/kg)与厄洛替尼(每日口服50 mg/kg)联用能强力抑制 PC-9/HGF 肿瘤的生长,第39天抑制率达93.7%。该抑制效果优于厄洛替尼、克唑替尼和贝伐珠单抗的三联方案。[2] 使用 TAS-115(每日口服75 mg/kg,持续4天)治疗可在体内抑制 PC-9/HGF 肿瘤的血管生成(通过 CD31+ 血管密度测量)。TAS-115 的抗血管生成效果比贝伐珠单抗更强。[2] 厄洛替尼与 TAS-115 联用能显著延迟在停止为期39天的治疗疗程后的肿瘤再生长。停止治疗10天后,厄洛替尼+TAS-115 组的肿瘤仅增长至停止治疗时初始大小的1.7倍,而厄洛替尼+克唑替尼组和厄洛替尼+克唑替尼+贝伐珠单抗组的肿瘤分别增长至4.5倍和3.3倍。[2] 这种延迟的再生长与即使在停止治疗10天后,肿瘤中持续的血管生成抑制(低血管密度)和高凋亡细胞数量相关。[2] |
| 酶活实验 |
动员位移测定用于酶抑制的研究。简而言之,0.3 μg/mL 重组 MET(rMET,N 端谷胱甘肽 S-转移酶 (GST) 标签;Carna Biosciences)和 1.5 μmol/L FL-肽 2 (Caliper Life Sciences) 或 2 μg/mL 重组 VEGFR2将(rVEGFR2,氨基酸 790 末端,N 末端 6His 标记;Upstate)和 1.5 μmol/L FL-Peptide 22(Caliper Life Sciences)添加到含有 1/2 米氏常数 (Km) 水平的 25 μL 混合物中ATP、100 mmol/L HEPES (pH 7.2)、0.003% (w/v) Brij35、0.04% (v/v) Tween 20、10 mmol/L MgCl2、1 mmol/L 二硫苏糖醇,完整迷你不含 EDTA 的蛋白酶抑制剂混合物片剂(Roche Diagnostics,KK)和 PhosSTOP 磷酸酶抑制剂混合物片剂(Roche Diagnostics,KK),仅在 rVEGFR2 的情况下添加 0.05% (w/v) CHAPSO。 28℃孵育90分钟后,加入15mmol/L EDTA终止反应。使用 LabChip EZ Reader 版本 2.1.82.0(UCC 版本:1.96,CCD 版本:102)计算磷酸化肽。利用逻辑回归分析,根据药物处理孔和对照孔中产生的磷酸化肽的量确定50%抑制浓度(IC50)。 ProfilerPro 试剂盒 1-8(Caliper Life Sciences)用于进行 192 种激酶面板检测,然后使用迁移率变动检测进行分析。
|
| 细胞实验 |
将 Transwell 胶原包被室上室中的 MRC-5(1000 个细胞/300 μL)和肿瘤细胞(8000 个细胞/800 mL)与或不与 TAS-115(1.0 μM)或厄洛替尼(0.3微米)。接下来是拆除上室。利用 MTT 测定来确定细胞活力[2]。
细胞活力实验(MTT法): 将肿瘤细胞(PC-9, HCC827, PC-9/Vec, PC-9/HGF)接种于96孔板中。24小时后,加入包含 TAS-115、厄洛替尼、HGF 或其组合的试剂。细胞继续培养72小时。然后向每孔加入MTT溶液,孵育2小时。移除培养基,用二甲基亚砜溶解甲瓒晶体,在550 nm(参考波长630 nm)处测量吸光度。相对于未处理对照组计算生长百分比。[2] 共培养实验: 将含有或不含 TAS-115 或厄洛替尼的肿瘤细胞置于Transwell系统的下室。将成纤维细胞(MRC-5细胞)置于上室。共培养72小时后,移除上室,对下室进行MTT实验以评估肿瘤细胞活力。[2] 蛋白质印迹法(Western Blot): 从处理过的细胞制备裂解液。蛋白质通过SDS-PAGE分离,转移至膜上,封闭后与一抗(如抗磷酸化-Met、总Met、磷酸化-Akt、总Akt、磷酸化-Erk、总Erk、磷酸化-VEGFR-2、总VEGFR-2)孵育。洗涤后,膜与辣根过氧化物酶标记的二抗孵育。使用增强化学发光底物显示免疫反应条带。[2] VEGF/HGF 产生量测定: 细胞在含血清的培养基中培养。48小时后收集上清液,离心并储存。使用商业酶联免疫吸附测定(ELISA)试剂盒,按照制造商说明书测定HGF和VEGF的浓度。在450 nm处测量颜色强度。[2] |
| 动物实验 |
小鼠:TAS-115 的剂量范围为 12.5、50 和 200 mg/kg/d。舒尼替尼的推荐日剂量为 40 mg/kg。在 SC-9 异种移植模型中,采用口服药物进行长期给药时,疗程连续 14 天或 42 天。治疗期间每周测量两次肿瘤体积 (TV) 和体重。在每个研究周期结束时,评估抗肿瘤疗效[1]。皮下异种移植疗效模型:将培养的 PC-9/Vec 或 PC-9/HGF 肿瘤细胞皮下植入雄性裸鼠侧腹。当肿瘤体积达到 100-200 mm³ 时,将小鼠随机分组。TAS-115 以 75 mg/kg 的剂量口服,每日一次。厄洛替尼以50 mg/kg的剂量口服,每日一次。贝伐珠单抗以100 µg/只小鼠的剂量腹腔注射,每周一次。治疗持续39天。每周测量肿瘤大小三次,并计算肿瘤体积。39天后,部分组停止治疗,以监测肿瘤复发情况,再观察10天。[2]
血管生成评估的短期治疗模型:将已建立皮下肿瘤(≈100 mm³)的裸鼠用药物(例如厄洛替尼、TAS-115)治疗4天。第4天处死小鼠,取出肿瘤,并通过CD31免疫组化染色评估血管生成情况。[2] |
| 毒性/毒理 (Toxicokinetics/TK) |
在裸鼠中,每日口服TAS-115(75 mg/kg)联合每日口服厄洛替尼(50 mg/kg),持续39天,未观察到明显的不良反应,包括体重减轻。[2]
该手稿指出,基于既往研究,存在一个潜在的担忧:抗VEGF疗法(TAS-115作用机制的一部分)可能诱发肿瘤的恶性进展,例如局部侵袭和远处转移增加。因此,生物标志物对于优化MET/VEGFR双重抑制剂的使用可能至关重要。[2] |
| 参考文献 |
|
| 其他信息 |
TAS-115 被描述为一种新型口服抑制剂,对 VEGFR-2 和 MET 均有活性。[2]
该研究提出,使用厄洛替尼联合 TAS-115 来三重抑制 EGFR、MET 和血管生成(通过 VEGFR-2),可能是控制因 HGF/MET 激活而对 EGFR 酪氨酸激酶抑制剂 (TKI) 产生耐药性的 EGFR 突变型肺癌进展的有效策略。[2] 在所用的实验条件下,双药方案(厄洛替尼 + TAS-115)在延缓治疗停止后肿瘤复发方面的疗效比临床上可用的三药方案(厄洛替尼 + 克唑替尼 + 贝伐珠单抗)更为显著。[2] |
| 分子式 |
C28H27FN4O7S2
|
|---|---|
| 分子量 |
614.664987802505
|
| 精确质量 |
614.13
|
| 元素分析 |
C, 54.71; H, 4.43; F, 3.09; N, 9.12; O, 18.22; S, 10.43
|
| CAS号 |
1688673-09-7
|
| 相关CAS号 |
Pamufetinib;1190836-34-0
|
| PubChem CID |
118130255
|
| 外观&性状 |
White to off-white solid powder
|
| tPSA |
196
|
| 氢键供体(HBD)数目 |
4
|
| 氢键受体(HBA)数目 |
10
|
| 可旋转键数目(RBC) |
7
|
| 重原子数目 |
42
|
| 分子复杂度/Complexity |
891
|
| 定义原子立体中心数目 |
0
|
| InChi Key |
NUYQWFCUOAVQAL-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C27H23FN4O4S.CH4O3S/c1-29-26(34)19-14-18-21(15-24(19)35-2)30-11-10-22(18)36-23-9-8-17(13-20(23)28)31-27(37)32-25(33)12-16-6-4-3-5-7-16;1-5(2,3)4/h3-11,13-15H,12H2,1-2H3,(H,29,34)(H2,31,32,33,37);1H3,(H,2,3,4)
|
| 化学名 |
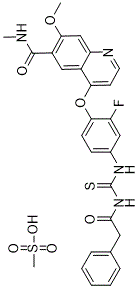
4-[2-fluoro-4-[(2-phenylacetyl)carbamothioylamino]phenoxy]-7-methoxy-N-methylquinoline-6-carboxamide;methanesulfonic acid
|
| 别名 |
TAS115 mesylate; TAS115; Pamufetinib; TAS-115; TAS 115; Pamufetinib mesylate
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~75 mg/mL (~122.02 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (4.07 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (4.07 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL 澄清 DMSO 储备液添加到 900 μL 玉米油中并混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.6269 mL | 8.1344 mL | 16.2689 mL | |
| 5 mM | 0.3254 mL | 1.6269 mL | 3.2538 mL | |
| 10 mM | 0.1627 mL | 0.8134 mL | 1.6269 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
|
|
|
|
|
|
|