| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 50g |
|
||
| 100g |
|
||
| Other Sizes |
|
| 靶点 |
- Trans-Anethole binds to estrogen receptor (ER) and exerts estrogenic activity, with an EC50 of 12.5 μM in recombinant yeast estrogen screen[1]
- Trans-Anethole regulates key enzymes of carbohydrate metabolism, including hexokinase (HK), phosphofructokinase (PFK), and glucose-6-phosphatase (G6Pase); it increases HK and PFK activities by 35% and 42%, respectively, and decreases G6Pase activity by 28% in streptozotocin (STZ)-induced diabetic rats[5] - Trans-Anethole inhibits the growth of Aspergillus flavus (fungal target: cell membrane integrity), with a minimum inhibitory concentration (MIC) of 0.5 mg/mL[7] |
|---|---|
| 体外研究 (In Vitro) |
- 重组酵母中的雌激素活性:Trans-Anethole 以浓度依赖方式诱导转染ER的重组酵母细胞产生β-半乳糖苷酶活性。在12.5 μM(EC50)时,酶活性达到最大响应的50%;在100 μM时,酶活性是空白对照的8.2倍,证实其雌激素活性[1]
- 对细胞的细胞毒性和异雌激素作用:在大鼠分离肝细胞生物转化实验中,100 μM Trans-Anethole 经代谢后产生的产物可使MCF-7人乳腺癌细胞增殖率提高25%(异雌激素作用);而未代谢的100 μM Trans-Anethole 对MCF-7细胞增殖无显著影响。此外,200 μM Trans-Anethole 处理分离的大鼠肝细胞24小时后,细胞存活率下降18%(细胞毒性)[2] - 对黄曲霉菌的抗真菌活性:Trans-Anethole 在体外可抑制黄曲霉菌孢子萌发和菌丝生长。在0.5 mg/mL(MIC)浓度下,可完全抑制孢子萌发;在1.0 mg/mL浓度下,对菌丝生长的抑制率达85%,对黄曲霉素生成的抑制率达90%(相较于对照组)[7] - 对糖代谢酶的调节作用:在STZ诱导糖尿病大鼠的肝匀浆中,Trans-Anethole(100 μg/mL,体外孵育)可使HK活性升高30%、PFK活性升高38%,同时使G6Pase活性降低25%(相较于糖尿病对照组匀浆)[5] |
| 体内研究 (In Vivo) |
- 实验性血栓模型中的保护作用:对雄性Wistar大鼠采用三氯化铁诱导颈动脉血栓。血栓诱导前,每日口服50 mg/kg和100 mg/kg Trans-Anethole 持续7天,与对照组相比,动脉完全闭塞时间分别延长45%和68%。它还可使血栓重量分别降低32%(50 mg/kg)和55%(100 mg/kg),并使100 mg/kg组的血浆血栓素B2(TXB2)水平降低28%[4]
- 糖尿病大鼠中的降血糖作用:STZ诱导的糖尿病大鼠每日通过灌胃给予20 mg/kg和40 mg/kg Trans-Anethole,持续21天。40 mg/kg剂量可使空腹血糖水平较糖尿病对照组降低52%,同时使糖代谢酶恢复正常:肝HK活性升高42%、PFK升高38%、G6Pase降低28%。此外,40 mg/kg组的血清胰岛素水平升高35%[5] - 大鼠中的抗生育作用:雄性白化大鼠每日口服100 mg/kg Trans-Anethole,持续60天。与对照组相比,精子数量减少65%、精子活力降低58%、血清睾酮水平下降42%。组织学检查显示,睾丸曲细精管直径减小、生殖细胞数量减少[6] |
| 酶活实验 |
- 雌激素受体介导的β-半乳糖苷酶活性测定:将转染人ER和β-半乳糖苷酶报告基因的重组酵母细胞接种到含不同浓度Trans-Anethole(0.1–200 μM)的培养基中。细胞在30°C孵育24小时后,用裂解缓冲液裂解,加入邻硝基苯基-β-D-半乳糖吡喃糖苷(ONPG)底物,37°C孵育30分钟,在420 nm处测定吸光度以检测β-半乳糖苷酶活性,通过剂量-响应曲线计算EC50[1]
- 糖代谢酶活性测定:将STZ诱导糖尿病大鼠的肝组织在冰浴缓冲液中匀浆,匀浆在10,000 × g下离心15分钟,上清液用于酶活性测定。HK活性:反应体系含上清液、葡萄糖、ATP和NADP+,通过监测340 nm处NADPH的生成量计算活性;G6Pase活性:反应体系含上清液和葡萄糖-6-磷酸,用钼酸铵试剂在620 nm处测定释放的磷酸量;PFK活性:通过监测340 nm处NADH的氧化量测定(反应体系含上清液、果糖-6-磷酸、ATP和NADH偶联酶)[5] - 黄曲霉菌酶抑制测定:将黄曲霉菌菌丝在缓冲液中匀浆并离心,获得粗酶提取物。提取物与Trans-Anethole(0.25–2.0 mg/mL)和细胞壁合成相关酶底物(如UDP-葡萄糖)共同孵育,通过HPLC定量剩余底物以测定酶活性。在0.5 mg/mL Trans-Anethole 浓度下,细胞壁合成酶活性被抑制60%[7] |
| 细胞实验 |
- 重组酵母雌激素筛选实验:将转染ER的酵母细胞接种到含Trans-Anethole(0.1–200 μM)的96孔板培养基中,30°C孵育24小时后,用台盼蓝排斥法检测细胞活力(确保无细胞毒性),并按Enzyme Assay中描述的方法测定β-半乳糖苷酶活性,以17β-雌二醇作为阳性对照[1]
- MCF-7细胞增殖实验:将MCF-7细胞以5×10³个/孔接种到96孔板,贴壁24小时后,更换为含经生物转化的Trans-Anethole(25–200 μM,来自大鼠肝细胞代谢)或未转化Trans-Anethole 的培养基。孵育72小时后,通过MTT法(570 nm处吸光度)测定细胞增殖,计算相对于对照组的增殖率[2] - 大鼠分离肝细胞实验:通过胶原酶灌注法从雄性Wistar大鼠中分离肝细胞,接种到6孔板,贴壁4小时后加入Trans-Anethole(50–200 μM)。孵育24小时后,通过乳酸脱氢酶(LDH)释放法(490 nm处吸光度)和台盼蓝染色测定细胞活力,收集培养基通过HPLC分析Trans-Anethole 的代谢产物[2] - 黄曲霉菌孢子萌发实验:将黄曲霉菌孢子悬浮于含Trans-Anethole(0.125–2.0 mg/mL)的马铃薯葡萄糖肉汤(PDB)中,28°C孵育,在6、12、24小时通过显微镜观察孢子萌发情况,萌发率定义为芽管长度超过孢子直径的孢子百分比[7] |
| 动物实验 |
实验性血栓模型(大鼠):雄性Wistar大鼠(200-220 g)随机分为3组(每组n=6):对照组(生理盐水)、反式茴香脑50 mg/kg组和反式茴香脑100 mg/kg组。反式茴香脑溶于0.5%羧甲基纤维素(CMC)溶液中,每日灌胃给药,连续7天。第8天,暴露左侧颈动脉,将浸有40%氯化铁溶液的滤纸敷于动脉壁10分钟以诱导血栓形成。使用多普勒血流仪监测血流,记录血栓完全闭塞所需时间。处死后,切取动脉称量血栓[4]
- STZ诱导的糖尿病大鼠模型:雄性Sprague-Dawley大鼠(180-200 g)通过单次腹腔注射STZ(60 mg/kg,溶于pH 4.5的柠檬酸缓冲液)诱导糖尿病。7天后,选择空腹血糖>250 mg/dL的大鼠,并将其分为3组(每组n=6):糖尿病对照组(生理盐水)、反式茴香脑20 mg/kg组和反式茴香脑40 mg/kg组。反式茴香脑溶于0.5% CMC溶液中,每日灌胃给药,持续21天。每周使用血糖仪测量空腹血糖。研究结束时,处死大鼠,收集肝组织进行酶活性测定;收集血清用于胰岛素测定[5] - 抗生育模型(大鼠):雄性白化大鼠(180–200 g)分为两组(每组 n=5):对照组(生理盐水)和反式茴香脑 100 mg/kg 组。反式茴香脑溶于玉米油中,每日灌胃给药,持续 60 天。每 15 天从尾静脉采集血样,用 ELISA 法测定血清睾酮水平。60 天后,处死大鼠;取出睾丸进行组织学检查,并收集附睾进行精子计数和活力评估[6] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
/茴香脑的生物转化/……茴香酸……是主要的尿代谢产物。……给药剂量可定量回收。 反式茴香脑是研究的四种食品添加剂之一,发现其主要通过被动扩散从消化道吸收。吸收动力学部分取决于化合物脂溶系数的差异。 ……在兔和大鼠中,对用于制备茴香味酒精饮料的反式茴香脑进行了静脉和口服给药后的研究。无论给药途径如何,该物质均能迅速从动物体内排出。静脉注射后,该物质主要集中在肝脏、肺脏和脑组织中;口服后,大部分物质则残留在胃中。 反式茴香脑是主要通过被动扩散机制从消化道吸收的化合物之一。 已鉴定并测定了茴香脑在大鼠体内的代谢产物。大多数尿液代谢物也在胆汁中检测到。 代谢/代谢物 茴香脑在兔、小鼠、豚鼠和狗体内生成对丙烯基苯酚。茴香脑在大鼠体内生成对丙烯基苯酚。(数据来自表格) 茴香脑在人、兔和大鼠体内生成茴香酸。茴香脑在大鼠体内生成对甲氧基肉桂醇。 氧化脱甲基反应生成对羟基丙烯基苯和对羟基肉桂酸,是茴香脑的主要生物转化途径。与烯丙基化合物相比,丙烯基取代基的肉桂酰衍生物代谢更为广泛;并且还发生了β-氧化代谢。 - 大鼠肝细胞中的生物转化:分离的大鼠肝细胞将反式茴香脑(100 μM)代谢为两种主要代谢物(通过HPLC-MS鉴定)。反式茴香脑在肝细胞培养中的半衰期为 4.2 小时,65% 的母体化合物在 12 小时内被代谢[2] - 大鼠口服吸收:糖尿病大鼠口服反式茴香脑(40 mg/kg)后,血浆峰浓度 (Cmax) 为 1.8 μg/mL,达峰时间为 1.5 小时 (Tmax),表观分布容积 (Vd) 为 25 L/kg。血浆半衰期 (t1/2) 为 3.8 小时[5] |
| 毒性/毒理 (Toxicokinetics/TK) |
相互作用
用 50 mg/kg 戊巴比妥钠处理的小鼠的平均睡眠时间,在服用 20 和 50 mg 某些化合物后大约增加了一倍;茴香脑的活性较低。 - 肝细胞毒性:反式茴香脑在分离的大鼠肝细胞中表现出剂量依赖性的细胞毒性。在 100 μM 时,LDH 释放增加 12%(轻度毒性);在 200 μM 浓度下,LDH 释放量增加 35%,台盼蓝阳性细胞比例达到 22%(中度毒性)[2] - 生殖毒性:雄性大鼠口服反式茴香脑(100 mg/kg)60 天后出现生殖毒性,包括精子数量(65%)、活力(58%)和睾酮水平(42%)降低,但体重或肝肾重量无显著变化(表明无全身毒性)[6] |
| 参考文献 | |
| 其他信息 |
茴香脑呈白色晶体或液体状,具有茴香油的气味和甜味。 (NTP,1992)
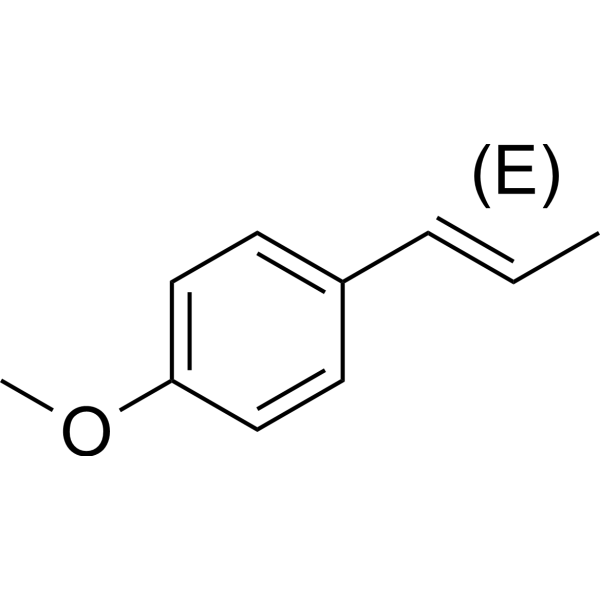
茴香脑是一种单甲氧基苯,其结构为甲氧基苯在4位被丙-1-烯-1-基取代。它是一种植物代谢产物。 据报道,茴香脑存在于苹果属植物、细辛属植物以及其他有相关数据的生物体中。 茴香脑是酿酒酵母(Saccharomyces cerevisiae)中发现或产生的代谢产物。 - 反式茴香脑是土耳其茴香属植物、茴香(Foeniculum vulgare)和八角(Illicium verum)精油的主要成分[1,4,7]。 - 反式茴香脑广泛用于食品工业作为调味剂,以及化妆品工业作为香料成分,其食品用途通常被认为是安全的(GRAS)[3]。 - 雌激素活性反式茴香脑通过与雌激素受体 (ER) 结合发挥作用,激活雌激素反应基因(例如重组酵母中的 β-半乳糖苷酶)[1] - 反式茴香脑的抗血栓作用与 TXB2 水平降低有关,TXB2 可抑制血小板聚集和血栓形成[4] |
| 分子式 |
C10H12O
|
|---|---|
| 分子量 |
148.2017
|
| 精确质量 |
148.089
|
| CAS号 |
4180-23-8
|
| 相关CAS号 |
26795-32-4
|
| PubChem CID |
637563
|
| 外观&性状 |
White to yellow <20°C powder,>21°C liquid
|
| 密度 |
0.9875
|
| 沸点 |
234-237ºC
|
| 熔点 |
23ºC
|
| 闪点 |
90ºC
|
| 折射率 |
1.559-1.562
|
| LogP |
2.728
|
| tPSA |
9.23
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
1
|
| 可旋转键数目(RBC) |
2
|
| 重原子数目 |
11
|
| 分子复杂度/Complexity |
121
|
| 定义原子立体中心数目 |
0
|
| SMILES |
O(C([H])([H])[H])C1C([H])=C([H])C(/C(/[H])=C(\[H])/C([H])([H])[H])=C([H])C=1[H]
|
| InChi Key |
RUVINXPYWBROJD-ONEGZZNKSA-N
|
| InChi Code |
InChI=1S/C10H12O/c1-3-4-9-5-7-10(11-2)8-6-9/h3-8H,1-2H3/b4-3+
|
| 化学名 |
1-methoxy-4-[(E)-prop-1-enyl]benzene
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~674.76 mM)
H2O : ~1 mg/mL (~6.75 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (16.87 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (16.87 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (16.87 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: 50 mg/mL (337.38 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶. 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 6.7476 mL | 33.7382 mL | 67.4764 mL | |
| 5 mM | 1.3495 mL | 6.7476 mL | 13.4953 mL | |
| 10 mM | 0.6748 mL | 3.3738 mL | 6.7476 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。