| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
Angiotensin II receptor type 1 (AT1R)
|
|---|---|
| 体外研究 (In Vitro) |
在与 Flag-AT1R-cherry、HA-β-arrestin-1 和 TRPC3-GFP 共转染的 HEK293 细胞中,TRV120027 TFA (100 nM) 极大地增强了 AT1R 和 TRPC3 与免疫沉淀的 β-arrestin-1 的相互作用[2] 。当 HEK293 细胞与 AT1R、β-arrestin-1 和 TRPC3 共转染时,TRV120027 TFA (100 nM) 会导致 [Ca2+]i 增加。当将 Pyr3 预孵育应用于与 Flag-AT1R-Cherry、HA-β-arrestin-1 和 TRPC3-GFP 共转染的 HEK293 细胞时,这种上升会受到显着抑制 [2]。
G蛋白偶联受体(GPCR)激活引发的急性激素分泌是许多基本生理过程的基础。GPCR信号传导受β-arrestins负调控,β-arrestin是衔接分子,也激活不同的细胞内信号通路。在这里,我们发现TRV120027是一种血管紧张素II受体1型(AT1R)的β-抑制蛋白-1偏置激动剂,通过与瞬时受体电位阳离子通道亚家族C3(TRPC3)偶联来刺激急性儿茶酚胺分泌。我们发现TRV120027促进TRPC3或磷酸肌醇特异性磷脂酶C(PLCγ)募集到AT1Rβarrestin-1信号复合物中。用β-arrestin-2上的对应物替换β-arrestin-1的C端区域,或使用特定的TAT-P1肽阻断β-arrestin-1和PLCγ之间的相互作用,可以消除TRV120027诱导的TRPC3激活。综上所述,我们的结果表明,GPCR arresten复合物通过与离子通道偶联在质膜上启动非脱敏信号传导。这种快速通信途径可能是几种细胞过程的共同机制。[2] 特别是,我们发现β-arrestin-1和β-arrestin-2在TRV120027刺激的原代嗜铬细胞钙增加中起相反的作用(图3e,g)。β-arrestin-1敲除消除了TRV120027诱导的儿茶酚胺分泌所需的钙增加,而β-arrestin-2敲除则增加了TRV120007给药后的细胞内钙。β-arrestin亚型在TRV120027诱导的钙增加中发挥不同作用的现象,增加了这两种亚型在特定细胞环境中相互对立的越来越长的生理效应列表。据我们所知,TRV120027在心脏和肾素系统中的大多数有益作用主要是由β-arrestin-2介导的AT1R信号传导介导的。同样值得注意的是,阿片受体的偏置激动剂已被表征为具有β-arrestin亚型信号选择性。对于AT1R激动剂,TRV120027在等活性模型分析中显示出更多的β-arrestin-1偏倚分子疗效,而TRV120026显示出更多β-arrestin-2偏倚分子疗效(补充图39)。因此,未来的研究旨在确定保留激活β-arrestin-2偏置AT1R信号传导能力但缺乏Gq和βarrestin-1信号传导的配体,这可能会导致治疗心血管疾病的更有益的候选药物[2]。 |
| 体内研究 (In Vivo) |
在增加心输出量和肾血流量的同时,TRV120027 TFA(静脉注射;每分钟 0.3 或 1.5 µg/kg;输注速度,0.5 mL/min)可降低心脏前负荷和后负荷、全身和肾血管阻力以及左心室外部做功。添加到呋塞米中。患有实验性心力衰竭的犬保留其 GFR 和肾排泄功能 [1]。
在这项研究中,与早期研究一致,TRV120027起到了动脉血管舒张剂的作用,这可以从平均动脉压和全身血管阻力的剂量依赖性降低中得到证明。这种血管舒张作用是迅速可逆的。在灌注后清除中,两组的平均动脉压相似,这表明与基线相比,灌注后清除平均动脉压的降低是一种时间效应或继发于呋塞米诱导的利尿作用,而不是TRV120027的持续作用。右心房压力的降低没有统计学意义,这表明TRV120027对动脉血管系统的血管舒张作用比其对静脉系统的影响更为突出。观察到的肺毛细血管楔压降低可能是由于后负荷减少或静脉扩张。尽管与呋塞米+赋形剂组相比没有显著差异,但与基线相比,呋塞米+TRV120027组的心输出量趋于增加。这可能是心脏前负荷和后负荷改善的次要原因,但正如体内和体外数据所表明的那样,通过β-arrestin信号传导对心脏收缩性的积极影响也可能发挥作用。加入TRV120027后,肺血管阻力也降低了,这可能对许多同时患有肺动脉高压和右心衰的抗利尿激素缺乏症患者有益。综上所述,这些血流动力学数据表明,TRV10027可能有助于减轻左心和右心的负担。这也得到了观察到的ANP减少的支持:ANP是由心脏在心脏应激时分泌的,因此减少可以被解释为心脏卸载的神经体液指标。本研究中的BNP测量值比ANP测量值更具可变性,但与F+V组相比,F+T组的BNP也趋于下降。[1] TRV120027与基线相比,肾血流量增加,但与单独使用呋塞米组相比,这并不显著。在C2期间,与单独使用呋塞米相比,肾血管阻力往往较低。尽管肾灌注压显著降低,但与单独使用呋塞米相比,在整个C2至C4期间,尿流量和尿钠钾排泄量保持不变。单独使用呋塞米组的肾小球滤过率趋于增加,这可能是因为它抑制了肾小球小管反馈,在生理条件下,当钠输送增加到肾小球旁装置时,肾小球小管反馈会降低肾小球滤过率。值得注意的是,长期服用环利尿剂会增加对远端肾单位的钠输送,导致远端肾单位段肥大和增生,对呋塞米的作用不敏感;然而,这些变化的临床重要性尚不清楚。尽管肾灌注压降低,但添加TRV120027仍能维持肾小球滤过率,这通常会降低肾小球的静水滤过压。然而,促进肾小球滤过的静水压不仅取决于肾脏灌注压,还取决于传入和传出肾小球小动脉的不同张力。有趣的是,在大多数情况下,血管紧张素II会减少肾血流量,但通过收缩输出小动脉来维持肾小球滤过率,而对输入小动脉的影响很小,从而增加肾小球滤过压。β-arrestin偏置的AT1R配体如TRV120027如何影响传入和传出小动脉张力尚不清楚。还不清楚TRV120027是否影响足细胞功能和过滤系数。值得注意的是,在HF的绵羊模型中,氯沙坦也维持了GFR和尿钠排泄,尽管肾灌注压降低。 为了更好地描述肾小管钠处理,我们使用锂清除技术来评估钠的近端和远端部分再吸收。在给药期间,尽管TRV120027降低了肾灌注压,但两组之间的钠重吸收没有差异,预计这种作用会增加钠重吸收。保留的钠排泄可以用TRV120027阻断血管紧张素II的管状作用来解释,血管紧张素Ⅱ是肾灌注压降低时钠再吸收增加的重要介质。有趣的是,在灌注后清除中,呋塞米+TRV120027组的远端钠重吸收分数显著降低。这可以用醛固酮来解释,在C3期间,TRV120027往往会降低醛固酮的血浆水平。醛固酮通过盐皮质激素受体促进远端小管对钠的再吸收。因此,TRV120027的醛固酮减少作用可能特别重要,因为醛固酮会影响肾单位段,而肾单位段是循环利尿剂不起作用的。尽管这些发现的临床影响仍有待证实,但这些数据表明TRV120027具有增强或保护肾脏的潜力。[1] HF的一个标志是神经体液激活。血管紧张素II和醛固酮的增加,如果不被拮抗,会促进钠潴留、血管收缩和器官纤维化,这些都会导致心力衰竭的进展。与血管紧张素受体阻滞剂一样,血浆肾素活性随着TRV120027的加入而显著增加。这可能部分是由于肾灌注压降低,但也可能是由于TRV120027拮抗了血管紧张素II对肾素分泌的抑制作用。尽管单独使用呋塞米组血管紧张素II有增加的趋势,但我们无法评估呋塞米+TRV120027组的血管紧张素II水平,因为血管紧张素Ⅱ测定与TRV120027交叉反应。重要的是,考虑到由血管紧张素II刺激的醛固酮分泌随TRV120027而减少,这表明肾素的下游信号传导被有效阻断,这意味着TRV1200217对血浆肾素活性的增加影响不大。[1] 总之,当添加到呋塞米中时,TRV120027可以减轻心脏负荷,在给药期间保护肾功能,并导致梗死后更持续的利尿,这可能是由于醛固酮抑制。这些发现表明,TRV120027可能是治疗ADHF的有前景的新药,需要进一步的研究[1]。 |
| 酶活实验 |
电解质通过火焰光度法进行测量。菊粉用蒽酮法测定。如前所述,测量ANP、B型利钠肽、血管紧张素II、血浆肾素活性和醛固酮。钠的近端再吸收分数用锂清除技术计算如下:(1-[锂清除率/肾小球滤过率{GFR}])×100。钠的远端再吸收分数计算为:([锂清除率-钠清除率]/锂清除率)×100[1]。
|
| 细胞实验 |
钙测量[2]
[Ca2+]i的测量如前所述51,52。在实验前,将来源于WT、β-arrestin-1−/−或β-arrestin 2−/-小鼠的小鼠肾上腺嗜铬细胞培养2-4天。所有使用原代嗜铬细胞或HEK293细胞进行的钙测量实验均在室温(22-25°C)下进行。将来源于WT、β-arrestin-1−/−或β-arrestin-2−/-小鼠或转染了不同质粒的HEK293细胞的原代细胞在成像缓冲液I(10 mM葡萄糖、150 mM NaCl、,5mM KCl,1.3mM MgCl2,1.2mM NaH2PO4,3mM CaCl2,20mM HEPES、pH 7.4)。在无Ca2+浴中,成像缓冲液I的3 mM CaCl2被5 mM EGTA替代。通过细胞内Ca2+成像系统测量[Ca2+]i浓度的变化。将来自野生型或不同敲除小鼠的分离的小鼠肾上腺嗜铬细胞在含有2μM Fura-2/AM的溶液中在37°C下孵育30分钟。然后,我们使用Fura-2强度的F340/F380比值来监测AT1R激动剂(如Ang II(100 nM)、SII(1μM)和TRV120027(100 nM))对细胞内钙变化的影响。我们通过双波长比计量荧光法测量了原代细胞内的Ca2+浓度。我们通过基于单色仪的系统用340至380 nm的交替光激发Fura-2。冷却的电荷耦合器件用于测量产生的荧光信号。我们通过F340与F380的比值计算了[Ca2+]i的相对变化。使用Igor软件(WaveMetrix)分析电生理记录。采用t检验或双向方差分析(ANOVA)进行统计分析。 原代嗜铬细胞中的电流测量[2] 从8周龄的野生型雌性小鼠中分离肾上腺嗜铬细胞,并在孵育70-100小时后在用于膜片钳实验的盖玻片上培养。我们使用全细胞膜片钳记录了来自野生型或不同敲除小鼠的肾上腺嗜铬细胞的膜电流。这些原代细胞培养物的细胞外缓冲液含有145mM NaCl,2.8毫摩尔氯化钾,10mM HEPES,1.0mM MgCl2·6H2O,2.0mM氯化钙2.2H2O,10mM葡萄糖和用NaOH调节的pH 7.4。K+外向电流被50 mM四乙基铵阻断,Na+电流的激活被100 nM河豚毒素消除。用内溶液(145mM CsCl,8.0毫摩尔氯化钠,1.0mM氯化镁2.6H2O,10mM HEPES,0.4mM GTP和2.0mM Mg-ATP(用CsOH调节pH至7.3)。当高电阻密封大于1.5千兆欧时,我们用吸力破坏了原代细胞膜。来自野生型小鼠或敲除小鼠的单个原代细胞的漏电流大于-30 pA,未纳入进一步分析。我们监测了无间隙记录和一些细胞参数,如Ccell、Rs(串联电阻)、Rm(膜电阻),以确定贴片的恒定性。在全细胞记录过程中,我们使用放大器电路来最小化电容电流,Rs被补偿了80%(参考文献52)。当浸泡在含有1μM河豚毒素和1μM 4-AP的细胞外溶液中,电压钳制在-60 mV时,TRV120027诱导单个原代小鼠嗜铬细胞中的内向电流。在浴中加入TRV120027(终浓度,5μM)以刺激原代细胞。TRPC3抑制剂Pyr3在浴中的最终浓度为5μM。我们在重力作用下以约12ml的速率用标准外溶液灌注记录室 h−1.我们通过数据采集系统(2012,DigiData 1322A,Axon)和放大器机器记录了离子电流。我们使用pClamp版本9软件来控制命令电压。所有实验和记录均在室温(28°C)下进行。我们使用膜片钳放大器(2012,HEKA EPC10)和patchmaster软件。来源于野生型或敲除小鼠的原代细胞的电流和电压信号经过低通滤波(DC至10KHz),并在20KHz下采集。使用Igor软件包分析数据、图表和电流轨迹。 连续免疫沉淀实验[2] 用TRV120027(100 nM)或对照载体刺激共转染Flag-AT1R-樱桃、HA-β-arrestin-1和TRPC3-GFP的HEK293细胞(通常每个细胞有6个100 mm的培养皿)1分钟。首先通过20000g离心1小时分离质膜组分,然后用PBS洗涤。用Anti-Flag M2琼脂糖免疫沉淀含有Flag-AT1R的蛋白质复合物,然后用3*Flag肽(终浓度,100μg ml-1)洗脱。然后用抗HA珠或抗GFP珠对含有Flag-AT1R的复合物进行免疫沉淀。通过特异性抗体检测到与Flag-AT1R-HA-β-arrestin-1相关的TRPC3或与AT1R–TRPC3相关的PLCγ1。 共免疫沉淀[2] 如前所述进行共免疫沉淀。HEK293细胞与Flag-AT1R-樱桃、TRPC3-GFP(野生型/截短型)和HA-β-arrestin1(野生型-截短型/突变体)共转染。转染48小时后,将细胞饥饿12小时,然后用Ang II(100 nM)、TRV120055(30 nM)或TRV120027(100 nM)刺激1分钟。随后,用冷PBS洗涤细胞,然后收集在冷裂解缓冲液中。使用不同的抗体偶联珠(Flag或HA偶联珠)对细胞裂解物进行免疫沉淀,在4°C下孵育过夜。用冷裂解缓冲液广泛洗涤含有AT1R或arrestin的免疫复合物至少五次,并用特异性抗体通过蛋白质印迹进行分析。 BRET测定[2] BRET测定如前所述。为了测量β-arrestin-1在质膜上的募集,将HEK293细胞与编码Flag-AT1R、Luc-β-arrestin-1、TRPC3和Lyn-YFP的质粒共转染。对于分子间BRET,HEK293细胞与编码Flag-AT1R、Luc-β-arrestin-1或Luc-β-rarestin-2和TRPC3-YFP或TRPV1-YFP/TRPC6-YFP的质粒共转染。对于分子内BRET,将HEK293细胞与编码Flag-AT1R、HA-β-arrestin-1和Luc-TRPC3-YFP质粒的质粒共转染48小时。饥饿12小时后,收获细胞并用PBS洗涤至少三次,然后在37°C下用AngII(100 nM)、TRV120027或其他AT1R激动剂刺激细胞1分钟。随后,我们在室温下用腔肠素h孵育转染的细胞(终浓度为5μM),并使用两种不同的发光方式进行测量(荧光素酶为480/20nm,黄色荧光蛋白为530/20nm)。所有BRET测量均由Mithras LB 940平板读数器进行,信号是通过计算黄色荧光蛋白发出的光强度与萤光素酶发出的强度的比值来确定的。 共聚焦显微镜[2] 如前所述进行共聚焦显微镜检查26,55。将编码HA-β-arrestin-1、TRPC3-GFP和Flag-AT1R-樱桃的质粒共转染HEK293细胞。转染后第二天,将细胞以每皿3×105个细胞的密度接种在35 mm的纤维连接蛋白涂层玻璃底上。第二天,细胞被饥饿,然后在37°C下用Ang II(100 nM)或TRV120027(100 nM)刺激1分钟。然后使用LSM 780激光扫描共聚焦显微镜对样品进行分析。 |
| 动物实验 |
动物/疾病模型:雄性杂种犬(体重20.5–30 kg)[1]
剂量:0.3或1.5 µg/kg/min;输注速率0.5 mL/min 给药途径:静脉注射 实验结果:在犬中观察到剂量依赖性的血管舒张、心肌收缩力增强和心肌耗氧量降低。 研究在两组雄性杂种犬(体重20.5–30 kg;每组n=6)中进行。动物饲喂低钠饮食(希尔思I/d饮食;希尔思宠物营养)。如前所述29,动物右心室植入了带有心外膜导线的起搏器。至少恢复10天后,将起搏器编程为每分钟240次刺激。在起搏后第11天进行急性实验。在急性实验前一天晚上,犬只禁食,并口服300毫克碳酸锂,以便后续评估肾小管功能。实验当天,停止起搏,动物用戊巴比妥和芬太尼麻醉,进行气管插管,并进行机械通气(呼吸频率12次/分;潮气量15毫升/公斤体重),同时给予氧气。在股静脉插入导管,用于输注菊粉、生理盐水和研究药物。在股动脉插入导管,用于测量动脉血压和采集血样。将一根带有球囊尖端、流速导向的热稀释导管经颈静脉送入肺动脉,以测量心脏充盈压和心输出量。通过左侧腰部切口和腹膜后分离,将导管插入输尿管,用于定时收集尿液。术前准备完成后,重新建立起搏,起搏频率为240次/分钟。肾动脉连接电磁流量探头,用于测量肾血流量。给予体重调整剂量的菊粉推注,并开始持续输注菊粉(1 mL/min)和生理盐水(1 mL/min)。平衡60分钟后,进行30分钟的基线清除率测定(C1)。所有清除率测定均包括尿液收集、血流动力学测量以及在清除率测定中途采集血样。完成基线清除后,停止生理盐水输注,开始输注呋塞米(1 mg/kg/小时;输注速率0.5 mL/min)。此外,将动物随机分为两组。一组(F+V)接受赋形剂(生理盐水,0.5 mL/min)输注。另一组(F+T)接受TRV120027(Sar-Arg-Val-Tyr-Ile-His-Pro-D-Ala-OH;0.3 µg/kg/min,溶于生理盐水;输注速率0.5 mL/min)输注。经过15分钟的导入期后,进行第二次30分钟的清除(C2)。此后,F+V组继续接受生理盐水(0.5 mL/min)输注,而F+T组接受TRV120027,剂量为1.5 µg/kg/min(溶于生理盐水;输注速率0.5 mL/min)。同样,在15分钟的导入期后,进行30分钟的清除试验(C3)。之后,停止呋塞米和赋形剂或TRV-120027的输注,并改为生理盐水输注(1 mL/min)。经过30分钟的清除期后,进行最终的30分钟输注后清除试验(C4)。压力和肾血流量以数字方式记录并进行离线分析。心输出量采用热稀释法测量。肾血流量采用电磁流量探头(Carolina Medical Electronics,King,NC)测量。肾灌注压计算为平均动脉压减去右心房压。[1] |
| 参考文献 |
|
| 其他信息 |
TRV120027 已用于研究心力衰竭和肾脏疾病治疗的临床试验。
背景:TRV120027 是一种新型的血管紧张素 II 1 型受体 β-arrestin 偏向性配体;它拮抗经典的 G 蛋白介导的偶联,但与经典的血管紧张素 II 1 型受体拮抗剂不同,它激活 β-arrestin 介导的信号通路。因此,TRV120027 抑制血管紧张素 II 介导的血管收缩,同时通过 β-arrestin 偶联增强心肌细胞收缩力。我们假设在实验性心力衰竭模型中,TRV120027 与呋塞米联用可产生有益的心肾效应。 方法和结果:研究对象为两组经快速起搏诱导心力衰竭的麻醉犬(每组 n=6)。在进行基线清除后,一组(F+V)接受呋塞米(1 mg/kg/小时)加生理盐水输注90分钟,另一组(F+T)接受相同剂量的呋塞米加TRV120027(0.3和1.5 µg/kg/分钟,每次持续45分钟);在药物输注期间进行两次清除。洗脱后,进行输注后清除;组间P<0.05。F+V组和F+T组在给药期间均使利尿和钠排泄增加至相似程度,但输注后清除时,F+T组的尿流量和尿钠排泄量更高。两组的肾小球滤过率均保持正常。F+T组的肾血流量增加,但与F+V组相比差异无统计学意义。与F+V组相比,F+T组降低了平均动脉压、全身血管阻力和肺血管阻力以及心房利钠肽水平。F+T组的肺毛细血管楔压下降幅度大于F+V组。 结论:当与呋塞米联用时,新型β-arrestin偏向性血管紧张素II 1型受体配体TRV120027可维持呋塞米介导的利钠作用和利尿作用,同时降低心脏前负荷和后负荷。这些结果支持TRV120027作为一种有前景的新型心力衰竭治疗药物。[1] 总之,当与呋塞米联用时,TRV120027可减轻心脏负荷,在给药期间维持肾功能,并在输注后产生更持久的利尿作用,这可能是由于醛固酮抑制所致。这些发现表明,TRV120027 可能是一种有前景的治疗急性失代偿性心力衰竭 (ADHF) 的新药,值得进一步研究。[1] G 蛋白偶联受体 (GPCR) 激活触发的急性激素分泌是许多基本生理过程的基础。GPCR 信号传导受到 β-arrestin 的负调控,β-arrestin 是一种衔接分子,也能激活不同的细胞内信号通路。本文揭示,TRV120027 是一种血管紧张素 II 受体 1 型 (AT1R) 的 β-arrestin-1 偏向性激动剂,它通过与瞬时受体电位阳离子通道亚家族 C 3 (TRPC3) 偶联来刺激急性儿茶酚胺分泌。我们发现,TRV120027 促进 TRPC3 或磷脂酰肌醇特异性磷脂酶 C (PLCγ) 募集到 AT1R-β-arrestin-1 信号复合物。将β-arrestin-1的C端区域替换为β-arrestin-2的对应区域,或使用特异性TAT-P1肽段阻断β-arrestin-1与PLCγ的相互作用,均可消除TRV120027诱导的TRPC3激活。综上所述,我们的结果表明,GPCR-arrestin复合物通过与离子通道偶联,在质膜上启动非脱敏信号传导。这种快速通讯通路可能是多种细胞过程的共同机制。[2] |
| 分子式 |
C45H68F3N13O12
|
|---|---|
| 分子量 |
1040.099
|
| 精确质量 |
1039.506249
|
| 相关CAS号 |
TRV-120027;1234510-46-3
|
| PubChem CID |
146014793
|
| 序列 |
{Sar}-Arg-Val-Tyr-Ile-His-Pro-{d-Ala};
H-Sar-Arg-Val-Tyr-Ile-His-Pro-D-Ala-OH.TFA; sarcosyl-L-arginyl-L-valyl-L-tyrosyl-L-isoleucyl-L-histidyl-L-prolyl-D-alanine trifluoroacetic acid
|
| 短序列 |
GRVYIHPA; {Sar}-RVYIHP-{d-Ala}
|
| 外观&性状 |
White to off-white solid powder
|
| tPSA |
395 Ų
|
| 氢键供体(HBD)数目 |
13
|
| 氢键受体(HBA)数目 |
18
|
| 可旋转键数目(RBC) |
26
|
| 重原子数目 |
73
|
| 分子复杂度/Complexity |
1770
|
| 定义原子立体中心数目 |
8
|
| SMILES |
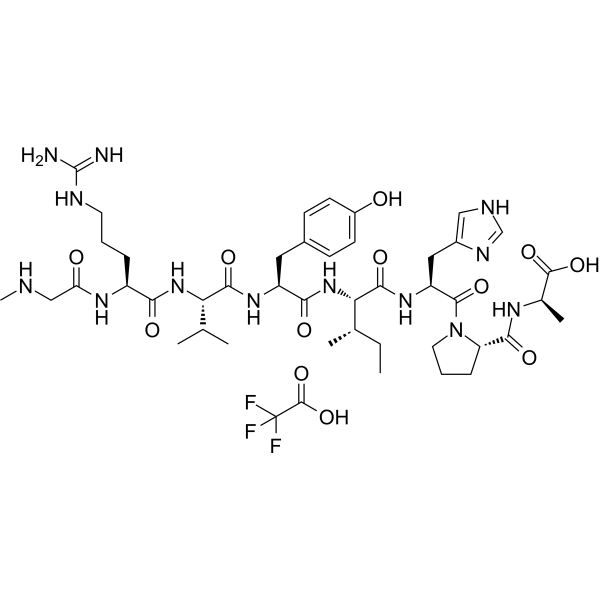
CC[C@H](C)[C@@H](C(=O)N[C@@H](CC1=CN=CN1)C(=O)N2CCC[C@H]2C(=O)N[C@H](C)C(=O)O)NC(=O)[C@H](CC3=CC=C(C=C3)O)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)CNC.C(=O)(C(F)(F)F)O
|
| InChi Key |
TWQGSTLQYSYFSJ-UAPIXIKHSA-N
|
| InChi Code |
InChI=1S/C43H67N13O10.C2HF3O2/c1-7-24(4)35(40(63)53-31(19-27-20-47-22-49-27)41(64)56-17-9-11-32(56)38(61)50-25(5)42(65)66)55-37(60)30(18-26-12-14-28(57)15-13-26)52-39(62)34(23(2)3)54-36(59)29(51-33(58)21-46-6)10-8-16-48-43(44)45;3-2(4,5)1(6)7/h12-15,20,22-25,29-32,34-35,46,57H,7-11,16-19,21H2,1-6H3,(H,47,49)(H,50,61)(H,51,58)(H,52,62)(H,53,63)(H,54,59)(H,55,60)(H,65,66)(H4,44,45,48);(H,6,7)/t24-,25+,29-,30-,31-,32-,34-,35-;/m0./s1
|
| 化学名 |
(2R)-2-[[(2S)-1-[(2S)-2-[[(2S,3S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-5-(diaminomethylideneamino)-2-[[2-(methylamino)acetyl]amino]pentanoyl]amino]-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-3-methylpentanoyl]amino]-3-(1H-imidazol-5-yl)propanoyl]pyrrolidine-2-carbonyl]amino]propanoic acid;2,2,2-trifluoroacetic acid
|
| 别名 |
TRV120027 TFA; TRV-120027 (TFA); TRV-120027 TFA; (2R)-2-[[(2S)-1-[(2S)-2-[[(2S,3S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-5-(diaminomethylideneamino)-2-[[2-(methylamino)acetyl]amino]pentanoyl]amino]-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-3-methylpentanoyl]amino]-3-(1H-imidazol-5-yl)propanoyl]pyrrolidine-2-carbonyl]amino]propanoic acid;2,2,2-trifluoroacetic acid; TRV 120027 TFA
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮和光照。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
Note: 如何溶解多肽产品?请参考本产品网页右上角“产品说明书”文件,第4页。 配方 1 中的溶解度: ≥ 2.5 mg/mL (2.40 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (2.40 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (2.40 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 0.9614 mL | 4.8072 mL | 9.6145 mL | |
| 5 mM | 0.1923 mL | 0.9614 mL | 1.9229 mL | |
| 10 mM | 0.0961 mL | 0.4807 mL | 0.9614 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。