| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 2mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
AMPK (EC50 = 0.8 μM)
The primary target of A-769662 is AMP-activated protein kinase (AMPK), a key regulator of cellular energy metabolism. - In [1]: It selectively activates AMPK heterotrimers, with an EC50 of ~0.8 μM for recombinant human AMPKα2β1γ1 and ~1.2 μM for AMPKα1β1γ1. It shows no significant activity against other kinases (e.g., PKA, PKCα, mTOR) with IC50/Ki > 10 μM [1] - In [2]: For mouse AMPKα2β2γ3 (predominant in skeletal muscle), the EC50 is ~0.6 μM. It does not activate closely related kinases like SNF1 (yeast AMPK homolog) or inhibit phosphatases targeting AMPK [2] - In [3]: It activates AMPKα1-containing complexes in human colon cancer HCT116 cells with an EC50 of ~1.5 μM, with no cross-reactivity with PI3K-Akt or MAPK pathways [3] - In [4]: In rat liver microsomes, A-769662 does not inhibit cytochrome P450 enzymes (CYP1A2, CYP2C9, CYP3A4) at concentrations up to 10 μM, indicating low drug-drug interaction potential [4] |
|---|---|
| 体外研究 (In Vitro) |
A-769662 在激活杆状病毒表达的 AMPK α1,β1,γ1 重组亚型方面同样有效(EC50=0.7 μM)。 A-592107 发挥剂量依赖性 AMPK 激活作用,从不同组织和物种纯化的 AMPK 中观察到的 EC50 仅存在微小变化。使用大鼠心脏、大鼠肌肉或人胚胎肾细胞 (HEK) 测定 A-769662 的 EC50,结果发现它们分别为 2.2 μM、1.9 μM 或 1.1 μM[1]。 A-769662 激活 LKB1 表达 (HEK293) 和 LKB1 缺陷 (CCL13) 细胞中的内源性 AMPK。 A-769662 以变构方式激活包含 1 个和精氨酸 298 (R298G) 取代的 AMPK 复合物。在含有突变体 1 的复合物中,A-769662 抑制 Thr-172 去磷酸化的程度与野生型复合物相似[2]。 A769662 (300 M) 对 MEF 细胞的毒性作用。 A769662 可逆地抑制蛋白酶体活性[3]。
1. 调控肝脏糖代谢(来自[1]): - 原代小鼠肝细胞用A-769662(0.1 μM、0.5 μM、1 μM、5 μM)处理24小时,浓度依赖性抑制胰高血糖素诱导的葡萄糖生成:1 μM时抑制率约45%,5 μM时达68%(葡萄糖氧化酶法检测)。Western blot显示AMPK下游底物ACC(Ser79)磷酸化水平升高,1 μM时p-ACC/ACC比值较对照增加3.2倍[1] 2. 促进骨骼肌脂肪酸氧化(来自[2]): - 小鼠比目鱼肌肌管用A-769662(0.2 μM、1 μM、5 μM)处理16小时,脂肪酸氧化率([14C]-棕榈酸掺入法)较对照增加~35%(1 μM)和~60%(5 μM)。qPCR分析显示,5 μM时脂肪酸转运蛋白1(FATP1)mRNA表达上调2.1倍[2] 3. 抑制结肠癌细胞增殖(来自[3]): - HCT116细胞用A-769662(0.5 μM、2 μM、8 μM)处理72小时,细胞活力(MTT法)呈剂量依赖性降低,IC50约为3.2 μM。流式细胞术显示G1期细胞周期阻滞:G1期细胞比例从对照的52%升至8 μM处理的71%。Western blot显示cyclin D1表达降低,细胞周期抑制剂p21水平升高[3] 4. 体外代谢(来自[4]): - 大鼠肝微粒体与A-769662(1 μM、5 μM)孵育0-120分钟,LC-MS/MS分析代谢产物:5 μM时120分钟仅剩余12%母药,两种主要代谢产物(M1、M2)占总放射性的~65%。人血浆孵育4小时未观察到显著代谢[4] |
| 体内研究 (In Vivo) |
A-769662(30 mg/kg,腹腔注射)显着降低 SD 大鼠的呼吸交换比 (RER)。用 30 mg/kg A-769662 (0.905 nmol/g) 或 500 mg/kg 二甲双胍 (0.574 nmol/g) 治疗的动物肝脏中丙二酰辅酶 A 水平分别降低 33% 和 58%。虽然较低剂量的 A-769662(3 和 10 mg/kg)对糖尿病 ob/ob 小鼠没有影响,但较高剂量(30 mg/kg,bid)显着降低饲喂血浆葡萄糖(降低 30%–40%) )[1]。
1. 肥胖小鼠的降糖作用(来自[1]): - 8-10周龄雄性db/db小鼠(高血糖模型)每日口服灌胃A-769662(10 mg/kg、30 mg/kg、100 mg/kg),持续14天。14天时,30 mg/kg组空腹血糖(FBG)较溶剂组(10% DMSO + 90%生理盐水)降低~22%,100 mg/kg组降低~45%。葡萄糖耐量试验(GTT)显示100 mg/kg组曲线下面积(AUC)减少~30%,肝脏甘油三酯含量降低~38%[1] 2. 高脂饮食(HFD)小鼠的胰岛素敏感性改善(来自[2]): - C57BL/6小鼠高脂饮食12周诱导胰岛素抵抗后,每日腹腔注射A-769662(50 mg/kg),持续7天。胰岛素耐量试验(ITT)显示胰岛素敏感性增加2.3倍(葡萄糖清除率评估)。骨骼肌AMPK活性(激酶活性法)较溶剂组高1.8倍,p-ACC(Ser79)水平升高[2] 3. 异种移植模型的抗肿瘤疗效(来自[3]): - 携带HCT116异种移植瘤(体积~100 mm³)的裸鼠,每日两次口服灌胃A-769662(20 mg/kg、60 mg/kg),持续21天。60 mg/kg组肿瘤生长抑制率(TGI)达~58%(肿瘤体积:380±45 mm³ vs 溶剂组900±62 mm³)。肿瘤组织Western blot显示p-AMPK(Thr172)和p21水平升高,cyclin D1降低[3] 4. 大鼠体内药代分布(来自[4]): - 雄性SD大鼠口服(10 mg/kg)或静脉注射(5 mg/kg)A-769662,口服生物利用度约38%。半衰期(t1/2):口服~3.2小时,静脉注射~1.9小时。血药浓度峰值(Cmax):口服1小时达2.1 μg/mL。1小时时肝脏和骨骼肌药物浓度分别为~3.5 μg/g和~1.8 μg/g,高于血浆浓度(1.9 μg/mL)[4] |
| 酶活实验 |
为了测定糖原磷酸化酶 b (GPb) 活性,将 1.5 μg/mL 兔 GPb 添加到含有 20 mM Na2HPO4 (pH 7.2)、2 mM MgSO4、1 mM β-NADP(β-烟酰胺腺嘌呤二核苷酸磷酸)的反应混合物中, 1.4 U/mL G-6-PDH(6-磷酸葡萄糖脱氢酶)和 3 U/mL PGM(磷酸葡萄糖变位酶)。添加指定浓度的 AMP 或测试化合物后,将糖原(终浓度 1 mg/mL)添加到测定介质中,开始反应。通过测量 340 nm 处的吸光度,在 25°C 孵育 10 分钟后评估 GPb 活性。
1. AMPK激活实验(来自[1]): - 试剂制备:纯化Sf9细胞表达的重组人AMPKα2β1γ1和α1β1γ1;反应缓冲液含50 mM Tris-HCl(pH7.4)、10 mM MgCl₂、0.2 mM ATP、1 mM DTT、100 μM AMPK底物肽(AMARA肽:AMARAASAAALARRR);加入[γ-³²P]ATP(比活度~2500 cpm/pmol)[1] - 实验设置:A-769662用DMSO系列稀释(0.01 μM~10 μM),加入反应混合物(DMSO终浓度≤1%)。加入AMPK(终浓度20 nM)启动反应,30°C孵育40分钟。设置溶剂(DMSO)和阳性对照(5-氨基咪唑-4-甲酰胺核糖核苷酸AICAR,1 mM)组(n=3)[1] - 检测:取25 μL反应混合物点样到P81滤纸,1%磷酸洗涤3次(每次5分钟),丙酮漂洗后风干。液体闪烁计数测放射性,计算相对于溶剂组的激活倍数,四参数逻辑模型拟合EC50[1] 2. CYP酶抑制实验(来自[4]): - 试剂制备:制备大鼠肝微粒体(0.5 mg/mL)和人CYP酶超微粒体(CYP1A2、CYP2C9、CYP3A4);反应缓冲液含50 mM磷酸钾(pH7.4)、1 mM NADPH、特异性CYP底物(如CYP1A2用非那西丁)[4] - 实验设置:A-769662(0.1 μM、1 μM、10 μM)与微粒体/底物在37°C孵育30分钟,乙腈终止反应。HPLC-UV检测特异性底物的代谢产物[4] - 分析:计算相对于溶剂组的抑制率,所有浓度下抑制率<10%,表明无CYP抑制活性[4] |
| 细胞实验 |
经 A-769662 处理或未经 A-769662 处理的 MEF 细胞的细胞活力测定如下:通过胰蛋白酶消化收获细胞,并在室温下黑暗中与 0.5 mg/mL RNase 和 50 μg/mL 碘化丙啶一起孵育;使用 FACScanto 流式细胞仪,使用 488 nm 激发激光和 600 nm 碘丙啶荧光检测,通过流式细胞术分析细胞活力。通过胰蛋白酶消化收获细胞,通过离心收集,在 PBS 中洗涤,并在 -20°C 下在 80% 乙醇中固定过夜,以确定细胞周期每个阶段的细胞百分比。然后将这些固定的细胞离心以除去固定剂,并将它们在含有 0.5 mg/mL RNase 和 50 μg/mL 碘化丙啶的 PBS 中在室温、黑暗中孵育 20 分钟。如上所述,进行流式细胞术分析。 MODFIT 程序用于计算 G1、S 和 G2 细胞的百分比。在指定时间,使用连接到具有 20 倍物镜的倒置显微镜的相机捕获细胞培养物图像。
1. 肝细胞葡萄糖生成实验(来自[1]): - 细胞制备:胶原酶灌注法分离原代小鼠肝细胞,接种到24孔板(1×10⁵个细胞/孔),DMEM(10% FBS)培养过夜[1] - 药物处理:更换为含A-769662(0.1 μM~5 μM)和胰高血糖素(10 nM)的无糖DMEM,孵育24小时,收集上清[1] - 检测:葡萄糖氧化酶试剂盒测上清葡萄糖浓度;RIPA裂解液提取细胞总蛋白,BCA法测蛋白浓度用于标准化,计算相对于仅胰高血糖素组的葡萄糖生成抑制率[1] 2. 肌管脂肪酸氧化实验(来自[2]): - 细胞制备:小鼠比目鱼肌卫星细胞在含2%马血清的DMEM中分化为肌管(7天),接种到12孔板(5×10⁴个细胞/孔)[2] - 药物处理:A-769662(0.2 μM~5 μM)处理细胞16小时,加入[14C]-棕榈酸(0.5 μCi/孔)孵育2小时,加入CO₂捕获液收集氧化的[14C]-棕榈酸[2] - 检测:液体闪烁计数测捕获液放射性,按蛋白含量标准化脂肪酸氧化率[2] 3. 癌细胞增殖与细胞周期实验(来自[3]): - 增殖实验:HCT116细胞接种到96孔板(5×10³个细胞/孔),A-769662(0.5 μM~8 μM)处理72小时。加入MTT(5 mg/mL)孵育4小时,DMSO溶解甲瓒结晶,测570 nm吸光度,计算IC50[3] - 细胞周期实验:HCT116细胞(2×10⁵个细胞/孔,6孔板)用8 μM A-769662处理48小时,70%乙醇固定,PI(50 μg/mL)+RNase A(100 μg/mL)染色,流式细胞术分析,计算G1、S、G2/M期细胞比例[3] |
| 动物实验 |
适应环境后,瘦鼠和ob/ob小鼠根据体重和上午8点测得的血糖水平(尾部采血)随机分配到各个治疗组。每个治疗组选取一部分小鼠(n = 10只瘦型ob/+小鼠和n = 10只ob/ob同窝小鼠)采集基线血浆胰岛素样本。ob/ob小鼠和瘦型同窝小鼠的研究以两种不同的方式进行:首先进行短期研究(5天),然后进行长期研究(14天),以便更全面地评估疗效并描述先前研究中观察到的体重变化。为期 5 天的研究的治疗组如下:ob/ob 载体(0.2% 羟丙基甲基纤维素 [HPMC],腹腔注射,每日两次),A-592107(10 或 100 mg/kg,腹腔注射,每日两次),A-769662(3 或 30 mg/kg,腹腔注射,每日两次),AICAR(375 mg/kg,皮下注射,每日两次),或二甲双胍(450 mg/kg,口服,每日一次,下午服用载体),以及接受载体(腹腔注射,每日两次)治疗的瘦型同窝仔鼠。为期14天的ob/ob小鼠及其瘦型同窝仔鼠研究的治疗组如下:ob/ob小鼠接受赋形剂(0.2% HPMC,腹腔注射,每日两次)、A-769662(3、10或30 mg/kg,腹腔注射,每日两次)或二甲双胍治疗;瘦型同窝仔鼠接受赋形剂或30 mg/kg A-769662(腹腔注射,每日两次)治疗。
1. db/db小鼠降血糖实验(引自[1]): - 动物模型:雄性db/db小鼠(8-10周龄,空腹血糖>16 mmol/L)饲养于12小时光照/12小时黑暗循环环境中,喂以标准饲料[1] - 药物制剂:A-769662溶解于10% DMSO + 90%生理盐水中,配制成浓度分别为1 mg/mL、3 mg/mL和10 mg/mL的溶液[1] - 分组和给药:将小鼠分为 4 组(每组 n=6):载体组(10 mL/kg,灌胃)、A-769662 10 mg/kg、30 mg/kg、100 mg/kg(灌胃,每日一次),连续给药 14 天 [1] - 样本采集:每 3 天通过尾静脉采血(血糖仪)测量空腹血糖 (FBG)。实验结束时,处死小鼠;收集肝组织用于甘油三酯测定(脂质提取试剂盒)和蛋白质印迹分析[1] 2. 高脂饮食小鼠胰岛素敏感性实验(引自[2]): - 动物模型:C57BL/6小鼠(6周龄)喂食高脂饮食(60%脂肪)12周以诱导胰岛素抵抗[2] - 药物制剂:A-769662溶解于5% DMSO + 10% Tween 80 + 85%生理盐水中,配制成5 mg/mL的溶液[2] - 给药:小鼠分为2组(n=5/组):溶剂组(10 mL/kg,腹腔注射),A-769662组(50 mg/kg,腹腔注射,每日一次),连续7天[2] - 疗效评估:进行胰岛素耐量试验(胰岛素0.75 U/kg,腹腔注射);分别于 0、15、30、60 和 90 分钟时测量血糖。收集骨骼肌进行 AMPK 活性测定 [2] 3. HCT116 异种移植实验(引自 [3]): - 肿瘤接种:将 HCT116 细胞(5×10⁶ 个细胞/只小鼠)皮下注射到 6-8 周龄裸鼠的右侧腹部 [3] - 给药:当肿瘤体积达到约 100 mm³ 时,将小鼠分为 3 组(每组 n=5):载体组(10% DMSO + 90% 生理盐水,10 mL/kg,灌胃)、A-769662 20 mg/kg 组和 60 mg/kg 组(灌胃,每日两次),持续 21 天 [3] - 监测:每 2 天测量一次肿瘤体积(长×宽²/2)和体重。在实验终点,切除肿瘤组织进行蛋白质印迹和组织学分析(H&E染色)[3] |
| 药代性质 (ADME/PK) |
1. 大鼠药代动力学(引自[4]): - 研究设计:雄性Sprague-Dawley大鼠(250-300 g)分为两组(每组n=4):口服组(10 mg/kg)和静脉注射组(5 mg/kg)A-769662 [4]
- 样本采集:分别于给药后0.083、0.25、0.5、1、2、4、6、8、12小时采集血样。血浆通过离心(3000×g,10分钟)分离[4] - 参数:口服生物利用度(F)= ~38%;t1/2(口服)= ~3.2小时,t1/2(静脉注射)= ~1.9小时;Cmax(口服)= ~2.1 μg/mL(1小时);口服 AUC₀-∞ = ~15.6 μg·h/mL,静脉注射 AUC₀-∞ = ~20.3 μg·h/mL [4] 2. 组织分布(引自 [4]): - 大鼠(口服 10 mg/kg)分别于给药后 1、3、6 小时处死。收集肝脏、骨骼肌、肾脏和脑组织。 A-769662 的浓度通过 LC-MS/MS 测定:肝脏(1 小时时为 3.5 μg/g)、骨骼肌(1 小时时为 1.8 μg/g)、肾脏(1 小时时为 1.2 μg/g)、脑(1 小时时为 0.3 μg/g)[4] 3. 体外代谢(引自 [4]):- 大鼠肝微粒体:A-769662 (5 μM) 的半衰期约为 45 分钟;鉴定出两种主要代谢物(M1:羟基化衍生物,M2:葡萄糖醛酸苷结合物)[4] - 人血浆:孵育 4 小时后未观察到明显的代谢(92% 的母体药物残留)[4] |
| 毒性/毒理 (Toxicokinetics/TK) |
1. 小鼠急性毒性(引自[1]):- 雌性ICR小鼠分别灌胃给予A-769662(50 mg/kg、150 mg/kg、300 mg/kg)。50 mg/kg和150 mg/kg剂量组未观察到死亡;300 mg/kg剂量组导致20%的小鼠死亡(1/5)。150 mg/kg剂量组观察到轻度嗜睡,48小时内消退[1]。
2. 大鼠亚慢性毒性(引自[4]):- 大鼠每日一次灌胃给予A-769662(10 mg/kg、30 mg/kg、60 mg/kg),连续28天。未观察到体重、食物摄入量或器官重量(肝脏、肾脏、心脏)的显著变化。血清ALT、AST、BUN、Cr均在正常范围内。主要器官未发现组织学病变[4] 3. 血浆蛋白结合率(引自[4]):- 通过超滤法(截留分子量30 kDa)测定。将A-769662(0.1 μM、1 μM、10 μM)加入人、大鼠、小鼠血浆中。在所有浓度下,结合率分别为~91%(人)、~88%(大鼠)、~86%(小鼠)[4] |
| 参考文献 | |
| 其他信息 |
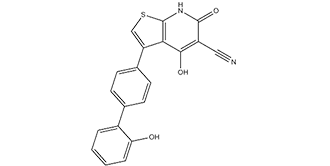
4-羟基-3-[4-(2-羟基苯基)苯基]-6-氧代-7H-噻吩并[2,3-b]吡啶-5-腈是联苯类化合物。
1. 作用机制(来自[1]):A-769662通过与γ亚基调节域结合激活AMPK,变构增强AMPK活性而不增加细胞内AMP水平。它还能抑制 AMPK 磷酸酶,延长 AMPK 磷酸化(Thr172)及其下游信号传导(例如,ACC 抑制、促进葡萄糖摄取)[1] 2. 代谢疾病潜力(引自[1][2]):作为一种选择性 AMPK 激活剂,A-769662 在临床前模型中可改善高血糖、胰岛素抵抗和肝脂肪变性,支持其在 2 型糖尿病和非酒精性脂肪性肝病 (NAFLD) 治疗中的潜力。然而,由于担心长期使用可能产生脱靶效应,它尚未进入临床试验阶段[1][2] 3. 抗肿瘤机制(引自[3]):在癌细胞中,A-769662 通过上调 p21 和下调细胞周期蛋白 D1 来激活 AMPK,从而诱导 G1 期细胞周期阻滞。它还能抑制肿瘤生长所需的合成代谢(例如蛋白质合成),这为与其他抗癌药物联合使用提供了理论依据[3] 4. 药代动力学优势(引自[4]):A-769662具有中等的口服生物利用度(约38%),并优先分布于代谢组织(肝脏、骨骼肌),这与其作用靶点相符。低CYP抑制作用降低了药物相互作用的风险,使其成为临床前研究的理想工具化合物[4] |
| 分子式 |
C20H12N2O3S
|
|---|---|
| 分子量 |
360.3859
|
| 精确质量 |
360.056
|
| 元素分析 |
C, 66.65; H, 3.36; N, 7.77; O, 13.32; S, 8.90
|
| CAS号 |
844499-71-4
|
| 相关CAS号 |
844499-71-4
|
| PubChem CID |
54708532
|
| 外观&性状 |
Off-white to yellow solid powder
|
| 密度 |
1.6±0.1 g/cm3
|
| 沸点 |
630.1±55.0 °C at 760 mmHg
|
| 熔点 |
268.39° C
|
| 闪点 |
334.9±31.5 °C
|
| 蒸汽压 |
0.0±1.9 mmHg at 25°C
|
| 折射率 |
1.781
|
| LogP |
2.81
|
| tPSA |
125.35
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
2
|
| 重原子数目 |
26
|
| 分子复杂度/Complexity |
647
|
| 定义原子立体中心数目 |
0
|
| SMILES |
N#CC1=C(O)C2=C(SC=C2C2C=CC(C3C(O)=CC=CC=3)=CC=2)NC1=O
|
| InChi Key |
CTESJDQKVOEUOY-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C20H12N2O3S/c21-9-14-18(24)17-15(10-26-20(17)22-19(14)25)12-7-5-11(6-8-12)13-3-1-2-4-16(13)23/h1-8,10,23H,(H2,22,24,25)
|
| 化学名 |
4-hydroxy-3-[4-(2-hydroxyphenyl)phenyl]-6-oxo-7H-thieno[2,3-b]pyridine-5-carbonitrile
|
| 别名 |
A-769662; A 769662; A-769662; 4-Hydroxy-3-(2'-hydroxy-[1,1'-biphenyl]-4-yl)-6-oxo-6,7-dihydrothieno[2,3-b]pyridine-5-carbonitrile; A 769662; A769662; 6,7-DIHYDRO-4-HYDROXY-3-(2'-HYDROXY[1,1'-BIPHENYL]-4-YL)-6-OXO-THIENO[2,3-B]PYRIDINE-5-CARBONITRILE; MFCD11977269; UNII-P68477CD2C; A769662
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: ~72 mg/mL (~199.8 mM)
Water: <1 mg/mL Ethanol: <1 mg/mL |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (6.94 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (6.94 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (6.94 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: 1% DMSO+30% polyethylene glycol+1% Tween 80: 30mg/mL 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.7748 mL | 13.8739 mL | 27.7477 mL | |
| 5 mM | 0.5550 mL | 2.7748 mL | 5.5495 mL | |
| 10 mM | 0.2775 mL | 1.3874 mL | 2.7748 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
A769662 inhibits proteasomal function by an AMPK-independent mechanism.FEBS Lett.2008 Jul 23;582(17):2650-4. |
|---|
Inhibition of proteasomal activity by A769662 is reversible.FEBS Lett.2008 Jul 23;582(17):2650-4. |
A769662 affects the in vitro activity of purified 26S proteasomes but not the in vitro activity of purified 20S proteasomes.FEBS Lett.2008 Jul 23;582(17):2650-4. |
A769662 has toxic effects on MEF cells.FEBS Lett.2008 Jul 23;582(17):2650-4. |
|---|
A-769662 allosterically activates AMPK and protects against dephosphorylation of Thr-172.J Biol Chem.2007 Nov 9;282(45):32539-48 |
A-769662 activates endogenous AMPK in LKB1-expressing (HEK293) and LKB1-deficient (CCL13) cells.J Biol Chem.2007 Nov 9;282(45):32539-48 |