| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 2mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|

| 靶点 |
NF-κB; MAPK; Caspase-3/9
|
|---|---|
| 体外研究 (In Vitro) |
异补骨脂素治疗以剂量依赖性方式刺激软骨结节的积累。 Isopsoralen 以时间依赖性方式增加软骨形成标记基因(如胶原蛋白 II、胶原蛋白 X、OCN、Smad4 和 Sox9)的表达。此外,异补骨脂素还可诱导 p38 MAP 激酶和细胞外信号调节激酶 (ERK) 的激活,但不会诱导 c-jun N 末端激酶 (JNK) 的激活。 Isopsoralen 以时间依赖性方式显着增加 BMP-2 蛋白表达,并通过 BMP-2 或 MAPK 信号通路介导软骨调节作用。
Angelicin在结构上与补骨脂素有关,补骨脂素是一种众所周知的化学光敏剂,用于治疗不同的皮肤病。为了验证当归的活性,我们使用人SH-SY5Y神经母细胞瘤细胞来研究其细胞毒性,尽管其作用机制尚未完全阐明。在这里,我们通过细胞活力分析检测了当归的细胞毒性,通过DNA梯状条带分析检测了DNA断裂,并通过蛋白质印迹分析检测了胱天蛋白酶和Bcl-2家族蛋白的激活。我们的研究结果表明,Angelicin以剂量和时间依赖的方式增加细胞毒性,在48小时的孵育时IC(50)为49.56μM。此外,当归剂量依赖性下调包括Bcl-2、Bcl-xL和Mcl-1在内的抗凋亡蛋白的表达,表明参与了内源性线粒体介导的凋亡途径,该途径不参与Fas/FasL诱导的caspase-8介导的外源性、MAP激酶和PI3K/AKT/GSK-3β途径。此外,我们阐明了胱天蛋白酶-9和胱天蛋白酶-3的剂量依赖性上调,这表明当归诱导的细胞凋亡主要是通过内源性胱天蛋白酶介导的途径介导的。特别是,半胱氨酸天冬氨酸蛋白酶-3抑制剂DEVD-fmk诱导了当归诱导的细胞毒性的降低,这证实了在这种凋亡过程中,固有的半胱氨酸天冬氨酰蛋白酶依赖途径并不能阻止使用MAP激酶和GSK-3抑制剂的细胞毒性。总之,我们的数据表明,angelicin是一种有效的诱导人SH-SY5Y神经母细胞瘤细胞凋亡的天然化合物,这表明该化合物可能在人类癌症神经母细胞癌的未来治疗中发挥作用。[1] 包括EB病毒(EBV)和卡波济氏肉瘤相关疱疹病毒(KSHV)在内的人类γ-巨噬细胞病毒是重要的病原体,因为它们在宿主中持续存在并导致各种恶性肿瘤。然而,很少有抗病毒药物可以有效地控制gammaherpes病毒的复制。在这里,我们确定了Angelicin对小鼠gammaherpesvirus 68(MHV-68)的抗病毒活性,该病毒在遗传和生物学上与人类gammaherpes病毒有关。Angelicin是一种天然存在的呋喃香豆素三环芳香族化合物,在病毒进入后以剂量依赖的方式有效地抑制了MHV-68的裂解复制。当归抗病毒活性的IC50估计为28.95μM,而当归的CC50高于2600μM。此外,与当归一起孵育有效地抑制了12-O-十四烷酰佛波醇-13-乙酸酯(TPA)诱导的人γ-巨噬细胞病毒在EBV和KSHV感染细胞中的裂解复制。总的来说,这些结果表明,MHV-68可以成为筛选针对人类γ-巨噬细胞病毒的新型抗病毒药物的有用工具,当归可能为开发针对γ-巨噬细胞的抗病毒药物提供先导结构。[2] Angelicin对细胞活力的影响[3] 为了确定Angelicin是否对RAW 264.7细胞具有潜在的细胞毒性,在LPS存在或不存在的情况下孵育细胞18小时后,通过MTT法评估细胞存活率(图2A)。结果表明,当归在0、12.5、25和50μM的浓度下对RAW 264.7细胞的存活率没有影响。然而,发现当归浓度高达100μM会降低细胞存活率。因此,这些观察结果表明,当归的作用不是由于细胞毒性。 Angelicin对LPS刺激的RAW 264.7细胞产生促炎细胞因子的影响[3] 在这项研究中,我们使用ELISA试剂盒测量培养上清液中TNF-α(图2B-a)和IL-6(图2B-b)的水平。与对照组相比,单独用LPS处理RAW 264.7细胞导致细胞因子产生显著增加。然而,与LPS组相比,当归预处理、LPS刺激的细胞中TNF-α和IL-6的水平以剂量依赖的方式显著降低。 Angelicin对LPS诱导的急性肺损伤小鼠BALF炎症细胞计数的影响 注射LPS 6小时后,总细胞(图3A)、中性粒细胞(图3B)和巨噬细胞(图3C)的数量明显高于对照组(P<0.01)。此外,与LPS组相比,当归(5-10mg/kg)预处理降低了总细胞数(P<0.05)和中性粒细胞数(P<0.01或P<0.05)。相比之下,与LPS组相比,当归(1mg/kg)没有减少巨噬细胞的数量(P<0.05)。 |
| 体内研究 (In Vivo) |
在性激素剥夺的小鼠中,异补骨脂素/Angelicin对雄性和雌性小鼠均具有显着的骨保护作用。异补骨脂素治疗 8 周可改善小梁骨微结构并增加骨强度。 Wistar大鼠静脉注射后异补骨脂素的消除半衰期为5.35小时。异补骨脂素组织曲线下面积依次减小的顺序为肾>肺>肝>心>脾>脑。 Wistar大鼠口服异补骨脂素后消除半衰期为5.56 h,生物利用度为70.35%。
当归素/Angelicin对LPS诱导的急性肺损伤小鼠细胞因子产生的影响[3] LPS攻击后6小时,收集BALF以研究细胞因子的水平。与对照组相比,LPS攻击显著增加了BALF中TNF-α(图4A)和IL-6(图4B)的水平。我们发现,与LPS组相比,当归显著降低了TNF-α和IL-6的产生。 当归素/Angelicin对LPS诱导的急性肺损伤小鼠肺组织学变化的影响[3] 为了评估经LPS处理的小鼠经当归治疗后的组织学变化(图5),在注射LPS后6小时收集肺部进行h&E染色。对照组肺组织未见明显组织学改变。相比之下,在LPS组中,肺标本的肺结构变化最为显著,如肺泡壁增厚、肺泡出血、间质水肿和炎性细胞浸润。然而,用当归(1、5和10mg/kg)预处理显著减轻了这些病理变化(图5)。 Angelicin对LPS诱导的肺W/D比值的影响[3] 肺水肿是炎症的典型症状,由肺W/D比值表示(图6)。与对照组相比,LPS刺激后肺W/D比值显著增加。相比之下,在当归组中,肺水肿的形成明显减少。 当归素/Angelicin对LPS诱导的急性肺损伤小鼠MPO活性的影响[3] 中性粒细胞是急性肺损伤炎症反应的重要组成部分。为了研究当归是否有效阻止LPS诱导的肺多形核细胞积聚的增加,评估了MPO的活性(图7)。与对照组相比,我们发现LPS滴注后6小时MPO活性显著增加。然而,腹腔注射当归显著抑制了MPO活性。 当归素/Angelicin对LPS诱导的急性肺损伤小鼠NF-κB和MAPK活化的影响[3] 众所周知,NF-κB(图8A)和MAPK(图8B)信号通路在调节炎症介质的产生中起着重要作用。因此,我们研究了当归对磷酸ERK、磷酸JNK、磷酸p38、磷酸IκBα和磷酸NF-κB p65活化的影响。Western印迹结果显示,LPS刺激增加了MAPK、磷酸化IκBα和磷酸化NF-κB p65的磷酸化水平。除ERK磷酸化外,这种LPS诱导的蛋白质磷酸化被当归(1、5和10mg/kg)显著阻断。 |
| 酶活实验 |
发起人报告人分析[2]
为了进行启动子活性分析,在转染前24小时将293T细胞(1.2×105/孔)接种在24孔板中。使用聚乙烯亚胺共转染每个孔共650 ng质粒DNA,并在转染后1小时用Angelicin处理。一个含有上游210 bp RTA序列的萤光素酶报告质粒克隆到pGL3-basic(pGL3-RTAp)中,是英国利物浦大学Ebrahimi博士的一份礼物。质粒DNA混合物包括萤光素酶报道质粒pGL3-RTAp(50 ng)、pCMV-β-gal(80 ng)和Flag-mRTA(0.04–10 ng)。加入质粒pCMV2标志(260-269.96 ng)作为填充DNA,得到650 ng的总DNA。根据制造商的说明使用萤光素酶测定系统。转染后48小时,用1×PBS洗涤细胞,并用1×被动裂解缓冲液裂解。经过一个冻融循环后,将细胞离心以分离细胞碎片。将细胞裂解物(20μl)加入萤光素酶底物缓冲液(40μl)中,用Victor 3测量萤光素酶活性。将细胞裂解物(20μl)加入β-半乳糖苷酶底物(30μl)中并孵育20分钟。通过PowerWave XS(Bio-Tek)测量β-半乳糖酶的活性,并将其用作内部对照。 菌斑减少试验[2] 为了确定MHV-68抗病毒活性的IC50,使用MHV-68 WT进行了斑块减少试验,如前所述,并进行了轻微修改(Harper,2000)。简而言之,Vero细胞以5×104个细胞/孔的速度接种在12孔板上。第二天,将细胞与MHV-68(约100 pfu/孔)一起孵育90分钟,并在去除病毒接种物后加入含有10%FBS和0.6%甲基纤维素的DMEM覆盖培养基。将测试化合物以指定浓度稀释到正常生长培养基中进行预处理(病毒采用前3小时)或覆盖培养基中用于后处理,并加入细胞中。孵育5天后,将细胞固定并用0.2%结晶紫在20%乙醇中染色。然后计数斑块,并确定IC50值,即使用Prism 6将斑块数量减少50%所需的Angelicin量。 细胞因子测定[3] 根据制造商推荐的方案,使用夹心ELISA试剂盒(Biolegend)测量BALF上清液中TNF-α和IL-6的浓度。在450nm处读取微孔板的光密度,TNF-α和IL-6的水平表示为每毫升BALF的象形或纳克。 MPO测定[3] 使用从南京建成生物工程研究所购买的检测试剂盒测定肺部MPO活性。LPS处理6小时后,在乙醚麻醉下处死小鼠并切除右肺。将100毫克肺组织均质化并在提取缓冲液中流化,以获得5%的匀浆。匀浆在4°C下以13000g离心30分钟,无细胞提取物在-20°C下储存,直至进一步使用。通过使用96孔板读数器测量460nm处的吸光度变化来测定酶活性。 |
| 细胞实验 |
ATDC5 细胞以每孔 5×103 个细胞的密度接种在 96 孔板中,在含有 10% FBS 的培养基中孵育过夜,然后接受不同浓度的异补骨脂素。 24 小时孵育期后,用磷酸盐缓冲盐水 (PBS) 洗涤细胞后,用含有 100 μg/ml MTT 的培养基在 37°C 下处理细胞 2 小时。 PBS 洗涤后,将细胞溶解在 200 μl DMSO 中。通过使用分光光度计测量 540 nm 波长处的吸光度,对所得溶解的紫色甲臜进行定量。
细胞活力测定[1] 根据制造商的方案,使用细胞毒性测定试剂盒CCK-8测定细胞存活率。将细胞铺入96个孔中,密度为50-60%融合。在饥饿培养基中孵育24小时后,如图例所示,用不同浓度的Angelicin处理细胞。化学处理48小时后,将CCK-8(10μl)加入板的每个孔中并孵育3小时。使用96孔微量滴定板读数器(分子装置)测定CCK-8在450 nm处的吸光度。测量每组三个孔的平均浓度。 DNA断裂检测[1] 为了检测凋亡DNA断裂,使用梯形DNA断裂试验进行DNA断裂试验。简而言之,如图图例所述,在不同浓度的Angelicin处理后收集细胞,并在PBS中洗涤。然后用500μl基因组DNA提取缓冲液(0.1 M NaCl、10 mM EDTA、0.3 M Tris-HCl、0.2 M蔗糖,pH 8.0)裂解细胞。将裂解物与20μl 10%SDS溶液一起孵育,并在65°C下孵育30分钟。在4°C和12000 rpm下离心10分钟后,加入120μl乙酸钾(pH 5.3)并在冰上储存1小时。将2μl(10mg/ml)RNase加入上清液中,在室温下孵育30分钟。通过在苯酚/氯仿提取中洗涤所得颗粒并用乙醇沉淀来提取DNA,然后用蒸馏水溶解。在含有溴化乙锭的0.8%琼脂糖凝胶中通过电泳观察DNA断裂。 蛋白质印迹分析[1] 将人SH-SY5Y神经母细胞瘤细胞在含有0.5%FBS的DMEM中的60 mm培养皿上饥饿24小时。如每个图例所示,用不同浓度的Angelicin预处理细胞,然后用冰冷的PBS洗涤两次。细胞在裂解缓冲液(2%SDS、Na3VO4和蛋白酶抑制剂混合物)中裂解。在冰上孵育10分钟并以10%振幅超声处理10秒后,将裂解物离心(13000 rpm,20分钟)。收集上清液,通过Bradford法测定蛋白质浓度。通过SDS-PAGE(8%、10%或15%的还原凝胶)分离等量的蛋白质,转移到聚偏二氟乙烯膜上,并用5%的脱脂乳封闭。将膜在4°C的第一抗体中孵育过夜。然后在TBST(10 mM Tris,140 mM NaCl,0.1%吐温-20,pH 7.6)中洗涤膜,与适当的二抗一起孵育,并在TBST中再次洗涤。通过增强化学发光观察条带并将其暴露于X射线胶片。通过Bio-profile Bio-1 D应用程序量化每个条带的相对丰度,并将表达水平归一化为β-actin。 细胞毒性试验[2] 如前所述(Cho等人,2008),通过3-(4,5-二甲基噻唑-2-基)-2,5-二苯基溴化四唑(MTT)试验评估了Angelicin的细胞毒性。简而言之,将104个细胞接种在100μl完全培养基中,放入96孔板的每个孔中,与2μl体积的不同浓度的当归一起孵育24小时。处理后,向每个孔中加入10μl MTT溶液(1×PBS中的5mg/ml),混合物在37°C下再孵育3小时。然后将平板离心,丢弃上清液,并向每个孔中加入100μl DMSO。在晶体溶解后,在570nm处测量还原的MTT量。 细胞培养和治疗[3] RAW 264.7小鼠巨噬细胞系购自中国细胞系库。在37°C下,在空气中5%CO2的加湿气氛下,在添加了10%热灭活胎牛血清的Dulbecco改良Eagle培养基中培养细胞。在所有实验中,细胞在有或没有不同浓度的Angelicin的情况下孵育,Angelicin总是在LPS(1μg/mL)处理前1小时加入。 MTT法测定细胞活力[3] MTT用于评估细胞存活率。机械刮取RAW 264.7细胞,在37°C、5%CO2培养箱中以4×105个细胞/mL的密度将100μL细胞铺在96孔板上1小时。然后用50μL不同浓度的Angelicin(0-200μg/mL)处理细胞1小时,然后用50µL LPS(4μg/mL)刺激。LPS刺激18小时后,向每个孔中加入20μL MTT(5mg/mL),并将细胞进一步孵育4小时。然后去除上清液,用150μL/孔DMSO溶解。在微孔板读数器上在570nm处测量光密度。 促炎细胞因子(TNF-α和IL-6)产生的测量[3] 在任何处理之前,将Angelicin溶解在DMSO中。将RAW 264.7细胞(4×105个细胞/mL)接种到24孔板中,用12.5、25和50μg/mL的Angelicin预处理1小时,然后用1mg/L的LPS处理24小时。收集无细胞上清液,按照制造商的方案通过ELISA分析TNF-α和IL-6。 |
| 动物实验 |
LPS诱导的急性肺损伤(ALI)模型[3]
所有小鼠随机分为五组:对照组、LPS组和Angelicin(1、5和10 mg/kg)+ LPS组。在诱导急性肺损伤前,腹腔注射Angelicin(剂量分别为1、5和10 mg/kg)。预处理Angelicin一小时后,用乙醚麻醉BALB/c小鼠,并将10 μg LPS溶于50 μL磷酸盐缓冲液(PBS)中,经鼻内滴注,以诱导肺损伤。对照组小鼠仅给予50 μL不含LPS的PBS。LPS暴露六小时后,用乙醚窒息法处死小鼠。通过气管插管,用0.5 mL高压灭菌的PBS对肺脏进行三次灌洗,灌洗总量达1.3 mL。切除的肺脏置于无菌离心管中,并储存于−80°C。从每个样本中回收的支气管肺泡灌洗液(BALF)经离心(4°C,3000 rpm,10 min)以沉淀细胞。将细胞沉淀重悬于PBS中,使用血细胞计数器进行细胞总数计数,并制备细胞涂片,采用Wright-Giemsa染色法进行细胞分类计数。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
目的:探讨不同浓度补骨脂素和异补骨脂素的鼻腔吸收规律。方法:建立大鼠原位鼻腔循环实验模型,并采用高效液相色谱法(HPLC)测定补骨脂素和异补骨脂素的含量。结果:补骨脂素和异补骨脂素的鼻腔吸收符合零级动力学,且随着浓度的增加而达到饱和。结论:制备补骨脂素和异补骨脂素鼻用制剂需要合适的浓度。 补骨脂素类化合物是一类新型药物,其中补骨脂素和异补骨脂素是其活性成分。本研究采用液相色谱-串联质谱法,研究了静脉注射给药于Wistar大鼠后,这两种化合物的药代动力学、组织分布和排泄情况。补骨脂素和异补骨脂素的消除半衰期分别为4.88小时和5.35小时。给药后,补骨脂素在各组织中的药时曲线下面积(AUC)依次为:肝 > 肺 > 心 > 肾 > 脾 > 脑;异补骨脂素则为:肾 > 肺 > 肝 > 心 > 脾 > 脑。给药后,51.27%的补骨脂素和56.25%的异补骨脂素以原形排出体外,尿液是主要的排泄途径。此外,还研究了Wistar大鼠口服补骨脂素和异补骨脂素后的药代动力学。补骨脂素和异补骨脂素的消除半衰期分别为4.13小时和5.56小时,相对生物利用度分别为61.45%和70.35%。总体而言,结果表明,补骨脂素类化合物具有较高的口服生物利用度,静脉注射后能迅速广泛分布于组织中,但清除和排泄缓慢。 生物半衰期 ……静脉注射补骨脂素和异补骨脂素后,Wistar大鼠的消除半衰期分别为4.88小时和5.35小时。……口服补骨脂素和异补骨脂素后,Wistar大鼠的消除半衰期分别为4.13小时和5.56小时…… |
| 毒性/毒理 (Toxicokinetics/TK) |
毒性概述
鉴定和用途:异补骨脂素是一种天然呋喃香豆素。它曾被用作实验性疗法。人体研究:异补骨脂素在体外作为雌激素受体α激动剂发挥作用,并显著促进MCF-7细胞增殖。当归素在光活化后形成DNA单加合物。在人体细胞中,异补骨脂素促进姐妹染色单体交换。动物研究:腹腔注射和口服异补骨脂素均对大鼠、小鼠和兔具有强效的镇静、抗惊厥和中枢肌肉松弛作用。异补骨脂素在细菌和动物细胞中具有光致突变性,可生成DNA单加合物。 许多呋喃香豆素的作用机制是基于其与DNA和其他细胞成分(如RNA、蛋白质以及膜蛋白,例如磷脂酶A2和C、钙依赖性和cAMP依赖性蛋白激酶和表皮生长因子)形成光加合物的能力。呋喃香豆素可插入DNA碱基对之间,并在紫外线A照射后生成环加合物。(L579) 相互作用 光化学遗传毒性可通过对大多数标准体外遗传毒性检测方法进行适当改进来检测。检测潜在光遗传毒性物质最灵敏的方法似乎是在体外研究哺乳动物细胞中的DNA损伤(DNA链断裂、染色体畸变、微核)。在之前的论文中,我们提出利用中国仓鼠V79细胞的微核试验来研究光致基因毒性化合物。该试验适用于检测具有不同光活化机制的多种光致基因毒性化合物。为了拓展该试验的实验经验,本文进一步展示了对16种潜在光敏剂进行筛选试验的数据。我们同时考察了这些化合物的光致断裂性和光致细胞毒性。迄今为止,所有在光微核试验中被检测为光致基因毒性的物质也表现出光致细胞毒性,反之则不然。在本研究测试的化合物中,噻洛芬酸、5-巯基嘌呤(5-MOP)、白芷素、硝西泮、苄氟噻嗪和达卡巴嗪均具有光致基因毒性和光致细胞毒性。此外,硫唑嘌呤的代谢产物6-巯基嘌呤对这两个终点均呈阳性,而硫唑嘌呤则呈阴性。硫唑嘌呤似乎是一种在体外缺乏光(基因)毒性,但可通过酶促代谢转化为光敏剂的化合物。本研究的结果将光微核试验的数据库扩展至35种化合物,这些化合物均采用相同的方案和相同的照射条件进行测试。本文总结并讨论了所有这些化合物的光基因毒性结果,并探讨了它们不同的光活化机制、光细胞毒性和光致癌性。 本研究发现,补骨脂粗提物在体外可抑制乙酰胆碱酯酶活性,并能改善东莨菪碱引起的大鼠抑制性回避反应和水迷宫空间行为能力的损伤。在所有组分中,氯仿组分对乙酰胆碱酯酶活性的抑制作用最强,并能减轻东莨菪碱诱导的抑制性回避反应损伤。高效液相色谱法鉴定出补骨脂素和异补骨脂素是补骨脂氯仿提取物中的两种主要成分,它们也能减轻抑制性回避反应的损伤程度。结果表明,补骨脂素和异补骨脂素是补骨脂的主要活性成分,能够逐步逆转东莨菪碱诱导的遗忘症,其作用部分与抑制乙酰胆碱酯酶(AchE)活性并激活中枢胆碱能神经系统有关。单功能补骨脂素联合UVA辐射不具有致红斑性,且致突变性低于双功能补骨脂素联合UVA辐射。因此,近年来,它们作为治疗多种皮肤疾病的潜在药物受到了广泛关注。本研究旨在探讨小鼠接受单功能补骨脂素联合UVA辐射治疗后的免疫学副作用。我们发现,白芷素联合UVA辐射能够抑制小鼠对二硝基氟苯的接触性超敏反应。这种免疫反应的降低与脾脏抑制细胞的存在有关,这些细胞能将抑制作用传递给正常受体。用白芷素和UVA辐射治疗也降低了治疗部位Thy-1+和Ia+树突状表皮细胞的数量。我们得出结论,虽然这种单功能补骨脂素不具有光毒性,但它在小鼠体内具有免疫抑制活性。 由于使用8-甲氧基补骨脂素和长波紫外线A (UVA) 辐射治疗银屑病等皮肤疾病会产生不良副作用,因此,使用致红斑性、致突变性较低且通常无光毒性的单功能补骨脂素受到了广泛关注。然而,人们对单功能补骨脂素的免疫抑制特性知之甚少。本研究旨在探讨肠外给药单功能补骨脂素白芷素联合UVA辐射对免疫反应的影响。注射白芷素后进行UVA照射可显著抑制对同种异体抗原的迟发型超敏反应,且呈剂量依赖性。同样,经白芷素和UVA处理动物的脾细胞对同种异体抗原的增殖能力也显著降低。这种抑制作用特异性针对用于致敏白芷素和UVA处理动物的同种异体抗原,并伴有脾脏中抗原特异性抑制性T淋巴细胞的出现。这些数据表明,全身性给予单功能补骨脂素后进行UVA照射对免疫反应的影响与注射双功能补骨脂素后观察到的影响相似。这些发现还提示,使用双功能补骨脂素和UVA照射引起的严重皮肤光毒性并非诱导全身免疫抑制的必要条件。此外,白芷素联合UVA可诱导全身性抗原特异性免疫抑制,且无明显的皮肤光毒性,这提示该化合物及其相关化合物可能用于特异性抑制不必要的免疫反应。 有关异补骨脂素(共12种)的更多相互作用(完整)数据,请访问HSDB记录页面。 非人类毒性值 小鼠腹腔注射LD50:254 mg/kg 大鼠腹腔注射LD50:165 mg/kg 大鼠口服LD50:322 mg/kg |
| 参考文献 |
|
| 其他信息 |
欧芹素是一种呋喃香豆素。
据报道,欧芹素存在于大穗香豆(Hoita macrostachya)、秋曼陀罗(Mandragora autumnalis)以及其他有相关数据的生物体中。 欧芹素存在于芫荽中。欧芹素是欧芹(Angelica archangelica)根和叶的成分之一。欧芹素存在于欧洲防风草和患病芹菜的根和表面。欧芹素是一种呋喃香豆素。它也存在于沥青木(Bituminaria bituminosa)中。它被列入国际癌症研究机构(IARC)第3类致癌物清单(欧芹素与紫外线A辐射)。(维基百科)。 另见:欧芹根(部分);库伦科里叶(Cullen corylifolium)果实(部分)。 作用机制 365纳米紫外线与欧芹素的联合作用抑制了λ噬菌体注入宿主细胞。本文从噬菌体头部内部DNA的光化学诱导交联角度探讨了注射抑制现象。根据ppp方法,利用量子化学计算得到的黄毒素、补骨脂素和当归素的第一激发态电子结构非常相似。 治疗用途 /探索治疗/ 背景:现代研究表明,补骨脂素对多种动物和人类的肿瘤生长具有显著的抑制作用。目的:利用色谱技术和分离纯化方法从传统中药补骨脂(Psoralea corylifolia L.)中分离得到香豆素类化合物——补骨脂素和异补骨脂素,并观察补骨脂素和异补骨脂素对裸鼠骨肉瘤移植瘤生长的抑制作用及不良反应。方法:以补骨脂(Psoralea corylifolia L.)的干燥成熟果实为原料,采用乙醇回流法制备补骨脂粗提物。采用柱层析法分离粗提物;根据核磁共振氢谱(¹H-NMR)和碳谱(¹³C-NMR)对化合物进行结构鉴定,鉴定出两种化合物分别为补骨脂素和异补骨脂素,含量分别为99.7%和99.6%。建立裸鼠骨肉瘤模型;将裸鼠随机分为:生理盐水组、补骨脂素低剂量组、补骨脂素高剂量组、异补骨脂素低剂量组、异补骨脂素高剂量组和顺铂组。观察各组裸鼠骨肉瘤的体积和重量抑制率;采用放射免疫分析法测定血清碱性磷酸酶活性;测定外周血细胞和骨髓有核细胞计数。采用光学显微镜观察心脏、肝脏、脾脏、肺脏、肾脏及肿瘤的组织病理学;采用电子显微镜观察肿瘤细胞的精细结构。结果:补骨脂素和异补骨脂素低剂量组的肿瘤体积抑制率分别为43.75%和40.18%,肿瘤重量抑制率分别为38.83%和37.77%。补骨脂素和异补骨脂素高剂量组的肿瘤体积抑制率分别为67.86%和66.96%,肿瘤重量抑制率分别为49.47%和47.87%。补骨脂素和异补骨脂素均能显著降低血清碱性磷酸酶(AKP)水平。补骨脂素和异补骨脂素可诱导骨肉瘤细胞凋亡或坏死。给予高剂量补骨脂素和异补骨脂素后,观察到扭体、疲乏和活动减少等毒性反应。肾脏组织病理学检查显示肾小管间质扩张和充血,以及肾细胞间隙炎症细胞聚集。补骨脂素和异补骨脂素未对骨髓或心脏、肺、肝脏和脾脏等其他器官造成明显的毒性副作用。结论:补骨脂素和异补骨脂素对裸鼠骨肉瘤移植瘤具有生长抑制作用,并能诱导肿瘤细胞凋亡或坏死,且无明显毒性作用。 /EXPL THER/ 据报道,补骨脂(Psoralea corylifolia L.)果实中发现的呋喃香豆素类化合物——当归素,具有抗炎活性。本研究旨在探讨白芷素对卵清蛋白(OVA)诱导的小鼠过敏性哮喘的保护作用。小鼠分别于第0天和第14天进行OVA致敏,并于第21天至第23天进行三次OVA激发。在首次OVA致敏后,于OVA激发前1小时腹腔注射白芷素(2.5、5、10 mg/kg)。采用酶联免疫吸附试验(ELISA)检测支气管肺泡灌洗液(BALF)中IL-4、IL-5和IL-13的水平以及血清中IgE的水平。采用苏木精-伊红(H&E)染色检测肺组织学变化。结果显示,白芷素显著抑制了炎症细胞向肺部的浸润。组织学研究表明,白芷素显著减轻了OVA诱导的肺损伤。同时,白芷素治疗呈剂量依赖性地抑制了卵清蛋白(OVA)诱导的支气管肺泡灌洗液(BALF)中IL-4、IL-5和IL-13的产生以及血清中IgE的水平。此外,白芷素还被发现能够抑制气道高反应性和NF-κB的激活。总之,我们的结果表明,白芷素通过抑制NF-κB的激活来抑制过敏性气道炎症和高反应性。 /EXPL THER/ 异补骨脂素是一种呋喃香豆素类化合物,具有雌激素样活性。本研究旨在探讨异补骨脂素在脊髓损伤(SCI)动物模型中的雌激素样神经保护作用。结果表明,腹腔注射异补骨脂素(5和10 mg/kg/天,持续两周)显著改善了SCI小鼠的后肢运动功能,这体现在BMS评分和倾斜平面角度测试中。形态学数据显示,异补骨脂素显著减轻了脊髓灰质的损伤,并诱导雌激素受体α(ERα)水平上调。ERα拮抗剂MPP(0.3 mg/kg)可阻断异补骨脂素的神经保护作用,而雌激素受体β(ERβ)拮抗剂PHTPP(0.3 mg/kg)则无此作用。异补骨脂素治疗可增加脊髓损伤(SCI)小鼠脊髓中磷酸化PI3K和AKT(P-PI3K和P-AKT)的水平,并表现出显著的抗凋亡活性。这些结果表明,异补骨脂素通过激活ERα并调节PI3K/AKT通路,发挥类似雌激素的神经保护作用,对抗SCI诱导的细胞凋亡。 /EXPL THER/ 先前的研究报道,白芷素对多种肿瘤细胞具有抗增殖作用。然而,据我们所知,白芷素单药治疗对人肝癌的疗效仍有待研究。本研究在体外和体内评估了白芷素的抗肿瘤活性,并探讨了其作用的分子机制。结果表明,白芷素以剂量和时间依赖的方式诱导肝癌细胞凋亡。此外,在HepG2和Huh-7细胞中,白芷素诱导的细胞凋亡被证实是线粒体依赖性的,涉及磷脂酰肌醇-4,5-二磷酸3-激酶/RAC丝氨酸/苏氨酸蛋白激酶信号通路。此外,在荷肝肿瘤异种移植小鼠模型中,给予白芷素可抑制肿瘤生长,且未产生明显的副作用。这些结果表明,白芷素可能具有作为治疗肝癌患者的新型治疗药物的潜力。 /EXPL THER/ 背景:白芷素是一种呋喃香豆素类化合物,存在于补骨脂(Psoralea corylifolia L.)果实中。本研究旨在探讨白芷素对脂多糖(LPS)刺激的RAW 264.7细胞和LPS诱导的体内急性肺损伤模型炎症的保护作用。材料与方法:在LPS给药24小时后,测定RAW 264.7细胞培养上清液中肿瘤坏死因子α(TNF-α)和白细胞介素(IL)-6的浓度。采用气管内滴注LPS诱导急性肺损伤模型。 LPS吸入6小时后,采集支气管肺泡灌洗液和肺组织样本,进行酶联免疫吸附试验(ELISA)、组织学和蛋白质印迹分析。结果:结果表明,白芷素预处理显著降低了体外和体内TNF-α和IL-6的水平,并显著降低了LPS诱导的急性肺损伤(ALI)小鼠肺组织中的炎症细胞数量、肺湿重/干重比以及髓过氧化物酶活性。此外,蛋白质印迹分析结果表明,白芷素抑制了LPS诱导的ALI中IκB、NF-κBp65、p38 MAPK和JNK的磷酸化。结论:这些结果提示,白芷素可能通过抑制NF-κB和MAPK通路,在预防炎症性疾病方面具有潜在优势。我们的数据表明,白芷素可能是一种潜在的新型药物,可用于临床预防炎症反应和疾病。 背景:白芷素是一种呋喃香豆素类化合物,存在于补骨脂(Psoralea corylifolia L.)果实中。本研究旨在探讨白芷素对脂多糖(LPS)刺激的RAW 264.7细胞和LPS诱导的体内急性肺损伤模型的抗炎保护作用。材料与方法:在LPS给药24小时后,测定RAW 264.7细胞培养上清液中肿瘤坏死因子α(TNF-α)和白细胞介素(IL)-6的浓度。采用气管内滴注LPS诱导急性肺损伤模型。 LPS吸入6小时后,采集支气管肺泡灌洗液和肺组织样本,进行酶联免疫吸附试验(ELISA)、组织学和蛋白质印迹分析。结果:结果表明,白芷素预处理显著降低了体外和体内TNF-α和IL-6的水平,并显著降低了LPS诱导的急性肺损伤(ALI)小鼠肺组织中的炎症细胞数量、肺湿重/干重比以及髓过氧化物酶活性。此外,蛋白质印迹分析结果表明,白芷素抑制了LPS诱导的ALI中IκBα、NF-κBp65、p38 MAPK和JNK的磷酸化。结论:这些结果提示白芷素可能通过抑制NF-κB和MAPK通路发挥预防炎症性疾病的潜在作用。我们的数据表明,白芷素可能是一种潜在的新型炎症反应和疾病预防药物。[3] |
| 分子式 |
C11H6O3
|
|---|---|
| 分子量 |
186.16354
|
| 精确质量 |
186.031
|
| 元素分析 |
C, 68.89; H, 5.44; N, 9.45; O, 5.40; S, 10.82
|
| CAS号 |
523-50-2
|
| 相关CAS号 |
29462-18-8; 29462-19-9 (HCl)
|
| PubChem CID |
10658
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.4±0.1 g/cm3
|
| 沸点 |
362.6±27.0 °C at 760 mmHg
|
| 熔点 |
132-134ºC
|
| 闪点 |
173.1±23.7 °C
|
| 蒸汽压 |
0.0±0.8 mmHg at 25°C
|
| 折射率 |
1.667
|
| LogP |
2.01
|
| tPSA |
43.35
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
0
|
| 重原子数目 |
14
|
| 分子复杂度/Complexity |
284
|
| 定义原子立体中心数目 |
0
|
| SMILES |
O=C1C=CC2=CC=C(OC=C3)C3=C2O1
|
| InChi Key |
XDROKJSWHURZGO-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C11H6O3/c12-10-4-2-7-1-3-9-8(5-6-13-9)11(7)14-10/h1-6H
|
| 化学名 |
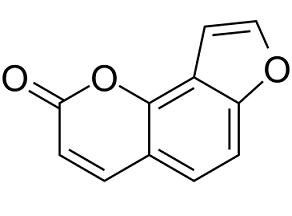
furo[2,3-h]chromen-2-one
|
| 别名 |
Knoll brand of bentazepam; QM 6008; Angelicin; 523-50-2; ISOPSORALEN; 2H-Furo[2,3-H]chromen-2-one; furo[2,3-h]chromen-2-one; Angecin; 2-Oxo-(2H)-furo(2,3-h)-1-benzopyran; Furo(2,3-h)coumarin; QM-6008; Bentazepam; Thiadipone; Tiadipone; Bentazepam [USAN:INN]; CI-718; Tiadipona; Thiadipone
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: 14~33.3 mg/mL (75.2~179.0 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (13.43 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (13.43 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL 澄清 DMSO 储备液加入到 900 μL 玉米油中并混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 5.3717 mL | 26.8586 mL | 53.7172 mL | |
| 5 mM | 1.0743 mL | 5.3717 mL | 10.7434 mL | |
| 10 mM | 0.5372 mL | 2.6859 mL | 5.3717 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT01931436 | Completed | Drug: Qing'E pill | Menopause | Shanghai University of Traditional Chinese Medicine |
August 2013 | Phase 1 |