| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| Other Sizes |
|
| 靶点 |
DU145 cell growth is inhibited by astaxanthin (50, 100, 150, and 200 µM; 48 hours) (IC50<200 µM) [1]. By preventing proliferation, promoting apoptosis, and hindering migration and invasion, astaxanthin (200 µM; 24 hours) lowers the expression of STAT3 and related pathway proteins (at the protein and mRNA levels) [1]. Additionally, astaxanthin shields RPE cells from oxidative stress and abnormal activation brought on by high glucose by downregulating VEGF at the protein level [2]. In K562 cells, astaxanthin (1-50 µM; 72 hours) increases the expression of the PPARγ protein in a dose- and time-dependent way [3].
|
|---|---|
| 体外研究 (In Vitro) |
虾青素(50、100、150 和 200 µM;48 小时)抑制 DU145 细胞生长(IC50<200 µM)[1]。通过防止增殖、促进细胞凋亡、阻碍迁移和侵袭,虾青素(200 µM;24 小时)可降低 STAT3 和相关通路蛋白的表达(在蛋白和 mRNA 水平)[1]。此外,虾青素通过在蛋白质水平下调 VEGF 来保护 RPE 细胞免受氧化应激和高葡萄糖引起的异常激活 [2]。在 K562 细胞中,虾青素(1-50 µM;72 小时)以剂量和时间依赖性方式增加 PPARγ 蛋白的表达 [3]。
MTT实验表明,Astaxanthin 以剂量依赖性方式显著抑制人前列腺癌DU145细胞的增殖。处理48小时后,与对照组相比,50 µM、100 µM和200 µM浓度下的抑制率分别为27%、38%和50%。半数抑制浓度(IC50)据报道小于200 µM。[1] 蛋白质印迹分析显示,用200 µM Astaxanthin 处理DU145细胞24小时可降低STAT3的蛋白表达水平。[1] RT-PCR分析证实,200 µM Astaxanthin 处理24小时可下调STAT3的mRNA表达水平。[1] 克隆形成实验表明,200 µM Astaxanthin 处理24小时可抑制DU145细胞的克隆形成能力,克隆抑制率为48%。当与siRNA介导的STAT3敲低(si-STAT3)联合使用时,抑制率提高至83%。[1] 使用Annexin V-FITC/PI染色的流式细胞术分析显示,用200 µM Astaxanthin 处理DU145细胞24小时,可使细胞凋亡百分比从8.5%(对照)增加至13.1%。Astaxanthin 与si-STAT3联用进一步将凋亡率提高至18.5%。[1] Transwell迁移和侵袭实验表明,200 µM Astaxanthin 处理24小时可降低DU145细胞的迁移和侵袭能力。与对照组相比,迁移抑制率约为41%,侵袭抑制率约为36%。与si-STAT3联用将这些抑制率分别提高至71%和56%。[1] 蛋白质印迹和RT-PCR分析进一步表明,Astaxanthin 处理可下调STAT3通路相关蛋白和基因(JAK2、Bcl-2、NF-κB p65)的表达,并上调促凋亡蛋白和基因(Bax、Caspase-3、Caspase-9)的表达。[1] |
| 体内研究 (In Vivo) |
在不穿衣服的小鼠中,虾青素(200 mg/kg;每天一次灌胃,持续三周)可防止肿瘤异种移植物 (DU145) 的形成 [1]。在大鼠中,虾青素(125 或 500 mg/kg;在动物饲料中;7 天)可显着降低氧化应激并提供心脏保护作用 [4]。
在裸鼠中建立的DU145异种移植瘤模型中,与接受生理盐水的对照组相比,每天一次灌胃给予200 mg/kg剂量的Astaxanthin,持续3周,能显著抑制肿瘤生长。[1] 当Astaxanthin与瘤内递送si-STAT3联合使用时,其肿瘤生长抑制效果增强。[1] |
| 细胞实验 |
细胞凋亡分析 [1]
细胞类型: DU145 细胞 测试浓度: 200 µM(预孵育) 孵育持续时间:24小时 实验结果:凋亡细胞百分比从8.5%增加到13.1%(与空白对照相比)。 细胞迁移测定[1] 细胞类型: DU145 细胞 测试浓度: 200 µM 孵育时间:24小时 实验结果:DU145细胞表现出迁移和侵袭减弱(大约41%的细胞不能从一个室移动到另一个室,36%的细胞不能从一个室移动到另一个室)与对照组相比, 的细胞无法通过 Transwell 膜)。 细胞增殖测定[2] 细胞类型: ARPE-19 细胞 测试浓度: 50 µM(孵育前) 孵育时间:7天 实验结果:当暴露于高葡萄糖时,细胞增殖显着减弱。 蛋白质印迹分析[1] 细胞类型: DU145 细胞 测试浓度: 200 µM 孵育时间: 24 h 实验结果: STAT3在蛋白和mRNA水平上的表达均减少(下调JAK2、BCL-2和NF-κB的蛋白表达) , 上调 BAX , 蛋白表达 MTT细胞活力/增殖实验: 将DU145细胞以每孔10^3-10^4个细胞的密度接种到96孔板中。用不同浓度的Astaxanthin(0、50、100、200 µM)处理细胞48小时。随后,向每孔加入MTT溶液,孵育4小时。形成的甲臜晶体用DMSO溶解,使用酶标仪在490 nm波长处测量吸光度。[1] 克隆形成实验: 根据实验组处理DU145细胞(例如,用si-STAT3或对照siRNA转染48小时,然后用200 µM Astaxanthin 处理24小时)。处理后,接种有限数量的细胞并培养10-14天以形成克隆。然后用4%多聚甲醛固定克隆,用0.1%结晶紫染色并计数。[1] 流式细胞术凋亡实验: 收集来自不同处理组的DU145细胞,用Annexin V-FITC和碘化丙啶(PI)在避光条件下染色5分钟,然后通过流式细胞仪分析以确定凋亡细胞的百分比。[1] 细胞迁移和侵袭实验(Transwell): 对于迁移实验,将处理后的DU145细胞重悬于含2%血清的培养基中,并接种到Transwell小室的上室。下室填充含10%血清的培养基作为化学引诱剂。孵育16小时后,迁移至膜下侧的细胞用4%多聚甲醛固定,结晶紫染色,并在显微镜下计数。对于侵袭实验,在接种细胞前,用基质胶预涂上室膜;其他步骤与迁移实验相同。[1] 蛋白质印迹分析: 裂解在不同条件下处理的DU145细胞以提取总蛋白。等量蛋白(30 µg)通过SDS-PAGE分离,转印至膜上,并用针对STAT3、JAK2、Bcl-2、Bax、Caspase-3、Caspase-9、NF-κB p65和β-肌动蛋白(作为内参)的特异性一抗进行孵育。使用合适的检测系统显色蛋白条带。[1] RT-PCR(逆转录聚合酶链反应): 使用商业裂解试剂从处理过的DU145细胞中提取总RNA。将1微克RNA逆转录成cDNA。使用针对STAT3、JAK2、Bcl-2、Bax、Caspase-3、Caspase-9、NF-κB p65和β-肌动蛋白的特异性引物进行定量PCR,以评估mRNA表达水平。[1] |
| 动物实验 |
动物/疾病模型:裸鼠(约20克;DU145肿瘤异种移植模型)[1]。
剂量:200 mg/kg 给药途径:灌胃(po);每日一次,持续3周。 实验结果:对肿瘤生长有显著的抑制作用。 动物/疾病模型:雌性C57BL/6小鼠(7周龄)[4]。 剂量:125或500 mg/kg 给药途径:饲料;持续7天。 实验结果: 两个治疗组(125 mg/kg 和 500 mg/kg)的平均梗死面积分别显著缩小至 45.1% 和 39.1%。125 mg/kg 组和 500 mg/kg 组的心肌挽救率分别为 26% 和 36%。9-HETE 水平呈剂量依赖性显著降低。9-HETE 是花生四烯酸的区域异构体氧化产物,被认为是自由基介导氧化的产物。 DU145 异种移植瘤裸鼠模型:将处于对数生长期的 DU145 细胞皮下接种到裸鼠左侧腋窝(每只小鼠 2 x 10^7 个细胞)。肿瘤形成后(约 2 周),将荷瘤小鼠随机分组。一组小鼠每日一次经胃内灌注给予虾青素,剂量为200 mg/kg体重。虾青素配制成浓度为40 mg/mL的混悬液,每只小鼠灌注100 µL(假设小鼠平均体重为20 g)。对照组灌注等体积的生理盐水。治疗持续3周后,处死小鼠,切除肿瘤并称重。另一组实验中,小鼠接种预先转染si-STAT3或对照载体的DU145细胞(接种前24小时),随后按所述方法给予虾青素或载体处理。[1] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
本研究比较了大西洋鲑(Salmo salar)和大西洋大比目鱼(Hippoglossus hippoglossus)在饲喂添加66 mg/kg干物质虾青素的饲料112天后,肌肉、肝脏、全肾和血浆中虾青素(3,3'-二羟基-β,β-胡萝卜素-4,4'-二酮)的表观消化率系数(ADC)和类胡萝卜素组成。虾青素来源由75%的全反式虾青素、3%的9Z-虾青素和22%的13Z-虾青素组成,其中(3R,3'R)-虾青素、(3R,3'S; meso)-虾青素和(3S,3'S)-虾青素的比例为1:2:1。饲喂56天和112天后,大西洋大比目鱼体内虾青素的表观消化率(ADC)显著高于大西洋鲑鱼(P < 0.05)。全反式虾青素的表观消化率显著高于9Z-虾青素的表观消化率(P < 0.05)。鲑鱼所有血浆和组织样本中的类胡萝卜素含量均显著高于大比目鱼。鲑鱼肌肉中虾青素的保留率为3.9%,而大比目鱼为0。与饲料相比,全反式虾青素选择性地积累在鲑鱼肌肉以及鲑鱼和大比目鱼的血浆中。与血浆相比,13Z-虾青素选择性地积累在鲑鱼和大比目鱼的肝脏和全肾中。大比目鱼血浆、肝脏和全肾中均检测到了碘黄素(3,3',4'-三羟基-β,β-胡萝卜素-4'-酮)的3',4'-顺式和反式乙醇酸异构体,表明其虾青素代谢途径与鲑鱼相似。总之,大比目鱼虾青素表观消化率(ADC)高于大西洋鲑鱼,可能是由于大比目鱼采食量较低,以及其虾青素代谢转化能力更强,导致虾青素保留率较低。 本研究旨在探讨大西洋鲑鱼(尤其是其肝脏)中虾青素(Ax)的代谢。本研究采用活体鲑鱼,在处死前饲喂含有60 ppm 15,15'(14)C标记虾青素的饲料。采集血液、胆汁、肝脏、胃肠道及其内容物、肌肉、皮肤、剩余胴体和粪便样本进行闪烁计数。实验结束时,在胃肠道内容物和粪便中检测到最高的14C标记Ax放射性(71.36%),胆汁中为7.13%,肝脏、肌肉和皮肤样本中为10.68%。从鲑鱼胆汁中提取14C标记Ax的代谢物,并使用薄层色谱(TLC)和高效液相色谱(HPLC)进行分析。结果发现主要成分为14C标记Ax及其顺式异构体,未观察到14C标记Ax的结合物。这些结果表明,在大西洋鲑鱼肝脏中,(14)C标记的虾青素并未与更大的无色化合物结合。 代谢/代谢物 给八条成年雌性虹鳟鱼喂食一份含有标记的(14)C-虾青素和(3)H-角黄素或(3)H-玉米黄素的强制喂食餐。喂食96小时后,处死虹鳟鱼,并解剖取出肝脏、皮肤、肌肉和卵巢。虾青素在肌肉中的积累量略高于角黄素,但在所有组织中,虾青素和角黄素的浓度均显著高于玉米黄素。(3)H-玉米黄素的代谢物仅在肝脏中发现,而(14)C-凤凰黄素是唯一检测到的(14)C-虾青素代谢色素,且存在于所有检测的组织中。在所有鳟鱼的肝脏中均检测到了(3)H-虾青素,表明(3)H-角黄素和(3)H-玉米黄素是虾青素的前体,并且鲑科鱼类可能拥有此前未知的类胡萝卜素氧化途径。标记的视黄醇1和视黄醇2仅在肝脏中检测到,(3)H-玉米黄素是这两种维生素A形式的主要前体。 本研究测定了摄食量、生长速度和温度(8℃和12℃)对大西洋鲑表观消化率系数(ADC)、血液中各虾青素E/Z异构体的吸收以及虾青素(3,3'-二羟基-β,β-胡萝卜素-4,4'-二酮)代谢的影响。血浆中碘黄素(3,4,3'-三羟基-β,β-胡萝卜素-4-酮)的积累被用来指示虾青素的代谢转化。 |
| 毒性/毒理 (Toxicokinetics/TK) |
相互作用
本研究探讨了从黄腐病菌(Xanthophyllomyces dendrorhous)突变体中分离得到的虾青素对乙醇诱导的大鼠胃黏膜损伤的体内保护作用。实验组大鼠预先分别给予两种剂量的虾青素(分别为5和25 mg/kg体重)处理3天,随后给予80%乙醇处理3天;对照组大鼠仅接受80%乙醇处理3天。结果显示,口服虾青素(5和25 mg/kg体重)可显著减轻乙醇诱导的胃黏膜损伤,并抑制胃黏膜脂质过氧化物水平的升高。此外,虾青素预处理还显著提高了超氧化物歧化酶、过氧化氢酶和谷胱甘肽过氧化物酶等自由基清除酶的活性。组织学检查清楚地表明,经虾青素预处理后,乙醇引起的急性胃黏膜损伤几乎消失。 |
| 参考文献 |
|
| 其他信息 |
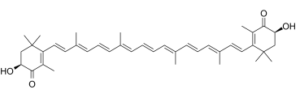
虾青素是一种胡萝卜素酮,由β,β-胡萝卜素-4,4'-二酮组成,其3位和3'位分别连接两个羟基(3S,3'S非对映异构体)。它是一种类胡萝卜素色素,主要存在于动物(甲壳类动物、棘皮动物)中,但也存在于植物中。虾青素可以以游离形式(作为红色色素)、酯形式或蓝色、棕色或绿色色素蛋白的形式存在。它具有抗凝血、抗氧化、食用色素、植物代谢物和动物代谢物等多种功能。它既是胡萝卜素酮又是胡萝卜素醇,来源于β-胡萝卜素的氢化物。虾青素是萜类化合物中的一种酮类胡萝卜素。它被归类为叶黄素,但实际上是一种不具有维生素A活性的类胡萝卜素。它存在于大多数具有红色色素的水生生物中。虾青素已被证实具有抗氧化和抗炎作用。它可能作为着色剂存在于鱼饲料或某些动物饲料中。
据报道,橙色农杆菌(Agrobacterium aurantiacum)、红酵母(Phaffia rhodozyma)和其他一些有相关数据的生物体中均含有虾青素。 虾青素是一种天然和合成的叶黄素类化合物,属于非维生素A原类胡萝卜素,具有潜在的抗氧化、抗炎和抗肿瘤活性。服用后,虾青素可作为抗氧化剂,降低氧化应激,从而防止蛋白质和脂质氧化以及DNA损伤。通过减少活性氧(ROS)和自由基的产生,它还可以防止ROS诱导的核因子κB(NF-κB)转录因子的激活以及炎症细胞因子(如白细胞介素-1β(IL-1β)、IL-6和肿瘤坏死因子-α(TNF-α))的产生。此外,虾青素可能抑制环氧合酶-1 (COX-1) 和一氧化氮 (NO) 的活性,从而减轻炎症。氧化应激和炎症在多种疾病的发病机制中起着关键作用,包括心血管疾病、神经系统疾病、自身免疫性疾病和肿瘤性疾病。 药物适应症 已研究用于治疗眼部疾病/感染、癌症/肿瘤(未具体说明)和哮喘。 治疗用途 本研究假设口服卡达克斯(二琥珀酸二钠虾青素)可抑制代表性、特征明确的小鼠腹膜炎症模型中多个相关生物靶点的氧化损伤。采用先前开发的基于质谱(LC/ESI/MS/MS)的方法,在黑鼠(C57/BL6)模型系统中检测了多种不同的氧化途径。在小鼠接受 Cardax 或载体(不含药物的亲脂性乳剂)灌胃治疗 500 mg/kg,每日一次,连续 7 天后,于第 8 天评估腹腔灌洗液样本(上清液)中的体内氧化应激标志物,共 5 个时间点:(1)治疗前基线(t=0);(2)腹腔注射硫代乙醇酸盐 16 小时以诱导中性粒细胞浸润;(3)腹腔注射酵母细胞壁(酵母聚糖;t=16 小时/4 小时硫代乙醇酸盐+酵母聚糖)4 小时;(4)腹腔注射硫代乙醇酸盐 72 小时以诱导单核细胞/巨噬细胞浸润;以及(5)72 小时/4 小时硫代乙醇酸盐+酵母聚糖。在第二和第五个时间点观察到对花生四烯酸 (AA) 和亚油酸 (LA) 底物的统计学显著节约效应。当以氧化底物的浓度进行标准化后,在第三时间点(中性粒细胞募集/活化达到最大值)观察到 8-异前列烷-F(2α) (8-iso-F(2α)) 的统计学显著降低,在第五时间点(单核细胞/巨噬细胞募集/活化达到最大值)观察到 5-HETE、5-oxo-EET、11-HETE、9-HODE 和 PGF(2α) 的统计学显著降低。随后,我们利用圆二色谱 (CD) 和紫外/可见吸收光谱 (UV/Vis) 在体外评估了 Cardax 的光学非活性立体异构体 (meso-dAST) 与人 5-脂氧合酶 (5-LOX) 的直接相互作用,并以哺乳动物 15-LOX 作为替代物(已有 X 射线荧光光谱数据报道)进行了后续的分子对接计算。结果表明,该内消旋化合物能够与酶的溶剂暴露表面相互作用并结合。这些初步研究为更详细地评估该化合物对 5-LOX 酶的治疗作用奠定了基础,5-LOX 酶在人类慢性疾病(如动脉粥样硬化、哮喘和前列腺癌)中发挥着重要作用。/二琥珀酸二钠虾青素/ 动脉粥样硬化斑块的组成,而不仅仅是宏观病变的大小,与其破裂的易感性和血栓形成的风险有关。本研究通过关注脂质质量、巨噬细胞、细胞凋亡、胶原蛋白、金属蛋白酶表达以及斑块完整性,评估了抗氧化剂α-生育酚和虾青素在渡边遗传性高脂血症(WHHL)兔中的潜在抗动脉粥样硬化作用。31只WHHL兔被分为三组,分别饲喂标准饲料(对照组,n=10)、添加500 mg/kg α-生育酚的标准饲料(n=11)或添加100 mg/kg 虾青素的标准饲料(n=10),持续24周。结果发现,两种抗氧化剂,尤其是虾青素,均显著降低了斑块中巨噬细胞的浸润,但对脂质积累没有影响。根据胶原蛋白和平滑肌细胞的分布,虾青素治疗组兔的所有病变均被归类为早期斑块。两种抗氧化剂均能改善斑块稳定性并显著减少细胞凋亡,细胞凋亡主要发生在巨噬细胞中,同时降低基质金属蛋白酶3的表达和斑块破裂。虽然两种抗氧化剂均未改变病变大小与脂质积累之间的正相关性,但病变大小与细胞凋亡仅在对照组中呈正相关。虾青素和α-生育酚可能通过减少巨噬细胞浸润和细胞凋亡来改善动脉粥样硬化斑块的稳定性。α-生育酚和虾青素减少细胞凋亡可能是这些抗氧化剂新的抗动脉粥样硬化特性。 实验治疗:虾青素是一种不具有维生素A活性的类胡萝卜素,可能通过增强免疫反应发挥抗肿瘤活性。本研究旨在探讨膳食虾青素对移植性甲基胆蒽诱导的纤维肉瘤(Meth-A肿瘤)细胞的生长和肿瘤免疫的影响。这些肿瘤细胞表达一种肿瘤抗原,该抗原可在同基因小鼠中诱导T细胞介导的免疫反应。BALB/c小鼠在皮下接种肿瘤细胞(3×10⁵个细胞,2倍最小致瘤剂量)前0、1和3周,分别饲喂添加虾青素(0.02%,40微克/公斤体重/天,以微珠形式)的化学成分明确的饲料。接种3周后,测定肿瘤的大小和重量。我们还通过在体外培养中用Meth-A肿瘤细胞重新刺激肿瘤引流淋巴结(TDLN)和脾细胞,测定了细胞毒性T淋巴细胞(CTL)活性和干扰素-γ(IFN-γ)的产生。在肿瘤接种前1周和3周开始补充虾青素的小鼠,其肿瘤的大小和重量均显著低于对照组。这种抗肿瘤活性与喂食虾青素的小鼠肿瘤引流淋巴结(TDLN)和脾细胞中更高的CTL活性和IFN-γ产生水平平行。接种肿瘤前三周喂食虾青素的小鼠,其TDLN细胞的CTL活性最高。当在接种肿瘤的同时开始补充虾青素时,除脾细胞的IFN-γ产生外,膳食虾青素对上述其他参数均无影响。小鼠喂食0.02%虾青素四周后,血清总虾青素浓度约为1.2 μmol/L,且似乎随着虾青素补充时间的延长而增加。我们的研究结果表明,膳食虾青素抑制了Meth-A肿瘤细胞的生长,并刺激了针对Meth-A肿瘤抗原的免疫反应。 实验治疗:在本研究中,我们利用合成虾青素衍生物(Cardax;琥珀酸二钠虾青素)的口服生物利用度提高,评估了其作为心脏保护剂的潜在作用。我们采用亚慢性口服给药的方式,将虾青素作为饲料补充剂,对Sprague-Dawley大鼠进行了7天的给药。动物分别接受两种浓度的卡达克斯(Cardax)饲料(0.1%和0.4%;分别约为125和500 mg/kg/天)或不含药物的对照饲料,持续7天。在第8天进行梗死研究。左前降支(LAD)冠状动脉闭塞30分钟后,再灌注2小时,然后处死动物。该方案导致平均梗死面积(IS)占危险面积(AAR)的百分比(IS/AAR,%)为61±1.8%。AAR通过注射专利蓝染料进行定量,IS通过氯化三苯基四氮唑(TTC)染色进行测定。在饲料中添加0.1%和0.4%的卡达克斯(Cardax)7天后,IS/AAR(%)平均值显著降低,分别降至45±2.0%(挽救率26%)和39±1.5%(挽救率36%)。两种浓度(分别为400±65 nM和1634±90 nM)的卡达克斯补充7天后,心肌中游离虾青素的浓度均达到理想水平,表明口服补充后,其在实体组织靶器官中的负载量极佳。同时观察到,补充琥珀酸二钠虾青素后,多种脂质过氧化产物的血浆水平也呈下降趋势,这与已报道的体外抗氧化作用机制相符。这些结果表明,该化合物在心脏保护方面的潜在应用价值已扩展至择期心血管手术患者群体,对于这些患者,7天的口服预处理(类似于他汀类药物)可显著降低围手术期诱发的心肌梗死面积。 (琥珀酸二钠虾青素) 如需了解更多关于虾青素(共7种)的治疗用途(完整)数据,请访问HSDB记录页面。 虾青素是一种天然类胡萝卜素,存在于藻类、浮游植物和虾等海洋生物中。[1] 研究表明,虾青素抑制侵袭性前列腺癌DU145细胞的增殖、克隆形成、迁移和侵袭,并促进其凋亡,主要通过降低STAT3蛋白和mRNA的表达水平来实现。[1] 在体外和体内模型中,虾青素的抗肿瘤作用与STAT3基因沉默(si-STAT3)具有协同作用。 [1] 作者提出虾青素是一种潜在的天然产物,可用于抑制侵袭性前列腺癌细胞。[1] |
| 分子式 |
C40H52O4
|
|---|---|
| 分子量 |
596.8385
|
| 精确质量 |
596.386
|
| CAS号 |
472-61-7
|
| PubChem CID |
5281224
|
| 外观&性状 |
Dark purple to black solid powder
|
| 密度 |
1.1±0.1 g/cm3
|
| 沸点 |
774.0±60.0 °C at 760 mmHg
|
| 熔点 |
215-216ºC
|
| 闪点 |
435.8±29.4 °C
|
| 蒸汽压 |
0.0±6.0 mmHg at 25°C
|
| 折射率 |
1.595
|
| LogP |
8.16
|
| tPSA |
74.6
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
4
|
| 可旋转键数目(RBC) |
10
|
| 重原子数目 |
44
|
| 分子复杂度/Complexity |
1340
|
| 定义原子立体中心数目 |
2
|
| SMILES |
CC1=C(C(C[C@@H](C1=O)O)(C)C)/C=C/C(=C/C=C/C(=C/C=C/C=C(/C=C/C=C(/C=C/C2=C(C(=O)[C@H](CC2(C)C)O)C)\C)\C)/C)/C
|
| InChi Key |
MQZIGYBFDRPAKN-UWFIBFSHSA-N
|
| InChi Code |
InChI=1S/C40H52O4/c1-27(17-13-19-29(3)21-23-33-31(5)37(43)35(41)25-39(33,7)8)15-11-12-16-28(2)18-14-20-30(4)22-24-34-32(6)38(44)36(42)26-40(34,9)10/h11-24,35-36,41-42H,25-26H2,1-10H3/b12-11+,17-13+,18-14+,23-21+,24-22+,27-15+,28-16+,29-19+,30-20+/t35-,36-/m0/s1
|
| 化学名 |
(6S)-6-Hydroxy-3-[(1E,3E,5E,7E,9E,11E,13E,15E,17E)-18-[(4S)-4-hydroxy-2,6,6-trimethyl-3-oxo-1-cyclohexenyl]-3,7,12,16-tetramethyloctadeca-1,3,5,7,9,11,13,15,17-nonaenyl]-2,4,4-trimethyl-1-cyclohex-2-enone
|
| 别名 |
Astaxanthin
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: (1). 本产品在运输和储存过程中需避光。 (2). 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮。 (3). 该产品在溶液状态不稳定,请现配现用。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~2 mg/mL (~3.35 mM)
Acetone :< 1 mg/mL |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 3.33 mg/mL (5.58 mM) in 0.5% CMC-Na/saline water (这些助溶剂从左到右依次添加,逐一添加), 悬浮液; 超声和加热处理
*生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: 3.33 mg/mL (5.58 mM) in 20% HP-β-CD in Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浮液; 超声和加热处理 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.6755 mL | 8.3775 mL | 16.7549 mL | |
| 5 mM | 0.3351 mL | 1.6755 mL | 3.3510 mL | |
| 10 mM | 0.1675 mL | 0.8377 mL | 1.6755 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。