| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
Natural product/phenolic alkaloid; Anticancer; antiviral; Zika virus (ZIKV); Ebola virus (EBOV)
- Cephaeline targets histone H3 acetylation regulators (induces histone H3 acetylation) to inhibit mucoepidermoid carcinoma cancer stem cells (MEC CSCs). [3] - Cephaeline targets nuclear factor erythroid 2-related factor 2 (NRF2) (inhibits NRF2 signaling pathway); the IC50 values for inhibiting A549 and H1299 lung cancer cell viability were ~12.5 μM and ~15.3 μM, respectively. [4] |
|---|---|
| 体外研究 (In Vitro) |
Cephaeline是组蛋白H3乙酰化的诱导剂和黏液表皮样癌癌症干细胞的抑制剂。单次服用Cephaeline导致MEC细胞的存活率降低,肿瘤生长和细胞迁移潜力停止。根据H3K9ac水平的增加和肿瘤球体形成的破坏判断,Cephaeline的给药导致染色质组蛋白乙酰化。有趣的是,UM-HMC-1和UM-HMC-3A细胞系中的ALDH水平升高,而UM-HMC-2的酶活性降低。
结论:通过调节肿瘤细胞的生存力、迁移、增殖和破坏癌症细胞产生肿瘤球的能力,Cephaeline在所有检测的MEC细胞系中均表现出抗癌特性[3]。
Cephaeline对癌症细胞显示出显著的抑制作用,并且Cephaeline在24、48和72小时对H460和A549的IC50对于H460细胞分别为88、58和35nM,对于A549细胞分别为89、65和43nM。同时,我们证明了铁蛋白脱羧酶是cephaeline抗肺癌的关键机制。最后,我们发现cephaeline通过靶向NRF2诱导了癌症细胞中的铁蛋白脱失[4]。 Cephaeline是emetine的去甲基类似物,对ZIKV和EBOV感染具有相似的抗病毒功效[2]。 - 抑制黏液表皮样癌干细胞(MEC CSCs)活性: 1. 球形成实验:MEC CSCs经Cephaeline(5、10、20 μM)处理7天,呈剂量依赖性降低球形成效率(对照组~35%,5、10、20 μM组分别降至~22%、~12%、~5%)和球直径(对照组~120 μm,处理组分别降至~90、~65、~40 μm)。[3] 2. CSC标志物下调:Western blot和qPCR显示,20 μM Cephaeline使MEC CSC标志物(CD44、CD133、ALDH1A1)的蛋白表达降低~60%–75%,mRNA表达降低~55%–70%(vs对照组)。[3] 3. 诱导组蛋白H3乙酰化:免疫荧光和Western blot显示,10、20 μM Cephaeline使乙酰化组蛋白H3(Lys9/14)水平较对照组升高~2.0–3.5倍,且不影响总组蛋白H3水平。[3] - 靶向NRF2促进铁死亡抗肺癌活性: 1. 抑制细胞活力:A549/H1299肺癌细胞经Cephaeline(0–40 μM)处理48小时,CCK-8实验显示IC50值分别为~12.5 μM(A549)和~15.3 μM(H1299)。[4] 2. 诱导铁死亡:15 μM Cephaeline使细胞内活性氧(ROS)水平升高~2.8倍,脂质过氧化产物(MDA)含量升高~3.2倍,谷胱甘肽(GSH)水平降低~55%(vs对照组,流式细胞术和比色法检测)。[4] 3. 抑制NRF2通路:Western blot显示,10、15、20 μM Cephaeline剂量依赖性降低NRF2蛋白水平(~40%–80%)及其下游靶基因(HO-1、NQO1)表达(~35%–75%,vs对照组)。[4] |
| 体内研究 (In Vivo) |
本研究旨在探讨cephaeline在体内的抗癌症活性及其作用机制。为了研究cephaeline在体内的抗肿瘤作用,构建了皮下肿瘤异种移植物模型。经过12天的药物治疗后,发现与对照组相比,5和10mg/kgcephaeline在体内具有显著的抗肿瘤作用。同时,在皮下肿瘤异种移植物模型中测得的ED50为3mg/kg,最低有效浓度(MEC)为2.5mg/kg。然而,10 mg/kg cephaeline在体内具有与脱铁诱导剂erastin相同的抗肺癌癌症作用(图7(A-D))。同时,还发现cephaeline、Emetine和对照组的小鼠体重没有显著差异(图7(E))。此外,为了验证cephaeline通过在体内诱导脱铁作用而发挥抗肺癌癌症作用,我们通过蛋白质印迹检测了不同组肿瘤组织中脱铁的关键蛋白,结果与体外研究结果一致(图7(F)和图88)。[4]
本研究在EBOV小鼠模型中测试了Emetine和cephaeline的保护作用。将6至8周龄的雌性BALB/c小鼠(每组n=6)注射1000倍于小鼠适应埃博拉病毒(MA-EBOV)50%(LD50)平均致死剂量的IP。在感染MA-EBOV之前,小鼠在通过IP接种病毒前3小时开始接受Emetine(1mg/kg/天)、cephaeline(5mg/kg/天)或VC(对照组)治疗。IP给药MA-EBOV后,小鼠继续用Emetine、cephaeline或VC IP治疗7天。每天监测动物的存活情况。正如预期的那样,所有对照组动物均死于EBOV感染,平均死亡时间为8.33±1.03 d.p.i。相比之下,67%或六分之四的小鼠在两个治疗组中都存活了下来(图4c和补充图S5e-f)。与Emetine和cephaeline治疗ZIKV感染的效果相似,这些药物在体内有效地抑制了EBOV感染。[2] - 裸鼠肺癌移植瘤模型抗瘤活性: 1. 模型建立:向4–6周龄BALB/c裸鼠右侧腋下皮下注射A549细胞(5×10⁶个细胞/只)。[4] 2. 药物处理:当肿瘤体积达~100 mm³时,将小鼠分为2组(n=6):对照组(生理盐水)和Cephaeline组(20 mg/kg,腹腔注射,每2天1次,共21天)。[4] 3. 药效结果:Cephaeline使肿瘤体积较对照组减少~65%(从~1200 mm³降至~420 mm³),肿瘤重量减少~60%(从~1.8 g降至~0.72 g)。[4] 4. 机制验证:Cephaeline处理组的肿瘤组织中,乙酰化组蛋白H3(Lys9/14)水平较对照组升高~2.5倍,NRF2/HO-1蛋白水平降低~55%–70%(免疫组化和Western blot检测)。[4] |
| 酶活实验 |
In vitro RNA polymerase assays[/体外RNA聚合酶检测[2]
RNA聚合酶检测试剂盒购自Profoldin。按照制造商的说明,在10µL的反应中进行RNA合成测定。将23ng纯化的寨卡病毒NS5加入3µL的384孔小容量板中后,将依美汀的连续稀释液加入3µL的孔中。将混合物在室温下预孵育30分钟。在4µL的每个孔中加入含有单链聚核糖核苷酸、10µM NTP混合物、20 mM Tris-HCl、pH 8.0、1 mM DTT和8 mM MgCl2的主混合物。将反应在37°C下孵育1小时,然后通过加入10µL的荧光染料停止反应。使用Tecan平板读数器测量荧光强度(Ex=485±5,Em=535±10 nm)。 |
| 细胞实验 |
使用UM-HMC-1、UM-HMC-2和UM-HMC-3A MEC细胞系,通过MTT法测定Cephaeline对肿瘤存活率的影响。进行体外伤口愈合划痕试验以解决细胞迁移问题,同时使用组蛋白H3赖氨酸9(H3k9ac)的免疫荧光染色来鉴定Cephaeline给药后肿瘤细胞的乙酰化状态。癌症干细胞的存在通过流式细胞术鉴定ALDH酶活性和通过使用体外肿瘤球形成的功能测定来评估[3]。
使用H460和A549肺癌癌症细胞。在用Cephaeline处理24小时后,通过细胞计数Kit-8测定法检测Cephaeline对肺癌细胞的抑制率。随后,将25、50和100nM的浓度用于体外实验。用CCK-8检测Cephaeline对肺癌癌症细胞的抑制作用。CCK-8试剂盒是一种基于WST-8的快速、高灵敏度、非放射性比色检测试剂盒,广泛应用于细胞增殖和细胞毒性检测。将A549和H460细胞系接种在96孔板中,密度为每孔5×103(100μL),然后放入培养箱中预培养24小时。然后分别在24、48和72小时用不同浓度的Cephaeline(5、15、25、50、100、200和400 nM)处理细胞。最后,在培养皿中孵育1-4小时之前,向每个孔中加入10μL CCK-8溶液。用酶标仪在450nm处测量吸光度。使用GraphPad Prism计算IC50值。首先,创建了一个数据表,将Cephaeline浓度的对数(5、15、25、50、100、200和400 nM)与反应百分比相关联。随后,使用非线性回归曲线拟合确定IC50值和标准误差。[4] 如前所述进行抑制试验。简而言之,Vero E6细胞在37°C下用Emetine或Cephaeline(0-2.0µM)或单独的DMEM预处理1小时,并在Emetine、Cephaeline或单独的DME存在下用MOI=0.1的GFP表达EBOV感染37°C 1小时。然后在Emetine、Cephaeline或DMEM存在下进一步孵育细胞72小时。72小时后,在Biotek Synergy HTX平板读数器上定量绿色荧光蛋白信号。通过比较Emetine或Cephaeline处理的感染细胞与DMEM处理的对照的荧光读数来确定感染。在Prism 5中使用四参数逻辑回归计算EC50和EC90值[2]。 - MEC CSCs功能实验流程: 1. 球形成实验:将MEC CSCs以1×10³个细胞/孔接种于超低吸附6孔板,加入含Cephaeline(5、10、20 μM)的无血清培养基,37°C、5% CO₂培养7天。计数直径>50 μm的球状体,通过图像分析软件测量直径。[3] 2. CSC标志物检测:MEC CSCs经20 μM Cephaeline处理48小时后,裂解细胞进行Western blot(抗CD44、CD133、ALDH1A1抗体),或提取总RNA进行qPCR(检测CD44、CD133、ALDH1A1 mRNA,以GAPDH为内参)。[3] - 肺癌细胞铁死亡相关实验流程: 1. 细胞活力实验:A549/H1299细胞以5×10³个细胞/孔接种于96孔板,培养24小时后加入Cephaeline(0–40 μM),继续培养48小时。加入CCK-8试剂,检测450 nm处吸光度并计算细胞活力。[4] 2. 铁死亡标志物检测:A549细胞经15 μM Cephaeline处理24小时后,用DCFH-DA荧光探针检测细胞内ROS(流式细胞术);通过硫代巴比妥酸反应检测MDA含量;用5,5'-二硫代双-(2-硝基苯甲酸)法检测GSH水平。[4] 3. NRF2通路检测:A549细胞经10、15、20 μM Cephaeline处理24小时后,裂解细胞进行Western blot(抗NRF2、HO-1、NQO1抗体,β-肌动蛋白为内参)。[4] |
| 动物实验 |
评估依米丁和头孢菌素对小鼠MA-EBOV的保护效力[2]
6至8周龄的雌性BALB/c小鼠被随机分为若干组(每组6只)。所有小鼠均通过腹腔注射1000倍致死剂量(LD50)的MA-EBOV进行攻击。在攻击前3小时开始,分别给予依米丁(1 mg/kg/天)、头孢菌素(5 mg/kg/天)或等体积的PBS(对照组)进行治疗,持续至攻击后6天。所有动物在攻击后14天内监测疾病症状和体重变化,并在之后14天内观察生存情况。 体内肿瘤模型[4] 本研究使用5周龄的雌性BALB/c-nu小鼠。经过一段时间的适应性喂养后,将肺癌H460细胞系(1 × 10⁶个细胞溶于0.1 mL PBS)注射到每只小鼠的右侧背部,建立皮下肿瘤模型。模型构建成功后,将24只小鼠随机分为四组:对照组(溶剂)、erastin组(20 mg/kg)和cephaeline治疗组(5、10 mg/kg)。腹腔注射12天后,用CO₂窒息法处死小鼠,并收集肿瘤组织进行后续评估。 - A549肺癌异种移植小鼠模型: 1. 动物准备:BALB/c裸鼠(4-6周龄,雄性)适应环境1周(自由摄食/饮水,25℃,12小时光照/黑暗循环)。 [4] 2. 肿瘤诱导:将A549细胞(5×10⁶个细胞,溶于100 μL PBS + Matrigel,1:1)皮下注射到每只小鼠的右侧腹部。[4] 3. 药物配制:将头孢利林溶于DMSO(5% v/v),并用无菌生理盐水稀释至最终浓度。[4] 4. 给药:对肿瘤体积约为100 mm³的小鼠,每2天腹腔注射一次头孢利林(20 mg/kg),持续21天;对照组小鼠注射等体积的DMSO-生理盐水混合液。[4] 5. 样本采集:末次注射后24小时处死小鼠。取出肿瘤组织测量体积/重量,部分肿瘤组织用福尔马林固定(用于免疫组织化学)或储存于-80°C(用于蛋白质印迹)。[4] |
| 参考文献 |
[1]. Determination of emetine and cephaeline in Ipecac roots by high- performance liquid chromatography. Journal of Chromatography A. 1982 Apr; 238( 2):525-529.
[2]. Emetine inhibits Zika and Ebola virus infections through two molecular mechanisms: inhibiting viral replication and decreasing viral entry. Cell Discov. 2018 Jun 5;4:31. [3]. Cephaeline is an inductor of histone H3 acetylation and inhibitor of mucoepidermoid carcinoma cancer stem cells. J Oral Pathol Med. 2022 Jul;51(6):553-562. [4]. Cephaeline promotes ferroptosis by targeting NRF2 to exert anti-lung cancer efficacy. Pharm Biol. 2024 Dec;62(1):195-206. |
| 其他信息 |
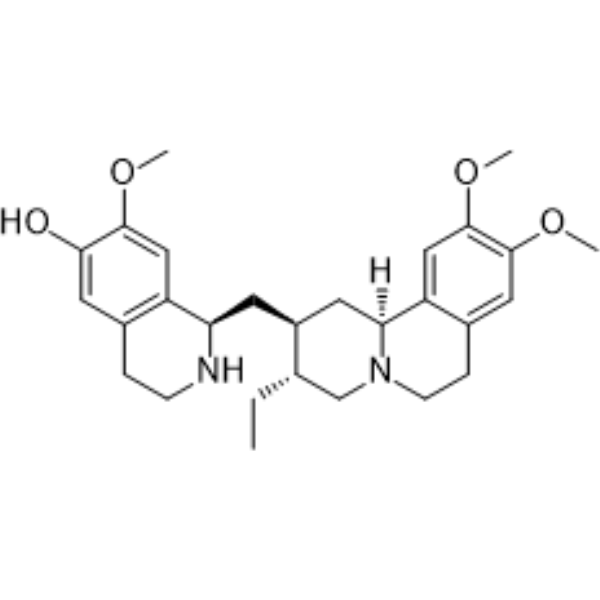
头孢碱是一种吡啶并异喹啉类化合物,其结构包含一个在6'位具有羟基、在7'、10和11位具有甲氧基取代基的依美坦。它来源于依美坦的氢化物。
据报道,头孢碱存在于鼠尾草(Alangium salviifolium)、反枝多斯滕尼亚(Dorstenia contrajerva)以及其他有相关数据的生物体中。 - 天然来源和检测方法:头孢碱是从吐根(例如,Psychotria ipecacuanha)的根中分离得到的主要生物碱。文献[1]建立了一种HPLC定量方法:C18色谱柱(250×4.6 mm),流动相(甲醇-水-氨水,70:30:0.1,v/v/v),流速1.0 mL/min,检测波长280 nm,线性范围0.1–10 μg/mL(r²>0.999)。[1] - 抗癌机制: 1. 在MEC CSC中:头孢菌素诱导组蛋白H3乙酰化(可能通过抑制组蛋白去乙酰化酶HDACs,尚未明确证实),从而下调CSC相关基因并抑制CSC自我更新。 [3] 2. 在肺癌中:头孢菌素抑制NRF2(抗氧化防御的主要调节因子),降低NRF2下游抗氧化酶(HO-1、NQO1)的表达,从而增加细胞内氧化应激并促进铁死亡(铁依赖性细胞死亡)。[4] |
| 分子式 |
C28H38N2O4
|
|---|---|
| 分子量 |
466.6123
|
| 精确质量 |
466.283
|
| 元素分析 |
C, 72.07; H, 8.21; N, 6.00; O, 13.71
|
| CAS号 |
483-17-0
|
| 相关CAS号 |
Cephaeline hydrochloride;3738-70-3
|
| PubChem CID |
442195
|
| 外观&性状 |
Light yellow to yellow solid powder
|
| 密度 |
1.21g/cm3
|
| 沸点 |
614ºC at 760mmHg
|
| 熔点 |
115-116ºC
|
| 闪点 |
325.1ºC
|
| 蒸汽压 |
1.15E-15mmHg at 25°C
|
| 折射率 |
1.614
|
| 来源 |
Indian Ipecac roots; Cephaelis ipecacuanha
|
| LogP |
4.907
|
| tPSA |
63.19
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
6
|
| 重原子数目 |
34
|
| 分子复杂度/Complexity |
664
|
| 定义原子立体中心数目 |
4
|
| SMILES |
O(C([H])([H])[H])C1=C(C([H])=C2C([H])([H])C([H])([H])N3C([H])([H])[C@]([H])(C([H])([H])C([H])([H])[H])[C@@]([H])(C([H])([H])[C@]4([H])C5=C([H])C(=C(C([H])=C5C([H])([H])C([H])([H])N4[H])O[H])OC([H])([H])[H])C([H])([H])[C@@]3([H])C2=C1[H])OC([H])([H])[H]
|
| InChi Key |
DTGZHCFJNDAHEN-OZEXIGSWSA-N
|
| InChi Code |
InChI=1S/C28H38N2O4/c1-5-17-16-30-9-7-19-13-27(33-3)28(34-4)15-22(19)24(30)11-20(17)10-23-21-14-26(32-2)25(31)12-18(21)6-8-29-23/h12-15,17,20,23-24,29,31H,5-11,16H2,1-4H3/t17-,20-,23+,24-/m0/s1
|
| 化学名 |
(1R)-1-[[(2S,3R,11bS)-3-ethyl-9,10-dimethoxy-2,3,4,6,7,11b-hexahydro-1H-benzo[a]quinolizin-2-yl]methyl]-7-methoxy-1,2,3,4-tetrahydroisoquinolin-6-ol
|
| 别名 |
Cephaeline; 483-17-0; Cephaelin; Cepheline; 7',10,11-Trimethoxyemetan-6'-ol; CHEBI:3533; Dihydropsychotrine; (1R)-1-[[(2S,3R,11bS)-3-ethyl-9,10-dimethoxy-2,3,4,6,7,11b-hexahydro-1H-benzo[a]quinolizin-2-yl]methyl]-7-methoxy-1,2,3,4-tetrahydroisoquinolin-6-ol;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 本产品在运输和储存过程中需避光。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~214.31 mM)
Ethanol : ~33.33 mg/mL (~71.43 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (5.36 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (5.36 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (5.36 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.1431 mL | 10.7156 mL | 21.4312 mL | |
| 5 mM | 0.4286 mL | 2.1431 mL | 4.2862 mL | |
| 10 mM | 0.2143 mL | 1.0716 mL | 2.1431 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。