| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|

| 靶点 |
Endogenous Metabolite
|
|---|---|
| 体内研究 (In Vivo) |
ω-3脂肪酸可降低甘油三酯(TG)水平,但低密度脂蛋白胆固醇(LDL-C)水平的相应增加可能会影响心血管风险升高患者实现脂质目标。AMR101是一种研究药物,含有≥96%的纯二十碳五烯酸乙酯。III期多中心、安慰剂对照、随机、双盲、12周开放标签扩展研究(MARINE)调查了AMR101在229名TG水平非常高(≥500mg/dl)的患者中的疗效和安全性。AMR101 4 g/天显著降低了安慰剂调整后的TG水平中位数,与基线相比降低了33.1%(p<0.0001),AMR101 2 g/天降低了TG水平19.7%(p=0.0051)。LDL-C的变化很小,不显著。AMR101可以在不增加LDL-C水平的情况下显著降低TG。[1]
甲状腺激素影响几乎所有脂质代谢途径的反应。据报道,甲状腺功能减退症患者的血浆游离脂肪酸(FFA)浓度通常在正常范围内。然而,在这项研究中,我们发现一些甲状腺功能减退症患者的血浆FFA浓度高于正常范围。这些患者的甲状腺功能障碍症状比血浆游离脂肪酸浓度较低的患者轻。根据这些发现,我们假设FFA浓度的变化一定与甲状腺功能有关。然后,我们使用动物模型研究了高纯度二十碳五烯酸乙酯(EPA-E)对1-甲基-2-咪唑硫醇(MMI)诱导的甲状腺功能减退大鼠甲状腺功能的影响,EPA-E是一种来源于鱼油的n-3多不饱和脂肪酸。口服EPA-E抑制了MMI诱导的甲状腺功能减退大鼠甲状腺激素水平的降低和甲状腺滤泡的变化。这些发现表明,FFA可能影响甲状腺功能,EPA-E可能预防MMI诱导的甲状腺功能减退[2] ω-3脂肪酸改善脂肪代谢的确切机制尚不完全清楚。本研究旨在确定二十碳五烯酸(EPA)乙酯给药对参与脂肪生成和脂肪酸氧化途径的几种肌肉、肝脏和脂肪组织基因表达水平的影响。喂食标准饮食(对照动物)或高脂肪饮食的雄性Wistar大鼠每天口服EPA乙酯(1g/kg)灌胃治疗5周。高脂饮食导致血浆胆固醇水平显著升高(P<0.01),EPA可逆转这一现象(P<0.001)。EPA治疗组的循环甘油三酯水平也显著降低(P<0.05)。EPA给药诱导了一些脂肪生成基因的显著下调,如肌肉乙酰辅酶a羧化酶β(ACCβ)(P<0.05)和肝脏脂肪酸合酶(FAS)(P<.05)。此外,在喂食对照饮食的EPA处理动物中观察到葡萄糖激酶(GK)基因表达的降低(P<0.01),而在喂食高脂肪饮食的组中发现GK mRNA水平显著升高。另一方面,在EPA处理组中没有发现参与β氧化的基因发生改变,如乙酰辅酶A合酶4(ACS4)、乙酰辅酶A合成酶5(ACS5)或乙酰辅酶A氧化酶(ACO)。令人惊讶的是,与预期相反,在EPA治疗后,观察到肝脏PPARalpha的表达水平显著降低(P<0.01)。这些发现表明,EPA乙酯处理能够下调参与脂肪酸合成的一些基因,而不影响β氧化相关基因的转录激活[3]。 |
| 动物实验 |
29只雄性Wistar大鼠(6周龄)饲养于温度控制在22±2℃、光暗周期为12小时的房间内。动物被随机分为四组:对照组、对照组+EPA组(CEPA)、超重组和超重+EPA组(OEPA)。所有动物均适应4天,期间自由摄取标准饲料和去离子水。适应期结束后,对照组和CEPA组饲喂标准颗粒饲料,该饲料含有76%的碳水化合物、6%的脂肪和18%的蛋白质(362 kcal/100 g)。而超重组和OEPA组则饲喂自助餐式饲料,该饲料由以下食物组成:肉酱、薯片、培根、巧克力、饼干和颗粒饲料(比例为2:1:1:1:1:1)。该饮食的组成如下:蛋白质提供的能量占9%,碳水化合物提供的能量占29%,脂肪提供的能量占62%(按干重计)。所有动物均可自由摄取水和食物,持续5周。对照组和高脂饮食的脂肪酸组成分析方法如前所述,结果发现对照组和高脂饮食均不含EPA。因此,大鼠获取EPA的唯一途径是灌胃。因此,在维持饮食35天的同时,CEPA组和OEPA组分别给予1 g/kg体重的纯化EPA乙酯。Nobukata等人此前报道,该剂量的EPA乙酯对预防糖尿病有益。对照组和超重组也按照其他研究中所述的方法,灌胃给予相同体积的水,持续35天。这些未接受任何其他类型脂肪酸(例如与EPA或油酸链长相同的饱和脂肪酸)治疗的对照组和超重组,更可能被视为我们研究设计中的对照组。这是因为已有研究表明,补充某些其他脂肪酸能够改变脂肪含量以及本研究计划测定的生化和激素标志物的循环水平。[3]
本研究实验使用了5周龄雄性Wistar大鼠。根据初始体重,将大鼠分为两组,每组6只。通过皮下注射MMI(每日1 mg)并同时口服二十碳五烯酸乙酯/EPA-E(每日300 mg/kg)(或等体积生理盐水作为对照),持续4周,诱导大鼠甲状腺功能减退。 4周后,用氯仿麻醉大鼠,并采集血液样本和甲状腺组织。部分甲状腺组织立即用液氮冷冻,并在80℃下保存直至使用。[2] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
二十碳五烯酸乙酯脱酯后转化为活性EPA,然后在小肠被吸收。口服后5小时达到血浆峰浓度。由于EPA会整合到磷脂、甘油三酯和胆固醇酯中,因此仅有极少量(<1%)残留在血浆中。 二十碳五烯酸乙酯不经肾脏排泄。 活性EPA的稳态分布容积为88升。 EPA的总血浆清除率为684毫升/小时。 代谢/代谢物 转化为活性EPA后,经肝脏β-氧化代谢为乙酰辅酶A。 生物半衰期 EPA的半衰期为89小时。 |
| 毒性/毒理 (Toxicokinetics/TK) |
9831415 大鼠口服LD50 >20 gm/kg Yakkyoku. Pharmacy., 41(1621), 1990
9831415 大鼠腹腔注射LD50 15 gm/kg Yakkyoku. Pharmacy., 41(1621), 1990 9831415 大鼠皮下注射LD50 >20 gm/kg Yakkyoku. Pharmacy., 41(1621), 1990 9831415 小鼠口服LD50 >20 gm/kg Yakkyoku. Pharmacy., 41(1621), 1990 9831415 小鼠腹腔注射LD50 >20 gm/kg Yakkyoku.药学,41(1621),1990 |
| 参考文献 |
|
| 其他信息 |
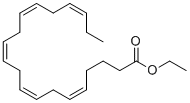
乙基(5Z,8Z,11Z,14Z,17Z)-二十碳五烯酸是一种长链脂肪酸乙酯,由(5Z,8Z,11Z,14Z,17Z)-二十碳五烯酸的羧基与乙醇的羟基缩合而成。它可用作降胆固醇药物、海洋代谢物、抗精神病药物、抗抑郁药物和前药。它是一种长链脂肪酸乙酯和多不饱和脂肪酸酯。其功能与全顺式-5,8,11,14,17-二十碳五烯酸相关。
二十碳五烯酸乙酯或二十碳五烯酸乙酯是ω-3脂肪酸二十碳五烯酸(EPA)的合成衍生物。它可用作严重高甘油三酯血症(甘油三酯水平 > 500 mg/dL)的辅助治疗,并可降低某些甘油三酯升高患者的心血管事件风险。于 2012 年 7 月 26 日获得 FDA 批准。 二十碳五烯酸乙酯是一种高纯度的 ω-3 脂肪酸,可降低血清甘油三酯水平。二十碳五烯酸乙酯可降低血清甘油三酯水平,且不会升高低密度脂蛋白胆固醇,但会增加骨骼肌中的胆固醇和甘油三酯含量。 另见:二十碳五烯酸(具有活性成分)。 药物适应症 二十碳五烯酸乙酯适用于作为最大耐受剂量他汀类药物治疗的辅助用药,以降低成年患者发生心肌梗死、卒中、冠状动脉血运重建和需要住院治疗的不稳定型心绞痛的风险。这些患者需伴有甘油三酯升高(≥150 mg/dL)和已确诊的心血管疾病,或患有糖尿病并具有≥2项其他心血管疾病危险因素。它还可作为饮食的辅助疗法,用于降低重度(≥500 mg/dL)高甘油三酯血症成年患者的甘油三酯水平。 FDA 标签 适用于作为他汀类药物的辅助疗法,以降低心血管风险。 高甘油三酯血症的治疗 作用机制 研究表明,EPA 可减少肝脏极低密度脂蛋白甘油三酯 (VLDL-TG) 的合成和/或分泌,并增强循环 VLDL 颗粒中 TG 的清除。其潜在作用机制包括:增加 β-氧化;抑制酰基辅酶 A:1,2-二酰甘油酰基转移酶 (DGAT);减少肝脏脂肪生成;以及增加血浆脂蛋白脂肪酶活性。 |
| 分子式 |
C22H34O2
|
|---|---|
| 分子量 |
330.512
|
| 精确质量 |
330.255
|
| 元素分析 |
C, 79.95; H, 10.37; O, 9.68
|
| CAS号 |
86227-47-6
|
| 相关CAS号 |
Eicosapentaenoic Acid;10417-94-4;Eicosapentaenoic acid ethyl ester-d5;1392217-44-5
|
| PubChem CID |
9831415
|
| 外观&性状 |
Colorless to light yellow liquid
|
| 密度 |
0.9±0.1 g/cm3
|
| 沸点 |
417.0±34.0 °C at 760 mmHg
|
| 闪点 |
103.1±24.0 °C
|
| 蒸汽压 |
0.0±1.0 mmHg at 25°C
|
| 折射率 |
1.496
|
| LogP |
7.32
|
| tPSA |
26.3
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
2
|
| 可旋转键数目(RBC) |
15
|
| 重原子数目 |
24
|
| 分子复杂度/Complexity |
425
|
| 定义原子立体中心数目 |
0
|
| SMILES |
C(/CCCC(=O)OCC)=C/C/C=C\C/C=C\C/C=C\C/C=C\CC
|
| InChi Key |
SSQPWTVBQMWLSZ-AAQCHOMXSA-N
|
| InChi Code |
InChI=1S/C22H34O2/c1-3-5-6-7-8-9-10-11-12-13-14-15-16-17-18-19-20-21-22(23)24-4-2/h5-6,8-9,11-12,14-15,17-18H,3-4,7,10,13,16,19-21H2,1-2H3/b6-5-,9-8-,12-11-,15-14-,18-17-
|
| 化学名 |
ethyl (5Z,8Z,11Z,14Z,17Z)-icosa-5,8,11,14,17-pentaenoate
|
| 别名 |
Eicosapentaenoic Acid Ethyl Ester; Epadel; Miraxion; AMR-101; EPA-E; LAX-101; ethyl icosapentate; 86227-47-6; ICOSAPENT ETHYL; Eicosapentaenoic acid ethyl ester; Epadel; ethyl eicosapentaenoate; Vascepa; Timnodonic acid ethyl ester; EPA E; LAX 101; MND 21; MND-21; AMR 101; AMR101; MND21; EPAE; LAX101
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~302.57 mM)
Ethanol : ~50 mg/mL (~151.29 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 5 mg/mL (15.13 mM) (饱和度未知) in 10% EtOH + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,将 100 μL 50.0 mg/mL 澄清乙醇储备液加入到 400 μL PEG300 中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: 5 mg/mL (15.13 mM) (饱和度未知) in 10% EtOH + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 例如,若需制备1 mL的工作液,可将 100 μL 50.0 mg/mL 澄清乙醇储备液加入到 900 μL 20% SBE-β-CD 生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 5 mg/mL (15.13 mM) (饱和度未知) in 10% EtOH + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: 2.5 mg/mL (7.56 mM) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL 澄清的 DMSO 储备液加入到400 μL PEG300中,混匀;再向上述溶液中加入50 μL Tween-80,混匀;然后加入450 μL 生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 5 中的溶解度: 2.5 mg/mL (7.56 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 例如,若需制备1 mL的工作液,可将100μL 25.0mg/mL澄清的DMSO储备液加入到900μL 20%SBE-β-CD生理盐水中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 配方 6 中的溶解度: ≥ 2.5 mg/mL (7.56 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL 澄清 DMSO 储备液加入到 900 μL 玉米油中并混合均匀。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.0256 mL | 15.1281 mL | 30.2563 mL | |
| 5 mM | 0.6051 mL | 3.0256 mL | 6.0513 mL | |
| 10 mM | 0.3026 mL | 1.5128 mL | 3.0256 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Link: https://clinicaltrials.gov/ct2/show/NCT06710080
Conditions:Inflammation|Community Acquired Pneumonia (CAP)|Inflammation Plaque, AtheroscleroticLink: https://clinicaltrials.gov/ct2/show/NCT06466278
Conditions:Aortic Valve StenosisLink: https://clinicaltrials.gov/ct2/show/NCT05198843
Conditions:Anatomic Stage IV Breast Cancer AJCC v8|Metastatic Triple-Negative Breast Inflammatory Carcinoma
Title:The Effect of E-EPA on Circulating LDL and Plasma Lipid Metabolism
Status:Completed
updateDate:2025-09-22
Ctid:NCT04152291
Link: https://clinicaltrials.gov/ct2/show/NCT04152291
Conditions:Atherosclerosis|Low-density Lipoproteins Aggregation Susceptibility|Low-density Lipoprotein Lipid Composition|Cardiovascular DiseasesLink: https://clinicaltrials.gov/ct2/show/NCT03428477
Conditions:Liver Metastasis|Colon CancerLink: https://clinicaltrials.gov/ct2/show/NCT06280976
Conditions:Coronary Artery Disease|Atherosclerosis|Heart AttackLink: https://clinicaltrials.gov/ct2/show/NCT04682665
Conditions:Colon Cancer Liver MetastasisLink: https://clinicaltrials.gov/ct2/show/NCT02719327
Conditions:Alzheimer's DiseaseLink: https://clinicaltrials.gov/ct2/show/NCT04239950
Conditions:HypertriglyceridemiaLink: https://clinicaltrials.gov/ct2/show/NCT04216251
Conditions:Colorectal Adenoma|Colorectal Cancer|Endoscopic Surgery|Eicosapentaenoic Acid|Gastrointestinal MicrobiomeLink: https://clinicaltrials.gov/ct2/show/NCT04562467
Conditions:Cardiovascular Diseases|Cardiovascular Risk Factor|Triglycerides High|Diabetes Mellitus, Type 2Link: https://clinicaltrials.gov/ct2/show/NCT04505098
Conditions:Covid19|Atherosclerosis|Cardiovascular Diseases|Upper Respiratory Tract InfectionsLink: https://clinicaltrials.gov/ct2/show/NCT02926027
Conditions:HypertriglyceridemiaLink: https://clinicaltrials.gov/ct2/show/NCT04811404
Conditions:Bipolar DisorderLink: https://clinicaltrials.gov/ct2/show/NCT01492361
Conditions:Cardiovascular DiseasesLink: https://clinicaltrials.gov/ct2/show/NCT02422446
Conditions:Type 2 Diabetes|Coronary Artery DiseaseLink: https://clinicaltrials.gov/ct2/show/NCT04177680
Conditions:HypertriglyceridemiaLink: https://clinicaltrials.gov/ct2/show/NCT04412018
Conditions:COVID-19|Inflammatory ResponseLink: https://clinicaltrials.gov/ct2/show/NCT03661047
Conditions:Colon CancerLink: https://clinicaltrials.gov/ct2/show/NCT03885661
Conditions:Lipid Disorder|Triglycerides High|DyslipidemiasLink: https://clinicaltrials.gov/ct2/show/NCT04460651
Conditions:COVID19Link: https://clinicaltrials.gov/ct2/show/NCT02940223
Conditions:Advanced Malignant Neoplasm|FatigueLink: https://clinicaltrials.gov/ct2/show/NCT00231738
Conditions:Myocardial Infarction, Unstable Angina Pectoris, Sudden Cardiac Death, Stroke, Peripheral Artery DiseaseLink: https://clinicaltrials.gov/ct2/show/NCT01154985
Conditions:SteatohepatitisLink: https://clinicaltrials.gov/ct2/show/NCT00634361
Conditions:Schizophrenia ProdromeLink: https://clinicaltrials.gov/ct2/show/NCT00419146
Conditions:Schizophrenia|Schizophreniform Disorders|Schizoaffective Disorder|Psychotic DisordersLink: https://clinicaltrials.gov/ct2/show/NCT00839449
Conditions:Subarachnoid Hemorrhage|Cerebral VasospasmLink: https://clinicaltrials.gov/ct2/show/NCT00001146
Conditions:Bipolar Disorder|Involutional Depression|Mood DisorderLink: https://clinicaltrials.gov/ct2/show/NCT00146211
Conditions:Huntington DiseaseLink: https://www.clinicaltrialsregister.eu/ctr-search/search?query=2009-010520-25
Condition:HypertriglyceridemiaLink: https://www.clinicaltrialsregister.eu/ctr-search/search?query=2009-013458-33
Condition:Healthy volunteersintended indication of the product: primary and secondary prevention of cardiovascular morbidity and mortalityLink: https://www.clinicaltrialsregister.eu/ctr-search/search?query=2007-001921-86
Condition:HAART-induced hypertriglyeridemia in HIV infected subjectsLink: https://www.clinicaltrialsregister.eu/ctr-search/search?query=2005-002088-98
Condition:HUNTINGTON'S DISEASE