| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| Other Sizes |
|
| 靶点 |
BTK/Bruton’s tyrosine kinase
|
|---|---|
| 体外研究 (In Vitro) |
1. BTK激酶抑制
- 剂量依赖性抑制BTK自磷酸化(Tyr223),生化实验IC₅₀=5.9 nM,细胞实验IC₅₀=6.4 nM,抑制可逆(Hill系数-0.84 ± 0.07)[1,5]
2. 选择性 - 对其他激酶(如JAK2、SYK、EGFR)选择性>100倍(1 μM浓度下)[3] 3. 代谢特性 - 人醛氧化酶(AOX)介导酰胺水解,生成羧酸代谢物M1,酶动力学参数Km=11.2 μM,Vmax=1.8 nmol/min/mg(重组人AOX)[2] |
| 体内研究 (In Vivo) |
1. 抗关节炎疗效(大鼠CIA模型)
- 口服30–100 mg/kg剂量依赖性减轻胶原诱导关节炎(CIA)大鼠踝关节肿胀(ED₅₀=45 mg/kg),100 mg/kg时肿胀减少70%,伴随滑膜增生和中性粒细胞浸润显著改善[1,3]
- 外周血单个核细胞(PBMCs)中BTK磷酸化抑制率≥90%(100 mg/kg组),与疗效强相关(r²=0.89)[1] 2. 种属药代差异 - 人源化PXB嵌合小鼠中清除率低(CL<10 mL/min/kg),口服生物利用度<5%。人类单次口服35–105 mg后,多数血浆浓度低于定量限(<1 ng/mL),提示快速AOX代谢[2,3] |
| 酶活实验 |
- 生化实验:重组人BTK(10 nM)与ATP(10 μM)、GDC-0834(0.01–1000 nM)孵育,ELISA检测肽底物(KKLPQpYASL)磷酸化,三次重复实验计算IC₅₀=5.9 nM[1]
- 细胞实验:抗IgM刺激的Ramos细胞(1×10⁶ cells/mL)与药物共孵15分钟,流式检测磷酸化BTK(Tyr223),IC₅₀=6.4 nM[1] |
| 动物实验 |
模型:雄性Lewis大鼠(180–200 g),用牛II型胶原蛋白(CIA)诱导。从诱导后第21天开始,每日口服GDC-0834(30、60、100 mg/kg)或赋形剂(0.5%甲基纤维素),持续7天[1]
- 给药:配制成0.5%甲基纤维素混悬液。每日测量踝关节周长;取关节进行组织病理学检查(H&E染色)[1] - PK/PD模型:血浆GDC-0834浓度(LC-MS/MS)与PBMC中BTK磷酸化抑制呈正相关(r² = 0.89),确定体内疗效的EC₅₀为5.6 μM[1] |
| 药代性质 (ADME/PK) |
- 代谢:主要通过人AOX(而非CYP酶)经酰胺水解代谢为M1。非人物种(猴、狗、大鼠)的水解作用可忽略不计,因此不适用于预测人体药代动力学[2]
- 清除率:大鼠的清除率为25 mL/min/kg;小鼠的清除率为18 mL/min/kg。由于AOX活性强,预计人体清除率更高[2,3] - 口服生物利用度:人体<5%(可能由于首过代谢),而大鼠为25%[2] |
| 毒性/毒理 (Toxicokinetics/TK) |
安全性:大鼠在剂量高达 200 mg/kg(10 倍治疗剂量)时未观察到明显毒性。在 100 mg/kg 剂量下观察到轻度血小板减少症(血小板计数 ↓15%)[1]
- hERG 抑制:在 10 μM 浓度下未观察到显著抑制(>30%),表明 QT 间期延长的风险较低 |
| 参考文献 |
|
| 其他信息 |
机制:竞争性BTK抑制剂与ATP结合口袋结合(晶体结构:PDB 5V9P)。阻断BCR信号传导,减少促炎细胞因子(TNF-α、IL-6)的分泌[1,5]
- 临床意义:尽管人体药代动力学数据不佳,但由于自身免疫性疾病领域存在未被满足的医疗需求,该药物仍迅速进入I期临床试验。人体内有限的全身暴露表明可能需要局部或局部给药[2,3] - 专利状态:专利号WO2010037798A1 (2010)涵盖了用于治疗关节炎的BTK抑制剂[3] |
| 分子式 |
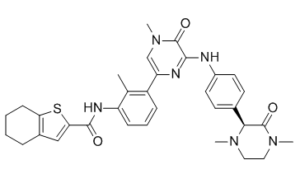
C33H36N6O3S
|
|---|---|
| 分子量 |
596.742345809937
|
| 精确质量 |
596.257
|
| 元素分析 |
C, 66.42; H, 6.08; N, 14.08; O, 8.04; S, 5.37
|
| CAS号 |
1133432-50-4
|
| 相关CAS号 |
GDC-0834;1133432-49-1;GDC-0834 Racemate; 1133432-50-4; GDC-0834 (S-enantiomer); GDC-0834 S-Enantiomer; N-[3-(6-{4-[(2S)-1,4-Dimethyl-3-oxopiperazin-2-yl]anilino}-4-methyl-5-oxo-4,5-dihydropyrazin-2-yl)-2-methylphenyl]-4,5,6,7-tetrahydro-1-benzothiophene-2-carboxamide; N-[3-[6-[4-[(2S)-1,4-dimethyl-3-oxopiperazin-2-yl]anilino]-4-methyl-5-oxopyrazin-2-yl]-2-methylphenyl]-4,5,6,7-tetrahydro-1-benzothiophene-2-carboxamide; CHEMBL3401292; C33H36N6O3S; CDOOFZZILLRUQH-LJAQVGFWSA-N; 1133432-46-8
|
| PubChem CID |
25234917
|
| 外观&性状 |
Brown to reddish brown solid powder
|
| LogP |
4.507
|
| tPSA |
131.04
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
6
|
| 重原子数目 |
43
|
| 分子复杂度/Complexity |
1140
|
| 定义原子立体中心数目 |
1
|
| SMILES |
CC1=C(C=CC=C1NC(=O)C2=CC3=C(S2)CCCC3)C4=CN(C(=O)C(=N4)NC5=CC=C(C=C5)[C@H]6C(=O)N(CCN6C)C)C
|
| InChi Key |
CDOOFZZILLRUQH-GDLZYMKVSA-N
|
| InChi Code |
InChI=1S/C33H36N6O3S/c1-20-24(9-7-10-25(20)36-31(40)28-18-22-8-5-6-11-27(22)43-28)26-19-39(4)33(42)30(35-26)34-23-14-12-21(13-15-23)29-32(41)38(3)17-16-37(29)2/h7,9-10,12-15,18-19,29H,5-6,8,11,16-17H2,1-4H3,(H,34,35)(H,36,40)/t29-/m1/s1
|
| 化学名 |
(R)-N-(3-(6-((4-(1,4-dimethyl-3-oxopiperazin-2-yl)phenyl)amino)-4-methyl-5-oxo-4,5-dihydropyrazin-2-yl)-2-methylphenyl)-4,5,6,7-tetrahydrobenzo[b]thiophene-2-carboxamide
|
| 别名 |
GDC0834 S-enantiomer; GDC-0834 S-enantiomer; GDC 0834.
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~167.58 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (4.19 mM) (饱和度未知) in 10% DMSO + 40% PEG300 +5% Tween-80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80+,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.6758 mL | 8.3789 mL | 16.7577 mL | |
| 5 mM | 0.3352 mL | 1.6758 mL | 3.3515 mL | |
| 10 mM | 0.1676 mL | 0.8379 mL | 1.6758 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
 Proteomic correlation profiling revealed that aldehyde oxidase (AO/ADO) is an enzyme present in cytosolic fractions containing the hydrolytic enzyme activity involved in the metabolism of GDC-0834.Drug Metab Dispos.2015 Jun;43(6):908-15. |
|---|
 Homology model for aldehyde oxidase (AO) using the human sequence and the mouse crystal structure (PDB ID 3ZYV).
Formation of M1 after incubation of GDC-0834 (0.8µM) in (A) fresh whole blood and (B) plasma in human (○), rat ( |
 IC50curves for the inhibition by GDC-0834 (0–50 or 0–100μM) of AO-mediated metabolism of AO probe substrates in human liver cytosol (A) carbazeran (formation of 4-hydroxycarbazeran), (B) DACA (formation of DACA-9(10H)-acridone), (C)O6-benzylguanine (formation of 8-oxobenzylguanine), (D) phthalazine (formation of phthalazinone), (E) zaleplon (formation of 5-oxozaleplon), and (F) zoniporide (formation of 2-oxozoniporide).Drug Metab Dispos.2015 Jun;43(6):908-15. |