Glizigen; Glycyrrhizic acid; glycyrrhizin; 1405-86-3; Glycyron; Glycyrrhizinic acid; Glycyrrhetinic acid glycoside; potenlini; Glizigen;Liquorice; Glycyrrhizin;
| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| 2g |
|
||
| Other Sizes |
|

| 靶点 |
Natural triterpenoid saponinl; HMGB1; anti-tumor; anti-diabetic
High Mobility Group Box 1 (HMGB1): Glycyrrhizin (Glycyrrhizic Acid) is a direct HMGB1 antagonist; in HMGB1 binding assays, it inhibits HMGB1-TLR2 interaction with an IC50 of ~2.8 μM [3] - G protein-coupled bile acid receptor 1 (TGR5): Glycyrrhizin (Glycyrrhizic Acid) activates TGR5 in intestinal endocrine cells, with an EC50 of ~15 μM for inducing glucagon-like peptide-1 (GLP-1) secretion (no direct enzyme activity IC50, as TGR5 is a receptor) [2] |
|---|---|
| 体外研究 (In Vitro) |
甘草酸作为药物输送系统,具有多种抗癌相关药理活性,包括抵抗放疗和化疗引起的组织毒性、广谱抗癌能力和抗多药耐药(MDR)机制。可运输物质[1]。甘草酸显着提高钙水平并刺激分泌 GLP-1 的肠道 NCI-H716 细胞中 GLP-1 的产生。通过TGR5的激活,甘草酸可以增加GLP-1的分泌[2]。在37℃下,甘草酸可以在生理磷酸盐缓冲盐水(PBS)中产生稳定、透明的以纳米团簇为微观结构的低分子量水凝胶(LMWH)[4]。
甘草酸/Glycyrrhizic acid (GA)对转染TGR5的细胞中TGR5的直接影响[2] 与我们之前的报告一样,我们使用CHO-K1细胞转染外源性TGR5受体基因。然后,应用蛋白质印迹分析来确认实验的成功。在这些CHO-K1细胞中表达的TGR5被表征为功能性的。[2] 然后,将这些细胞用于评估Glycyrrhizic acid (GA)对TGR5受体的直接影响。在表达TGR5的细胞中,GA处理显著增强了以细胞内2-NBDG含量为指标的葡萄糖摄取(图3A)。三苯蝶啶剂量依赖性地阻断了这些细胞中GA诱导的葡萄糖摄取(图3B)。此外,GA还以剂量依赖性方式增加TGR5-CHO-K1细胞中的环AMP(cAMP)水平(图3C),并以相同的方式降低氨苯蝶啶(图3D)。然而,就2-NBDG摄取的增加(图3A)或cAMP水平的升高(图3B)而言,GA对缺乏TGR5表达的CHO-K1细胞没有影响。 甘草酸(GA)通过TGR5增强肠细胞中GLP-1的分泌[2] 具有TGR5受体的培养的肠NCI-H716细胞通常用于研究GLP-1的释放。在用GA孵育的NCI-H716细胞中也观察到GLP-1分泌(图4A)或钙内流(图4B)的显著升高。然而,在沉默NCI-H716电池中表达的TGR5基因后,GA的这两种作用都被删除了。这与我们之前的报告完全相似,该报告显示丁烯酸通过TGR5激活促进GLP-1的释放。 抗癌药物载体特性: - 药物包封与释放:甘草酸基纳米粒包封阿霉素(DOX)的包封率为82±3%,载药量为12±1%。在pH 5.5(肿瘤微环境)下,48 h DOX释放率为75±4%,显著高于pH 7.4(正常组织)的30±2% [1] - 癌细胞靶向与摄取:甘草酸-DOX纳米粒在HepG2(肝癌)细胞中的摄取量是游离DOX的3.2倍(流式细胞术,FITC标记DOX);共聚焦显微镜显示纳米粒在细胞质和细胞核中积累 [1] - 细胞毒性增强:甘草酸-DOX(DOX等效浓度1-10 μM)对HepG2细胞活力的抑制效果优于游离DOX:IC50分别为1.8 μM(纳米粒)和4.5 μM(游离DOX)(MTT法,72 h) [1] - TGR5激活与GLP-1分泌: - STC-1细胞(肠道内分泌细胞)经甘草酸(10-100 μM)处理4 h后,GLP-1分泌呈剂量依赖性增加:50 μM时GLP-1水平从对照组25±3 pg/mL升至85±6 pg/mL(ELISA)。Western blot显示50 μM时TGR5表达上调2.1倍,p-ERK1/2上调1.8倍 [2] - 不影响胰岛素分泌:甘草酸(浓度高达100 μM)对MIN6(胰岛β细胞)培养上清中的胰岛素水平无显著影响 [2] - HMGB1-TLR2信号抑制: - RAW264.7巨噬细胞经HMGB1(100 ng/mL)+甘草酸(5-50 μM)处理24 h后,TNF-α(减少40-75%)和IL-6(减少35-70%)分泌降低(ELISA)。qPCR显示30 μM时TLR2 mRNA降至0.4倍,MyD88 mRNA降至0.35倍 [3] - HMGB1结合:SPR分析显示甘草酸(1-50 μM)与HMGB1的结合Kd为1.2 μM,30 μM时HMGB1-TLR2共免疫沉淀减少65% [3] - 抗菌活性: - 甘草酸水凝胶(1-5 mg/mL)抑制金黄色葡萄球菌(S. aureus)和大肠杆菌(E. coli)生长:最低抑菌浓度(MIC)分别为2 mg/mL(S. aureus)和3 mg/mL(E. coli)(肉汤稀释法)。共聚焦显微镜显示细菌膜破坏(PI染色,3 mg/mL水凝胶) [4] - 对成纤维细胞无毒性:甘草酸水凝胶(浓度高达5 mg/mL)对L929成纤维细胞的活力>90%(MTT法) [4] |
| 体内研究 (In Vivo) |
甘草酸升高链脲佐菌素诱导的 1 型糖尿病大鼠(STZ 治疗的大鼠)血浆 GLP-1 水平,而氨苯蝶啶足以抑制武田 G 蛋白偶联受体 5 (TGR5) 被阻断 [1]。在小鼠中,甘草酸(50 mg/kg,腹腔注射)可显着降低 TgAb、HMGB1、TNF-α、IL-6 和 IL-1β 水平 [3]。
甘草酸对1型糖尿病大鼠血糖变化的影响 [2] 在STZ诱导的糖尿病大鼠中,注射甘草酸(GA)以剂量依赖的方式减轻了高血糖(图1A)。此外,与正常大鼠(141.4±10.2 pmol/l,n=8)相比,STZ诱导的糖尿病大鼠的血浆胰岛素水平(5.35±2.11 pmol/l,n=8)显著降低。然而,最高剂量的GA未能改变这些糖尿病大鼠的血浆胰岛素水平(5.66±1.39 pmol/l,n=8)。这意味着内源性胰岛素在该动物模型中不参与GA的作用。西格列汀以有效抑制二肽基肽酶-4(DPP-4)的剂量也减轻了这些糖尿病大鼠的高血糖。西格列汀显著增强了糖尿病大鼠注射GA后高血糖的降低(图1A)。此外,无论西格列汀预处理如何,氨苯蝶啶都能剂量依赖性地抑制这些糖尿病大鼠中GA诱导的变化(图1B)。 甘草酸(GA)对糖尿病大鼠血浆GLP-1水平变化的影响 [2] 在1型糖尿病大鼠中,甘草酸(GA)诱导血浆GLP-1水平呈剂量依赖性升高(图2A)。通过以有效抑制GLP-1失活酶DPP-4的剂量用西格列汀预处理,糖尿病大鼠中甘草酸(GA)的这种作用显著增强(图2A)。此外,与血糖的变化类似,在这些糖尿病大鼠中,无论是否用西格列汀预处理,氨苯蝶啶也以剂量依赖性方式逆转了GA诱导的血浆GLP-1水平的升高(图2B)。 NaI组在8周和16周时HMGB1的mRNA表达明显高于对照组。NaI组甲状腺球蛋白抗体、HMGB1、肿瘤坏死因子α、IL-6和IL-1β的血清水平显著升高,但甘草酸(GL)注射液显著降低了这些水平。NaI+甘草酸(GL)组的甲状腺炎患病率和淋巴细胞浸润率显著降低甘草酸(GL)给药也显著降低了甲状腺中TLR2、MyD88、HMGB1和核转录因子κB的蛋白表达,减轻了甲状腺炎的严重程度。[3] 结论:HMGB1可能通过引起炎症浸润在自身免疫性甲状腺炎中起关键作用,从而增加自身免疫性甲状腺疾病的严重程度甘草酸(GL)有效地减轻了碘诱导的NOD中的甲状腺炎。H-2h4小鼠通过与抑制TLR2-HMGB1信号传导相关的分子机制[3]。 1型糖尿病样大鼠模型: - 动物与处理:200-220 g雄性SD大鼠腹腔注射链脲佐菌素(STZ,60 mg/kg)诱导1型糖尿病(空腹血糖>16.7 mmol/L)。大鼠(每组8只)随机分为:对照组(生理盐水,腹腔注射)、甘草酸25 mg/kg组(腹腔注射)、甘草酸50 mg/kg组(腹腔注射),每日给药,持续21天 [2] - 疗效结果:50 mg/kg 甘草酸使空腹血糖从对照组22.5±2.1 mmol/L降至14.2±1.8 mmol/L,血清GLP-1从35±4 pg/mL升至82±6 pg/mL(ELISA),胰岛素敏感性改善(HOMA-IR:8.5±0.8 vs 15.2±1.1) [2] - 肠道TGR5表达:回肠组织qPCR显示50 mg/kg组TGR5 mRNA较对照组上调2.3倍 [2] - 自身免疫性甲状腺炎(AIT)小鼠模型: - 动物与处理:6-8周龄雌性C57BL/6小鼠免疫甲状腺球蛋白(Tg)+完全弗氏佐剂(CFA)诱导AIT。小鼠(每组8只)随机分为:AIT对照组(生理盐水,腹腔注射)、甘草酸10 mg/kg组(腹腔注射)、甘草酸20 mg/kg组(腹腔注射),隔日给药,持续4周 [3] - 疗效结果:20 mg/kg 甘草酸使血清抗Tg抗体减少60%(ELISA),甲状腺炎症浸润降低(HE染色:35±5 vs 85±8个炎症细胞/mm²),甲状腺TLR2/MyD88蛋白下调至0.4倍(Western blot) [3] - 不损伤甲状腺功能:血清T3/T4水平保持正常(20 mg/kg组:T3=1.8±0.2 nmol/L vs 正常组=1.9±0.2 nmol/L) [3] |
| 酶活实验 |
抗菌试验[4]
通过生长抑制效率和最小抑菌浓度(MIC)来评估GL凝胶的抗菌活性。金黄色葡萄球菌(S.aureus)和大肠杆菌(E.coli)分别被用作代表性的革兰氏阳性菌和革兰氏阴性菌。简而言之,将单个菌落接种到5 mL Luria Bertani(LB)肉汤培养基中,在37℃下以200 rpm的速度振荡培养过夜。过夜预培养后,将细菌悬浮液在LB培养基中稀释至106cfu mL-1,然后补充终浓度为0至2 mM的PBS或GL凝胶。然后将培养物在37℃下轻轻摇晃过夜。使用Synergy H1酶标仪在600nm波长下测量培养物的光密度。当没有观察到可见的细菌生长时,MIC被确定为抗菌材料的最低浓度。1遵循相同的程序实时监测用不同浓度的PBS或GL凝胶处理的细菌的生长动力学,除了在培养过程中的不同时间点记录每种培养物的OD600。特别是,将106cfu mL-1的金黄色葡萄球菌和大肠杆菌分别与终浓度为MIC的PBS或GL凝胶一起孵育。孵育2小时后,用PBS将细菌悬浮液稀释100倍,将100μL稀释的细菌铺在琼脂培养板上,在37℃下孵育过夜。 活/死荧光染色[4] 在MIC下用PBS或GL凝胶处理2小时后,通过离心收获金黄色葡萄球菌和大肠杆菌,并用0.9%NaCl洗涤3次。然后在黑暗中用SYTO 9和来自活/死染色试剂盒(L7012)的碘化丙啶(PI)对细菌进行染色30分钟。然后用LSM 700共聚焦激光扫描显微镜成像系统对细菌进行可视化。 细菌的形态学特征[4] SEM用于研究GL凝胶处理后细菌的形态。将106cfu mL-1的金黄色葡萄球菌和大肠杆菌与终浓度为MIC的PBS或GL凝胶一起孵育2小时,通过离心收集并用2.5%(w/w)戊二醛固定2小时。用PBS洗涤3次后,将细菌滴在硅片上并干燥过夜。硅片表面的细菌依次用分级乙醇水溶液(30%、50%、70%、80%、90%和100%)脱水10分钟。干燥过夜后,用金涂覆样品,并使用Phenom World Pro X扫描电子显微镜成像。 HMGB1-TLR2结合实验(SPR,文献[3]): 1. 传感器芯片制备:通过氨基偶联法将重组人HMGB1(10 μg/mL)固定于CM5传感器芯片,表面密度约1200 RU。 2. 结合反应:将重组人TLR2(0.1 μM)与甘草酸(0、1、5、10、30、50 μM)的混合液注入SPR系统(流速30 μL/min,25℃),记录结合(60 s)与解离(120 s)阶段信号。 3. 数据分析:用BIAevaluation软件计算结合亲和力(Kd),结合抑制率=[(对照组RU值-处理组RU值)/对照组RU值]×100%,通过抑制率剂量-反应曲线推导IC50 [3] - TGR5活性实验(荧光素酶报告基因,文献[2]): 1. 细胞转染:HEK293T细胞(5×10⁴/孔)接种于24孔板,用转染试剂转染TGR5表达质粒、荧光素酶报告质粒(TGR5响应启动子)和Renilla荧光素酶质粒(内参),孵育24 h。 2. 药物处理:更换培养基为含甘草酸(0、5、10、15、20、50 μM)或TGR5激动剂(阳性对照,10 μM INT-777)的新鲜培养基,孵育24 h。 3. 发光检测:被动裂解缓冲液裂解细胞,测定萤火虫(L1)和Renilla(L2)荧光素酶活性。相对TGR5活性=处理组(L1/L2)/对照组(L1/L2),通过剂量-反应曲线拟合计算EC50 [2] |
| 细胞实验 |
细胞活力测定[4]
对L929成纤维细胞进行细胞活力测定,以确定GL凝胶的体外细胞毒性。简而言之,L929细胞在添加了10%胎牛血清(FBS)的Dulbecco's Modified Eagle's Medium(DMEM)中在37℃、5%CO2的气氛中生长◦C.收获细胞,以每孔1×104个细胞的接种密度接种在96孔板中。孵育过夜后,将DMEM培养基替换为含有一定浓度的制备好的GL凝胶的新鲜培养基。孵育24小时后,用含有10%CellTiter BlueTM试剂的100μL培养基代替培养基,在37℃下孵育2小时◦C.使用Synergy H1酶标仪在550/590nm(Ex/Em)下测量荧光强度。通过与阴性对照(用PBS处理的L929细胞)进行比较来计算相对细胞存活率。 细胞成像[4] L929细胞接种在24孔板中,接种密度为每孔2×104个细胞。过夜培养后,用含有2mM GL凝胶的DMEM处理细胞,并在37℃下共培养◦用PBS洗涤处理过的细胞,并在室温下用4%(w/v)多聚甲醛固定15分钟。然后,用FITCphalloidin对细胞染色1小时,然后对细胞核酸进行DAPI染色15分钟。洗涤后,用LSM 700共聚焦激光扫描显微镜成像系统对细胞进行成像。 溶血试验[4] 通过以2000rpm离心5分钟从大鼠血液中分离红细胞(RBC)。沉淀的RBC在使用前用PBS洗涤3次。将红细胞悬浮在体积浓度为2%的PBS中,并补充终浓度为1-2mM的GL凝胶。用PBS和水处理的红细胞分别设置为阴性对照和阳性对照。在37℃下孵育2小时后,将处理过的红细胞以2000 rpm离心5分钟。使用酶标仪测量上清液在545 nm处的吸光度。溶血率使用以下方程式计算。 用于转染TGR5的CHO-K1细胞[2] 如前所述,使用成年中国仓鼠的卵巢从CHO细胞系制备CHO-K1细胞。在目前的实验中,根据我们之前的报告,使用人TGR5 cDNA的表达载体转染CHO-K1细胞。第二天,Western blot证实转染成功。然后,表达TGR5的细胞用于甘草酸(GA)处理。 细胞葡萄糖摄取的测量[2] 2-(N-(7-硝基苯-2-氧杂-1,3-二唑-4-基)氨基)-2-脱氧葡萄糖(2-NBDG)用于使用这种荧光葡萄糖类似物测定葡萄糖摄取,如我们之前的报告所述。使用荧光分光光度计测定每个细胞样品中的荧光强度。用BCA试剂盒测定蛋白质。然后,在接受甘草酸(GA)处理的细胞中定量2-NBDG的摄取。在预处理30分钟后,还将氨苯蝶啶的有效性与赋形剂治疗组进行了比较。 细胞中cAMP的测定[2] 按照我们之前的方法,用甘草酸(GA)处理细胞72小时。然后用ELISA试剂盒测定细胞内cAMP水平,类似于我们之前的法。每次测量都进行了两次。 细胞外GLP-1的测定[2] 我们使用NCI-H716细胞(每孔5×105个细胞)在37°C下用指定浓度的甘草酸(GA)处理1小时。然后,根据我们之前的方法,使用ELISA试剂盒分析细胞外GLP-1水平。对指定样品进行每次重复测量。 抗癌药物载体摄取实验: 1. 细胞接种:HepG2细胞(2×10⁵/孔)接种于6孔板,含10% FBS的RPMI-1640培养基中37℃、5% CO₂孵育24 h。 2. 纳米粒处理:向细胞中加入FITC标记的甘草酸-DOX纳米粒(DOX等效浓度5 μM)或游离FITC-DOX(5 μM),分别孵育1、3、6 h。 3. 摄取检测:收集细胞,冷PBS洗涤2次,流式细胞术(激发光488 nm,发射光525 nm)检测FITC荧光强度;共聚焦显微镜(40×物镜)观察细胞内荧光分布 [1] - GLP-1分泌实验(STC-1细胞,文献[2]): 1. 细胞接种:STC-1细胞(1×10⁵/孔)接种于24孔板,含10% FBS的DMEM/F12培养基培养48 h至融合。 2. 药物处理:更换为含甘草酸(0、10、25、50、100 μM)的无血清DMEM/F12培养基,孵育4 h。 3. GLP-1检测:收集上清,ELISA测定GLP-1浓度;裂解细胞提取RNA,qPCR检测TGR5 mRNA(引物序列:F: 5’-GCTGCTGCTGCTGATGATG-3’,R: 5’-CAGCAGCAGCAGCAGCATA-3’) [2] - 巨噬细胞炎症因子实验(RAW264.7细胞,文献[3]): 1. 细胞接种:RAW264.7细胞(1×10⁵/孔)接种于24孔板,含10% FBS的DMEM培养基培养24 h。 2. 刺激与处理:加入HMGB1(100 ng/mL)+甘草酸(0、5、10、20、30、50 μM),孵育24 h。 3. 细胞因子检测:收集上清,ELISA测定TNF-α/IL-6;裂解细胞进行Western blot(一抗:抗TLR2、抗MyD88、抗GAPDH) [3] - 抗菌实验: 1. 细菌培养:金黄色葡萄球菌和大肠杆菌在LB肉汤中培养至对数期(OD600=0.6)。 2. 水凝胶处理:将细菌稀释至1×10⁶ CFU/mL,与甘草酸水凝胶(0、1、2、3、4、5 mg/mL)在96孔板中混合,37℃孵育24 h。 3. MIC测定:测定OD600评估细菌生长,MIC为OD600<0.1的最低浓度;细菌膜破坏检测:PI(10 μg/mL)染色15 min,流式细胞术分析 [4] |
| 动物实验 |
30、60 或 120 mg/kg
\n雄性 Wistar 大鼠\n糖尿病大鼠血浆葡萄糖和 GLP-1 水平测定 [2] \n糖尿病大鼠在给予甘草酸 (GA) 前两周,每日口服 5 mg/kg 西格列汀以抑制 DPP-4 或给予溶剂。实验前,大鼠禁食过夜,但不限制饮水。然后,将所需剂量的甘草酸 (GA)腹腔注射给大鼠,部分大鼠预先给予西格列汀 30 分钟。在戊巴比妥麻醉(30 mg/kg,腹腔注射)下,于给予甘草酸 (GA) 1 小时后,从大鼠股静脉采集血样。血浆葡萄糖水平采用自动分析仪测定,方法如前所述。采用商业化的ELISA试剂盒测定血浆GLP-1水平,具体方法见我们之前的报告。\n \n共80只雄性NOD.H-2h4小鼠在4周龄时随机分为对照组和碘补充(NaI)组。对照组饲喂普通水,NaI组饲喂0.005%碘化钠溶液。另取24只雄性NOD.H-2h4小鼠随机分为三组(每组8只):对照组、NaI组和碘补充后GL治疗组(NaI+GL)。NOD.H-2h4小鼠饲喂0.005%碘化钠溶液8周以诱导自身免疫性甲状腺炎。碘治疗后,小鼠腹腔注射GL,持续4周。采用组织病理学方法评估甲状腺淋巴细胞浸润的严重程度。采用酶联免疫吸附试验(ELISA)检测血清中HMGB1、肿瘤坏死因子α、白细胞介素(IL)-6、IL-1β和甲状腺球蛋白抗体滴度。采用免疫组织化学染色和实时聚合酶链式反应(RT-PCR)检测HMGB1表达。采用Western blot检测TLR2、HMGB1、MyD88和核转录因子κB的表达。[3] \n1型糖尿病样大鼠模型: \n1. 动物选择:雄性Sprague-Dawley大鼠(200-220 g,n=32)饲养于SPF级动物房(12小时光照/黑暗循环,22±2℃),自由摄食饮水。适应环境1周。 \n2.糖尿病诱导:大鼠禁食12小时后,腹腔注射链脲佐菌素(STZ,60 mg/kg,溶于0.1 M柠檬酸缓冲液,pH 4.5)。正常对照组大鼠仅注射柠檬酸缓冲液。7天后测定空腹血糖;空腹血糖>16.7 mmol/L的大鼠被纳入研究。 \n3. 分组和治疗:将糖尿病大鼠随机分为3组(每组n=8): \n- 糖尿病对照组:每日腹腔注射生理盐水。 \n- 甘草酸组(25 mg/kg):每日腹腔注射甘草酸(25 mg/kg,溶于生理盐水,超声处理使其溶解)。 \n- 甘草酸 50 mg/kg:每日一次腹腔注射甘草酸(50 mg/kg,溶剂相同)。 \n治疗持续时间:21 天。每周测量:体重、空腹血糖。 \n4. 样本采集:第 21 天处死大鼠。采集血清(用于检测 GLP-1、胰岛素、HOMA-IR)、回肠组织(用于 TGR5 qPCR)、肝脏/肾脏(用于 HE 染色)[2] \n- 自身免疫性甲状腺炎 (AIT) 小鼠模型: \n1. 动物选择:雌性 C57BL/6 小鼠(6-8 周龄,n=32)饲养于 SPF 级条件下。适应环境 1 周。 \n2. AIT诱导:小鼠背部两个皮下注射Tg(100 μg/只),Tg乳化于CFA(含4 mg/mL结核分枝杆菌)中。第14天进行加强免疫。正常对照组小鼠仅注射CFA。 \n3. 分组和治疗:第21天(通过抗Tg抗体检测确认AIT),将小鼠随机分为3组(每组n=8): \n- AIT对照组:每隔一天腹腔注射生理盐水。 \n- 甘草酸10 mg/kg组:每隔一天腹腔注射甘草酸(10 mg/kg,溶于生理盐水)。 \n- 甘草酸 20 mg/kg:每隔一天腹腔注射甘草酸(20 mg/kg,溶剂相同)。 \n治疗持续时间:4周。 \n4. 样本采集:第49天,处死小鼠。采集血清(用于抗Tg、T3/T4检测)、甲状腺(用于HE染色、Western blot)、脾脏(用于免疫细胞分析)[3] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
甘草酸主要经首过水解生成甘草次酸后被吸收。因此,口服100 mg甘草酸后,血浆中主要代谢产物甘草次酸的浓度为200 ng/ml,而甘草酸则检测不到。尿液中仅检测到少量甘草酸,提示其在胃肠道存在部分吸收。 甘草酸在中枢室呈双相消除,第二消除相与剂量相关。大部分给药剂量经胆汁排泄,其中甘草酸可以原形排出,并经历肠肝循环。另一方面,主要代谢产物甘草次酸则形成葡萄糖醛酸苷和硫酸盐结合物。这些结合物能高效地转运至胆汁和十二指肠,在那里,共生细菌水解这些结合物,生成甘草次酸,并进一步被重吸收。这种重吸收行为似乎与3α-羟基类固醇脱氢酶的活性有关,该酶能非常有效地将代谢物从血浆转运至胆汁。约1.1-2.5%的给药剂量甘草酸可在尿液中检测到,这表明该化合物的循环和重吸收量极低。 甘草酸在中心室和稳态下的表观分布容积分别为37-64 ml/kg和59-98 ml/kg。 甘草次酸在十二指肠的持续重吸收导致其终末血浆清除率延迟。据报道,甘草酸的全身清除率在 16-25 ml·kg/h 范围内。 甘草酸在大鼠小肠内被吸收;门静脉快速注射甘草酸后,血液中未检测到甘草次酸;口服后,血液中可检测到甘草次酸。 高效液相色谱法 (HPLC) 可快速、精确地测定实验动物和人体体液及组织中的甘草酸 (GZA) 和甘草次酸 (GRA)。从血浆和组织中,用有机溶剂提取甘草酸和甘草次酸,提取物可直接用于 HPLC 分析。由于内源性化合物的干扰以及甘草次酸与葡萄糖醛酸苷或硫酸盐的结合,从胆汁或尿液中提取和测定甘草酸和甘草次酸较为困难。从尿液或胆汁中提取甘草酸和甘草次酸的方法包括离子对结合后用有机溶剂萃取或固相萃取。甘草次酸结合物可通过色谱分离或β-葡萄糖醛酸酶预处理进行测定。甘草次酸和甘草酸的药代动力学可以用双相消除模型来描述,其消除过程从中心室开始,并具有剂量依赖性的第二消除相。根据剂量不同,甘草酸在人体内的第二消除相半衰期为3.5小时,而甘草次酸的半衰期为10-30小时。甘草次酸和甘草酸的大部分均经胆汁排泄。甘草酸可以未经代谢直接排出,并经历肠肝循环;而甘草次酸在经胆汁排泄前,会与甘草次酸葡萄糖醛酸苷或硫酸盐结合。口服的甘草酸几乎完全被肠道细菌水解,并以甘草次酸的形式进入体循环。甘草酸目前在治疗慢性肝炎方面具有临床应用价值。它也被用作食品和嚼烟中的甜味剂。在一些高暴露人群中,曾报道出现高血压和电解质紊乱等严重副作用。为了分析暴露于该化合物的健康风险,本研究对甘草酸及其活性代谢物的动力学进行了定量评估。甘草酸及其代谢产物受复杂的动力学过程影响,包括肠肝循环和首过代谢。在人体中,这些过程的详细信息通常难以获得。因此,我们建立了一个模型,用于描述甘草酸及其活性代谢产物甘草次酸在大鼠体内的全身和胃肠道动力学。由于该模型基于生理学结构,因此可以直接整合先前关于吸收、肠肝循环和首过代谢的体外和体内研究数据。该模型表明,甘草酸及其代谢产物能够有效地从血浆转运至胆汁,这可能与肝脏转运蛋白3α-羟基类固醇脱氢酶有关。甘草次酸被重新吸收后,其经胆汁排泄的代谢产物发生细菌水解,导致观察到的甘草次酸血浆末端清除延迟。这些机制性发现源于对实验数据的分析,并通过基于生理的药代动力学模型进行建模,最终可用于对人类暴露于含甘草酸产品的健康风险进行定量评估。版权所有 2000 Academic Press。 为了评估异生物质结合物胆汁排泄的多样性,本研究在大鼠中对甘草酸(甘草甜素)进行了研究。大鼠静脉注射10 mg/kg甘草酸,并同时静脉输注抑制剂二溴磺酞和吲哚菁绿。吲哚菁绿不影响甘草酸的胆汁排泄,而二溴磺酞则显著降低了其排泄。二溴磺酞可提高血浆中甘草酸的浓度,而吲哚菁绿则无此作用。在Eisai高胆红素血症大鼠中,甘草酸的胆汁排泄严重受损,导致血浆浓度升高。研究结果表明,甘草酸的胆汁排泄是由甘草苷元葡萄糖醛酸苷和二溴磺酞钠共有的系统介导的,而非吲哚菁绿介导的,并且该系统在Eisai高胆红素血症大鼠中存在遗传缺陷。 代谢/代谢物 口服后,甘草酸几乎完全被肠道细菌水解,生成活性代谢物甘草次酸(可进入体循环)和两分子葡萄糖醛酸。该代谢物被运输到肝脏并被吸收,在那里代谢形成葡萄糖醛酸苷和硫酸盐结合物。 向大鼠门静脉快速注射甘草酸后,血液中某种物质的水平升高,该物质似乎是甘草次酸代谢形成的葡萄糖醛酸结合物。 生物半衰期 根据剂量不同,人体第二消除相的半衰期为3.5小时。 |
| 毒性/毒理 (Toxicokinetics/TK) |
孕期及哺乳期影响
◉ 哺乳期使用概述 甘草(Glycyrrhiza glabra)根含有甘草酸(也称甘草酸或甘草酸根苷)以及甘草酸钾盐和钙盐的混合物。甘草酸在肠道内代谢为活性成分甘草次酸。脱甘草酸甘草(DGL)已去除甘草酸。甘草被认为是一种催乳剂,一些亚洲的专有配方中也含有甘草以增加乳汁分泌;然而,目前尚无科学有效的临床试验支持这种用途。事实上,甘草通常会降低血清催乳素水平,这可能会在哺乳初期减少乳汁分泌。服用甘草的女性可能会出现血压升高的情况。催乳剂绝不能取代对影响乳汁分泌的可控因素的评估和咨询。据报道,土耳其的一些母亲使用甘草来改善乳汁的口感和质量。 在一些服用甘草的女性的母乳中可以检测到甘草酸,但尚未进行测量甘草次酸的研究。甘草与其他草药混合制成茶饮,用于短期治疗婴儿肠绞痛,安全有效。然而,有两名婴儿的母亲过量饮用含有甘草的草药茶,导致婴儿出现茴香脑中毒症状。由于这两篇论文均报道了草药混合物,因此无法确定单独使用甘草的效果。美国食品药品监督管理局(FDA)将甘草和甘草提取物列为“一般公认安全”(GRAS)的食品。长期过量食用甘草会导致高血压、低钾血症和肾上腺激素紊乱,因此哺乳期妇女应避免食用。膳食补充剂无需获得美国食品药品监督管理局 (FDA) 的广泛上市前批准。制造商有责任确保产品安全,但无需在上市前证明膳食补充剂的安全性和有效性。膳食补充剂可能含有多种成分,标签所示成分与实际成分或含量往往存在差异。制造商可以委托独立机构验证产品或其成分的质量,但这并不代表产品安全有效。鉴于上述问题,针对某一产品的临床试验结果可能并不适用于其他产品。关于膳食补充剂的更多详细信息,请访问 LactMed 网站的其他页面。 ◉ 对母乳喂养婴儿的影响 两名分别为 15 天和 20 天大的母乳喂养婴儿因过去 7 至 10 天体重增长不足入院,据称原因是“喂养困难”。父母报告称,婴儿在过去一天出现烦躁不安和呕吐。其中一位母亲还报告感到困倦和虚弱。检查发现,婴儿无发热,但肌张力低下、嗜睡、呕吐、哭声微弱、吸吮力差,对疼痛刺激反应迟钝。婴儿的实验室检查结果、心电图和血压均正常,败血症检查结果为阴性。两位母亲每天饮用超过 2 升的草药茶混合物,据称其中含有甘草、茴香、八角和山羊豆,以刺激泌乳。母亲停止母乳喂养和饮用草药茶后,婴儿的症状在24至36小时内有所改善。受影响的母亲在停止饮用草药茶后,症状也迅速缓解。两天后,恢复母乳喂养,婴儿未再出现任何症状。两个婴儿在6个月大时健康状况良好。作者将母亲和婴儿的症状归因于茴香脑,茴香脑存在于茴芹和小茴香中;然而,他们并未检测母乳中的茴香脑含量,也未检测草药茶中的茴香脑含量。 ◉ 对泌乳和母乳的影响 一位有长期过量摄入甘草史的女性出现闭经、严重头痛、高血压和低钾血症。她的血清催乳素水平升高,停用甘草后一个月内仍异常,停用6个月后恢复正常。 在一项纳入25名男性和25名女性的研究中,研究人员测量了基础血清催乳素水平和促甲状腺激素刺激后的血清催乳素水平,以确定正常血清催乳素值。经常食用甘草的受试者基础血清催乳素浓度和刺激后血清催乳素浓度均较低。 一项研究对长期(>6个月)服用利培酮导致血清催乳素水平升高的女性患者,使用了一种名为芍药甘草汤(中文)和芍药甘草汤(日文)的传统非标准化牡丹甘草汤进行研究。患者接受两种治疗方案:一种是每日服用5毫克溴隐亭,持续4周;另一种是每日服用22.5克牡丹甘草煎剂(相当于25毫克甘草次酸),持续4周;另一种是先服用上述两种药物,后服用顺序相反。血清催乳素水平评估结果显示,两种治疗方案均使患者在治疗4周和8周时血清催乳素水平较基线降低21%至28%。 40名产后5天主诉乳汁不足的妇女接受了复方草药补充剂治疗,每日3次,每次2粒Lactare胶囊(印度马德拉斯Pharma Private Ltd.公司生产;目前由印度钦奈TTK Pharma公司销售)。每粒胶囊含有野生芦笋200毫克、南非醉茄(Withania somnifera)100毫克、胡芦巴50毫克、甘草50毫克和大蒜20毫克。治疗第4天,所有婴儿均无需补充喂养。在母亲接受治疗的第5天,每次喂奶前后均对婴儿进行称重,以确定其摄入的奶量。在测试称重当天,婴儿的平均奶量为388毫升,液体和热量摄入量均被认为充足。由于本研究缺乏随机化、双盲、安慰剂对照以及对母亲进行母乳喂养技巧指导,因此不能被视为这些草药具有催乳作用的有效证据。此外,婴儿每天仅哺乳6至8次,这不足以在哺乳的这个阶段最大限度地增加乳汁供应。 产后14至90天且报告泌乳失败的妇女接受了母乳喂养技巧指导,并被鼓励进行纯母乳喂养。如果她们的婴儿在1周内体重增加不足15克,则随机分配接受两汤匙含有野生芦笋的混合物或相同的安慰剂,持续4周。每100克混合物包含:天门冬15克、莳萝1克、番薯1克、甘草1克、菠菜2.5克、孜然0.5克和泛醇1克。64名随机分组的女性中,11名未完成试验。在治疗前和治疗4周后,于晨间哺乳前测量血清催乳素水平。记录婴儿体重增长和补充喂养次数,并在治疗初期和治疗4周后再次记录。治疗4周后,治疗组和安慰剂组在血清催乳素变化、婴儿体重增长或补充喂养次数方面均无差异。研究期间未出现任何副作用或肝功能检查异常。 日本一项研究比较了由13种草药(包括甘草)组成的混合物与麦角新碱对产后妇女泌乳和血清催乳素水平的影响。该草药混合物名为“雄桂条血饮”,随机分配给41名妇女,剂量为每日3次,每次2克干燥水提取物。另有41名妇女随机分配接受每日0.375毫克麦角新碱治疗。治疗从分娩当天开始,但未明确治疗持续时间。分别于第1天和第6天测量血浆催产素和催乳素水平;每日测量乳汁量,但未明确测量方法。服用草药的妇女在第1天和第6天的血清催乳素水平高于服用麦角新碱的妇女;服用草药组女性在第1天血浆催产素水平较低,但在第6天两组间无差异。服用草药组女性在第4、5和6天的乳汁量均高于对照组。然而,这项研究存在严重的缺陷,导致其结果无法解释。首先,乳汁量的测量结果会因测量方法的不同而存在相当大的差异,但该研究并未具体说明所采用的测量方法。其次,一些研究表明,麦角新碱会导致血清催乳素水平和乳汁分泌量下降。由于缺乏安慰剂组,因此所观察到的差异可能是麦角新碱的负面影响,而非草药制剂的正面作用。由于本研究使用的是多种成分的复方制剂,其中甘草只是其中一种成分,因此研究结果可能与单独使用甘草的研究结果有所不同。 在印度一项非对照、非盲的多中心研究中,1132名自述母乳不足的患者服用了一种复方制剂(Lactancia,Corona Remedies Pvt. Ltd.),每次30克,每日两次。该产品含有天门冬(野生芦笋、沙塔瓦里)、孜然、甘草、菠菜以及氨基酸、维生素、矿物质和DHA。大多数母亲(1049名)的泌乳情况得到改善,婴儿体重也有所增加。然而,由于没有安慰剂对照组,结果不能归因于该产品。 蛋白质结合 甘草酸不与任何血浆蛋白结合,因为它不被全身吸收。另一方面,其主要活性代谢物甘草次酸与血清蛋白(如白蛋白)的结合力非常强。 体外毒性: - 正常细胞:甘草酸(浓度高达 50 μM)对 LO2(正常肝细胞)和 CCD-841(正常结肠细胞)的存活率 >85%(MTT 法,72 小时)[1];甘草酸水凝胶(浓度高达 5 mg/mL)对 L929 成纤维细胞的存活率 >90% [4] - 无遗传毒性:Ames 试验结果为阴性(50-500 μM 甘草酸)[3] - 体内毒性: - 糖尿病大鼠:50 mg/kg 甘草酸(21 天)未引起体重减轻(220 ± 15 g vs. 糖尿病对照组 215 ± 12 g)或器官损伤(肝/肾 HE 染色:无坏死/炎症;血清 ALT:30 ± 4 U/L vs. 对照组 32 ± 5 U/L;BUN:15 ± 2 mg/dL vs. 16 ± 2 mg/dL)[2] - AIT 小鼠: 20 mg/kg 甘草酸(4 周)对血清皮质醇(180 ± 20 ng/mL vs. 正常值 175 ± 15 ng/mL)或电解质平衡(K⁺:4.5 ± 0.3 mmol/L vs. 4.6 ± 0.2 mmol/L)无影响 [3] |
| 参考文献 |
|
| 其他信息 |
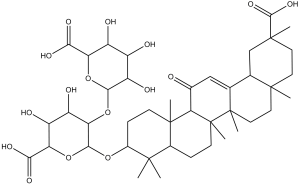
甘草酸是一种三萜皂苷,是3β-羟基-11-氧代油酸-12-烯-30-酸的葡萄糖醛酸衍生物。它是一种EC 3.4.21.5(凝血酶)抑制剂和植物代谢产物。它是一种葡萄糖醛酸、三羧酸、五环三萜、烯酮和三萜皂苷。它是甘草酸(3-)的共轭酸。
甘草酸提取自甘草(Glycyrrhiza glabra)的根。它是一种三萜糖苷,含有甘草次酸,具有广泛的药理和生物活性。从植物中提取后,它可以以甘草酸铵和单铵甘草酸的形式获得。甘草酸在日本和中国被开发为治疗慢性肝炎的保肝药物。自2014年1月起,甘草酸作为甘草提取物的一部分,被美国食品药品监督管理局(FDA)批准为食品甜味剂。加拿大卫生部也曾批准其用于非处方产品,但目前所有相关产品均已停产。 据报道,甘草酸存在于山毛榉(Hypomontagnella monticulosa)、白花甘草(Glycyrrhiza pallidiflora)以及其他有相关数据的生物体中。 甘草甜素是一种皂苷类化合物,赋予光果甘草(Glycyrrhiza glabra)主要甜味,并具有潜在的免疫调节、抗炎、保肝、神经保护和抗肿瘤活性。甘草酸能调节某些参与炎症和氧化应激的酶,并下调某些促炎介质,从而保护机体免受炎症和活性氧(ROS)引起的损伤。甘草酸还可能抑制易感肿瘤细胞的生长。 甘草酸是酿酒酵母(Saccharomyces cerevisiae)中发现或产生的代谢产物。 它是一种广泛使用的抗炎剂,从甘草根中分离得到。甘草酸代谢为甘草次酸,后者抑制11β-羟基甾醇脱氢酶和其他参与皮质类固醇代谢的酶。因此,甘草酸(甘草的主要甜味成分)因其引起高盐皮质激素血症(伴钠潴留和钾流失)、水肿、血压升高以及肾素-血管紧张素-醛固酮系统抑制的能力而受到研究。 另见:依诺酮(含有活性成分);甘草酸二钾(活性成分);甘草根(部分)……查看更多…… 药物适应症 甘草酸作为一种天然甜味剂广泛应用于食品中。作为一种治疗剂,它已被用于多种制剂中,据报道具有抗炎、抗溃疡、抗过敏、抗氧化、抗肿瘤、抗糖尿病和保肝作用。由于其特性,甘草酸的适应症包括:治疗经前综合征、病毒感染、降血脂和降血糖。它也被用于治疗消化性溃疡和其他胃部疾病。 作用机制 甘草酸以α和β两种形式存在。α形式主要存在于肝脏和十二指肠中,因此,人们认为该药物的抗炎肝脏作用主要归因于这种异构体的作用。甘草酸的抗炎作用是通过抑制TNF-α和caspase-3实现的。它还能抑制NF-κB转位到细胞核内并清除自由基。一些研究表明,甘草酸可通过JNK、ERK和PI3K/AKT通路抑制CD4+ T细胞增殖。甘草酸的抗病毒活性包括抑制病毒复制和免疫调节。甘草酸的抗病毒活性似乎具有广谱性,能够覆盖多种不同类型的病毒,例如牛痘病毒、单纯疱疹病毒、新城疫病毒和水疱性口炎病毒。甘草酸对代谢的影响被认为与其对11β-羟基类固醇脱氢酶1型的抑制活性有关,而11β-羟基类固醇脱氢酶1型反过来又会降低己糖-6-磷酸脱氢酶的活性。另一方面,一些研究表明,甘草酸及其衍生物可能诱导非肝脏组织中的脂蛋白脂肪酶活性,因此被认为可以改善血脂异常。 甘草酸及其衍生物表现出显著的抗炎作用,可抑制组胺、5-羟色胺、缓激肽和甲醛诱导的水肿,并降低血管通透性。 药物递送系统如今已成为抗癌药物的重要组成部分。新型药物载体的设计有望显著提高抗肿瘤治疗的效果。甘草酸(GL)是从甘草根中提取的最重要活性成分,在该领域作为载体材料展现出巨大的潜力。近期研究表明,甘草酸与一线药物联合使用对癌症具有更好的治疗效果。甘草酸(GL)作为药物递送系统的载体材料,展现出一系列抗癌相关的药理活性,例如广谱抗癌能力、抵抗化疗和放疗引起的组织毒性、增强药物吸收以及抗多药耐药(MDR)机制。本文综述了甘草酸药理机制的研究进展以及基于甘草酸的抗癌药物载体的开发,为甘草酸的应用前景提供了依据。新型甘草酸药物递送系统的设计将为抗癌治疗带来新的机遇和挑战。[1] 甘草酸(GA)属于三萜皂苷类化合物,存在于甘草根中,已知具有影响代谢调节的作用。近年来,胰高血糖素样肽-1(GLP-1)已被广泛应用于糖尿病治疗。然而,GLP-1在甘草酸诱导的抗糖尿病作用中的具体机制尚不清楚。因此,我们感兴趣的是了解GLP-1与GA诱导效应之间的关联。在链脲佐菌素(STZ)诱导的1型糖尿病大鼠模型中,GA可提高血浆GLP-1水平,而三氨蝶呤可在足以抑制Takeda G蛋白偶联受体5(TGR5)的剂量下阻断这一作用。利用转染TGR5基因的培养的中国仓鼠卵巢细胞(CHO-K1细胞)已证实GA对TGR5的直接作用。此外,在分泌GLP-1的肠道NCI-H716细胞中,GA可促进GLP-1分泌并显著升高钙离子水平。然而,在NCI-H716细胞中利用siRNA敲除TGR5后,GA的上述两种作用均减弱。因此,我们证实了GA可通过激活TGR5增强GLP-1的分泌。[2] 综上所述,我们首次证实GA可通过激活TGR5提高1型糖尿病大鼠的血浆GLP-1水平。因此,GA未来可能具有临床应用价值。[2] 高迁移率族蛋白B1 (HMGB1) 是一种非组蛋白,在自身免疫性疾病中发挥重要作用。然而,HMGB1在自身免疫性甲状腺炎发病机制中的意义尚未见报道。本研究旨在探讨HMGB1是否参与自身免疫性甲状腺炎的发病机制,以及HMGB1的直接抑制剂甘草酸(GL)是否能减轻自身免疫性甲状腺炎小鼠模型中甲状腺炎症浸润的严重程度。[3] 可注射的低分子量水凝胶(LMWH)由生物相容性材料制成,因其可制成任意尺寸和腔体形状,在生物医学应用领域备受关注。寻找无需复杂化学修饰即可具有固有抗菌活性的、结构简单、生物相容性良好的可注射LMWH,以避免繁琐的合成/纯化过程以及水凝胶在潮湿环境中易受细菌感染的问题,仍然是一个亟待解决的问题。本研究发现,天然化合物甘草酸(GL)在37℃的生理磷酸盐缓冲液(PBS)中可形成稳定的透明LMWH,其微结构为纳米团簇。此外,该水凝胶展现出优异的注射性和可塑性。抗菌研究表明,GL能够完全抑制革兰氏阳性金黄色葡萄球菌(S. aureus)的生长,而对革兰氏阴性大肠杆菌(E. coli)无抑制作用。此外,细胞活力和溶血试验表明,由于其天然来源,GL对哺乳动物细胞具有良好的生物相容性和血液相容性。我们制备的这种具有天然抗菌能力的、结构简单、生物相容性好、可注射、可塑性强的低分子肝素(LMWH)在生物材料和3D生物打印领域具有应用潜力。 总之,我们利用天然甘草酸作为凝胶剂,在生理PBS缓冲液中于37℃下构建了一种稳定的LMWH,无需额外的化学修饰。这种纳米团簇结构的LMWH展现出优异的注射性和可塑性。此外,与革兰氏阴性大肠杆菌相比,GL能完全抑制革兰氏阳性金黄色葡萄球菌的生长。另外,细胞活力和溶血试验表明,由于GL的天然来源,其对哺乳动物细胞具有较低的细胞毒性和良好的血液相容性。我们的研究提供了一种简单、生物相容性好、可注射、可塑性强的低分子肝素(LMWH),它具有固有的抗菌能力,将在生物材料和3D生物打印领域引起广泛关注。[4] 甘草酸(甘草酸)是从光果甘草(甘草根)中提取的一种三萜皂苷,具有多种生物活性,包括抗炎、免疫调节和作为药物载体的潜力。[1][2][3][4] - 药物载体优势:甘草酸具有固有的肿瘤靶向特性(通过肝癌细胞上的ASGPR受体)和pH敏感释放,可在提高抗癌药物疗效的同时降低脱靶毒性。[1] - TGR5介导的代谢调节:甘草酸激活肠道TGR5,促进GLP-1分泌,这是一种治疗1型糖尿病的新机制(可作为胰岛素替代疗法的补充)。增强胰岛素敏感性)[2] - HMGB1拮抗作用:甘草酸直接与HMGB1结合,阻断TLR2-MyD88信号通路,从而减轻自身免疫性炎症,且不损害靶器官功能(例如甲状腺激素合成),使其适用于自身免疫性疾病[3] - 抗菌机制:甘草酸水凝胶通过与脂质双层相互作用破坏细菌细胞膜,而非抑制酶活性,从而降低细菌耐药风险[4] |
| 分子式 |
C42H62O16
|
|
|---|---|---|
| 分子量 |
822.93
|
|
| 精确质量 |
822.403
|
|
| 元素分析 |
C, 61.30; H, 7.59; O, 31.11
|
|
| CAS号 |
1405-86-3
|
|
| 相关CAS号 |
Ammonium glycyrrhizinate;53956-04-0;Dipotassium glycyrrhizinate;68797-35-3
|
|
| PubChem CID |
14982
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| 密度 |
1.4±0.1 g/cm3
|
|
| 沸点 |
971.4±65.0 °C at 760 mmHg
|
|
| 熔点 |
220ºC decomposes
|
|
| 闪点 |
288.1±27.8 °C
|
|
| 蒸汽压 |
0.0±0.6 mmHg at 25°C
|
|
| 折射率 |
1.621
|
|
| LogP |
4.64
|
|
| tPSA |
267.04
|
|
| 氢键供体(HBD)数目 |
8
|
|
| 氢键受体(HBA)数目 |
16
|
|
| 可旋转键数目(RBC) |
7
|
|
| 重原子数目 |
58
|
|
| 分子复杂度/Complexity |
1730
|
|
| 定义原子立体中心数目 |
19
|
|
| SMILES |
C[C@]12CC[C@](C[C@H]1C3=CC(=O)[C@@H]4[C@]5(CC[C@@H](C([C@@H]5CC[C@]4([C@@]3(CC2)C)C)(C)C)O[C@@H]6[C@@H]([C@H]([C@@H]([C@H](O6)C(=O)O)O)O)O[C@H]7[C@@H]([C@H]([C@@H]([C@H](O7)C(=O)O)O)O)O)C)(C)C(=O)O
|
|
| InChi Key |
LPLVUJXQOOQHMX-QWBHMCJMSA-N
|
|
| InChi Code |
InChI=1S/C42H62O16/c1-37(2)21-8-11-42(7)31(20(43)16-18-19-17-39(4,36(53)54)13-12-38(19,3)14-15-41(18,42)6)40(21,5)10-9-22(37)55-35-30(26(47)25(46)29(57-35)33(51)52)58-34-27(48)23(44)24(45)28(56-34)32(49)50/h16,19,21-31,34-35,44-48H,8-15,17H2,1-7H3,(H,49,50)(H,51,52)(H,53,54)/t19-,21-,22-,23-,24-,25-,26-,27+,28-,29-,30+,31+,34-,35-,38+,39-,40-,41+,42+/m0/s1
|
|
| 化学名 |
(2S,3S,4S,5R,6R)-6-[(2S,3R,4S,5S,6S)-2-[[(3S,4aR,6aR,6bS,8aS,11S,12aR,14aR,14bS)-11-carboxy-4,4,6a,6b,8a,11,14b-heptamethyl-14-oxo-2,3,4a,5,6,7,8,9,10,12,12a,14a-dodecahydro-1H-picen-3-yl]oxy]-6-carboxy-4,5-dihydroxyoxan-3-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 本产品在运输和储存过程中需避光。 |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (3.04 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (3.04 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (3.04 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.2152 mL | 6.0759 mL | 12.1517 mL | |
| 5 mM | 0.2430 mL | 1.2152 mL | 2.4303 mL | |
| 10 mM | 0.1215 mL | 0.6076 mL | 1.2152 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT04028869 | Completed | Drug: Glycyrrhizic acid preparation | Autoimmune Liver Disease | Beijing Ditan Hospital | March 1, 2018 | |
| NCT04742660 | Completed | Drug: Ammonium Glycyrrhizinate | Postoperative Nausea | Konkuk University Medical Center | May 11, 2021 | Not Applicable |
| NCT05895773 | Completed | Drug: Povidone-Iodine Drug: Saline spray |
Ventilator Associated Pneumonia | Menoufia University | June 24, 2023 | Phase 2 Phase 3 |
| NCT05788705 | Not yet recruiting | Dietary Supplement: "apigenin" and "glycyrrhizin" |
Rheumatoid Arthritis | Adel A.Gomaa | July 2023 | Not Applicable |