| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
HIV-1 capsid
|
|---|---|
| 体外研究 (In Vitro) |
Lenacapavir 干扰 HIV-1 复制的早期和晚期阶段,但针对早期阶段更有效 [2]。 Lenacapavi (GS-6207) 是一种有效的 HIV 复制衣壳抑制剂。 Lenacapavi 在靶细胞 (EC50=23 pM)、全周期测定 (EC50=25 pM) 和生产细胞 (EC50=439 PM) 中表现良好。
在体外,LEN对SHIV表现出强大的抗病毒活性,就像对HIV-1一样。在猕猴中,单次皮下给药LEN显示出药物血浆水平的剂量比例增加和持久性。[3] |
| 体内研究 (In Vivo) |
通过病毒滴定在未经处理的猕猴中鉴定用于PrEP疗效评估的高剂量SHIV接种物。LEN治疗的猕猴在给药7周后接受高剂量SHIV攻击,血浆PCR、细胞相关前病毒DNA和血清学检测证实,大多数猕猴仍能免受感染。在激发时LEN血浆暴露量超过其模型调整的临床疗效目标的动物中,观察到完全保护和优于未治疗组。所有受感染的动物都具有亚保护性LEN浓度,并且没有表现出突发耐药性。这些数据证明了在临床相关LEN暴露的严格猕猴模型中有效预防SHIV,并支持LEN对人类HIV PrEP的临床评估。[3]
|
| 酶活实验 |
微尺度热电泳分析[1]
CA与Pep-1和PF74的结合亲和力是通过在Pep-1或PF74浓度增加的情况下测量荧光标记的CA六聚体的热泳来测定的。肽Pep-1是在分子相互作用核心中合成的,PF74是商业购买的。根据制造商的说明书(MO-L004 Monolith Protein labeling Kit),用Alexa Fluor 647类似物NT647对CA进行荧光标记。简言之,将20μM蛋白质与3M过量染料在室温下在标记试剂盒提供的缀合缓冲液中孵育过夜。通过与试剂盒一起提供的重力流柱过滤除去未反应的染料。将洗脱组分收集在2×MST缓冲液(40mM MOPS,pH 7.2,200mM NaCl和0.2%pluronic F-127)中。通过MST评估每个级分的荧光强度,并合并含有标记蛋白的级分。通过NanoDrop分光光度计测定蛋白质浓度。等分试样在使用前储存在−80°C下。将含有200 nM标记的CA六聚体和不断增加的Pep-1浓度(1–2000 nM)的反应混合物加载到毛细管中,并在20%LED功率、高MST功率和20 s MST准时下监测热泳。 体外HIV-1 CA组装测定。[2] 在存在和不存在小分子文库化合物(10μM)或2倍连续稀释的GS-6207的情况下,通过在350nm处测量样品吸光度随时间的变化来监测HIV-1 CA蛋白的体外组装。最终组装反应包含20μM CA、2M NaCl、50mM磷酸钠(pH 7.5)、0.005%消泡剂204(Sigma-Aldrich)和1%二甲基亚砜。在25°C下,使用M5读板器在96孔板或384孔板中监测350 nm处的样品吸光度值,在没有CA或NaCl的情况下校正吸光度值,并使用SoftMax Pro 6.3.1分析数据,如前所述38。 GS-6207结合测定。[2] 使用ProteOn XPR36平台(CA六聚体和五聚体蛋白)或Biacore T100平台(CA单体和Gag蛋白)进行表面等离子体共振生物传感器结合实验,如前所述21。数据使用ProteOn Manager 3.1.0或Scrubber 2.0进行分析,并符合一个简单的动力学模型,必要时添加了质量传输术语。 |
| 细胞实验 |
细胞毒性测定。[2]
对于MT-4细胞、PBMC、原代人CD4+T细胞和单核细胞衍生的巨噬细胞的细胞毒性评估,该方案与各自的抗病毒试验的方案相同,包括试验持续时间,只是没有向平板中添加病毒。先前已经描述了Huh-7、Gal-HepG2、Gal-PC-3和MRC-5细胞系以及原代人类肝细胞中的细胞毒性评估方案37。使用CellTiter Glo测量测试化合物对细胞活力的影响。使用GraphPad Prism 7.0进行数据分析以计算CC50值。 GS-6207电阻分析。[2] 如前所述,在感染HIV-1HXB2D的MT-2细胞中使用GS-6207浓度的两倍增量增加进行耐药HIV-1变体的剂量递增选择31。在滴定病毒接种物以使所有样本的m.o.i.正常化后,在5天的细胞保护抗病毒MT-2测定中评估每个新出现的病毒传代的抗性谱。如前所述,在固定、恒定药物浓度的条件下,在独立感染六种不同HIV-1分离株(BaL、92US657、91US0006、7406、7467和7576)的人PBMC中进行为期35天的病毒突破性选择21。在固定药物浓度下测试GS-6207,该固定药物浓度等于其0.23 nM的EC95值的4倍、8倍和16倍(分别为0.92 nM、1.9 nM和3.7 nM GS-6207),每个实验条件使用6个重复细胞培养物。在GS-6207存在的情况下出现的病毒通过群体测序进行基因分型。使用QiaAMP病毒RNA迷你试剂盒从模拟和GS-6207-选择的含病毒上清液中分离总RNA。使用Qiagen OneStep RT-PCR试剂盒与引物5’-CCAGTAGCAACCCTCTATTGTGC-3’和5’-CCCTAGGGCCCTCTAATT-3’组合,通过RT-PCR扩增编码HIV-1衣壳和相邻p2间隔肽的986bp片段。RT-PCR产物由Elim Biopharmaceuticals进行测序。为了鉴定密码子的变化,使用DNA Sequencer 4.9软件将所选HIV-1变体的基因序列与输入病毒和在没有GS-6207的情况下传代的病毒的基因序列进行比对。对于含有>1个密码子变化的样本,对PCR产物进行亚克隆,从单个菌落中分离DNA,并对CA基因进行测序,以评估所有观察到的取代的连锁。 |
| 动物实验 |
药物和制剂。[3]
\nLEN 和液相色谱-质谱内标 GS-224337 均为内部合成,并经过标准质量控制分析。抗病毒活性测定中,LEN 溶于 DMSO 中,配制成 10 mM 的储备液,并于 -0°C 冷冻保存。动物给药研究中,LEN 溶于赋形剂(58.03% 聚乙二醇 300、27.1% 水、6.78% 乙醇、6.61% 泊洛沙姆 188、1.48% 氢氧化钠)中,配制成 300 mg/mL 的溶液,于室温避光保存,直至给药。该制剂添加了临床制剂中未包含的赋形剂,以调整其在猕猴体内的药代动力学特征。 \n\n动物研究。[3] \n所有动物均饲养于Bioqual公司。在体内SHIV病毒滴度研究中,8只未经治疗的3-5岁印度雄性恒河猴(非近交系)接受了直肠内病毒攻击,共进行5轮攻击,病毒剂量从0.625到100 TCID50递增,其中100 TCID50的攻击重复两次以提高灵敏度(补充表2)。通过测量血浆病毒载量来确认感染状态。为了确定来那度胺(LEN)的药代动力学和暴露前预防(PrEP)的有效性,20只3-5岁的印度雄性恒河猴(非近交系)被随机分配到5个研究组,各组体重分布均匀(补充表2)。在研究第0周,每组4只动物分别在肩胛区域皮下注射5、10、20、50或75 mg/kg的来那度胺(LEN)。LEN配制成300 mg/mL的储备液,每次皮下注射不超过2 mL。兽医人员每天监测注射部位,持续2周,之后每周监测一次,直至研究结束。在第7周,11只动物经直肠途径接种1 mL含有100 TCID50 SHIV-SF162P3的RPMI培养基进行病毒攻击。采集全血,并根据需要制备血浆和外周血单核细胞(PBMC),用于常规血液学和临床化学分析、病毒载量分析、血清学分析以及药物浓度生物分析。如果动物在攻毒后 10 周内通过血浆 PCR 检测仍为 SHIV 阴性,并通过酶免疫测定仍为血清阴性,则认为该动物受到保护。\n\n在病毒滴度测定和 PrEP 疗效研究中均被确认为 SHIV 阳性的动物,在感染后 4 周至 10 周期间接受每日皮下注射抗逆转录病毒疗法,以防止艾滋病病情进展。配制的抗逆转录病毒疗法(ART)鸡尾酒疗法包含富马酸替诺福韦酯(5.1 mg/mL)、恩曲他滨(40 mg/mL)和多替拉韦(2.5 mg/mL),每日一次皮下注射,剂量为1 mL/kg。 \n\n\n\n \n \n\n查看更多\n\n猕猴血浆中来那度胺的生物分析。[3] \n\n血浆病毒载量检测。[3] \n使用QIAsymphony SP(Qiagen)自动化样品制备平台、Virus/Pathogen DSP midi试剂盒和cellfree500方案从500 μL血浆中提取病毒RNA。将针对SIVmac251 gag基因的反向引物(5′-CACTAGGTGTCTCTGCACTATCTGTTTTG-3′)与提取的RNA退火,然后使用SuperScript III逆转录酶和RNA酶抑制剂(Thermo Fisher Scientific)将其逆转录为cDNA。将所得 cDNA 用 RNase H(Thermo Fisher Scientific)处理,然后加入(2 个重复)定制的 4× TaqMan 基因表达预混液(Thermo Fisher Scientific),该预混液包含针对 SIVmac251 gag 基因的引物和荧光标记的水解探针(正向引物 5′-GTCTGCGTCATCTGGTGCATTC-3′,反向引物 5′-CACTAGGTGTCTCTGCACTATCTGTTTTG-3′,探针 5′-/56-FAM/CTTCCTCAGTGTGTTTCACTTTCTCTTCTGCG/3BHQ_1/-3′)。随后在 QuantStudio 3 实时荧光定量 PCR 系统(Thermo Fisher Scientific)上进行 qPCR。利用定量循环数据和包含 SIV gag 基因 730 bp 序列的、高度表征的定制 RNA 转录本的系列稀释液,插值计算每个反应中 SIV gag RNA 的平均拷贝数。检测的定量限约为每毫升样本中 62 个 RNA 拷贝。 \n\nELISA。[3] \n使用 Bio-Rad 公司的 GS HIV-1/HIV-2 PLUS O EIA 试剂盒,通过 ELISA 检测病毒血症研究动物的恒河猴血清样本中是否存在抗 HIV-1 抗体。将 150 μL 恒河猴血清与试剂盒提供的 50 μL 样本稀释液混合,加入预先包被有重组纯化 HIV-1 衣壳蛋白 (p24) 和跨膜糖蛋白 (gp160) 的检测板中,并在室温下孵育 1 小时。然后用试剂盒中含有氯化钠和 Tween 20 的洗涤缓冲液洗涤 3 次,再用含有模拟 HIV-1 gp160 和 p24 蛋白各种免疫优势表位的肽段的 HRP 标记抗原溶液孵育 1 小时。含有抗 HIV-1 抗体的孔与包被抗原的孔板以及结合溶液中的过氧化物酶标记抗原结合,形成固定的稳定抗原-抗体-抗原复合物。用上述洗涤缓冲液洗涤孔板 3 次,用四甲基联苯胺工作液显色,加入 1 N 硫酸终止反应,并使用 Versamax 微孔板读数仪和 Softmax Pro 6.5.1 软件在 450 nm 波长处进行分析。OD450 nm 吸光度值大于 0.2 的样本被判定为阳性。 \n\nIPDA。[3] \n使用 SHIV 适应性 IPDA 法 (SHIV-IPDA) 测定完整 SHIV 前病毒的数量。使用 QIAamp DNA Mini 试剂盒从未分选的 PBMC 中提取总基因组 DNA。分别通过分光光度法和荧光法评估 DNA 的质量和数量,然后对分离的 DNA 进行 SHIV-IPDA 分析。简而言之,SHIV-IPDA 包含一个三组分的多重液滴数字 PCR (ddPCR) 反应。第一组分是 SHIV 前病毒鉴别反应,靶向 SHIV 基因组中两个保守且易缺失的区域,以确定完整前病毒的数量;第二组分是 2-LTR DNA 环化反应,以确定 2-LTR 环化 DNA 的数量;第三组分是拷贝数参考/DNA 剪切反应,靶向核糖核酸酶 P/MRP 亚基 P30 (RPP30),以确定检测所需的细胞当量和 DNA 剪切指数。所有 ddPCR 反应均使用 Bio-Rad QX200 AutoDG ddPCR 系统和 Bio-Rad ddPCR 超混合液(不含 dUTP)进行。在进行 DNA 剪切指数校正并扣除完整 2-LTR 环化 DNA 后,以每百万个输入细胞报告完整前病毒的频率。使用 Bio-Rad QuantaSoft 1.7.4.0917 版本采集终点 ddPCR 数据。 \n\n血浆病毒基因型分析。[3] \n使用 MagMAX-96 病毒 RNA 分离试剂盒(Life Technologies)结合 Thermo Fisher Scientific KingFisher Flex 自动化提取平台,从每只病毒血症猴的 50 μL 血浆样本中提取总 RNA,并用 60 μL AVE 缓冲液洗脱。然后,根据制造商推荐的方案,使用 SuperScript IV 一步法 RT-PCR 系统(Life Technologies)和 Qiagen 一步法 RT-PCR 试剂盒,通过 RT-PCR 对每个样本中 gag 衣壳编码区进行单独扩增。使用引物(SIV-CA-F [5′-CCAAAAACAAGTAGACCAACAG-3′] 和 SIV-CA-R [5′-TGCAAAAGGGATTGGCAC-3′])扩增每个样本中的 SHIV 衣壳编码区,并将扩增产物送至 Elim Biopharmaceuticals Inc.,使用相同的引物组进行群体水平测序。为了鉴定密码子变化,使用 DNA Sequencher 软件(Gene Codes Corporation)将每个样本的衣壳编码序列与亲代攻击病毒株的序列进行比对。使用 BioEdit Sequence Alignment Editor 7.2.6 版对主要 HIV-1 亚型、HIV-2 和 SHIV-SF162P3 衣壳氨基酸序列进行比对。\n\n |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
皮下注射后,来那卡帕韦缓慢释放但完全吸收,血浆峰浓度出现在给药后 84 天。口服给药后的绝对生物利用度较低,约为 6% 至 10%。口服给药后的达峰时间 (Tmax) 约为 4 小时。口服和皮下给药后的平均稳态血药浓度峰值 (Cmax) (%CV) 为 97.2 (70.3) ng/mL。根据群体药代动力学分析,与未感染 HIV-1 的受试者相比,既往接受过大量治疗的 HIV-1 感染患者的来那卡帕韦暴露量(AUCtau、Cmax 和 Ctrough)高出 29% 至 84%。低脂餐对药物吸收的影响可忽略不计。 健康受试者单次静脉注射放射性标记的来那卡帕韦后,76%的总放射性从粪便中回收,不到1%从尿液中回收。血浆(69%)和粪便(33%)中的主要成分是未代谢的来那卡帕韦。 在接受过大量治疗的HIV-1感染患者中,稳态分布容积为976 L。 在接受过大量治疗的HIV-1感染患者中,来那卡帕韦的清除率为3.62 L/h。 代谢/代谢物 代谢在来那卡帕韦的清除中起的作用较小。它经CYP3A4和UGT1A1介导的氧化、N-去烷基化、氢化、酰胺水解、葡萄糖醛酸化、己糖结合、戊糖结合和谷胱甘肽结合代谢。来那卡帕韦的代谢产物尚未完全阐明。没有单一循环代谢产物占血浆药物暴露量的10%以上。 生物半衰期 口服给药后,中位半衰期为10至12天;皮下给药后,中位半衰期为8至12周。 |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
在上市前进行的小型开放标签临床试验中,10%的患者出现血清转氨酶升高,其中2例(3%)超过正常值上限的5倍,这两例患者均出现黄疸。然而,在这两例病例中,均发现了其他肝损伤原因,一例归因于酒精性肝炎,另一例归因于HIV复制成功控制后免疫反应恢复所致的“重建综合征”。两名患者均继续接受lenacapavir治疗,并顺利康复。自lenacapavir获批并广泛应用以来,尚未有已发表的lenacapavir相关肝损伤病例报告。lenacapavir等长效药物的缺点之一是,一旦出现毒性或不耐受,无法立即停止治疗。最后,对于既往患有慢性乙型或丙型肝炎的患者,在疗效不佳的抗逆转录病毒治疗方案中加入来那卡帕韦后,免疫反应的恢复可能导致重建综合征和慢性病毒性肝炎的复发。 可能性评分:E(不太可能是特异性临床表现明显的肝损伤的原因)。 妊娠和哺乳期影响 ◉ 哺乳期用药概述 目前尚无关于哺乳期使用来那卡帕韦的信息。由于该药物的蛋白结合率超过98.5%,因此其在乳汁中的含量可能很低。通过抗逆转录病毒疗法实现并维持病毒抑制可将母乳传播风险降低至1%以下,但并非为零。对于接受抗逆转录病毒疗法且病毒载量持续低于检测限的HIV感染者,如果她们选择母乳喂养,应予以支持。如果病毒载量未得到抑制,建议使用巴氏消毒的捐赠母乳或配方奶。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对泌乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白质结合 体外实验表明,来那卡帕韦与血浆蛋白的结合率约为99.8%。 |
| 参考文献 | |
| 其他信息 |
药效学
Lenacapavir 是一种具有延长药代动力学特征的抗病毒药物。Lenacapavir 通过抑制病毒复制来对抗 HIV-1 病毒:它干扰病毒生命周期中的多个关键步骤,包括病毒的摄取、组装和释放。在健康志愿者中,单次皮下注射 ≥100 mg 的剂量可使血浆浓度超过 95% 有效浓度 (EC95) 并维持 ≥12 周,而注射 ≥300 mg 的剂量可使血浆浓度超过 EC95 并维持 ≥24 周。在未接受过治疗的 HIV-1 感染者中,单次皮下注射 20-450 mg 的剂量,在注射后第九天,血浆 HIV-1 RNA 的平均最大 log10 转换值下降了 1.35-2.20。 Lenacapavir 是一种处方药,已获得美国食品药品监督管理局 (FDA) 的批准。它以两种不同的商品名获批用于以下用途: Lenacapavir 口服片剂和注射剂(商品名:Sunlenca) 用于治疗其他 HIV 药物无效且符合医疗保健提供者确定的特定条件的成人 HIV 感染者。用于治疗 HIV 的莱那卡帕韦 (Lenacapavir) 必须与其他 HIV 药物联合使用。 莱那卡帕韦口服片剂和注射剂(商品名:Yeztugo) 用于 HIV 暴露前预防 (PrEP),以降低体重至少 35 公斤 (77 磅)、HIV 检测呈阴性且有性传播 HIV 风险的成人和青少年感染 HIV 的风险。莱那卡帕韦用于 PrEP 时,应始终与安全性行为(例如使用安全套)联合使用,以降低感染其他性传播疾病的风险。 尽管已推出多种成功的疗法,但 HIV/AIDS 仍然是一个令人担忧的领域,这主要是由于多重耐药性的出现以及患者难以坚持治疗方案。莱那卡帕韦是一种首创的衣壳抑制剂,体外单药治疗即可达到皮摩尔级 HIV-1 抑制效果,与现有抗逆转录病毒药物几乎没有交叉耐药性,并且皮下给药具有更长的药代动力学特征。 2022年8月22日,欧盟委员会首次批准Lenacapavir用于治疗成人多重耐药HIV感染。同年12月22日,美国食品药品监督管理局(FDA)也批准了Lenacapavir上市。Lenacapavir是一种人类免疫缺陷病毒1型(HIV-1)衣壳抑制剂。其作用机制包括抑制HIV衣壳、细胞色素P450 3A、P-糖蛋白和乳腺癌耐药蛋白。Lenacapavir是一种人类免疫缺陷病毒(HIV)衣壳抑制剂,通常与其他抗逆转录病毒药物联合用于治疗多重耐药HIV感染患者。Lenacapavir具有长效作用,有口服片剂和皮下注射溶液两种剂型,半衰期较长,可每26周给药一次。 Lenacapavir治疗期间血清转氨酶水平短暂且通常轻微升高,但发生率较低,尚未发现与临床上明显的急性肝损伤病例相关。 LENACAPAVIR是一种小分子药物,其临床试验阶段最高为IV期(涵盖所有适应症),于2022年首次获批,目前有3个已获批适应症和2个在研适应症。 作用机制 HIV-1在其复制周期中会利用多种宿主因子,包括宿主细胞进入、核整合、复制和病毒颗粒组装。病毒衣壳与宿主细胞膜融合后,释放到宿主细胞质中。衣壳由约250个六聚体和12个五聚体组成,每个六聚体和五聚体均由单体衣壳蛋白(CA)构成。每个CA单体都具有N端结构域和C端结构域(NTD/CTD),并为宿主细胞机制提供相互作用表面。在组装的多聚体中,CA单体之间存在几个重要的蛋白质-蛋白质相互作用界面;这些蛋白质在组装的多聚体中的结合常数显著低于单个衣壳单体。为了促进HIV-1基因组整合,衣壳必须穿过核膜,它利用核孔复合体(NPC)来实现这一过程。两种已被证实对衣壳进入细胞核至关重要的宿主蛋白是切割和多聚腺苷酸化特异性因子亚基6(CPSF6)和核孔蛋白153(Nup153,一种存在于NPC复合体核质侧的蛋白),它们直接与衣壳结合。在多聚体CA组装体中,这两种蛋白都结合于相邻CA单体N端结构域(NTD)和C端结构域(CTD)之间的同一个苯丙氨酸-甘氨酸结合口袋。勒那卡帕韦含有一个二氟苄基环,该环与CPSF6/Nup153占据相同的结合口袋,在重叠结构中与CPSF6中的F321和Nup153中的F1417的苄基重叠。勒那卡帕韦与CA六聚体结合的晶体结构显示,每个六聚体结合六个勒那卡帕韦分子,形成广泛的疏水相互作用、两个阳离子-π相互作用和七个氢键,接触约2000 Ų的埋藏蛋白表面积。因此,勒那卡帕韦的强结合会竞争性地干扰衣壳与CPSF6和Nup153的相互作用。体外实验表明,在多种细胞系中,勒那卡帕韦对HIV-1复制的抑制作用EC50值约为12-314 pM,对早期复制步骤的抑制效果优于后期复制步骤。在极低浓度(0.5 nM)下,lenacapavir 可抑制病毒核转运;而在较高浓度(5-50 nM)下,它还会抑制病毒 DNA 合成和逆转录。由于 CPSF6 和 Nup153 对病毒核转运至关重要,lenacapavir 的结合很可能抑制了这些相互作用,从而阻断了衣壳的核转运。Lenacapavir 的作用机制可能不仅限于阻断与宿主细胞因子的相互作用。Lenacapavir 可提高 CA 组装的速率和程度,显著延长已组装 CA 结构的寿命,即使在高盐浓度下也是如此,并且还会改变已组装衣壳的形态。其稳定浓度约为 1:1,与观察到的分离 CA 六聚体的结合化学计量比非常接近。进一步的分析表明,lenacapavir 的结合会改变六聚体内部和六聚体之间的相互作用,从而改变最终组装体的结构和稳定性。在浓度递增的勒那卡帕韦溶液中连续传代培养HIV-1病毒,导致了主要耐药突变Q67H和N74D的出现,这些突变对其他抗逆转录病毒药物仍然敏感。进一步的传代培养又产生了其他突变L56I、M66I、K70N、N74S和T107N。所有已鉴定的耐药突变均位于勒那卡帕韦的结合位点,除Q67H突变体外,其余突变均表现出体外复制能力降低。其他研究表明,在与对其他抗逆转录病毒药物耐药相关的变异株或自然发生的多态性中,未发现来那卡帕韦耐药性,这表明联合治疗中交叉耐药的可能性极低。 药物适应症 来那卡帕韦与其他抗逆转录病毒药物联合使用,适用于治疗因耐药、不耐受或安全性问题导致当前抗逆转录病毒方案失败的、既往接受过大量治疗的成人多重耐药性1型人类免疫缺陷病毒(HIV-1)感染。 Sunlenca注射液与其他抗逆转录病毒药物联合使用,适用于治疗无法构建抑制性抗病毒方案的成人多重耐药性HIV-1感染(参见第4.2节和第5.1节)。 Sunlenca片剂与其他抗逆转录病毒药物联合使用,适用于治疗无法构建抑制性抗病毒方案的多重耐药HIV-1感染成人患者,用于在注射长效lenacapavir之前进行口服负荷治疗(参见第4.2节和第5.1节)。 Yeytuo片剂与安全性行为措施联合使用,用于暴露前预防(PrEP),以降低HIV-1感染风险增加的成人和青少年(体重至少35公斤)通过性途径感染HIV-1的风险:•口服负荷治疗•口服桥接治疗(参见第 4.2、4.4 和 5.1 节) 肝毒性概述 来那卡帕韦是一种人类免疫缺陷病毒 (HIV) 衣壳抑制剂,与其他抗逆转录病毒药物联合用于治疗多重耐药 HIV 感染患者。来那卡帕韦作用持续时间长,有口服片剂和皮下注射溶液两种剂型,半衰期长,可每 26 周给药一次。来那卡帕韦治疗期间血清转氨酶水平短暂且通常轻微升高的发生率较低,但尚未发现与临床上明显的急性肝损伤病例相关。 |
| 分子式 |
C39H32CLF10N7O5S2
|
|---|---|
| 分子量 |
968.2823
|
| 精确质量 |
967.14
|
| 元素分析 |
C, 48.38; H, 3.33; Cl, 3.66; F, 19.62; N, 10.13; O, 8.26; S, 6.62
|
| CAS号 |
2189684-44-2
|
| 相关CAS号 |
2283356-18-1 (HCl); 2937414-47-4 (Lenacapavir pacfosacil); 2189684-44-2;2283356-12-5 (sodium);
|
| PubChem CID |
133082658
|
| 外观&性状 |
White to light yellow solid powder
|
| LogP |
6.4
|
| tPSA |
175Ų
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
19
|
| 可旋转键数目(RBC) |
13
|
| 重原子数目 |
64
|
| 分子复杂度/Complexity |
2040
|
| 定义原子立体中心数目 |
3
|
| SMILES |
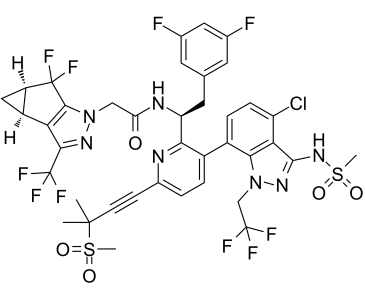
CC(C)(C#CC1=NC(=C(C=C1)C2=C3C(=C(C=C2)Cl)C(=NN3CC(F)(F)F)NS(=O)(=O)C)[C@H](CC4=CC(=CC(=C4)F)F)NC(=O)CN5C6=C([C@H]7C[C@H]7C6(F)F)C(=N5)C(F)(F)F)S(=O)(=O)C
|
| InChi Key |
BRYXUCLEHAUSDY-WEWMWRJBSA-N
|
| InChi Code |
InChI=1S/C39H32ClF10N7O5S2/c1-36(2,63(3,59)60)10-9-21-5-6-22(23-7-8-26(40)30-32(23)57(17-37(43,44)45)54-35(30)55-64(4,61)62)31(51-21)27(13-18-11-19(41)14-20(42)12-18)52-28(58)16-56-34-29(33(53-56)39(48,49)50)24-15-25(24)38(34,46)47/h5-8,11-12,14,24-25,27H,13,15-17H2,1-4H3,(H,52,58)(H,54,55)/t24-,25+,27-/m0/s1
|
| 化学名 |
N-((S)-1-(3-(4-chloro-3-(methylsulfonamido)-1-(2,2,2-trifluoroethyl)-1H-indazol-7-yl)-6-(3-methyl-3-(methylsulfonyl)but-1-yn-1-yl)pyridin-2-yl)-2-(3,5-difluorophenyl)ethyl)-2-((3bS,4aR)-5,5-difluoro-3-(trifluoromethyl)-3b,4,4a,5-tetrahydro-1H-cyclopropa[3,4]cyclopenta[1,2-c]pyrazol-1-yl)acetamide
|
| 别名 |
Lenacapavir; GS-6207; GS 6207; GS6207; GS 714207; GS-714207; GS714207; GS-CA-2; GS-CA2; GS-HIV;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~200 mg/mL (~206.55 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 6.25 mg/mL (6.45 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 62.5 mg/mL 的澄清 DMSO 储备液加入到 900 μL 玉米油中并混合均匀。 配方 2 中的溶解度: 2.5 mg/mL (2.58 mM) in 5% DMSO + 40% PEG300 + 5% Tween80 + 50% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.0328 mL | 5.1638 mL | 10.3276 mL | |
| 5 mM | 0.2066 mL | 1.0328 mL | 2.0655 mL | |
| 10 mM | 0.1033 mL | 0.5164 mL | 1.0328 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。