| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| Other Sizes |
|
| 靶点 |
HER2 (IC50 = 59 nM); EGFR (IC50 = 92 nM); KDR (IC50 = 800 nM); Src (IC50 = 1.4 μM)
Neratinib (HKI-272; PB272; Nerlynx) potently inhibits HER2 (IC₅₀ = 59 nM) and EGFR (IC₅₀ = 92 nM) tyrosine kinases. It weakly inhibits KDR (IC₅₀ = 0.8 μM) and Src (IC₅₀ = 1.4 μM), and shows no significant inhibitory activity against Akt, CDK1/2/4, IKK-2, MK-2, PDK1, c-Raf, and c-Met [1] |
|---|---|
| 体外研究 (In Vitro) |
Neratinib 弱抑制酪氨酸激酶 KDR 和 Src,IC50 分别为 0.8 μM 和 1.4 μM,与 HER2 相比活性低 14 倍和 24 倍。 Neratinib 对其他丝氨酸-苏氨酸激酶没有活性,例如 Akt、细胞周期蛋白 D1/cdk4、细胞周期蛋白 E/cdk2、细胞周期蛋白 B1/cdk1、IKK-2、MK-2、PDK1、c-Raf 和 Tpl-2。如酪氨酸激酶 c-Met。 Neratinib 选择性抑制转染 HER2 (3T3/neu) 的 3T3 细胞以及另外两种 HER-2 过表达 SK-Br-3 和 BT474 细胞的增殖,IC50 值为 2-3 nM,显示 >230 倍与未转染的 3T3 细胞以及 EGFR 和 HER2 阴性的 MDA-MB-435 和 SW620 细胞相比,其效力较高。 Neratinib 还抑制 EGFR 依赖性 A431 细胞的增殖,IC50 为 81 nM。 Neratinib 可减少 BT474 细胞中 HER2 受体的自身磷酸化,IC50 为 5 nM,并减少 A431 细胞中 EGFR 的 EGF 依赖性磷酸化,IC50 为 3 nM。 Neratinib 阻断 HER-2 导致下游 MAPK 和 Akt 通路的抑制,IC50 为 2 nM,比曲妥珠单抗更有效。 Neratinib 抑制 BT474 细胞中细胞周期蛋白 D1 的表达和 Rb 易感基因产生的磷酸化,IC50 为 9 nM,导致 G1-S 停滞并最终降低细胞增殖。激酶测定:Neratinib 在 DMSO 中制备为 10 mg/mL 库存,并在 25 mM HEPES(pH 7.5;0.002 ng/mL-20 μg/mL)中稀释。将 HER2(氨基酸 676-1255)或表皮生长因子受体 (EGFR)(氨基酸 645-1186)的纯化重组 COOH 末端片段 [用 100 mM HEPES (pH 7.5) 和 50% 甘油稀释] 进行浓度递增的培养将 Neratinib 溶解在 4 mM HEPES (pH 7.5)、0.4 mM MnCl2、20 μM 钒酸钠和 0.2 mM DTT 中,在 96 孔 ELISA 板中室温反应 15 分钟。通过添加 40 μM ATP 和 20 mM MgCl2 启动激酶反应,并在室温下进行 1 小时。洗涤板,并使用铕标记的抗磷酸酪氨酸抗体(15 ng/孔)检测磷酸化。洗涤和增强步骤后,使用 Victor2 荧光读数器(激发波长 340 nm,发射波长 615 nm)检测信号。根据抑制曲线计算抑制受体磷酸化 50% 的 Neratinib 浓度 (IC50)。细胞测定:将细胞(3T3、3T3/neu、A431、BT474、SK-Br-3、MDA-MB-435 和 SW480)暴露于不同浓度的 Neratinib 中 2 或 6 天。使用磺基罗丹明 B(一种蛋白质结合染料)测定细胞增殖。简而言之,用 10% 三氯乙酸固定细胞并用水充分洗涤。然后用 0.1% 磺基罗丹明 B 染色细胞并用 5% 乙酸洗涤。蛋白质相关染料溶解在 10 mM Tris 中,并在 450 nM 处测量吸光度。根据抑制曲线确定抑制细胞增殖 50% 的 Neratinib 浓度 (IC50)。
来那替尼(HKI-272;PB272;Nerlynx)选择性抑制HER2转染的3T3细胞(3T3/neu)以及HER2过表达的乳腺癌细胞系SK-Br-3和BT474的增殖,IC₅₀值为2-3nM,其效果比对未转染的3T3细胞和EGFR/HER2阴性细胞系MDA-MB-435、SW620强230倍以上[1] 在骨肉瘤细胞系U2-OS和143B中,来那替尼(HKI-272;PB272;Nerlynx)具有时间依赖性的抗增殖活性。通过下调磷酸化HER2(p-HER2)、PI3K和磷酸化Akt(p-Akt)的表达,减少细胞迁移和侵袭[1] 该药物可阻断HER2和EGFR下游信号通路,导致关键信号分子的磷酸化水平降低,进而抑制肿瘤细胞的增殖和存活[1] |
| 体内研究 (In Vivo) |
口服 Neratinib 可显着抑制 3T3/neu 异种移植物的生长,剂量为 10、20、40 和 80 mg/kg/天时,抑制率分别为 34%、53%、98% 和 98%。与 40 mg/kg/天给药 1 小时内 HER-2 磷酸化抑制 84% 一致,Neratinib 在 5、10 剂量时抑制 BT474 异种移植物的生长 70-82%、67% 和 93%和 40 毫克/公斤/天,分别。 Neratinib 对 SK-OV-3 异种移植物也有效,5 mg/kg/天和 60 mg/kg/天的抑制率分别为 31% 和 85%。 Neratinib 对 EGFR 依赖性 A431 异种移植物的效力低于 HER-2 依赖性肿瘤,在 5 和 20 mg/kg/天时分别具有 32% 和 44% 的抑制作用。 Neratinib 对表达低水平 HER-2 和 EGFR 的 MCF-7 和 MX-1 异种移植物几乎没有活性,在 80 mg/kg/天时仅抑制 28%,表明 Neratinib 对表达 HER-2 或 EGFR 的细胞具有选择性活性。
在体内,当按每日一次的计划口服给药时,HKI-272在HER-2和EGFR依赖性肿瘤异种移植物模型中具有活性。基于其良好的临床前药理学特征,HKI-272已被选为乳腺癌和其他HER-2依赖性癌症中作为抗肿瘤药物进一步开发的候选药物。[1] 口服给予来那替尼(HKI-272;PB272;Nerlynx)可显著抑制裸鼠体内HER2过表达肿瘤异种移植物的生长。通过抑制瘤内HER2信号传导和增殖,降低肿瘤体积和重量[1] 与标准化疗方案联合使用时,来那替尼(HKI-272;PB272;Nerlynx)在异种移植模型中增强抗肿瘤疗效,对肿瘤生长抑制表现出协同作用[1] |
| 酶活实验 |
将来那替尼在 DMSO 中制备成 10 mg/mL 储备液,在 25 mM HEPES(pH 7.5;0.002 ng/mL–20 μg/mL)中稀释。在 96 孔 ELISA 板中,将 HER2(氨基酸 676-1255)或表皮生长因子受体(EGFR)(氨基酸 645-1186)的纯化重组 COOH 末端片段稀释在 100 mM HEPES(pH 7.5)和 50% 中。甘油。然后将混合物与浓度递增的 Neratinib 在 4 mM HEPES (pH 7.5)、0.4 mM MnCl2、20 μM 钒酸钠和 0.2 mM DTT 中在室温下孵育 15 分钟。添加 40 μM ATP 和 20 mM MgCl2 以启动激酶反应,然后在室温下运行一小时。清洗板,然后使用铕标记的抗磷酸酪氨酸抗体(15 ng/孔)检测磷酸化。使用 Victor2 荧光读数器(激发波长为 340 nm,发射波长为 615 nm),在洗涤和增强阶段后检测信号。抑制曲线用于确定受体磷酸化被抑制 50% 时 Neratinib 的浓度 (IC50)。
将重组HER2和EGFR激酶结构域与ATP及特异性多肽底物在系列稀释的来那替尼(HKI-272;PB272;Nerlynx)存在下孵育,反应混合物在恒定温度下维持设定时间,采用分光光度法检测磷酸化底物。通过与溶媒对照组的信号强度对比计算抑制率,从量效曲线中得出IC₅₀值[1] 采用相同方案对KDR、Src及其他非靶标激酶进行激酶活性测定,以评估药物的选择性[1] |
| 细胞实验 |
将不同浓度的 Neratinib 应用于细胞(3T3、3T3/neu、A431、BT474、SK-Br-3、MDA-MB-435 和 SW480),持续两天或六天。一种称为磺基罗丹明 B 的蛋白质结合染料用于测量细胞增殖。总之,细胞用10%三氯乙酸固定后用水彻底清洗。用 0.1% 磺基罗丹明 B 染色细胞后,用 5% 乙酸冲洗。将蛋白质相关染料溶解在 10 mM Tris 中后,在 450 nM 处计算吸光度。抑制曲线用于计算neratinib抑制50%细胞增殖的浓度(IC50)。
将HER2过表达的SK-Br-3、BT474细胞及HER2转染的3T3细胞以5×10³个细胞/孔接种到96孔板中,用0.001-100nM的来那替尼(HKI-272;PB272;Nerlynx)处理72小时,采用比色法检测细胞活性以确定IC₅₀值[1] 用不同浓度的来那替尼(HKI-272;PB272;Nerlynx)处理骨肉瘤细胞U2-OS和143B 24、48和72小时,分别采用创伤愈合实验和Transwell实验评估细胞迁移和侵袭能力,通过蛋白质印迹法检测p-HER2、PI3K、Akt和p-Akt的表达水平[1] 为进行信号通路分析,用药物处理肿瘤细胞24小时后裂解,与针对下游信号分子磷酸化形式和总形式的抗体孵育,以评估对HER2/EGFR通路的抑制作用[1] |
| 动物实验 |
雌性无胸腺(裸鼠)肿瘤异种移植[1]
10、20、40、60 或 80 mg/kg/天 灌胃,42 天 肿瘤异种移植研究[1] 将肿瘤细胞(在组织培养中维持)或肿瘤碎片皮下植入雌性无胸腺(裸鼠)侧腹。对于雌激素依赖性细胞系(BT474、MCF-7 和 SK-OV-3),在肿瘤植入前 1 周,将激素缓释片(0.72 mg 17-β 雌二醇,60 天释放)植入动物体内。此外,将 SK-OV-3 细胞悬浮于 Matrigel 基底膜基质中进行植入。在肿瘤大小达到 90–200 mg 后开始治疗,并将动物随机分配到不同的治疗组(分期,第 0 天)。对于 3T3/neu 异种移植瘤,治疗于肿瘤植入后第二天(第 0 天)开始。HKI-272 配制于 0.5% 甲基纤维素-0.4% 聚山梨醇酯-80(吐温 80)溶液中,每日通过灌胃法口服给药。每 7 天测定一次肿瘤质量 [(长 × 宽²)/2]。除 3T3/neu 外,所有异种移植瘤研究中的肿瘤生长均以相对肿瘤生长表示:即平均肿瘤质量与第 0 天平均肿瘤质量的比值。肿瘤生长抑制率以载体对照组为参照进行计算。对数据进行对数转换后,采用单尾 Student's t 检验(方差相等)来验证抑制作用的统计学意义。[1] 异种移植瘤中 HER-2 磷酸化。[1] 将 BT474 肿瘤碎片(约 30 mm³)皮下植入无胸腺雌性裸鼠(每组 5 只)。当肿瘤体积达到 200–300 mg 时,给予动物单次口服剂量(40 mg/kg)的 HKI-272(溶于 pH 2.0 的水中)。分别于 1、3、6 和 24 小时切除对照组和治疗组动物的肿瘤并切碎。将肿瘤组织块悬浮于含有 10 mM Tris(pH 7.5)、5 mM EDTA、150 mM NaCl、1% Triton X-100、1% 脱氧胆酸钠、0.1% SDS、1 mM PMSF、10 μg/ml 胃蛋白酶抑制剂、10 μg/ml 亮抑蛋白酶肽、10 μg/ml 抑蛋白酶、2 mM 钒酸钠和 100 mM 氟化钠的溶液中,并在冰上用匀浆器进行匀浆裂解。离心澄清后,使用 Bio-Rad DC 蛋白测定试剂盒测定裂解液中的蛋白浓度。将每组 60 μg 裂解液混合,进行 SDS-PAGE 电泳和磷酸酪氨酸特异性抗体的免疫印迹分析。同时,将混合提取物与 4 μg 抗 HER-2 抗体在 4°C 下孵育 1 小时进行免疫沉淀。免疫复合物收集于蛋白A琼脂糖上,洗涤后,使用磷酸酪氨酸特异性抗体进行免疫印迹分析。分析单个肿瘤的提取物以确定动物间的差异。 携带HER2过表达的SK-Br-3或BT474异种移植瘤(肿瘤体积约100 mm³)的裸鼠被随机分为对照组和治疗组。奈拉替尼(HKI-272;PB272;Nerlynx)悬浮于0.5%羧甲基纤维素溶液中,以10-40 mg/kg/天的剂量连续21天口服给药。每隔3天测量一次肿瘤体积,并在治疗结束后处死小鼠,收集肿瘤组织进行增殖标志物的免疫组织化学分析[1]。在联合治疗实验中,将携带肿瘤异种移植的裸鼠接受奈拉替尼(HKI-272;PB272;Nerlynx)(20 mg/kg/天,口服)联合标准化疗药物治疗。药物在化疗前1小时给药,每7天重复一个治疗周期,共3个周期。记录小鼠的肿瘤重量和生存时间[1]。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
奈拉替尼及其主要活性代谢物M3、M6和M7的达峰时间(Tmax)为2-8小时。与高脂餐同服可使Cmax增加1.7倍,总暴露量增加2.2倍。与标准餐同服可使Cmax增加1.2倍,总暴露量增加1.1倍。与质子泵抑制剂等胃酸抑制剂合用可使 Cmax 降低 71%,总暴露量降低 65%。 97.1% 的总剂量经粪便排泄,1.13% 经尿液排泄。 稳态表观分布容积为 6433 L。 多次给药后,总清除率为 216 L/h(首次给药后)和 281 L/h(稳态)。 代谢/代谢物 奈拉替尼主要通过 CYP3A4 代谢。它也少量通过含黄素单加氧酶代谢。奈拉替尼活性代谢物 M3、M6、M7 和 M11 的全身暴露量分别为 15%、33%、22% 和 4%。 生物半衰期 单次给药后,平均消除半衰期为 7-17 小时。多次给药后,奈拉替尼的平均血浆半衰期为 14.6 小时,M3 为 21.6 小时,M6 为 13.8 小时,M7 为 10.4 小时。 奈拉替尼(HKI-272;PB272;Nerlynx) 具有口服生物利用度,口服给药后 2-8 小时达到血浆峰浓度。该药物在人体内的血浆半衰期为7-17小时,支持每日一次给药[1] 该药物广泛分布于肿瘤组织中,其肿瘤与血浆浓度比有利于有效靶向HER2过表达肿瘤[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
在奈拉替尼治疗期间,血清转氨酶水平升高并不罕见,发生率高达10%,但仅有1%至2%的患者其水平超过正常值上限5倍以上。在上市前研究中,未发现奈拉替尼相关的临床明显肝损伤病例,血清酶升高通常较轻且具有自限性,不伴有症状或黄疸。肝毒性可能是HER2蛋白激酶抑制剂的类效应,尽管不同药物的发生频率和严重程度有所不同。奈拉替尼相关肝损伤的具体细节,例如潜伏期、血清酶谱、临床特征和病程,尚未发表。其他酪氨酸激酶受体抑制剂通常在开始治疗后数天或数周内引起肝损伤,表现为肝细胞酶突然升高,病程中度至重度。免疫过敏和自身免疫特征并不常见。既往存在肝硬化或因肝肿瘤负荷导致肝功能损害的患者,发生临床显著肝损伤和肝衰竭的风险增加。然而,目前尚无确凿证据表明奈拉替尼与临床可见的肝损伤病例相关。 可能性评分:E(未经证实但怀疑是临床可见肝损伤的原因)。 妊娠和哺乳期用药 ◉ 哺乳期用药概述 目前尚无关于奈拉替尼在哺乳期临床应用的信息。由于奈拉替尼及其代谢物与血浆蛋白的结合率超过99%,因此其在乳汁中的含量可能很低。制造商建议在接受奈拉替尼治疗期间停止母乳喂养。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对泌乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白结合 奈拉替尼与人血浆蛋白的结合率超过99%。它可与人血清白蛋白和α1酸性糖蛋白结合。 在临床前研究中,奈拉替尼(HKI-272;PB272;Nerlynx) 在治疗剂量下显示出轻度至中度毒性,包括小鼠出现短暂性腹泻和轻微体重减轻。未观察到明显的肝肾毒性,血清ALT、AST和肌酐水平正常[1]。 奈拉替尼(HKI-272;PB272;Nerlynx)在人血浆中的血浆蛋白结合率约为95%,这可能会影响其分布和潜在的药物相互作用[1]。 |
| 参考文献 | |
| 其他信息 |
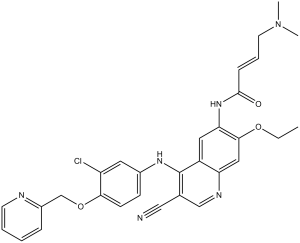
奈拉替尼是一种喹啉化合物,其3位连接有氰基,4位连接有3-氯-4-(2-吡啶甲氧基)苯胺基,6位连接有4-二甲氨基-反式-丁-2-烯酰胺基,7位连接有乙氧基。它是一种酪氨酸激酶抑制剂和抗肿瘤药物。它属于喹啉类和腈类化合物。
奈拉替尼于2017年7月获批用于人表皮生长因子受体2 (HER2) 阳性乳腺癌的延长辅助治疗。Puma Biotechnology Inc. 获得了该药物的批准,商品名为Nerlynx。目前,奈拉替尼正在研究用于治疗多种其他类型的癌症。 奈拉替尼是一种激酶抑制剂。奈拉替尼的作用机制是作为激酶抑制剂和P-糖蛋白抑制剂。 奈拉替尼是一种口服酪氨酸激酶受体抑制剂,用于早期乳腺癌的延长辅助治疗。奈拉替尼治疗期间血清转氨酶水平短暂升高的发生率较低,但尚未有确凿证据表明其与临床上明显的肝损伤伴黄疸病例相关。 奈拉替尼是一种口服的6,7-二取代-4-苯胺基喹啉-3-腈类化合物,是HER-2受体酪氨酸激酶的不可逆抑制剂,具有潜在的抗肿瘤活性。奈拉替尼与HER-2受体不可逆结合,从而降低细胞内的自身磷酸化,其作用机制可能是靶向受体ATP结合口袋中的半胱氨酸残基。用该药物处理细胞会导致下游信号转导事件和细胞周期调控通路受到抑制;细胞分裂周期停滞在 G1-S(Gap 1/DNA 合成)期转换;最终导致细胞增殖减少。奈拉替尼还能抑制表皮生长因子受体 (EGFR) 激酶和 EGFR 依赖性细胞的增殖。 另见:马来酸奈拉替尼(其活性成分)。 药物适应症 用于早期 HER2 过表达/扩增的乳腺癌成年患者,作为曲妥珠单抗辅助治疗后的延长辅助治疗。 FDA 标签 奈拉替尼适用于早期激素受体阳性、HER2 过表达/扩增的乳腺癌成年患者,且这些患者完成先前曲妥珠单抗辅助治疗的时间不足一年。 乳腺癌治疗 作用机制 奈拉替尼与 EGFR、HER2 和 HER4 结合并不可逆地抑制它们。这可以阻止受体上酪氨酸残基的自身磷酸化,并减少通过丝裂原活化蛋白激酶和Akt通路进行的致癌信号传导。 药效学 奈拉替尼是一种酪氨酸激酶抑制剂,对表皮生长因子受体 (EGFR)、HER2 和人表皮生长因子受体 4 (HER4) 阳性癌具有抗肿瘤作用。 奈拉替尼(HKI-272;PB272;Nerlynx)是一种不可逆的泛HER酪氨酸激酶抑制剂,它通过与HER2、EGFR和HER4的激酶结构域共价结合发挥抗肿瘤作用,从而永久阻断参与肿瘤细胞增殖、迁移和存活的下游信号通路[1]。 它主要用于治疗HER2阳性乳腺癌,尤其是对于既往接受过曲妥珠单抗治疗的患者,该药物可以克服由 HER2 胞外结构域截短或 EGFR 共激活引起的曲妥珠单抗耐药性 [1] |
| 分子式 |
C30H29CLN6O3
|
|---|---|
| 分子量 |
557.04
|
| 精确质量 |
556.198
|
| 元素分析 |
C, 64.68; H, 5.25; Cl, 6.36; N, 15.09; O, 8.62
|
| CAS号 |
698387-09-6
|
| 相关CAS号 |
Neratinib maleate;915942-22-2;Neratinib-d6;1259519-18-0
|
| PubChem CID |
9915743
|
| 外观&性状 |
White to light brown solid powder
|
| 密度 |
1.3±0.1 g/cm3
|
| 沸点 |
757.0±60.0 °C at 760 mmHg
|
| 熔点 |
184 °C
|
| 闪点 |
411.6±32.9 °C
|
| 蒸汽压 |
0.0±2.5 mmHg at 25°C
|
| 折射率 |
1.667
|
| LogP |
5.46
|
| tPSA |
112.4
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
8
|
| 可旋转键数目(RBC) |
11
|
| 重原子数目 |
40
|
| 分子复杂度/Complexity |
881
|
| 定义原子立体中心数目 |
0
|
| SMILES |
ClC1=C(C([H])=C([H])C(=C1[H])N([H])C1=C(C#N)C([H])=NC2=C([H])C(=C(C([H])=C12)N([H])C(/C(/[H])=C(\[H])/C([H])([H])N(C([H])([H])[H])C([H])([H])[H])=O)OC([H])([H])C([H])([H])[H])OC([H])([H])C1=C([H])C([H])=C([H])C([H])=N1
|
| InChi Key |
JWNPDZNEKVCWMY-VQHVLOKHSA-N
|
| InChi Code |
InChI=1S/C30H29ClN6O3/c1-4-39-28-16-25-23(15-26(28)36-29(38)9-7-13-37(2)3)30(20(17-32)18-34-25)35-21-10-11-27(24(31)14-21)40-19-22-8-5-6-12-33-22/h5-12,14-16,18H,4,13,19H2,1-3H3,(H,34,35)(H,36,38)/b9-7+
|
| 化学名 |
(E)-N-[4-[3-chloro-4-(pyridin-2-ylmethoxy)anilino]-3-cyano-7-ethoxyquinolin-6-yl]-4-(dimethylamino)but-2-enamide
|
| 别名 |
Neratinib; HKI-272; PB272; HKI272; PB 272; HKI 272; 698387-09-6; HKI-272; Neratinib (HKI-272); Nerlynx; HKI 272; UNII-JJH94R3PWB; JJH94R3PWB; PB-272; trade name: Nerlynx
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 2 mg/mL (3.59 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浮液;超声助溶。
例如,若需制备1 mL的工作液,可将100 μL 20.0mg/mL澄清的DMSO储备液加入到900μL 20%SBE-β-CD生理盐水中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 配方 2 中的溶解度: ≥ 0.83 mg/mL (1.49 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 8.3 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 View More
配方 3 中的溶解度: 30% PEG400+0.5% Tween80+5% propylene glycol: 5 mg/mL 配方 4 中的溶解度: 3.33 mg/mL (5.98 mM) in 0.5% MC 0.5% Tween-80 (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.7952 mL | 8.9760 mL | 17.9520 mL | |
| 5 mM | 0.3590 mL | 1.7952 mL | 3.5904 mL | |
| 10 mM | 0.1795 mL | 0.8976 mL | 1.7952 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Innovative Trial for Understanding the Impact of Targeted Therapies in NF2-Related Schwannomatosis (INTUITT-NF2)
CTID: NCT04374305
Phase: Phase 2 Status: Active, not recruiting
Date: 2024-11-18
Effect of HKI-272 on cell cycle regulatory proteins. BT474 cells were incubated with HKI-272 for 12–16 h at 37°C. Protein extracts were analyzed by immunoblotting using cyclin D1, p27, or retinoblastoma (Rb)-specific antibodies. Actin antibodies were used as control. Cancer Res. 2004 Jun 1;64(11):3958-65. |
In vivo activity of HKI-272. A, groups of 10 mice were implanted with 2 × 106 3T3/neu cells. Animals were treated with the vehicle or HKI-272 on days 1–10 (p.o.), beginning the day after implantation. B–E, mice were implanted with BT474 tumor fragments (30 mm3; B), 5 × 106 SK-OV-3 cells (C), 5 × 106 A431 cells (D), or MCF-7 tumor fragments (30 mm3; E). Cancer Res. 2004 Jun 1;64(11):3958-65. |
Inhibition of HER-2 phosphorylation in xenografts. BT474 tumor-bearing mice (5 animals/group) were treated with vehicle or a single dose of HKI-272. Tumors from control and treated mice were dissected at various times after compound administration. Cancer Res. 2004 Jun 1;64(11):3958-65. |