| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
- In canine osteosarcoma cells (D17 and HMPOS), the primary target of pamidronate disodium is associated with the regulation of cell viability, though no specific IC50, Ki, or EC50 values were reported [1]
- In human bone marrow mesenchymal stem cells (hBMSCs), pamidronate disodium targets the Wnt/β-Catenin signaling pathway, suppressing its activity; no specific IC50, Ki, or EC50 values were provided [2] - In rabbit osteoarthritic subchondral bone and cartilage, pamidronate disodium targets the expression balance of osteoprotegerin (OPG) and receptor activator of nuclear factor-κB ligand (RANKL), with no reported IC50, Ki, or EC50 values [3] |
|---|---|
| 体外研究 (In Vitro) |
在帕米膦酸盐浓度范围为 100 至 1000 μM 时,骨肉瘤细胞活力以浓度和时间依赖性方式显着降低,最大的降低在暴露 48 和 72 小时后最为一致。暴露于 1000 μM 帕米膦酸 72 小时后,治疗后的骨肉瘤细胞的细胞活力百分比最低为 34% [1]。 BMMSC 的成骨发育受 Wnt 和 β-catenin 信号传导调节,而帕酰胺酯二钠可抑制该信号传导。 BMMSC 的成骨异常可通过 Wnt3a 来挽救,Wnt3a 是 Wnt 和 β-catenin 信号传导的激活剂,可抵消帕米膦酸二钠的副作用 [2]。
1. 对犬骨肉瘤细胞的作用:将犬骨肉瘤细胞系(D17、HMPOS)用浓度为1、10、50、100μM的帕米膦酸钠处理24、48、72小时,采用MTT法检测细胞活力。对于D17细胞,24小时时各浓度均未显著降低细胞活力;48小时时仅100μM浓度组细胞活力略有下降(约为对照组的85%);72小时时50μM和100μM浓度组细胞活力分别降至对照组的70%和60%。对于HMPOS细胞,24小时时细胞活力未受影响;48小时时100μM浓度组细胞活力降至对照组的80%;72小时时50μM和100μM浓度组细胞活力分别为对照组的75%和55%。流式细胞术检测显示,用最高100μM的帕米膦酸钠处理72小时后,两种细胞系均未检测到凋亡变化[1] 2. 对人骨髓间充质干细胞(hBMSCs)的作用:用10、50、100μM的帕米膦酸钠处理hBMSCs。在7天和14天时检测成骨分化标志物碱性磷酸酶(ALP)活性:7天时50μM和100μM浓度组ALP活性分别为对照组的60%和40%;14天时分别为对照组的50%和30%。21天后通过茜素红染色检测矿化结节形成,结果显示药物处理组矿化结节显著减少,100μM浓度组结节数量仅为对照组的20%。Western blot分析表明,Wnt/β-Catenin信号通路相关蛋白(β-Catenin、Runx2、Osterix)的表达水平下调:100μM浓度组中β-Catenin表达量为对照组的30%,Runx2为40%,Osterix为35%。流式细胞术分析显示,hBMSCs的凋亡率随药物浓度升高而增加:100μM浓度组凋亡率约为25%,而对照组约为5%[2] 3. 对兔骨关节炎细胞及组织的作用:用50、100μM的帕米膦酸钠处理原代兔软骨细胞和软骨下骨细胞。实时荧光定量PCR(Real-time PCR)结果显示,在软骨下骨细胞中,与骨关节炎模型组相比,50μM和100μM浓度组OPG mRNA表达量分别上调1.5倍和2.0倍,RANKL mRNA表达量分别下调0.6倍和0.4倍;在软骨细胞中,与模型组相比,50μM和100μM浓度组Ⅱ型胶原mRNA表达量分别上调1.3倍和1.6倍,基质金属蛋白酶13(MMP-13)mRNA表达量分别下调0.7倍和0.5倍。兔骨关节炎软骨切片的免疫组化染色显示,帕米膦酸钠处理可增加软骨下骨区域OPG蛋白表达,降低RANKL蛋白表达[3] |
| 体内研究 (In Vivo) |
在早期骨关节炎的情况下,帕米膦酸可以有效预防甚至逆转软骨下骨丢失,从而减缓软骨的恶化。该过程可能与 RANKL、MMP-9 和 TLR-4 的下调以及 OPG 的上调有关[3]。
兔骨关节炎模型实验:采用新西兰大白兔,通过前交叉韧带切断术(ACLT)建立骨关节炎模型。术后2周,将兔子随机分为3组:模型组、帕米膦酸钠低剂量组(10μM,每关节0.2mL)、帕米膦酸钠高剂量组(100μM,每关节0.2mL)。药物通过关节腔内注射给药,每周1次,连续给药4周。术后8周,显微计算机断层扫描(micro-CT)分析显示,高剂量组软骨下骨矿物质密度(BMD)为模型组的1.2倍,骨小梁数量(Tb.N)为模型组的1.3倍,骨小梁间距(Tb.Sp)为模型组的0.8倍。软骨组织学评分(Mankin评分)显示,高剂量组评分为4.5分左右,显著低于模型组的8.0分左右。软骨下骨免疫组化检测显示,药物处理组OPG蛋白表达上调、RANKL蛋白表达下调,且高剂量组效果更显著[3] |
| 酶活实验 |
1. hBMSCs中ALP活性检测:将hBMSCs在含不同浓度帕米膦酸钠的成骨诱导培养基中培养7天和14天。用PBS清洗细胞后,加入裂解缓冲液裂解细胞。细胞裂解液在4℃下以12000×g离心10分钟,收集上清液。采用ALP检测试剂盒检测活性:将上清液与底物溶液(对硝基苯磷酸酯,pNPP)混合,在37℃下孵育30分钟,加入终止液终止反应,用酶标仪在405nm波长处测定吸光度。根据对硝基苯酚标准曲线计算ALP活性,并通过BCA法测定上清液蛋白浓度对ALP活性进行归一化处理[2]
2. 兔软骨下骨中OPG和RANKL蛋白的ELISA检测:将兔软骨下骨组织在含蛋白酶抑制剂的RIPA裂解缓冲液中匀浆。匀浆液在4℃下以10000×g离心15分钟,收集上清液。采用BCA法测定蛋白浓度。ELISA实验时,将100μL上清液(稀释至适宜浓度)加入预包被抗OPG或抗RANKL抗体的ELISA板孔中,37℃孵育1小时。用洗涤缓冲液清洗平板3次后,加入100μL辣根过氧化物酶(HRP)标记的二抗,37℃孵育30分钟。再次清洗平板后,加入100μL TMB底物溶液,在37℃避光条件下显色15分钟,加入终止液终止反应,在450nm波长处测定吸光度。根据标准曲线计算OPG和RANKL的浓度[3] |
| 细胞实验 |
1. 犬骨肉瘤细胞活力的MTT检测:将D17和HMPOS细胞以每孔5×10³个细胞的密度接种于96孔板,过夜培养。向孔中加入帕米膦酸钠,使终浓度分别为1、10、50、100μM,每个浓度设3个复孔。细胞在37℃、5%CO₂培养箱中孵育24、48、72小时。孵育结束后,每孔加入20μL MTT溶液(5mg/mL),继续孵育4小时。吸弃培养基,每孔加入150μL二甲基亚砜(DMSO)溶解甲臜结晶,用酶标仪在490nm波长处测定吸光度,细胞活力按(药物组吸光度/对照组吸光度)×100%计算[1]
2. hBMSCs中Wnt/β-Catenin通路蛋白的Western blot检测:用帕米膦酸钠处理hBMSCs 7天后,用PBS清洗细胞,加入含蛋白酶和磷酸酶抑制剂的RIPA裂解缓冲液裂解细胞。细胞裂解液在4℃下以12000×g离心15分钟,收集上清液。BCA法测定蛋白浓度后,取等量蛋白(每泳道30μg)通过10%十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)分离,转移至聚偏氟乙烯(PVDF)膜。膜用含5%脱脂牛奶的Tris缓冲盐溶液(TBST)室温封闭1小时,随后加入抗β-Catenin、Runx2、Osterix和GAPDH(内参)的一抗,4℃孵育过夜。用TBST清洗膜3次后,加入HRP标记的二抗,室温孵育1小时。采用增强化学发光(ECL)检测试剂盒显影蛋白条带,用ImageJ软件定量各条带的灰度值,各蛋白的相对表达量以GAPDH为内参进行归一化[2] 3. 兔细胞中OPG、RANKL、Ⅱ型胶原和MMP-13的Real-time PCR检测:采用TRIzol试剂从经帕米膦酸钠处理的兔软骨细胞和软骨下骨细胞中提取总RNA,用分光光度计检测RNA纯度和浓度(A260/A280比值在1.8-2.0之间)。采用逆转录试剂盒将RNA逆转录为互补DNA(cDNA)。Real-time PCR在PCR仪中进行,使用SYBR Green PCR Master Mix,反应条件为:95℃预变性5分钟,随后40个循环(95℃变性15秒,60℃退火延伸30秒)。设计并合成OPG、RANKL、Ⅱ型胶原、MMP-13和GAPDH(内参)的引物序列,采用2^(-ΔΔCt)法计算目标基因的相对mRNA表达量[3] |
| 动物实验 |
兔骨关节炎模型建立及给药:雄性新西兰白兔(体重2.5-3.0 kg)用戊巴比妥钠(静脉注射,30 mg/kg)麻醉。剃除右膝关节毛发并消毒,在膝关节外侧做纵行切口,暴露关节囊。用手术剪切断前交叉韧带,逐层缝合关节囊和皮肤。术后连续3天肌注青霉素以预防感染。前交叉韧带切断术后两周,将兔子随机分为三组(每组n=6):(1)模型组:每周一次关节内注射0.2 mL生理盐水,持续4周; (2)低剂量帕米膦酸钠组:每周一次关节内注射0.2 mL 10 μM帕米膦酸钠溶液,持续4周;(3)高剂量帕米膦酸钠组:每周一次关节内注射0.2 mL 100 μM帕米膦酸钠溶液,持续4周。帕米膦酸钠溶液由药物溶于生理盐水配制而成。术后8周(停药后4周),通过静脉注射过量戊巴比妥钠处死兔子。解剖右膝关节,收集股骨髁和胫骨平台,用于微型CT、组织学和免疫组织化学分析[3]
|
| 药代性质 (ADME/PK) |
吸收、分布和排泄
对于肌酐清除率 >90mL/min 的患者,90mg 静脉注射剂量达到 Cmax 1.92±1.08µg/mL,Tmax 为 4h,AUC 为 10.2±6.95µgh/mL。在肌酐清除率为 61-90mL/min 的患者中,90mg 静脉注射剂量达到 Cmax 1.86±0.50µg/mL,Tmax 为 4h,AUC 为 10.7—3.91µgh/mL。[A203264 在肌酐清除率为 30-60mL/min 的患者中,90mg 静脉注射剂量达到 Cmax 1.84±0.58µg/mL,Tmax 为 4h,AUC 为 10.1±3.38µgh/mL。对于肌酐清除率<30mL/min的患者,90mg静脉注射剂量达到Cmax 1.93±0.53µg/mL,Tmax为4h,AUC为34.0±8.37µgh/mL。 帕米膦酸钠完全经尿液排泄。给药后 120 小时,46±16% 的剂量已从尿液中排出。 帕米膦酸钠的平均总清除率为 107±50 mL/min,平均肾清除率为 49±28 mL/min。 代谢/代谢物 帕米膦酸钠在体内不代谢。 帕米膦酸钠不代谢,完全通过肾脏排泄。 排泄途径:帕米膦酸钠不代谢,完全通过肾脏排泄。 半衰期:平均±标准差消除半衰期为 28±7 小时。 生物半衰期 帕米膦酸钠的平均消除半衰期为 28±7 小时。 |
| 毒性/毒理 (Toxicokinetics/TK) |
毒性概述
帕米膦酸钠的作用机制是抑制骨吸收。帕米膦酸钠吸附于骨骼中的磷酸钙(羟基磷灰石)晶体,并可能直接阻断骨骼中这种矿物质成分的溶解。体外研究也表明,抑制破骨细胞活性有助于抑制骨吸收。帕米膦酸钠还靶向法尼基焦磷酸(FPP)合酶。含氮双膦酸盐(如帕米膦酸钠、阿仑膦酸钠、利塞膦酸钠、伊班膦酸钠和唑来膦酸钠)似乎作为异戊二烯二磷酸脂质的类似物发挥作用,从而抑制甲羟戊酸途径中的一种酶——FPP合酶。抑制破骨细胞中的这种酶可阻止异戊二烯类脂质(FPP 和 GGPP)的生物合成,而这些脂质对于小 GTP 酶信号蛋白的翻译后法尼基化和香叶基香叶基化至关重要。这种活性可抑制破骨细胞活性,并减少骨吸收和骨转换。在绝经后妇女中,它可降低升高的骨转换率,从而平均而言导致骨量净增加。 妊娠和哺乳期影响 ◉ 哺乳期用药概述 有限的信息表明,母亲静脉注射 30 mg 帕米膦酸钠后,乳汁中的药物浓度非常低。由于帕米膦酸钠的血清半衰期约为 3 小时,与钙高度结合,且口服吸收率很低(成人为 0.3% 至 3%),因此母乳喂养的婴儿不太可能吸收帕米膦酸钠。[1]在获得更多数据之前,给药后12至24小时停止哺乳应能确保母乳喂养的婴儿几乎不接触帕米膦酸钠。其他证据表明,长期帕米膦酸钠治疗结束后进行母乳喂养似乎对婴儿没有不良影响。一些专家建议,如果母亲在孕期或哺乳期接受过帕米膦酸钠治疗,则应在产后头两个月监测婴儿的血清钙水平。[2] ◉ 对母乳喂养婴儿的影响 一位母亲在产后6个月开始每月接受一次30毫克静脉注射帕米膦酸钠。每次给药后,她都会挤奶并丢弃乳汁48小时。在母亲接受帕米膦酸钠治疗期间,婴儿约80%的乳汁都是母乳喂养,在此期间,婴儿保持健康并正常生长。[1] 由于帕米膦酸钠在长期给药后可在体内持续存在数年,以下病例可能具有参考价值。三名患有成骨不全症或McCune-Albright综合征的女性接受了帕米膦酸钠静脉注射治疗,累积剂量分别为每年6、7.5和9 mg/kg,分别持续2年、4年和2.2年。她们最后一次给药分别在受孕前3个月、3个月、48个月(两名婴儿)和21个月。所有女性在哺乳期间均未恢复使用帕米膦酸钠,但她们在产后均进行了母乳喂养,其中一名母乳喂养了18个月,两名母乳喂养时间不详,一名母乳喂养了6周。所有婴儿均未出现帕米膦酸钠的不良反应。[3] 另有两名母亲在孕前和孕期接受了帕米膦酸钠静脉输注。其中一名母亲总共接受了240 mg的帕米膦酸钠,最后一次给药是在孕早期。她纯母乳喂养了婴儿6个月,并持续母乳喂养至婴儿12个月大。她的婴儿生长发育正常,没有不良反应。[4] 另一名女性在怀孕前一年接受了6个月的阿仑膦酸钠治疗,之后每4个月接受一次帕米膦酸钠治疗。她的婴儿母乳喂养了3个月(母乳喂养程度未说明)。婴儿在2个月大时出现轻度低钙血症,但在5个月大时钙水平正常,长骨发育也正常。[5] 一名女性在怀孕期间出现短暂性骨质疏松症,伴有足部疼痛。产后第3天和第8天以及2个月后,她接受了30毫克帕米膦酸钠静脉注射。医生嘱咐她在每次给药后24小时内丢弃母乳。她的母乳喂养婴儿(未说明喂养程度)在15个月大时生长发育正常。[6] ◉ 对泌乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白质结合 帕米膦酸钠在血清中的蛋白质结合率约为54%。 - 体外对人骨髓间充质干细胞(hBMSCs)的毒性:用浓度为10、50和100 μM的帕米膦酸钠处理7天,可增加hBMSCs的凋亡率。流式细胞术分析显示,对照组的凋亡率约为5%,而10 μM、50 μM和100 μM药物组的凋亡率分别约为10%、18%和25%。在用浓度高达 100 μM 的帕米膦酸钠处理犬骨肉瘤细胞(D17 和 HMPOS)72 小时后,未观察到明显的细胞毒性(例如细胞膜损伤),这表现为与对照组相比,乳酸脱氢酶 (LDH) 释放量没有显著增加 [1][2]。 |
| 参考文献 |
|
| 其他信息 |
1. 帕米膦酸钠是一种双膦酸盐类药物,常用于治疗骨质疏松症和骨转移等骨骼相关疾病。本研究旨在探讨其对犬骨肉瘤细胞的潜在抑制作用,为其在犬骨肉瘤治疗中的应用提供理论基础[1]。2. 研究揭示了帕米膦酸钠诱导骨坏死的新机制:该药物通过抑制人骨髓间充质干细胞(hBMSCs)中的Wnt/β-catenin信号通路,抑制成骨分化(降低碱性磷酸酶活性和矿化作用),并促进细胞凋亡,从而损害骨修复并导致骨坏死。这一发现为双膦酸盐的副作用提供了新的认识,并可能有助于制定降低骨坏死风险的策略[2]
3. 在兔骨关节炎模型中,帕米膦酸钠通过调节软骨下骨中OPG/RANKL的平衡(上调OPG并下调RANKL)来减少软骨下骨丢失,并通过增加软骨细胞中II型胶原的表达和降低MMP-13的表达来保护软骨,从而对骨关节炎关节发挥保护作用。这表明帕米膦酸钠可能具有治疗骨关节炎的潜力[3] 药效学 帕米膦酸是一种第二代含氮双膦酸盐,可抑制破骨细胞介导的骨丢失。它具有较宽的治疗指数和较长的作用持续时间,对于某些适应症,可以每3-4周给药一次。应告知患者血尿素氮升高、肾小管坏死和肾毒性的风险。 |
| 分子式 |
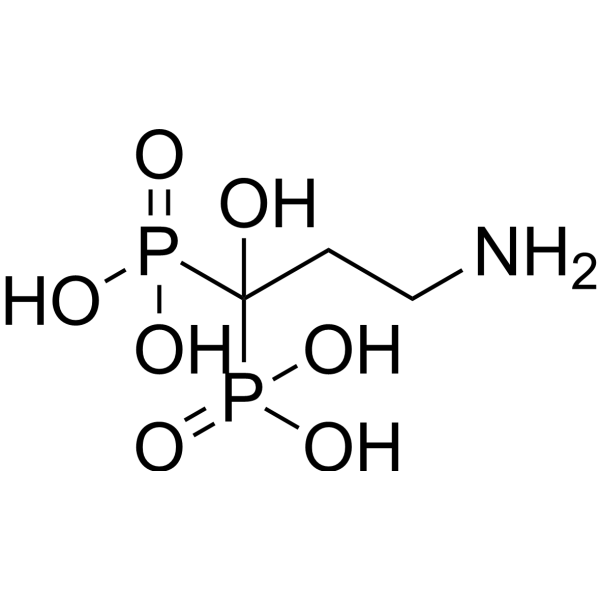
C3H11NO7P2
|
|---|---|
| 分子量 |
235.0695
|
| 精确质量 |
235.001
|
| 元素分析 |
C, 15.33; H, 4.72; N, 5.96; O, 47.64; P, 26.35
|
| CAS号 |
40391-99-9
|
| 相关CAS号 |
Pamidronate Disodium;57248-88-1; 89131-02-2 (monosodium);
109552-15-0 (disodium pentahydrate);40391-99-9 (free acid)
|
| PubChem CID |
4674
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.998 g/cm3
|
| 沸点 |
658.7ºC at 760 mmHg
|
| 熔点 |
226-228ºC
|
| 闪点 |
352.2ºC
|
| 折射率 |
1.611
|
| LogP |
-6.9
|
| tPSA |
180.93
|
| 氢键供体(HBD)数目 |
6
|
| 氢键受体(HBA)数目 |
8
|
| 可旋转键数目(RBC) |
4
|
| 重原子数目 |
13
|
| 分子复杂度/Complexity |
243
|
| 定义原子立体中心数目 |
0
|
| SMILES |
OC(P(O)(O)=O)(P(O)(O)=O)CCN
|
| InChi Key |
WRUUGTRCQOWXEG-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C3H11NO7P2/c4-2-1-3(5,12(6,7)8)13(9,10)11/h5H,1-2,4H2,(H2,6,7,8)(H2,9,10,11)
|
| 化学名 |
(3-amino-1-hydroxy-1-phosphonopropyl)phosphonic acid
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 本产品在运输和储存过程中需避光。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
H2O : ~5 mg/mL (~21.27 mM)
DMSO : ~1 mg/mL (~4.25 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 2 mg/mL (8.51 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶。
请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 4.2541 mL | 21.2703 mL | 42.5405 mL | |
| 5 mM | 0.8508 mL | 4.2541 mL | 8.5081 mL | |
| 10 mM | 0.4254 mL | 2.1270 mL | 4.2541 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。