| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
TGF-β-RI/ALK5 (transforming growth factor-beta receptor I/activin like kinase 5) (4 nM = IC50)
RepSox (SJN 2511) targets TGF-β type I receptor (also known as ALK5) with an IC50 value of 0.04 μM [1] RepSox (SJN 2511) exhibits high selectivity for ALK5 over other ALK family members (ALK1, ALK2, ALK3, ALK4) with IC50 values >10 μM, >10 μM, 5.2 μM, and >10 μM respectively [1] RepSox (SJN 2511) targets TGFβ receptor (ALK5) to block TGF-β-mediated signaling, with an IC50 of 0.04 μM consistent with previous reports [2] |
|---|---|
| 体外研究 (In Vitro) |
RepSox (GMP) (10 μM) 可诱导 MEF 分化为化学诱导多能干细胞 (CiPSC)[1]。 hCiPS 细胞由 RepSox (GMP)(10 μM,在 I-Stage III 诱导培养基中)从 HEF 诱导而来[2]。 EdU 掺入的增加证实 RepSox (GMP) 加 Forskolin 可以增加表达 MyoD 的 MEF 中增殖细胞的数量 [3]。
RepSox (SJN 2511) 呈剂量依赖性抑制ALK5激酶活性,在0.04 μM浓度下实现50%抑制 [1] RepSox (SJN 2511) 抑制Mv1Lu细胞中TGF-β1诱导的Smad2磷酸化,该细胞应答的EC50值为0.12 μM [1] RepSox (SJN 2511) 抑制转染3TP-Lux质粒(含TGF-β响应元件)的Mv1Lu细胞中TGF-β应答荧光素酶报告基因活性,1 μM浓度下可降低80%荧光素酶活性 [1] RepSox (SJN 2511) 诱导3T3-L1前脂肪细胞向棕色脂肪细胞分化,1 μM浓度下可使棕色脂肪细胞标志物UCP1、PGC-1α、PRDM16的mRNA表达分别上调12.8倍、4.5倍、3.2倍 [2] RepSox (SJN 2511) 促进白色脂肪细胞(分离自小鼠附睾白色脂肪组织)棕色化,0.5 μM浓度下可使UCP1蛋白水平上调5.3倍,线粒体含量(通过Mitotracker染色检测)增加2.7倍 [2] RepSox (SJN 2511) 阻断3T3-L1前脂肪细胞和白色脂肪细胞中TGF-β1诱导的Smad2/3磷酸化,1 μM浓度下可实现完全抑制 [2] RepSox (SJN 2511) 改变脂肪细胞脂滴形态(通过油红O染色观察),形成棕色脂肪细胞特征性的更小、更多的脂滴 [2] |
| 体内研究 (In Vivo) |
当注射到囊胚中时,RepSox 能够在体内有助于形成嵌合胚胎。用 RepSox 进行一天的治疗足以替代转基因 Sox2。
对高脂饮食喂养的C57BL/6小鼠给予RepSox (SJN 2511)(10 mg/kg,腹腔注射,每日一次,持续2周),可使附睾白色脂肪组织(eWAT)中UCP1的mRNA和蛋白表达分别上调7.2倍和4.8倍 [2] RepSox (SJN 2511) 增强小鼠棕色脂肪组织(BAT)活性,表现为BAT中线粒体DNA含量增加1.8倍,耗氧率提高2.1倍 [2] RepSox (SJN 2511) 使高脂饮食喂养的小鼠体重增长较对照组减少23%,且不影响进食量 [2] RepSox (SJN 2511) 改善高脂饮食喂养小鼠的糖耐量(曲线下面积减少31%)和胰岛素敏感性(胰岛素耐量试验曲线下面积减少27%) [2] |
| 酶活实验 |
ALK5荧光偏振结合试验。[1]
荧光偏振是一种在文献中有充分记载的方法。与荧光基团结合的激酶抑制剂化合物可以作为荧光配体来监测其他化合物与给定激酶的ATP竞争性结合。平面偏振光去极化的增加是由结合的配体释放到溶液中引起的,用极化/各向异性值来测量。在纯化的重组GST−ALK5(残基198−503)上检测化合物与ALK5的结合。用不同浓度的测试化合物取代罗丹明绿荧光标记的ATP竞争抑制剂24来计算结合pIC50。将GST−ALK5添加到含有62.5 mM Hepes, pH 7.5, 1 mM DTT, 12.5 mM MgCl2, 1.25 mM CHAPS和1 nM罗丹明绿色标记配体的缓冲液中,根据酶的活性位点滴定,最终ALK5浓度为10 nM。将酶/配体试剂40微升加入含有1 μL不同浓度化合物的384孔分析板中。在LJL Acquest荧光仪上立即读取,激发、发射和二向色滤光片分别为485、530和505 nm。Acquest计算每个孔的荧光偏振,然后导入曲线拟合软件,构建浓度-响应曲线。 ALK5自磷酸化试验。[1] 用PCR方法克隆了ALK5 (Franzen, P. 1993)(氨基酸162−503)的激酶结构域,并在杆状病毒/Sf9细胞系统中表达。该蛋白在C端被6-His标记,并通过Ni2+柱亲和层析纯化,获得的材料用于在自磷酸化实验中评估化合物的活性。纯化酶(10 nM)在50 μL Tris缓冲液中孵育(Tris 50 mM, pH 7.4;NaCl, 100 mM;MgCl2, 5 mM;MnCl2, 5 mM;和DTT, 10毫米)。将酶与不同浓度的化合物(试验中最终浓度为0.1% DMSO)在37℃下预孵育10分钟。然后加入3 μM ATP (0.5 μCi γ-33P-ATP)引发反应。在37°C下加热15分钟后,加入SDS - PAGE样品缓冲液(50 mM Tris-HCl, pH 6.9, 2.5%甘油,1% SDS和5% β-巯基乙醇)停止磷酸化。样品在95°C下煮沸5分钟,在12% SDS - PAGE上运行。干燥的凝胶暴露在荧光屏上过夜。使用Storm成像系统量化ALK5自磷酸化。 将重组ALK5激酶与特异性肽底物在ATP和不同浓度的RepSox (SJN 2511)(0.001-10 μM)存在下于30°C孵育60分钟。采用放射性闪烁法检测底物的磷酸化水平,相对于溶媒对照组计算激酶活性抑制率,通过四参数logistic模型拟合量效曲线确定IC50值 [1] 将重组ALK5蛋白固定在传感器芯片上,将不同浓度(0.01-5 μM)的RepSox (SJN 2511)注入芯片表面。利用表面等离子体共振(SPR)技术检测RepSox (SJN 2511)与ALK5的结合亲和力,通过传感图计算平衡解离常数(KD) [2] |
| 细胞实验 |
测定ALK5抑制剂抗tgf -β活性的细胞实验。[1]
化合物的活性在HepG2细胞中进行了转录试验。用PAI-1启动子驱动荧光素酶(萤火虫)报告基因稳定转染细胞。25与对照条件相比,稳定转染的细胞对TGF-β刺激的荧光素酶活性增加了10 - 20倍。 为检测化合物抗tgf -β活性,将细胞以35000个/孔的浓度接种于96孔微孔板中,接种于200 μL含血清培养基中。然后将微孔板置于37°C, 5% CO2 atm的细胞培养箱中24 h。在加入重组TGF-β (1 ng/mL)之前,将溶解于DMSO中的化合物以50 nM ~ 10 μM的浓度(DMSO的终浓度为1%)加入30min。孵育过夜后,用PBS洗涤细胞,加入10 μL被动裂解缓冲液裂解细胞。荧光素酶活性相对于对照组的抑制作用被用作化合物活性的测量。构建浓度-响应曲线,以图形方式确定IC50值。 将Mv1Lu细胞接种于6孔板,培养至80%汇合度。血清饥饿16小时后,用RepSox (SJN 2511)(0.01-1 μM)预处理细胞1小时,随后用TGF-β1(5 ng/mL)刺激30分钟。裂解细胞后,提取蛋白提取物进行western blot分析,使用磷酸化Smad2和总Smad2抗体评估对TGF-β信号通路的抑制作用 [1] 采用转染试剂将3TP-Lux报告质粒(含TGF-β响应元件)和海肾荧光素酶质粒(作为内参)转染至Mv1Lu细胞。转染24小时后,用RepSox (SJN 2511)(0.001-10 μM)和TGF-β1(5 ng/mL)处理细胞18小时。使用双荧光素酶报告基因检测系统测量荧光素酶活性,结果以海肾荧光素酶活性归一化 [1] 将3T3-L1前脂肪细胞接种于12孔板,在生长培养基中培养至汇合度。汇合后2天(第0天),加入含RepSox (SJN 2511)(0.1-1 μM)的分化培养基诱导分化。每2天更换一次培养基,第8天收集细胞,通过qPCR分析UCP1、PGC-1α、PRDM16的mRNA表达(以GAPDH为内参基因),并通过western blot分析UCP1的蛋白表达 [2] 通过胶原酶消化从小鼠eWAT中分离白色脂肪细胞,接种于6孔板。贴壁后,用RepSox (SJN 2511)(0.1-0.5 μM)处理细胞4天。进行油红O染色观察脂滴形态,通过Mitotracker染色在荧光显微镜下评估线粒体含量 [2] |
| 动物实验 |
雄性C57BL/6小鼠(6周龄)喂食高脂饮食(60%能量来自脂肪)4周以诱导肥胖。小鼠随机分为两组:对照组(n=8)和RepSox(SJN 2511)治疗组(n=8)。RepSox(SJN 2511)溶于DMSO和生理盐水的混合溶液中(DMSO终浓度<1%),以10 mg/kg的剂量腹腔注射,每日一次,持续2周。对照组注射等体积的溶剂。实验期间,每2天记录一次小鼠的体重和食物摄入量。在治疗的最后3天,使用代谢笼测量能量消耗。在处死前1天进行葡萄糖耐量试验(腹腔注射葡萄糖,2 g/kg)和胰岛素耐量试验(腹腔注射胰岛素,0.75 U/kg)。处死小鼠后,收集附睾白色脂肪组织(eWAT)、棕色脂肪组织(BAT)和肝脏组织,用于后续的基因和蛋白质表达分析[2]。
|
| 参考文献 |
[1]. Identification of 1,5-naphthyridine derivatives as a novel series of potent and selective TGF-beta type I receptor inhibitors. J Med Chem. 2004 Aug 26;47(18):4494-506.
[2]. RepSox, a small molecule inhibitor of the TGFβ receptor, induces brown adipogenesis and browning of white adipocytes. Acta Pharmacol Sin. 2019 Dec;40(12):1523-1531. |
| 其他信息 |
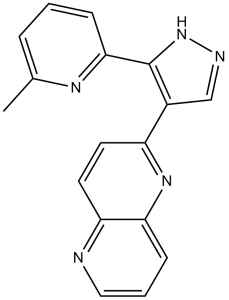
1,5-萘啶,2-[3-(6-甲基-2-吡啶基)-1H-吡唑-4-基]-是一种吡唑并吡啶类化合物。
对筛选先导化合物1进行优化,鉴定出新型1,5-萘啶氨基噻唑和吡唑衍生物,它们是转化生长因子-β I型受体ALK5的强效选择性抑制剂。化合物15和19分别以IC50 = 6 nM和4 nM抑制ALK5的自磷酸化,在结合和细胞实验中均显示出强效活性,并且对p38丝裂原活化蛋白激酶具有选择性。本文描述了化合物 19 与人 ALK5 复合物的 X 射线晶体结构,证实了分子对接研究提出的结合模式。[1] 与白色脂肪组织 (WAT) 不同,棕色脂肪组织 (BAT) 主要通过解偶联呼吸链进行产热来消耗能量。促进棕色脂肪前体细胞分化和白色脂肪褐变已成为治疗肥胖症及相关代谢疾病的研究热点。目前已发现多种分泌因子和一些小分子能够促进棕色脂肪生成。本文报道,单一小分子化合物 RepSox 足以在成纤维细胞培养基中诱导小鼠胚胎成纤维细胞 (MEF) 发生脂肪生成。 RepSox是转化生长因子-β受体I(TGF-β-RI)的抑制剂,其他TGF-β通路抑制剂,如SB431542、LY2157299、A83-01和曲尼司特,也能有效诱导MEF细胞分化为脂肪细胞。这些脂肪细胞表达棕色脂肪细胞特异性转录因子和产热基因,含有大量线粒体,并具有较高的线粒体呼吸活性。更有趣的是,RepSox还被发现能够促进棕色脂肪前体细胞的分化,并诱导白色脂肪前体细胞褐变。这些研究结果表明,TGF-β信号通路抑制剂可能被开发为治疗肥胖症和2型糖尿病的新疗法。[2] RepSox (SJN 2511)是一种新型的1,5-萘啶衍生物,被设计为选择性ALK5抑制剂,其通过与ALK5的ATP结合口袋结合并阻止ATP结合而发挥抑制作用。[1] RepSox (SJN 2511)通过双重机制调节脂肪细胞命运:阻断TGF-β/ALK5/Smad信号通路(抑制棕色脂肪生成)和激活PPARγ-PGC-1α转录轴(促进棕色脂肪标志物表达)[2] |
| 分子式 |
C17H13N5
|
|---|---|
| 分子量 |
287.32
|
| 精确质量 |
287.117
|
| 元素分析 |
C, 71.06; H, 4.56; N, 24.37
|
| CAS号 |
446859-33-2
|
| 相关CAS号 |
RepSox;446859-33-2
|
| PubChem CID |
449054
|
| 外观&性状 |
Light brown to yellow solid powder
|
| 密度 |
1.3±0.1 g/cm3
|
| 沸点 |
501.9±50.0 °C at 760 mmHg
|
| 熔点 |
195 °C
|
| 闪点 |
230.5±23.1 °C
|
| 蒸汽压 |
0.0±1.2 mmHg at 25°C
|
| 折射率 |
1.692
|
| LogP |
1.28
|
| tPSA |
67.35
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
4
|
| 可旋转键数目(RBC) |
2
|
| 重原子数目 |
22
|
| 分子复杂度/Complexity |
376
|
| 定义原子立体中心数目 |
0
|
| InChi Key |
LBPKYPYHDKKRFS-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C17H13N5/c1-11-4-2-5-16(20-11)17-12(10-19-22-17)13-7-8-14-15(21-13)6-3-9-18-14/h2-10H,1H3,(H,19,22)
|
| 化学名 |
2-[3-(6-methyl-2-pyridinyl)-1H-pyrazol-4-yl]-1,5-naphthyridine
|
| 别名 |
E-616452, SJN 2511; E 616452; 446859-33-2; 2-(3-(6-Methylpyridin-2-yl)-1H-pyrazol-4-yl)-1,5-naphthyridine; ALK5 Inhibitor II; ALK5 Inhibitor; SJN 2511; 2-[5-(6-methylpyridin-2-yl)-1H-pyrazol-4-yl]-1,5-naphthyridine; C17H13N5; E616452; RepSox; SJN-2511; SJN-2511; ALK5 Inhibitor II
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 7.5 mg/mL (26.10 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 75.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 7.5 mg/mL (26.10 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 75.0mg/mL澄清的DMSO储备液加入到900μL 20%SBE-β-CD生理盐水中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 1.67 mg/mL (5.81 mM) (饱和度未知) in 5% DMSO + 40% PEG300 + 5% Tween80 + 50% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: ≥ 1.67 mg/mL (5.81 mM) (饱和度未知) in 5% DMSO + 95% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 配方 5 中的溶解度: ≥ 0.33 mg/mL (1.15 mM) (饱和度未知) in 1% DMSO 99% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.4804 mL | 17.4022 mL | 34.8044 mL | |
| 5 mM | 0.6961 mL | 3.4804 mL | 6.9609 mL | |
| 10 mM | 0.3480 mL | 1.7402 mL | 3.4804 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。