| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
UBA1(IC50= 1 nM)
|
|---|---|
| 体外研究 (In Vitro) |
TAK-243 (MLN7243) 选择性杀死皮肤鳞状细胞癌 (cSCC) 系的子集。鳞状细胞癌移植 (SCCT) 和 SCCRDEBMet 细胞对 TAK-243 的持续治疗最敏感。 SCCIC1Met 细胞也会因长期暴露于 TAK-243 而被选择性杀死。 SCCRDEBMet 细胞的死亡对 TAK-243 脉冲表现出最大的敏感性。 MLN7243 可以降低泛素缀合物的细胞水平。 TAK-243 降低 UBA1 和 UBA6 硫酯以及 UBA6 特异性 E2 UBE2Z/USE1 的硫酯[1]。与正常造血细胞相比,TAK-243 对急性髓系白血病 (AML) 细胞表现出优先活性。 TAK-243 以浓度和时间依赖性方式降低人 AML 细胞系(OCI-AML2、TEX、U937 和 NB4)的生长和活力,处理 48 小时后 IC50 范围为 15-40 nM[2]。
TAK-243形成TAK-243-泛素加合物,并在体外有效抑制阿联酋。[1] TAK-243抑制短寿命蛋白质的周转并破坏细胞周期进程。[1] TAK-243诱导无法解决的内质网应激。[1] TAK-243治疗改变DNA损伤修复。[1] TAK-243在人癌症细胞中具有抗增殖活性。[1] |
| 体内研究 (In Vivo) |
TAK-243 显着延迟小鼠肿瘤生长 (T/C=0.02),且无毒性,小鼠体重、血清化学或器官组织学没有变化,证明了这一点。 TAK-243 降低了两个测试样本中的原发性 AML 肿瘤负荷,且无毒性[2]。
在证明肿瘤中存在大量TAK-243暴露后,我们接下来评估了TAK-243与阿联酋的靶点结合以及肿瘤样本中的下游通路调节。我们开发了免疫组织化学(IHC)检测方法来分析与阿联酋抑制相关的几种药效学(PD)生物标志物。针对TAK-243-泛素加合物(MIL90)产生的单克隆抗体用于监测肿瘤中阿联酋靶点的参与。使用几种生物标志物评估下游通路抑制;抗体用于检测多泛素化和单泛素化蛋白(使用FK2抗体,检测所有细胞形式的泛素结合物)、单泛素基化组蛋白H2B和切割的半胱氨酸天冬氨酸蛋白酶-3(作为凋亡的衡量标准)。携带WSU-DLCL2淋巴瘤或PHTX-132Lu(原发性NSCLC)异种移植物肿瘤组织的小鼠使用最大耐受剂量的TAK-243单次静脉注射给药。通过TAK-243-泛素加合物的存在评估的阿联酋靶点参与和下游通路抑制在肿瘤组织中都很明显(图3a)。单次给药后,TAK-243诱导了快速而持久的PD反应(图3b,c),与肿瘤组织中明显的UAE抑制一致。在评估的PD生物标志物中,最敏感地检测到加合物的形成,并且可以在非常低的TAK-243剂量(每公斤体重3毫克(mg/kg)是检查的最低剂量)下检测到加成物,这不足以调节下游PD读数(多泛素或单泛素化组蛋白H2B)或抗肿瘤疗效(数据未显示)。加合物可以在下游生物标志物调节前0.5-1.0小时检测到,这种滞后可能是由于检测灵敏度、从头开始的阿联酋合成和肿瘤中药物洗脱随时间变化的差异造成的。值得注意的是,在其最大耐受剂量下,TAK-243对HCT-116异种移植物中NAE依赖性neddylated cullin水平的抑制作用可以忽略不计,尽管对多泛素形成和泛素化组蛋白H2B水平有显著抑制作用(补充图11a,b)。这些数据表明,TAK-243深刻影响下游阿联酋生物标志物,而对体内NAE相关生物标志物几乎没有影响。[1] TAK-243在体内具有阿联酋特异性抗肿瘤功效[1] TAK-243的抗肿瘤活性是通过一组代表实体癌和血液癌的人类患者来源和细胞系来源的异种移植物(分别为PDX和CDX)肿瘤模型来测定的。我们使用以下CDX模型在小鼠体内建立皮下肿瘤:WSU-DLCL2(弥漫性大B细胞淋巴瘤)、HCT-116(结肠癌)、THP-1(急性髓细胞白血病)、CWR22(前列腺癌症)、Calu-6(肺,非小细胞腺癌(NSCLC))、HCC70(癌症三阴性乳腺癌)和MM1.S(多发性骨髓瘤),以及以下人类原发性PDX模型:PHTX-24c(结肠癌)、PHTX-132Lu(肺,NSCLC)、PHTX-55B(癌症三阴性乳腺病)、PHTX-235O(卵巢癌)癌症)和HNM626(颈部癌症)。携带肿瘤的小鼠服用TAK-243 3周,每周静脉注射两次(例如,周一和周四;表示为BIW),并监测肿瘤生长和动物体重。TAK-243治疗在所有检查的模型中都诱导了明显而强烈的抗肿瘤活性反应(图4、表2和补充图12a)。在体外和体内用TAK-243处理的人类癌症细胞系在敏感性上保持相似的等级顺序。TAK-243抑制小鼠和人类阿联酋,因为在小鼠组织中可检测到TAK-243-泛素加合物形成和下游PD读数(数据未显示);因此,小鼠可用于初步评估TAK-243的治疗窗口。在小鼠中观察到的剂量限制毒性是体重下降。在体内最大耐受剂量(23-26mg/kg)下,与治疗开始前相比,平均最大体重减轻<动物体重的12%(补充图12b)。 |
| 酶活实验 |
生化测定。[1]
在不同浓度的TAK-243存在下,随着时间的推移监测E1-UBL依赖性焦磷酸盐交换(PPiX)活性,以评估E1失活率。反应在1mM ATP存在下进行,反应方案和曲线拟合分析与之前描述的类似34。在TAK-243-UBL形成后,使用E1-E2 HTRF转巯基化试验,使用之前描述的回收方法的改进版本,评估了UAE、NAE和SAE的回收率。HTRF E2转巯基化试验用于确定UBA6抑制剂对重组纯化的UAE、NAE和SAE的IC50值。该测定如前所述进行。使用使用类似条件的AlphaScreen E2转巯基化测定格式来测量UBA6抑制剂对重组纯化UBA6的IC50值。使用生物素标记的USE1酶代替GST标记的E2。对于基于HTRF的定量中使用的抗体,使用6μg/ml链霉抗生物素蛋白偶联供体珠和15μg/ml抗Flag偶联受体珠进行检测。在KM处存在ATP浓度的情况下,测定每种E1酶的UBA6i IC50滴度。 体外E2∼UBL硫酯测定。[1] HTRF E2转巯基化试验用于对重组、纯化的UAE、NAE、SAE和ATG7酶进行TAK-243 IC50研究。该测定按照之前描述的5,14,35进行。使用类似条件的AlphaScreen E2转巯基化测定格式用于UBA6和UBA7。使用生物素化标记的E2酶代替GST标记的E2。使用6μg/ml链霉抗生物素蛋白偶联供体珠和15μg/ml抗Flag偶联受体珠代替HTRF检测抗体进行检测。在KM处ATP浓度存在的情况下,测定每种E1酶的TAK-243 IC50滴度。 结晶和结构测定。[1] 所有用于结晶研究的蛋白质构建体和试剂都是以类似于之前描述的方式产生的5。由于UAE的人类形态结晶困难,所有研究都使用了UAE的人源化酵母版本(也称为酿酒酵母的Uba1,UniProtKB P22515)。尽管酵母和人类阿联酋之间存在序列差异,但活性位点残基高度保守。例如,在TAK-243结合位点5Å内的25个残基中,有21个是相同的。此外,文献中详细记录了使用酵母UAE晶体结构作为模型系统来描述人类UAE的酶机制。基于人和酵母UAE活性位点的两个残基氨基酸差异,将Asn471Met和Lys519Arg(酵母编号)的取代物引入到酵母UAE的截短形式中(残基10-1024)。这两个替换是使TAK-243的效力与人类酶一致所必需的(数据未显示)。通过混合人源化酵母UAE、TAK-243、泛素和ATP-MgCl2形成晶体。将晶体短暂转移到冷冻保护剂(保持在冰上)中,冷冻保护剂由80%的储液(0.2 M甲酸镁,0.1 M Bis-Tris pH 6.5)和20%的聚乙二醇(PEG)-400组成,并在液氮中快速冷却。使用现有的酵母UAE坐标(蛋白质数据库(PDB)条目3CMM)作为起始模型,通过分子替换解决了该结构。使用Coot程序完成了模型的手动重建,并使用Refmac的CCP4i图形界面进行了细化。坐标已存入PDB,结构代码为5TR4。晶体学数据收集和细化统计见附表1。 激酶panel。[1] 在Reaction Biology Corporation进行的研究中,测量了TAK-243(1μM)对319种激酶的抑制活性。结果以激酶活性抑制百分比(对照百分比)表示。简而言之,激酶特异性底物在以下反应缓冲液中制备:20 mM 4-(2-羟乙基)哌嗪-1-乙磺酸(HEPES)(pH 7.5)、10 mM MgCl2、1 mM乙二醇四乙酸(EGTA)、0.02%Brij-35、0.02 mg/ml牛血清白蛋白(BSA)、0.1 mM Na3VO4、2 mM二硫苏糖醇(DTT)和1%DMSO。将每种测定特有的辅因子添加到底物溶液中。将待测激酶加入反应混合物中,将[α-32P]ATP(比活10μCi/μl)加入反应中并混合。将反应物在室温下孵育120分钟,然后将反应物点样在P81离子交换纸上。过滤器在0.75%磷酸中洗涤,并测量和分析放射性。Staurosporine被列为对照化合物。有关所测试激酶的完整列表,请参阅补充表2。 碳酸酐酶测定。[1] TAK-243通过将TAK-243滴定到含有25 nM人碳酸酐酶(HCA)-I或2.5 nM HCA-II与25μM荧光素二乙酸酯的反应中来确定IC50值(测定缓冲液:25 mM MOPS,pH 7.5和0.02%Triton-X100)。使用BMG Labtech Polarstar读数器在485nm的激发波长和520nm的发射波长下随时间测量碳酸酐酶的活性。该测定被格式化为基于荧光素释放乙酸盐的信号增益测定(缓解荧光素的淬灭)。通过将滴定曲线拟合到标准逻辑回归模型来计算IC50值。HCA-I和HCA-II数据请参考补充表2。 |
| 细胞实验 |
将正常角质形成细胞(正常人角质形成细胞 (NHK) 和隐性营养不良性大疱性表皮松解症角质形成细胞 (RDEBK))和 cSCC 细胞系接种到 96 孔板中,并使用 IncuCyte ZOOM 实时成像仪和 CellTox Green 分析活细胞数量和细胞死亡细胞毒性测定。相对 EC50 值使用 GraphPad Prism 测定。对于克隆形成测定,将细胞接种到六孔板中。按指定时间添加抑制剂(例如 TAK-243;0.01、0.1、1 和 10 μM),然后将细胞在无药物培养基中维持长达 2 周,以形成集落。将菌落固定在 10% 甲醇、10% 乙酸中,并用结晶紫染色[1]。
蛋白质印迹分析。[1] HCT-116和WSU-DLCL2细胞在McCoy的5A改良或RPMI-1460培养基中保持对数期生长,分别在37°C和5%CO2培养箱中补充10%胎牛血清。细胞在6孔细胞培养皿中生长,用DMSO(0.1%)或0.01、0.10或1.00μM的TAK-243处理指定时间。使用RIPA缓冲液制备全细胞提取物。如前所述,在非还原(E2硫酯)或还原条件下进行SDS-PAGE后,进行免疫印迹(除非另有说明,否则所有抗体均以1:1000的稀释度使用)3;通过SDS-PAGE对30μg总蛋白进行分级,并用以下蛋白质的一抗进行免疫印迹。 细胞硫酯测定。[1] 在6孔细胞培养皿中生长的HCT-116细胞用DMSO(0.1%)或增加浓度的TAK-243处理4小时,并使用RIPA缓冲液制备全细胞提取物。用于检测E2-UBL硫酯的细胞裂解物在非还原条件下通过SDS-PAGE进行分级,并用UBCH10、USE1、UBC12、UBC9和ATG7的一抗进行免疫印迹。使用小鼠或兔特异性Alexa-Fluor-680结合的二抗(有关所用所有抗体的信息,请参阅补充表3),并使用Li-Cor Odyssey红外成像系统对印迹进行成像。为了分析参与DNA损伤修复的E2硫酯,将HCT-116细胞与DMSO或TAK-243一起培养8小时。使用以下抗体在免疫印迹上检测E2-泛素硫酯:UBE2A和UBE2B、泛素结合酶E2 T(UBE2T)、增殖细胞核抗原、范可尼贫血互补组D2(FANCD2)和UBE1。所有一抗和二抗均以1:1000的稀释度使用。完整的抗体列表请参考补充表3,未剪切的蛋白质印迹图像请参考补充图15。 细胞周期分析。[1] 对数生长的HCT-116细胞(以6×105铺板)与DMSO、pevonidistat(0.25μM)或TAK-243(0.05μM或1μM)一起孵育16小时。收集细胞,用70%乙醇固定,在4°C下储存过夜。将固定的细胞离心并用PBS洗涤以去除乙醇。将颗粒在避光的冰上重新悬浮在碘化丙啶和PBS中的RNAse A中1小时。使用流式细胞术确定细胞周期分布,并使用BD FACSDeva软件版本6.1.1完成分析。门控策略由未经处理的对照细胞的正向(FSC)或侧向(SSC)散射来定义。对活的单PI阳性细胞进行门控,用于细胞周期分析(补充图16)。每个分析样本记录了10000个总事件和5000个门控事件。 Lys48免疫荧光法。[1] 将HCT-116细胞(1.5×104个细胞/孔)铺在96孔细胞培养板上,在37°C和5%CO2下孵育24小时以进行附着。将浓度逐渐增加的TAK-243添加到培养板中(起始浓度为20μM),并在37°C和5%CO2下培养3.5小时。细胞在2%多聚甲醛中固定10分钟,然后在室温下在0.5%Triton X-100中渗透10分钟。细胞在室温下用罗氏阻断缓冲液阻断1小时。将泛素Lys48特异性的第一抗体与细胞在室温下孵育1小时。使用Alexa-Fluor-488偶联的山羊抗兔IgG(目录号A-11034,Invitrogen;1:500)作为第二抗体,并在室温下与细胞孵育1小时。使用Opera共焦高内容筛选成像系统对图像进行分析。 内质网(ER)扩张的CellLights显微镜。[1] HCT-116细胞用CellLight ER-RFP、BacMam 2.0以20的感染复数(MOI)转导,24小时后用DMSO或0.1μM TAK-243处理,时间如补充图6所示。用该化合物处理后,将细胞加入一个保持在37°C、5%CO2的加湿室中,并连接到配备有自动xyz载物台、滤光轮和由MetaMorph软件控制的Orca ER相机的Eclipse TE2000-U显微镜(尼康仪器)上。 彗星试验。[1] 将Calu-6细胞以0.2×106个细胞/孔的密度接种到6孔培养皿中。在暴露于紫外线处理(20 J/m2)之前,用DMSO或1μMTAK-243处理细胞1小时。紫外线处理后,在t=0分钟时收获细胞,或在1μM TAK-243存在或不存在的情况下孵育6小时。根据Trevigen CometAssay方案进行碱性彗星试验的准备和执行。在21V的恒定电压下,用碱性缓冲液(含有200mM NaOH和1mM EDTA的pH 13溶液)在30分钟内进行电泳。在水中中和并用70%乙醇固定后,让载玻片干燥,最后在4°C下用1:5000稀释的SYBR绿在1×PBS中染色5分钟。在蒸馏水中快速再水化步骤后,使用4×泛荧光物镜在imageXpress MICRO上对载玻片进行成像。使用Comet Assay IV软件测量彗尾。 细胞活力测定。[1] 根据制造商的说明,细胞系在每种细胞系的适当细胞培养基中保持对数生长。在浓度逐渐增加的TAK-243存在下,将细胞在适当的完整培养基中一式三份铺在384孔培养板上,并在37°C下孵育72小时。根据制造商的方案,使用Cell Titer Glo检测试剂盒评估细胞存活率。 |
| 动物实验 |
小鼠[2]
TAK-243 的临床前疗效和毒性采用 AML 小鼠模型进行评估。将 OCI-AML2 细胞皮下注射到 SCID 小鼠体内,待肿瘤可触及后,给予小鼠 TAK-243(20 mg/kg,皮下注射,每周两次)。在另一个模型中,将来自两名患者的原代 AML 细胞注射到 NOD-SCID 小鼠的股骨中。注射两周后,给予小鼠 TAK-243(20 mg/kg,皮下注射,每周两次)。经过三周的治疗后,处死小鼠,并使用流式细胞术定量分析未注射股骨中 AML 的移植量[2]。 人类肿瘤体内异种移植模型的构建及疗效研究。[1] 将 8 至 12 周龄的小鼠侧腹皮下接种肿瘤碎片或无血清培养基中的肿瘤细胞悬液。雌性CB-17 SCID小鼠用于以下肿瘤模型:WSU-DLCL2(4.0 × 10⁶个细胞/只小鼠)、MM1.S(5.0 × 10⁶个细胞/只小鼠)、PHTX-132Lu(原发性非小细胞肺癌,2 × 3 mm肿瘤组织块)、THP-1(4.0 × 10⁶个细胞/只小鼠)、PHTX-24c(原发性结肠癌,2 × 3 mm肿瘤组织块)和THP-1 UBA3 A171T(先前已描述)。雄性CB-17 SCID小鼠用于CWR22模型(2 × 3 mm肿瘤组织块)。雌性CB-17 SCID小鼠(Taconic)用于PHTX-55B模型(原发性乳腺癌,2 × 3 mm肿瘤组织块)。免疫缺陷型雌性NOD SCID小鼠用于PHTX-235O模型(原发性卵巢癌,2 × 3 mm肿瘤组织块)。 mm肿瘤碎片)。HCT-116和Calu-6模型采用雌性裸鼠(Taconic)(5.0 × 10⁶个细胞/只)。CrownBio采用HNM626模型进行实验,将3 × 3 × 3 mm的肿瘤碎片植入雌性裸鼠的侧腹部。Medicilon采用HCC-70模型进行实验,将5.0 × 10⁶个细胞/只植入雌性裸鼠的侧腹部。 使用游标卡尺监测肿瘤生长。平均肿瘤体积的计算公式为:体积 (V) = W² × L/2,其中W和L分别为肿瘤的宽度和长度。当平均肿瘤体积达到约200 mm³时,将动物随机分为n = 6-10只一组(取决于模型)。我们的随机化方法采用了一种称为最小化的技术。为了减少各组小鼠基线特征的不平衡,我们采用了以下方法。具体而言,我们的方法减少了平均肿瘤体积和初始平均动物体重的不平衡。首先,我们使用简单随机化方法生成了大量候选设计,其中每组动物数量固定的每种可能设计出现的概率均等。候选设计的数量并非固定不变,而是不断添加新的候选设计,直到总计算时间达到 3 秒。对于每个候选设计,我们计算了其总体不平衡度。总体不平衡度定义为两项之和:第一项是各组肿瘤体积均值的方差除以总体体积均值的平方;第二项是各组动物体重均值的方差除以总体体重均值的平方。选择总体不平衡度最低的候选设计作为最终设计。每组小鼠的数量用于计算统计显著性。小鼠分别接受 20% 2-羟丙基-β-环糊精 (HPbCD) 或在为期 21 天的 BIW 给药方案下,对小鼠进行 TAK-243 治疗;未采用盲法。每周测量两次肿瘤生长和体重。在最后一次给药后 5 天内计算 TGI 百分比(对照组平均肿瘤体积 (MTV) – 治疗组 MTV / 对照组 MTV),统计分析方法如前所述43。 TAK-243联合放疗疗效实验。[1] 实验在中国无锡进行,将约30 mm³的肿瘤组织切片皮下植入6至9周龄的雌性BALB/c裸鼠右侧腹部,肿瘤组织切片分别取自LU-01-0030肿瘤组织(人非小细胞肺癌患者来源异种移植(PDX)模型)或BR-05-0026肿瘤组织(乳腺癌PDX模型)。当平均肿瘤体积达到约159 mm³(LU-01-0030)或177 mm³(BR-05-0026)时,将动物随机分为四组。TAK-243按每周两次(BIW)方案静脉给药,持续3周,具体给药日期见补充图8。在指定日期,采用2 Gy的聚焦放射线进行照射。治疗使用Rad Source RS-2000 X射线照射器。照射前,小鼠经腹腔注射1.0%戊巴比妥钠(80 mg/kg)麻醉。每只小鼠均以1 Gy/min的速率接受聚焦放射线照射。每周使用游标卡尺测量两次肿瘤大小。肿瘤体积的计算公式为:0.5 × (长 × 宽²)。在整个研究期间,每周测量约两次肿瘤大小和体重。当肿瘤体积达到约1000 mm³时,对小鼠实施安乐死。在第0至21天评估协同抗肿瘤作用。所有肿瘤体积在进行log10转换前均加1。对于每只小鼠,从后续各天的肿瘤体积对数中减去第0天的肿瘤体积对数。利用梯形法则,根据该差值随时间的变化计算每只动物的曲线下面积(AUC)值。药物A和B联合用药的协同评分定义为: 其中,AUCAB、AUCB和AUCctl分别代表联合用药组、A组、B组和对照组动物的AUC值。协同评分的标准误差基于动物间AUC值的变异性计算得出。采用双侧t检验来确定协同评分是否显著异于零。如果 P 值低于 0.05,且协同评分小于零,则认为该组合具有协同作用。 药代动力学 (PK) 分析。[1] 携带 WSU-DLCL2 NHL 异种移植瘤的 SCID 小鼠单次静脉注射 12.5、18.75 和 25 mg/kg 的 TAK-243(溶于 20% 羟丙基-β-环糊精溶液中),并在 72 小时内收集肿瘤和血浆样本。采用液相色谱-串联质谱 (LC/MS/MS) 方法测定 TAK-243 的暴露量,血浆和肿瘤的定量下限 (LLOQ) 分别为 1 nM 和 5 nM。 |
| 药代性质 (ADME/PK) |
TAK-243在荷瘤小鼠体内的药代动力学和药效学分析[1]
我们对免疫缺陷的CB-17 SCID小鼠(皮下接种弥漫性大B细胞淋巴瘤(WSU-DLCL2)肿瘤)在急性静脉注射TAK-243后,其药代动力学(PK)参数进行了表征。分析了这些小鼠的血浆和WSU-DLCL2肿瘤组织中TAK-243的暴露情况。在血浆中,TAK-243母体化合物的特征是清除率(CL)高(3.99至4.99升/小时/公斤体重(升/小时/公斤))和末端半衰期(t1/2)短(0.2-0.4小时)(补充图10a)。 TAK-243 可迅速形成 TAK-243-泛素加合物,而我们的药代动力学测量并未考虑以泛素加合物形式被隔离的 TAK-243。尽管 TAK-243 的血浆清除率很高,但该药物在稳态下的分布容积 (Vss) 仍然很高 (1.13–1.74 升/小时/公斤),其在肿瘤组织中的药时曲线下面积 (AUC) 比在血浆中高 5.8 至 8 倍,且肿瘤半衰期 (t1/2) 延长至 16.9–20.6 小时(补充图 10b)。[1] |
| 参考文献 |
|
| 其他信息 |
TAK-243 正在进行临床试验 NCT03816319(TAK-243 用于治疗复发或难治性急性髓系白血病、难治性骨髓增生异常综合征或慢性粒单核细胞白血病患者)。
UAE 抑制剂 TAK-243 是一种小分子泛素激活酶 (UAE) 抑制剂,具有潜在的抗肿瘤活性。UAE 抑制剂 TAK-243 与 UAE 结合并抑制其活性,从而阻止蛋白质泛素化及其后续被蛋白酶体降解。这会导致细胞内蛋白质过量,并可能引发内质网 (ER) 应激介导的细胞凋亡。这可以抑制肿瘤细胞的增殖和存活。 UAE,也称为泛素E1酶(UBA1;E1),在癌细胞中的活性高于正常健康细胞。 泛素-蛋白酶体系统(UPS)由一系列酶组成,负责维持细胞蛋白质稳态。包括蛋白酶体抑制剂和免疫调节酰亚胺类药物(IMiDs)在内的多种UPS调节剂的临床成功验证了该通路的治疗潜力。本研究发现TAK-243(曾用名MLN7243)是一种强效的、基于机制的小分子泛素激活酶(UAE)抑制剂。UAE是哺乳动物中主要的E1酶,负责调节泛素化级联反应。TAK-243处理导致细胞内泛素缀合物耗竭,进而破坏信号传导事件,诱导蛋白毒性应激,并损害细胞周期进程和DNA损伤修复通路。 TAK-243 治疗可导致癌细胞死亡,并且在原代人异种移植研究中,在耐受剂量下表现出抗肿瘤活性。由于其特异性和效力,TAK-243 可用于研究泛素生物学,并评估 UAE 抑制作为一种新的癌症治疗方法。[1] |
| 分子式 |
C19H20F3N5O5S2
|
|---|---|
| 分子量 |
519.517811775208
|
| 精确质量 |
519.085
|
| 元素分析 |
C, 43.93; H, 3.88; F, 10.97; N, 13.48; O, 15.40; S, 12.34
|
| CAS号 |
1450833-55-2
|
| PubChem CID |
71715374
|
| 外观&性状 |
White to off-white crystalline solid
|
| 密度 |
1.8±0.1 g/cm3
|
| 折射率 |
1.712
|
| LogP |
1.49
|
| tPSA |
186
|
| 氢键供体(HBD)数目 |
4
|
| 氢键受体(HBA)数目 |
13
|
| 可旋转键数目(RBC) |
7
|
| 重原子数目 |
34
|
| 分子复杂度/Complexity |
804
|
| 定义原子立体中心数目 |
4
|
| SMILES |
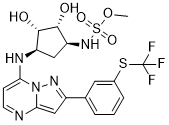
S(=O)(=O)(OC[C@@H]1[C@@H](O)[C@@H](O)[C@H](NC2=CC=NC3N2N=C(C=3)C2C=C(SC(F)(F)F)C=CC=2)C1)N
|
| InChi Key |
PUMGWJMQPGYZFC-IDCJVQTKSA-N
|
| InChi Code |
InChI=1S/C19H20F3N5O5S2/c1-32-34(30,31)26-14-8-13(17(28)18(14)29)24-15-5-6-23-16-9-12(25-27(15)16)10-3-2-4-11(7-10)33-19(20,21)22/h2-7,9,13-14,17-18,24,26,28-29H,8H2,1H3/t13-,14+,17+,18-/m1/s1
|
| 化学名 |
methyl ((1S,2R,3S,4R)-2,3-dihydroxy-4-((2-(3-((trifluoromethyl)thio)phenyl)pyrazolo[1,5-a]pyrimidin-7-yl)amino)cyclopentyl)sulfamate
|
| 别名 |
TAK-243; TAK 243; TAK243; MLN7243; 1450833-55-2; Uae inhibitor Sulfamic acid, [(1R,2R,3S,4R)-2,3-dihydroxy-4-[[2-[3-[(trifluoromethyl)thio]phenyl]pyrazolo[1,5-a]pyrimidin-7-yl]amino]cyclopentyl]methyl ester; TAK 243; UNII-V9GGV0YCDI; MLN-7243; MLN 7243; AOB87172; AOB-87172; AOB 87172
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : 50~100 mg/mL ( 96.24~192.48 mM )
Ethanol : ~25 mg/mL Water : ~1 mg/mL (~1.92 mM ) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (4.00 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.08 mg/mL (4.00 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.08 mg/mL (4.00 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: 5% DMSO + 40% PEG300 + 5% Tween80 + 50% ddH2O: 5mg/ml 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.9249 mL | 9.6243 mL | 19.2485 mL | |
| 5 mM | 0.3850 mL | 1.9249 mL | 3.8497 mL | |
| 10 mM | 0.1925 mL | 0.9624 mL | 1.9249 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT03816319 | Not yet recruiting | Drug: UAE Inhibitor TAK-243 | Myelodysplastic Syndrome Recurrent Acute Myeloid Leukemia |
National Cancer Institute (NCI) |
November 6, 2023 | Phase 1 |
| NCT02045095 | Terminated | Drug: MLN7243 | Advanced Malignant Solid Tumors | Millennium Pharmaceuticals Inc |
January 31, 2014 | Phase 1 |