| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
Src, in HuH7 cells (GI50 = 9 nM); Src, in PLC/PRF/5 cells (IC50 = 13 nM);
Src, in Hep3B cells (IC50 = 26 nM); Src, in HepG2 cells (IC50 = 60 nM) Tirbanibulin Mesylate, also known as KX2-391 Mesylate, is a substrate-specific Src inhibitor. The hepatic cell cancer (HCC) cell lines Huh7 (GI50=9 nM), PLC/PRF/5 (GI50=13 nM), Hep3B (GI50=26 nM), and HepG2 (GI50=60 nM) exhibit steep dose-response curves when exposed to tirbanibulin (KX2-391)[1]. It has been discovered that tirbanibulin mesylate (KX2-391 mesylate) inhibits some leukemia cells, such as those derived from chronic leukemia cells with the T3151 mutation, that are resistant to currently available commercial drugs. In NICH3T3/c-Src527F and SYF/c-Src527F cells, tirbanibulin mesylate (KX2-391 mesylate) is assessed in engineered Src driven cell growth assays and displays GI50 values of 23 nM and 39 nM, respectively[2]. |
|---|---|
| 体外研究 (In Vitro) |
体外活性:KX2-391 是一种 Src 抑制剂,针对 Src 底物袋。 KX2-391 显示针对 Huh7 (GI 50 = 9 nM)、PLC/PRF/5 (GI 50 = 13 nM)、Hep3B (GI 50 = 26 nM) 和 HepG2 (GI 50 = 60 nM) 的陡峭剂量反应曲线,四种肝细胞癌(HCC)细胞系。 KX2-391被发现可以抑制某些对目前市售药物有抗药性的白血病细胞,例如那些源自具有T3151突变的慢性白血病细胞的细胞。 KX2-391 在 NIH3T3/c-Src527F 和 SYF/c-Src527F 细胞中的工程化 Src 驱动细胞生长测定中进行评估,其 GI50 分别为 23 nM 和 39 nM。激酶测定:Tirbanibulin (KX2-391) 是一种 Src 抑制剂,针对 Src 底物袋。替巴尼布林 (KX2-391) 对 Huh7 (GI50=9 nM)、PLC/PRF/5 (GI50=13 nM)、Hep3B (GI50=26 nM) 和 HepG2 (GI50=60 nM) 显示陡峭的剂量反应曲线,四种肝细胞癌(HCC)细胞系。细胞测定:包括 Huh7、PLC/PRF/5、Hep3B 和 HepG2(NutriCyte,Buffalo,NY)在内的肝细胞系常规培养并维持在含有 2% 胎牛血清 (FBS) 的基础培养基中,温度为 37 °C,浓度为 5%二氧化碳。将细胞按每孔 4.0 × 103/190 μL 和 8.0 × 103/190 μL 接种在含有 1.5% FBS 的基础培养基中的 96 孔板中。在添加浓度范围为 6,564 至 0.012 nM 的 KX2-391 之前,将它们在 37 °C 和 5% CO2 下培养过夜,一式三份。处理过的细胞孵育3天。然后在第 3 天将 10 微升 3-(4,5-二甲基噻唑-2-基)-2,5-二苯基溴化四唑 (MTT) 溶液 (5 mg/mL) 添加到每个孔中,并将细胞孵育 4 小时。将甲臜产物用 10% SDS 溶解在稀 HCl 中。使用 BioTek Synergy HT 多平台酶标仪测量 570 nm 处的光密度。为了比较活性和效力,使用 KX2-391 进行平行实验。使用GraphPad Prism 5统计软件确定生长抑制曲线、50%抑制浓度(GI50)和80%抑制浓度(GI80)。数据经过标准化以表示最大响应的百分比,并以 570 nm 波长 (OD570) 信号格式的光密度报告。
KX-01 在10-250 nmol/L浓度范围内,孵育48小时后,能抑制ER/PR/HER2阴性的人乳腺癌细胞系MDA-MB-231、MDA-MB-157和MDA-MB-468的体外生长。[3] 在对达沙替尼耐药的MDA-MB-468细胞中,KX-01(在相同浓度范围内)抑制约75%的生长,而达沙替尼仅抑制约20%。[3] KX-01 (25 nmol/L) 能诱导MDA-MB-468细胞显著凋亡,而达沙替尼 (250 nmol/L) 不能。[3] 将 KX-01 (25 nmol/L) 与紫杉醇 (5 nmol/L) 共孵育24小时,可对MDA-MB-231细胞产生协同生长抑制(43.2%抑制),而两种药物单独使用仅产生适度的抑制(KX-01为11.2%,紫杉醇为14.1%)。在浓度范围内计算的联合指数值表明存在协同作用(CI < 1.0)。在MDA-MB-157和MDA-MB-468细胞中也观察到类似的协同模式。[3] KX-01 (25 nmol/L) 与紫杉醇 (5 nmol/L) 联合使用,在24小时后可使MDA-MB-231细胞的凋亡比单药处理增强约两倍。[3] KX-01 (200 nmol/L,24小时) 在体外通过免疫荧光染色观察,显著抑制了MDA-MB-231细胞中的微管形成。[3] 在3D侵袭实验中,用 KX-01 (25 和 50 nmol/L) 处理MDA-MB-231细胞可减少侵袭性星状结构的形成,在50 nmol/L时几乎完全抑制。[3] 在Boyden小室基质胶侵袭实验中,KX-01 (50 nmol/L) 在24小时后将MDA-MB-231细胞的侵袭显著降低了52.9%,数据已针对细胞数量进行了归一化以排除生长抑制的影响。[3] 在划痕愈合实验中,与对照组相比,KX-01 在5、10和25 nmol/L浓度下,24小时后可分别显著降低MDA-MB-231细胞的迁移率11.7%、15.6%和39.9%。[3] KX-01 (10, 25 nM) 与多柔比星联用在ER/PR/HER2阴性细胞系中表现出协同生长抑制,但在较高浓度 (50 nM) 下,该组合产生拮抗作用 (CI > 1.0)。[3] |
| 体内研究 (In Vivo) |
在癌症的临床前动物模型中,口服 KX2-391 显示可抑制原发性肿瘤生长并抑制转移。
在携带原位MDA-MB-231异种移植瘤(约80-100 mm³)的雌性无胸腺NUDE小鼠中,口服给予 KX-01(1 mg/kg 和 5 mg/kg,每日两次,持续28天)可剂量依赖性地使肿瘤体积分别减少35.3%和79.0%。[3] 在同一模型中,单独口服 KX-01(5 mg/kg,每日两次)40天使肿瘤体积减少61.1%。当与紫杉醇(3 mg/kg,每周一次腹腔注射)联合使用时,肿瘤体积减少93.0%,五只小鼠中有两只观察到肿瘤完全消退。[3] 在携带较大、已建立的MDA-MB-231肿瘤(约300 mm³)的小鼠中,单独口服较高剂量的 KX-01(15 mg/kg,每日一次)可显著抑制肿瘤生长(体积减少48.2%),但未导致消退。与较高剂量的紫杉醇(20 mg/kg,每周一次)联合使用可导致90.6%的肿瘤消退,使体积降至起始点以下。[3] 在MDA-MB-157异种移植瘤模型中也观察到 KX-01 单用及与紫杉醇联用具有类似的抗肿瘤效果。[3] 对经 KX-01 治疗的小鼠MDA-MB-231肿瘤进行免疫组织化学分析显示,Src磷酸化(P-Y416-Src)及其下游靶点FAK磷酸化(P-Y861-FAK)被显著抑制,而对总Src或FAK表达无显著影响。[3] TUNEL检测显示,与对照组相比,KX-01 处理使MDA-MB-231肿瘤中凋亡细胞数量显著增加(3-4倍)。[3] KX-01 治疗降低了MDA-MB-231肿瘤中Ki67阳性的增殖肿瘤细胞百分比(从对照组的58.7%降至37.3%),并适度降低了微血管密度(通过CD31染色评估)。[3] 肿瘤切片的免疫荧光染色显示,KX-01 处理破坏了微管网络,导致染色模式弥散且强度降低,这与对照组肿瘤中清晰的微管纤维或紫杉醇处理肿瘤中强烈稳定的微管阵列不同。KX-01 和紫杉醇联合使用导致微管蛋白染色模式弥散,并有微管碎片化的证据。[3] 对小鼠器官中人17号染色体DNA的定量实时PCR分析显示,与对照组相比,单独使用 KX-01 (5 mg/kg) 或与紫杉醇 (3 mg/kg) 联用治疗40天后,可显著减少或消除MDA-MB-231细胞向小鼠肺和肝脏的检测到的微转移。对骨髓转移未观察到显著影响。[3] |
| 酶活实验 |
Tirbanibulin (KX2-391) 是一种 Src 抑制剂,靶向 Src 的底物袋。
Tirbanibulin (KX2-391) 对四种肝细胞癌 (HCC) 细胞系表现出尖锐的剂量反应曲线:Hep3B (GI50=26 nM) )、HepG2 (GI50=60 nM)、PLC/PRF/5 (GI50=13 nM) 和 Huh7 (GI50=9 nM)。 该研究利用免疫组织化学技术对石蜡包埋的肿瘤组织进行染色,以评估体内Src及其下游靶点FAK的活性。使用针对Src磷酸化(活性)形式(P-Y416-Src)和FAK磷酸化形式(P-Y861-FAK)的特异性抗体,以及它们的总蛋白抗体对肿瘤切片进行染色。通过评估染色强度和分布来确定 KX-01 对这些激酶的抑制效果。[3] |
| 细胞实验 |
定期在含有2%胎牛血清(FBS)的基础培养基中于37°C和5%CO2培养和维持,肝细胞系如Huh7、PLC/PRF/5、Hep3B和HepG2使用(NutriCyte,纽约州布法罗)。使用含 1.5% FBS 的基础培养基以 4.0×103/190 μL 和 8.0×103/190 μL 接种于 96 孔板的每孔中。在 37°C 和 5% CO2 下再培养一晚后,添加浓度范围为 6,564 至 0.012 nM 的 KX2-391,一式三份。处理过的细胞的孵育持续三天。第 3 天,向每个孔中添加 10 微升 3-(4,5-二甲基噻唑-2-基)-2,5-二苯基溴化四唑 (MTT) 溶液 (5 mg/mL),然后进行 4 小时潜伏期。用 10% SDS 的稀 HCl 溶液溶解甲臜产物。使用 BioTek Synergy HT 多平台酶标仪,可发现 570 nm 处的光密度。使用 KX2-391 进行平行实验以比较效力和活性。名为 GraphPad Prism 5 的统计程序用于计算生长抑制曲线、50% 抑制浓度 (GI50) 和 80% 抑制浓度 (GI80)。数据以 570 nm 波长处的光密度 (OD570) 信号格式呈现,并标准化以表示最大响应的百分比。
对于细胞生长抑制实验(MTT法),将细胞(MDA-MB-231、MDA-MB-157、MDA-MB-468)与溶剂或不同浓度的 KX-01、紫杉醇、多柔比星或达沙替尼(5、10、25、50、100、250 nmol/L)孵育48小时。细胞生长以相对于溶剂对照的百分比表示。[3] 使用基于ELISA的DNA碎片化实验评估细胞凋亡。将细胞与药物孵育24小时,然后按照实验方案定量凋亡。[3] 对于3D侵袭("on-top")实验,将细胞接种在重组的细胞外基质层上。在铺板时向培养基中加入 KX-01(10、25、50 nmol/L)。每2天更换一次基质胶-培养基混合物和药物,总共4天。对侵袭性星状结构的形成进行拍照和分析。[3] 对于Boyden小室基质胶侵袭实验,将细胞在无血清培养基中与 KX-01(10、25、50 nmol/L)在上室孵育24小时。下室含有含血清的培养基作为化学引诱剂。孵育后,去除上表面未侵袭的细胞,对下表面的侵袭细胞进行固定、染色,使用图像软件计数,并针对细胞活力进行归一化。[3] 对于划痕(伤口愈合)实验,用移液器吸头在汇合的细胞单层上划出一道伤口。然后将细胞与溶剂或 KX-01(5、10、25 nmol/L)孵育24小时。在孵育开始和结束时对伤口闭合情况进行拍照,并使用图像软件测量间隙面积以计算间隙闭合百分比。[3] 对于细胞内的微管免疫荧光,将MDA-MB-231细胞与200 nmol/L KX-01 孵育24小时,然后固定并用荧光染料标记的抗α-微管蛋白抗体进行免疫染色。使用共聚焦显微镜捕获荧光图像。[3] 使用专用软件进行药物组合的协同性计算。根据单药及其组合的剂量反应数据确定联合指数值。CI < 1.0 表示协同,CI = 1.0 表示相加,CI > 1.0 表示拮抗。[3] |
| 动物实验 |
荷MDA-MB-231肿瘤小鼠;灌胃给药;1、5mg/kg剂量
异种移植手术及KX-01口服给药方法如文献(11)所述。简而言之,将5×10⁶个MDA-MB-231细胞悬浮于150μl PBS-Matrigel混合液(1:2)中,原位双侧注射至雌性裸鼠乳腺脂肪垫(每只小鼠两个肿瘤),建立乳腺脂肪垫肿瘤模型。当肿瘤体积达到约80-100mm³时开始治疗。第一项研究采用MDA-MB-231异种移植瘤模型,使用载体(超纯水)和两种剂量的KX-01(1、5mg/kg),每日两次(BID)灌胃给药(使用22g金属灌胃针),持续28天。为了评估KX-01的疗效,我们使用MDA-MB-157异种移植瘤(另一种ER/PR/HER2阴性模型)进行了类似的实验。第二项研究旨在测试KX-01联合紫杉醇对肿瘤生长的影响。我们用载体或KX-01(5mg/kg,每日两次)、每周一次腹腔注射紫杉醇或KX-01联合紫杉醇治疗MDA-MB-231异种移植瘤小鼠。所有组的治疗周期均为40天。第三项研究使用MDA-MB-157异种移植瘤,并采用相同的联合治疗方案。第四项研究测试了KX-01或KX-01联合紫杉醇治疗24天对较大MDA-MB-231肿瘤(约300mm³)的影响。在开始治疗前,肿瘤体积需达到约300mm³。在本实验中,小鼠接受更高剂量(15 mg/kg)的KX-01治疗,且每日给药一次而非两次。紫杉醇以20 mg/kg的剂量腹腔注射,每周一次。在所有实验中,每周两次测量肿瘤直径,并使用公式0.523×LM²(其中L为大直径,M为小直径)计算肿瘤体积。实验结束后,处死动物,取出肿瘤和小鼠器官。组织样本一部分保存在10%中性缓冲福尔马林中用于石蜡包埋,一部分速冻后用于实时PCR检测17号染色体,另一部分包埋后用于冰冻切片CD31染色。免疫组织化学(IHC)染色按照文献[3]所述方法在石蜡包埋的肿瘤组织上进行。异种移植研究使用4-5周龄的雌性无胸腺裸鼠(BALB/c)。将 5 × 10⁶ 个 MDA-MB-231 或 MDA-MB-157 细胞悬浮于 PBS-Matrigel 混合物(1:2 比例)中,双侧注射到乳腺脂肪垫,建立原位乳腺脂肪垫肿瘤模型。[3] 当肿瘤体积达到约 80-100 mm³ 时开始治疗。单药疗效研究中,小鼠分别接受赋形剂(超纯水)或 KX-01(1 mg/kg 或 5 mg/kg)治疗,每日两次(BID)灌胃给药,持续 28 天。每周两次使用游标卡尺测量肿瘤体积。[3] 与紫杉醇联合用药研究中,携带 MDA-MB-231 或 MDA-MB-157 异种移植瘤的小鼠接受以下治疗:赋形剂;单独使用KX-01(5 mg/kg,每日两次,灌胃给药);单独使用紫杉醇(3 mg/kg,每周一次,腹腔注射);或KX-01与紫杉醇联合用药,疗程40天。[3] 另一项研究测试了其对较大、已形成的肿瘤(约300 mm³)的影响。小鼠接受以下治疗:载体;单独使用较高剂量的KX-01(15 mg/kg,每日一次,灌胃给药);单独使用较高剂量的紫杉醇(20 mg/kg,每周一次,腹腔注射);或联合用药,疗程24天。[3] 为了评估转移情况,在40天联合用药研究结束后,收集小鼠器官(肺、肝、股骨骨髓),匀浆化,并提取基因组DNA。采用针对17号染色体上人特异性α-卫星DNA序列的定量实时PCR方法,检测并定量小鼠组织中的人肿瘤细胞DNA(微转移)。在DNA提取前,将已知数量的人乳腺癌细胞加入对照小鼠器官中,生成标准曲线。[3] KX-01以甲磺酸(MSA)盐粉末的形式提供,可溶于水。用超纯水口服给药。紫杉醇腹腔注射给药。[3] |
| 毒性/毒理 (Toxicokinetics/TK) |
在携带MDA-MB-231或MDA-MB-157异种移植瘤的小鼠中,单独使用KX-01(5 mg/kg,每日两次)或联合紫杉醇(3 mg/kg,每周一次)治疗长达40天,与载体对照组相比,未观察到明显的毒性或小鼠体重显著下降。[3]
在肿瘤体积较大的研究中,使用更高剂量(KX-01 15 mg/kg,每日一次 + 紫杉醇 20 mg/kg,每周一次),联合用药组小鼠在24天治疗结束时体重下降约10%(从平均19.4 g降至17.6 g),但未观察到其他明显的毒性迹象。[3] |
| 参考文献 |
|
| 其他信息 |
KX-01(也称为 KX2-391)是一种“首创”的肽模拟 Src 激酶抑制剂,其独特的额外作用机制涉及抑制微管聚合(前微管蛋白抑制)。[3] 该药物具有口服生物利用度,在研究开展时已完成 I 期临床试验,目前正在进行前列腺癌的 II 期试验和急性髓系白血病的 Ib 期试验。[3] 该研究表明,KX-01 的双重作用机制(Src 抑制 + 微管破坏)可能比单独抑制 Src 的药物具有更优的抗肿瘤活性,尤其适用于侵袭性 ER/PR/HER2 阴性乳腺癌。 [3]
与紫杉醇观察到的协同作用被认为源于通过两种不同的机制靶向微管:KX-01抑制微管组装,而紫杉醇则稳定微管,这可能导致微管断裂和功能障碍。[3] KX-01在达沙替尼耐药细胞系(MDA-MB-468)中有效,表明其可能对ATP竞争性Src抑制剂耐药的肿瘤有效。[3] |
| 分子式 |
C27H33N3O6S
|
|---|---|
| 分子量 |
527.63
|
| 精确质量 |
527.209
|
| 元素分析 |
C, 61.46; H, 6.30; N, 7.96; O, 18.19; S, 6.08
|
| CAS号 |
1080645-95-9
|
| 相关CAS号 |
1080645-95-9 (mesylate); 897016-82-9; 1038395-65-1 (HCl)
|
| PubChem CID |
25100013
|
| 外观&性状 |
White to off-white solid powder
|
| LogP |
4.232
|
| tPSA |
126.44
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
8
|
| 可旋转键数目(RBC) |
9
|
| 重原子数目 |
37
|
| 分子复杂度/Complexity |
633
|
| 定义原子立体中心数目 |
0
|
| SMILES |
S(C([H])([H])[H])(=O)(=O)O[H].O1C([H])([H])C([H])([H])N(C([H])([H])C([H])([H])OC2C([H])=C([H])C(C3=C([H])N=C(C([H])=C3[H])C([H])([H])C(N([H])C([H])([H])C3C([H])=C([H])C([H])=C([H])C=3[H])=O)=C([H])C=2[H])C([H])([H])C1([H])[H]
|
| InChi Key |
JGSYRKUPDSSTCB-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C26H29N3O3.CH4O3S/c30-26(28-19-21-4-2-1-3-5-21)18-24-9-6-23(20-27-24)22-7-10-25(11-8-22)32-17-14-29-12-15-31-16-13-29;1-5(2,3)4/h1-11,20H,12-19H2,(H,28,30);1H3,(H,2,3,4)
|
| 化学名 |
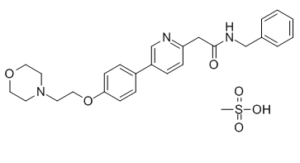
N-benzyl-2-[5-[4-(2-morpholin-4-ylethoxy)phenyl]pyridin-2-yl]acetamide;methanesulfonic acid
|
| 别名 |
KXO1 HCl; KX-01, KX 01 HCl; KXO1 HCl; Mesylate; KX-01, KX 01 Mesylate; KX2-391; KX-2-391 Mesylate; KX 2-391; KX2391; KX-2391; KX 2391 Mesylate
|
| HS Tariff Code |
2934.99.03.00
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: (1). 本产品在运输和储存过程中需避光。 (2). 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (4.74 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (4.74 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (4.74 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: Formulation 1: ≥ 5 mg/mL (9.5 mM) in 4% DMSO+30% PEG 300+ddH2O Formulation 2: ≥ 2.5 mg/mL (4.7 mM) in 10% DMSO + 40% PEG300 + 5% Tween80 + + 45% Saline 例如,要配制1 mL工作液,可取100 μL 25 mg/mL DMSO储备液,加入tO+400 μL PEG300,混匀(澄清液); 然后向上述溶液中加入50 μL Tween 80,混匀(澄清溶液); 最后,向上述溶液中加入450 μL生理盐水,混匀(澄清溶液)。 Preparation of saline: Dissolve 0.9 g sodium chloride in 100 mL ddH ₂ O to obtain a 澄清溶液。 Formulation 3: ≥ 2.5 mg/mL (4.7 mM) in 10% DMSO + 90% (20% SBE-β-CD in saline) 例如,若要配制1 mL工作液,可取100 μL 25 mg/mL DMSO储备液,加入900 μL 20% SBE-β-CD生理盐水中,混匀(澄清溶液) 。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 Formulation 4: ≥ 2.5 mg/mL (4.7 mM) in 10% DMSO + 90% Corn oil 例如,要配制1 mL工作液,可取100 μL 25 mg/mL DMSO储备液,加入900 μL玉米油中,混匀(澄清溶液)。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.8953 mL | 9.4763 mL | 18.9527 mL | |
| 5 mM | 0.3791 mL | 1.8953 mL | 3.7905 mL | |
| 10 mM | 0.1895 mL | 0.9476 mL | 1.8953 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
|