| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
HSP70 (IC50 = 0.5 μM); HSC70 (IC50 = 2.6 μM); Grp78 (IC50 = 2.6 μM)
Heat shock cognate 70 (Hsc70) and Heat shock protein 70 (Hsp70); IC50 values: ~0.5 μM (recombinant human Hsc70 ATPase activity), ~0.8 μM (recombinant human Hsp70-1A ATPase activity), and ~1.2 μM (recombinant murine Hsc70 ATPase activity) [1] - Heat shock protein 70 (Hsp70) and Heat shock cognate 70 (Hsc70); IC50 value: ~2.5 μM (inhibition of androgen receptor (AR) expression in LNCaP95 prostate cancer cells, used as a functional readout for Hsp70/Hsc70 inhibition) [3] |
|---|---|
| 体外研究 (In Vitro) |
VER-155008 对 Hsp90 无活性,IC50 > 200 μM,但它是 Hsc70 和 Hsp70 的抑制剂,对 Hsp70、Hsc70 和 Grp7 的 IC50 分别为 0.5 μM、2.6 μM 和 2.6 μM。 BT474、MB-468、HCT116 和 HT29 细胞属于 VER-155008 抑制增殖的人类结肠和乳腺肿瘤细胞系,其 GI50 分别为 10.4 μM、14.4 μM、5.3 μM 和 12.8 μM。 HCT116 和 BT474 癌细胞响应 VER-155008 (5–40 μM) 表现出客户蛋白降解。此外,VER-155008 会导致人类肿瘤细胞系发生凋亡[1]。在培养的神经元中,VER-155008 (0.05-5 μM) 可恢复 Aβ 诱导的轴突变性[2]。 VER-155008(10 μM 或 25 μM)抑制 Hsp70 并阻止 LNCaP95 细胞增殖。此外,VER-155008 还降低了雄激素受体剪接变异 7 (AR-V7) 和全长雄激素受体 (AR-FL) 蛋白的表达[3]。
HCT116结肠癌细胞中与Hsp90抑制剂协同诱导凋亡:VER155008单独对HCT116细胞的抗增殖活性较弱(GI50 > 20 μM)。但与Hsp90抑制剂(如1 μM 17-AAG,格尔德霉素类似物)联用时,VER155008(2-10 μM)呈剂量依赖性提高凋亡率:Annexin V/PI染色显示,17-AAG单独处理组凋亡率为12%,VER155008 5 μM单独处理组为8%,而联合处理组(17-AAG + VER155008 5 μM)为45%。Western blot证实联合组中caspase-3切割水平(较17-AAG单独组升高2.8倍)和PARP切割水平(较17-AAG单独组升高3.2倍)显著增加 [1] - 神经元中减少轴突退化和tau蛋白磷酸化:用5 μM Aβ1-42(诱导阿尔茨海默病样病理)处理原代皮质神经元后,VER155008(1-5 μM)呈剂量依赖性减少轴突退化:神经丝重链(NF-H,轴突标志物)免疫荧光染色显示,Aβ单独处理组轴突完整性评分为35%,而Aβ + VER155008 5 μM处理组为78%。Western blot还显示,VER155008处理组中tau蛋白在Ser396位点(较Aβ单独组降低45%)和Thr231位点(较Aβ单独组降低52%)的磷酸化水平显著降低 [2] - LNCaP95前列腺癌细胞中抑制雄激素受体(AR)表达和增殖:VER155008(2.5-20 μM)呈剂量依赖性降低LNCaP95细胞中AR蛋白水平:Western blot显示,10 μM VER155008处理24 h后,AR蛋白水平较溶媒组降低70%。实时定量PCR(qPCR)显示,10 μM VER155008处理后AR mRNA水平降低40%,表明其对AR的调控涉及转录和翻译后两个层面。此外,VER155008还抑制LNCaP95细胞增殖(MTT法测得GI50 ~15 μM,72 h),并降低AR靶基因表达(如10 μM处理后PSA mRNA水平降低65%) [3] |
| 体内研究 (In Vivo) |
在幼稚雌性 BALB/c 小鼠中,VER-155008(25 mg/kg,静脉注射)显示血浆清除率。在 HCT116 荷瘤裸 BALB/c 小鼠中,VER-155008(40 mg/kg,静脉注射)同样表现出快速血浆清除并降低肿瘤水平[1]。在 5XFAD 小鼠中,VER-155008(10 μmol/kg/天,腹腔注射)可减轻与淀粉样斑块相关的轴突肿胀,并改善记忆缺陷。 VER-155008(89.9 μmol/kg/天,腹膜内注射)还可减少 5XFAD 小鼠中的淀粉样斑块和淀粉样斑块相关蛋白 PHF-tau [2]。
APP/PS1转基因小鼠(阿尔茨海默病模型)中改善记忆缺陷和减少轴突退化:6月龄APP/PS1转基因小鼠经VER155008(30 mg/kg/天,溶于0.5%甲基纤维素中口服灌胃)处理4周后,Morris水迷宫测试显示:与溶媒处理转基因小鼠相比,VER155008处理组逃避潜伏期缩短50%,在目标象限停留时间增加2.3倍。海马组织免疫组化显示,VER155008处理组轴突退化(NF-H阳性断裂轴突)减少60%,磷酸化tau蛋白(Ser396位点)水平降低48%。野生型小鼠经VER155008处理后未观察到显著记忆改善 [2] |
| 酶活实验 |
Hsc70、Hsp70、Grp78和Hsp90荧光偏振(FP)测定[1]
如前所述,测定VER-155008对Hsp70和Hsp90的活性。Hsc70(aa 5-381)和Grp78(ATP酶结构域)的克隆和表达如下。制作了对应于氨基酸5-381的Hsc70的PCR片段。将纯化的PCR片段连接到pCR2.1-TOPO中。随后将其限制性消化并亚克隆到商业组氨酸标记载体pET101中用于表达分析。通过PCR扩增Grp78的ATP酶结构域,并将其克隆到pCR2.1-TOPO中。随后将其消化并连接到谷胱甘肽-s-转移酶标记的表达载体pGEX-4T-1中。按照Hsp70的描述,使用与FP探针相同的N 6-(6-氨基)己基-ATP-5-FAM进行Hsc70和Grp78的FP测定,但有以下修改。对于Hsc70,在22°C下孵育30分钟,蛋白质和探针浓度分别为0.3μM和20 nM,而对于Grp78,在22℃下孵育2小时,蛋白质和探头浓度分别为2μM和10 nM。FAM-ATP探针的K D对Hsc70为0.24μM,对Grp78为2μM。 BiaCore测定化合物与Hsp70的结合[1] 所有实验均在Biacore T100上在25°C下以30μL/min的流速进行。缓冲系统与Hsp70荧光偏振分析中使用的缓冲系统相同,含有1%DMSO和0.05%吐温20。双His标记的Hsp70被固定在NTA传感器芯片的表面上;约2000RU的蛋白质被固定。注入化合物90秒,在80秒时根据平衡结合确定Kds。 Hsp70 ATP酶测定[1] 使用ADP Hunter Plus检测试剂盒测量ATP周转率和随后产生的ADP。反应混合物在半体积、全黑色非结合板中制备,在标准试剂盒测定缓冲液中含有250 nM全长、GST标记的Hsp70、50μM ATP和浓度递增的VER-155008。反应在30°C下孵育90分钟,然后在FlexStation 3上读取,E x为530 nm,E m为590 nm,每孔读取6次。设置不含酶的反应来监测ATP的自发水解,并从含有Hsp70的反应中减去。 热变性萤光素酶的复性[1] 该测定基本上如前所述[24,25]进行。简而言之,Hsc70/Hsp70抑制剂在pH 7.5的兔网织红细胞裂解物(RRL,核酸酶处理)中稀释,该裂解物含有10 mM Tris、100 mM KCl、3 mM EDTA、1 mM DTT和ATP再生系统。最终ATP浓度为0.5 mM。化合物在室温下在上述混合物中预孵育15分钟,然后加入25 ng热变性萤光素酶(在40°C下变性30分钟)以启动复性反应,并在30°C下孵育60分钟。使用Bright glo试剂测定萤光素酶活性。 Hsc70/Hsp70 ATP酶活性实验(比色法):将重组Hsc70/Hsp70蛋白(人Hsc70、人Hsp70-1A或小鼠Hsc70)在实验缓冲液(20 mM Tris-HCl pH 7.5、10 mM KCl、5 mM MgCl2、1 mM DTT)中稀释至终浓度1 μg/孔。加入系列稀释的VER155008(0.1-10 μM),再加入ATP(终浓度1 mM)启动反应。混合物在37°C孵育60 min后,使用商品化无机磷酸盐(Pi)检测试剂盒检测ATP水解释放的Pi。在620 nm处测定吸光度,通过四参数逻辑模型拟合剂量-反应曲线计算IC50值 [1] - Hsp70-AR结合抑制实验(免疫沉淀法):取LNCaP95细胞裂解液(1 mg蛋白),与VER155008(0.5-10 μM)在4°C孵育1 h,随后加入抗Hsp70抗体偶联琼脂糖珠,4°C孵育过夜。用裂解缓冲液洗涤珠子3次,用SDS上样缓冲液洗脱结合蛋白。通过Western blot(抗AR抗体)检测与Hsp70结合的AR。密度分析显示,5 μM VER155008处理后,Hsp70-AR复合物形成较溶媒组减少约65% [3] |
| 细胞实验 |
细胞周期分析[1]
将HCT116细胞暴露于指定浓度的VER-155008和VER-82160中24小时。在用RNaseA/碘化丙啶染色之前,收集所有细胞并将其固定在冰上的70%乙醇中。在FACSArray细胞仪上收集数据,并用FACSDeva软件进行分析。 雄激素剥夺疗法最初对晚期前列腺癌症患者有效;然而,前列腺癌症逐渐对雄激素剥夺疗法产生耐药性,称为去势耐药性前列腺癌症(CRPC)。雄激素受体剪接变异体7(AR-V7)是CRPC的原因之一,与对新一代AR拮抗剂(恩杂鲁胺)的耐药性和预后不良有关。已知热休克蛋白70(Hsp70)抑制剂可以降低全长AR(AR-FL)的水平,但对其对表达AR-V7的CRPC细胞的影响知之甚少。在本研究中,我们研究了Hsp70抑制剂槲皮素和VER155008在表达AR-V7的前列腺癌症细胞系LNCaP95中的作用,并探讨了Hsp7调节AR-FL和AR-V7表达的机制。槲皮素和VER155008降低了细胞增殖,增加了凋亡细胞的比例,并降低了AR-FL和AR-V7的蛋白水平。此外,VER155008降低了AR-FL和AR-V7 mRNA水平。用Hsp70抗体进行免疫沉淀和质谱鉴定,Y-box结合蛋白1(YB-1)是通过与Hsp70相互作用在转录水平调节AR-FL和AR-V7的分子之一。VER155008降低了YB-1的磷酸化及其在细胞核中的定位,表明Hsp70参与AR调节可能是通过YB-1的激活和核转位介导的。总的来说,这些结果表明,Hsp70抑制剂通过YB-1抑制降低AR-FL和AR-V7的表达,对CRPC具有潜在的抗肿瘤活性[3]。 HCT116细胞凋亡实验(Annexin V-FITC/PI染色):将HCT116细胞以2×10⁵细胞/孔接种到6孔板中,过夜孵育。用VER155008(2-10 μM)单独处理或与1 μM 17-AAG联合处理48 h。收集细胞,用冷PBS洗涤,按照试剂盒说明书用Annexin V-FITC和碘化丙啶(PI)染色。通过流式细胞术定量凋亡细胞(Annexin V阳性/PI阴性:早期凋亡;Annexin V阳性/PI阳性:晚期凋亡)。使用流式细胞术软件分析数据,凋亡率计算为早期和晚期凋亡细胞之和 [1] - 原代皮质神经元轴突退化实验(免疫荧光):从E18大鼠胚胎中分离原代皮质神经元,在盖玻片上培养7天。用5 μM Aβ1-42单独处理或与VER155008(1-5 μM)联合处理24 h。用4%多聚甲醛固定细胞,0.1% Triton X-100透化,5% BSA封闭。神经元与抗NF-H抗体(轴突标志物)在4°C孵育过夜,随后与Alexa Fluor 488偶联二抗在室温孵育1 h。将盖玻片用含DAPI的封片液封片,通过计数完整NF-H阳性轴突(长度>50 μm)与断裂轴突的比例评分轴突完整性,每片盖玻片至少计数100个神经元 [2] - LNCaP95细胞AR表达实验(Western blot和qPCR):Western blot流程:将LNCaP95细胞以3×10⁵细胞/孔接种到6孔板中,过夜孵育,用VER155008(2.5-20 μM)处理24 h。用RIPA缓冲液裂解细胞,BCA法测定蛋白浓度,取30 μg蛋白进行SDS-PAGE分离。膜用抗AR抗体和抗β-肌动蛋白(内参)抗体孵育,条带强度通过密度分析定量。qPCR流程:用RNA提取试剂盒从处理后的LNCaP95细胞中提取总RNA,逆转录为cDNA,用AR特异性引物进行qPCR。采用2^(-ΔΔCt)法计算相对AR mRNA水平,以GAPDH为内参基因 [3] |
| 动物实验 |
配制方法 1:将 VER-155008 溶解于含 10% 二甲基亚砜 (DMSO) 的生理盐水中,并以 10 mmol/kg/天的剂量腹腔注射给 5XFAD 小鼠,连续 18 天。[1] 配制方法 2:将 VER-155008 以 25 mg/kg 的剂量溶于 10% DMSO/5% Tween 80/85% 生理盐水 (v/v/v) 溶液中,经尾侧静脉注射给雌性 BALB/c 小鼠。 [2] APP/PS1转基因小鼠阿尔茨海默病模型:将6月龄雄性APP/PS1转基因小鼠(每组n=8)和野生型同窝小鼠(每组n=8)随机分为载体组和VER155008组。VER155008溶于0.5%甲基纤维素(0.9%生理盐水)中,以30 mg/kg/天的剂量灌胃给药,持续4周;载体组仅灌胃0.5%甲基纤维素。在治疗的最后一周,进行Morris水迷宫实验以评估小鼠的记忆力:小鼠接受为期5天的训练(每天4次),以寻找隐藏的平台;并在第6天进行探针试验(移除平台),以测量小鼠在目标象限停留的时间。行为学测试结束后,对小鼠实施安乐死,取出脑组织,并解剖海马组织进行免疫组织化学(NF-H 和磷酸化 tau 染色)和蛋白质印迹分析[2] |
| 毒性/毒理 (Toxicokinetics/TK) |
体外细胞毒性:VER155008在非癌细胞中显示出较低的固有毒性:用VER155008(浓度最高达10 μM)处理24小时后,原代皮层神经元的存活率>90%(MTT法)[2]。在HCT116结肠癌细胞中,细胞毒性(细胞死亡)的IC50值>20 μM [1]。在 LNCaP95 前列腺癌细胞中,GI50(生长抑制)约为 15 μM,浓度低于 10 μM 时未观察到明显的细胞死亡 [3]
- 小鼠体内毒性:用 VER155008(30 mg/kg/天,口服,4 周)治疗的 APP/PS1 转基因小鼠与载体对照组相比,体重(载体组:+5.2% vs. VER155008:+4.8%)、食物消耗量以及血清 ALT、AST、BUN 和肌酐水平(肝肾功能标志物)均无显著变化。未观察到与治疗相关的死亡或在脑、肝、肾组织中出现明显的病理异常 [2] |
| 参考文献 |
|
| 其他信息 |
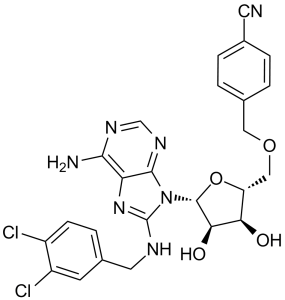
4-[[(2R,3S,4R,5R)-5-[6-氨基-8-[(3,4-二氯苯基)甲基氨基]-9-嘌呤基]-3,4-二羟基-2-氧杂环戊烷基]甲氧基甲基]苯甲腈是一种嘌呤核苷。
VER155008 是一种选择性的小分子 Hsc70 和 Hsp70 抑制剂,它与这些分子伴侣的 ATP 结合域结合,阻止 ATP 水解并破坏其分子伴侣功能。它通过阻断 Hsc70/Hsp70 介导的错误折叠蛋白(Hsp90 抑制后释放)的重折叠,增强 Hsp90 抑制剂诱导的细胞凋亡,导致蛋白毒性应激增加和细胞死亡 [1] - 在阿尔茨海默病模型中,VER155008 通过抑制 Hsc70 发挥神经保护作用,Hsc70 通常促进 tau 蛋白聚集和轴突变性。通过阻断 Hsc70,VER155008 可减少 tau 蛋白过度磷酸化并维持轴突完整性,从而改善记忆缺陷 [2] - 在前列腺癌中,VER155008 通过抑制 Hsp70 抑制 AR 表达,Hsp70 作为 AR 折叠和稳定的辅助伴侣蛋白发挥作用。 AR 水平降低会导致 AR 依赖性 LNCaP95 前列腺癌细胞增殖减少,这支持了其作为 AR 阳性前列腺癌治疗药物的潜力 [3] |
| 分子式 |
C25H23CL2N7O4
|
|
|---|---|---|
| 分子量 |
556.40
|
|
| 精确质量 |
555.118
|
|
| 元素分析 |
C, 53.97; H, 4.17; Cl, 12.74; N, 17.62; O, 11.50
|
|
| CAS号 |
1134156-31-2
|
|
| 相关CAS号 |
|
|
| PubChem CID |
25195348
|
|
| 外观&性状 |
Typically exists as White to pink solids at room temperature
|
|
| 密度 |
1.6±0.1 g/cm3
|
|
| 沸点 |
856.3±75.0 °C at 760 mmHg
|
|
| 闪点 |
471.7±37.1 °C
|
|
| 蒸汽压 |
0.0±0.3 mmHg at 25°C
|
|
| 折射率 |
1.748
|
|
| LogP |
2.71
|
|
| tPSA |
164.36
|
|
| 氢键供体(HBD)数目 |
4
|
|
| 氢键受体(HBA)数目 |
10
|
|
| 可旋转键数目(RBC) |
8
|
|
| 重原子数目 |
38
|
|
| 分子复杂度/Complexity |
831
|
|
| 定义原子立体中心数目 |
4
|
|
| SMILES |
ClC1=C(C([H])=C([H])C(=C1[H])C([H])([H])N([H])C1=NC2=C(N([H])[H])N=C([H])N=C2N1[C@@]1([H])[C@@]([H])([C@@]([H])([C@@]([H])(C([H])([H])OC([H])([H])C2C([H])=C([H])C(C#N)=C([H])C=2[H])O1)O[H])O[H])Cl
|
|
| InChi Key |
ZXGGCBQORXDVTE-UMCMBGNQSA-N
|
|
| InChi Code |
InChI=1S/C25H23Cl2N7O4/c26-16-6-5-15(7-17(16)27)9-30-25-33-19-22(29)31-12-32-23(19)34(25)24-21(36)20(35)18(38-24)11-37-10-14-3-1-13(8-28)2-4-14/h1-7,12,18,20-21,24,35-36H,9-11H2,(H,30,33)(H2,29,31,32)/t18-,20-,21-,24-/m1/s1
|
|
| 化学名 |
5'-O-[(4-Cyanophenyl)methyl]-8-[[(3,4-dichlorophenyl)methyl]amino]-adenosine
|
|
| 别名 |
VER 155008; VER155008; VER-155008; VER-155008; VER 155008; 5'-O-[(4-Cyanophenyl)methyl]-8-[[(3,4-dichlorophenyl)methyl]amino]-adenosine; VER155008; C25H23Cl2N7O4; 4-((((2R,3S,4R,5R)-5-(6-Amino-8-((3,4-dichlorobenzyl)amino)-9H-purin-9-yl)-3,4-dihydroxytetrahydrofuran-2-yl)methoxy)methyl)benzonitrile; 5'-O-[(4-Cyanophenyl)methyl]-8-[[(3,4-dichlorophenyl)-methyl]amino]-adenosine;
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (4.49 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (4.49 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (4.49 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: 1% CMC+0.5% Tween-80: 30 mg/mL 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.7973 mL | 8.9863 mL | 17.9727 mL | |
| 5 mM | 0.3595 mL | 1.7973 mL | 3.5945 mL | |
| 10 mM | 0.1797 mL | 0.8986 mL | 1.7973 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
VER-155008 administration rescued memory deficits in 5XFAD mice.Front Pharmacol.2018 Jan 30;9:48. |
|---|
VER-155008 penetrates into the brain after intraperitoneal administration in 5XFAD mice.Front Pharmacol.2018 Jan 30;9:48. |
VER-155008 administration reduced axonal swelling associated with amyloid plaques in 5XFAD mice.Front Pharmacol.2018 Jan 30;9:48. |
VER-155008 treatment reversed Aβ-induced axonal degeneration in cultured neurons.Front Pharmacol.2018 Jan 30;9:48. |
|---|
|
VER-155008 administration reduced amyloid plaques in 5XFAD mice. Aβ1-40/42was visualized by immunostaining in the perirhinal cortex and hippocampal CA1.(A)Representative images of Aβ1-40/42-positive amyloid plaques in the perirhinal cortex are shown. The amyloid plaques are indicated with white arrowheads.Front Pharmacol.2018 Jan 30;9:48. |