| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
Natural product
|
|---|---|
| 体外研究 (In Vitro) |
Arnebin-1对HUVECs增殖的影响[1]
PCNA是核细胞增殖的标志物。为了确定arnebin-1是否促进HUVEC的增殖,通过蛋白质印迹分析测量PCNA水平。在1×10−3µM至10−1µM的浓度范围内,单独使用arnebin-1对PCNA水平没有显著影响(图1B)。然而,在VEGF(1 ng/ml)存在的情况下,arnebin-1以浓度依赖的方式显著增加了PCNA的表达(图1C)。与我们之前的研究结果一致,我们发现arnebin-1对细胞存活率和增殖没有明显影响(因为在测试范围内通过MTT法评估PCNA表达没有变化),但与VEGF具有协同作用,因为它促进了HUVEC的增殖(图5A)。 Arnebin-1激活VEGFR2信号通路[1] 据报道,VEGFR2磷酸化激活了广泛的下游信号底物,这些底物与内皮细胞增殖、迁移和管形成密切相关。为了研究arnebin-1是否激活VEGFR2及其下游信号分子,我们筛选了一些与VEGFR2信号通路相关的基本激酶。如图2所示,arnebin-1以浓度依赖的方式显著增加了VEGF(1 ng/ml)诱导的VEGFR2、FAK、ERK和Src的磷酸化,这表明arnebin-1通过直接靶向VEGFR2并随后激活VEGFR2诱导的下游信号级联来发挥其促血管生成作用。这些结果与我们之前的研究一致,该研究表明,在VEGF存在的情况下,arnebin-1以浓度依赖的方式促进HUVEC的增殖、迁移和管形成。 Arnebin-1以PI3K依赖的方式上调HUVECs中eNOS、VEGF和HIF-1α的表达水平[1] 随后,我们研究了arnebin-1对HUVEC中eNOS和VEGF表达水平的影响。与载体处理的(对照)细胞相比,在1×10−3µM至10−1µM的浓度范围内,arnebin-1以浓度依赖的方式显著增加了HUVEC中eNOS的蛋白质表达(图3A)。此外,与对照组相比,10−2和10−1µM的arnebin-1也显著增加了VEGF蛋白的表达和分泌(图3B和C)。同样,arnebin-1也显著上调了HIF-1α的表达(图3D)。我们进一步研究了arnebin-1在HUVEC中上调eNOS、VEGF和HIF-1α是否是通过其对PI3K通路的影响介导的。在用10-1µM arnebin-1刺激前1小时用2µM LY294002处理,HIF-1α的蛋白表达显著降低(图3E)。同样,用2µM LY294002预处理后,eNOS的蛋白表达以及VEGF蛋白的表达和分泌也显著降低(图3F–H)。 Arnebin-1通过PI3K依赖途径促进HUVEC的增殖、迁移和管形成[1] 在之前的一项研究中,我们证实arnebin-1在VEGF(1 ng/ml)存在下以浓度依赖的方式显著促进HUVEC的增殖、迁移和管形成,在10-1µM时效果最大。在本研究中,我们研究了arnebin-1产生这些作用的机制。如图5所示,与对照组相比,低浓度VEGF(1ng/ml)刺激可增强HUVEC的增殖、迁移和管形成。此外,10−1µM的arnebin-1和VEGF具有协同作用,与单独用VEGF处理的细胞相比,显著增加了这些过程。然而,当HUVEC用PI3K抑制剂LY294002预处理时,arnebin-1和VEGF对细胞增殖、迁移和管形成的协同作用被消除(图5)。如图所示,LY294002预处理减弱了arnebin-1诱导的eNOS、VEGF和HIF-1α表达水平的增加(图3)。总的来说,这些结果表明,arnebin-1通过以PI3K依赖的方式上调eNOS、VEGF和HIF-1α,促进与血管生成相关的内皮细胞增殖、迁移和管形成过程。 |
| 体内研究 (In Vivo) |
Arnebin-1对糖尿病创面HIF-1α、eNOS和VEGF表达的影响[1]
为了研究促进血管新生的机制,在用arnebin-1治疗后,我们测量了HIF-1α及其靶基因、VEGF和eNOS的体内表达水平。Western blot分析显示,与非糖尿病伤口相比,糖尿病伤口中HIF-1α、eNOS和VEGF的蛋白表达水平显著降低(图6)。糖尿病组和赋形剂治疗组的HIF-1α、eNOS和VEGF水平没有显著差异。然而,用arnebin-1治疗后,糖尿病伤口中HIF-1α的表达显著增加(图6A)。与糖尿病组和赋形剂治疗组相比,arnebin-1治疗组的eNOS表达水平更高(图6B)。同样,arnebin-1在第7天显著增加了VEGF的蛋白表达(图6C)。综上所述,这些结果表明,arnebin-1通过上调HIF-1α、eNOS和VEGF的表达水平,促进糖尿病大鼠伤口的新生血管形成。 Arnebin-1对血管新生和糖尿病伤口愈合的影响[1] 在体外实验中,我们证明arnebin-1和低浓度VEGF显著增加了PCNA的表达,而不含VEGF的arnebin-1给药没有达到相同的结果。在体内,糖尿病伤口组织中的VEGF水平仍然较低,与糖尿病组和载体治疗组相比,局部应用arnebin-1软膏可上调PCNA的表达(图7A),这与我们的体外结果一致。为了确定arnebin-1在糖尿病伤口新生血管中的作用,检测了血管生成的生化标志物CD31的表达,以分析arnebin-1的作用。在我们之前的研究中,通过组织学分析,我们证明了用arnebin-1治疗的糖尿病伤口在受伤后第4天和第7天毛细血管密度增加。在本研究中,用抗CD31抗体对内皮细胞进行免疫荧光染色后,非糖尿病大鼠的伤口出现了阳性染色(图7B)。在糖尿病对照动物和载体治疗的糖尿病动物的伤口中,这种染色似乎显著减少。我们发现,在用arnebin-1治疗后的第7天,肉芽形成区域周围的CD31阳性血管数量增加。定量分析结果显示,arnebin-1治疗组的毛细血管密度明显大于糖尿病组(图7C)。此外,蛋白质印迹分析的结果表明,与未用arnebin-1治疗的其他糖尿病组相比,用arnebin1治疗后CD31的蛋白水平显著升高(图7D)。 |
| 细胞实验 |
细胞增殖试验[1]
通过线粒体MTT四氮唑试验检测细胞增殖。将HUVEC以3×103个细胞/孔的速度铺在96孔板上。一夜之间,用或不用LY294002(2µM)预处理HUVEC,然后用补充有载体[二甲亚砜(DMSO)]和Arnebin-1(10-1µM)的测试培养基替换培养基,添加或不添加1ng/ml VEGF。孵育24小时后,根据制造商的说明使用MTT试剂检测活细胞的数量。简而言之,将10µl MTT(5mg/ml)加入100µl培养基中,在37°C下培养4小时。去除上清液后,通过加入DMSO溶解甲赞晶体。使用Biotek Elx-800平板读数器测定培养基的吸光度(570nm)。 细胞迁移试验[1] 如前所述,使用Transwell室进行细胞迁移测定。该装置的底部腔室装有600µl的测试介质。将HUVEC(5×104个细胞/孔)加入上腔,在含有2%FBS的M199培养基中培养。孵育24小时后,去除膜表面上方的未迁移细胞。将迁移细胞用甲醇固定15分钟,然后用0.1%结晶紫染色20分钟。然后用30%冰醋酸冲洗膜。最后,在540nm下检查洗涤溶液以计数HUVEC的数量。 试管形成试验[1] 为了检查促血管生成作用Arnebin-1,我们使用了如前所述的实验性体外Matrigel系统。生长因子降低的Matrigel基底膜基质在4°C的冰上解冻过夜,所有移液管和96孔平底板在使用前均已预冷。在37°C下,每孔用50µl Matrigel涂覆96孔板30分钟。将HUVEC以每孔4×104个细胞的速度接种在100µl的检测培养基中。孵育16小时后,使用倒置显微镜拍摄管状结构。使用ImageJ软件量化总管长。 |
| 动物实验 |
动物及糖尿病诱导[1]
所有动物实验程序均经中山大学实验动物中心批准。如前所述,雄性Sprague-Dawley (SD)大鼠(体重250-300 g)饲养于无特定病原体(SPF)级不锈钢笼中。大鼠饲养于温度恒定在18-22℃、光暗周期为12小时的受控环境中,并可自由摄取食物和水。实验开始前,大鼠适应环境4周。大鼠禁食12小时后,每隔一天腹腔注射溶于生理盐水的阿洛克生单水合物(剂量为100 mg/kg),以诱导糖尿病。连续注射阿洛克生3天后,使用血糖仪测定大鼠的空腹血糖(FBG)水平。本研究将空腹血糖(FBG)水平 >16.7 mmol/L 的大鼠确诊为糖尿病大鼠。实验前后均监测了 FBG 水平。动物随机分为 4 组(1 组非糖尿病组和 3 组糖尿病组;n=6),具体如下:i) 非糖尿病组:大鼠连续 7 天给予蒸馏水(非糖尿病组);ii) 第一糖尿病组:糖尿病大鼠给予蒸馏水(糖尿病组);iii) 第二糖尿病组:糖尿病大鼠给予赋形剂(不含 Arnebin-1 的软膏;DM-赋形剂;D+V 组);iv) 第三糖尿病组:糖尿病大鼠接受 Arnebin-1 软膏治疗(DM-Arnebin-1;D+A 组),持续 7 天。 软膏的制备 [1] 如我们之前的研究所述,将含有西瑞奇(1.5 g)、蜂蜡(5 g)和猪油(0.15 g)的软膏在 70–75°C 下加热至溶解,然后加入 6.65 mg Arnebin-1(0.1%)并混合均匀。最后,将混合物搅拌至冷却至室温。该软膏用作测试化合物。 给药 [1] 如上所述,每只糖尿病大鼠背部有 3 个伤口,非糖尿病大鼠有 1 个伤口。在 D + V 组中,仅背部上方的伤口用赋形剂(不含测试化合物)处理。在糖尿病组中,仅尾部附近的伤口用蒸馏水处理。在D+A组中,仅对中间的伤口使用Arnebin-1(0.1%软膏)进行治疗。因此,每组大鼠治疗的伤口区域各不相同。顶部的伤口作为治疗伤口的载体对照。试验化合物软膏和载体每隔一天涂抹一次,用量足以薄薄地覆盖伤口。所有治疗持续到处死当天。大鼠通过腹腔注射过量巴比妥类药物处死。 组织采集[1] 在受伤后第7天,用过量戊巴比妥钠(200 mg/kg,腹腔注射)麻醉大鼠。切除伤口及其周围约5 mm的未受伤皮肤。将这些伤口组织快速冷冻于液氮中,直至进行蛋白质分离处理。 蛋白质印迹分析[1] 为了检测组织中PCNA、CD31、HIF-1α、VEGF和eNOS的水平,在伤后第7天收集用Arnebin-1或载体处理的伤口。切除后,将组织在裂解缓冲液中匀浆。如上所述,通过蛋白质印迹分析测定VEGF、eNOS和HIF-1α的表达水平。 |
| 参考文献 | |
| 其他信息 |
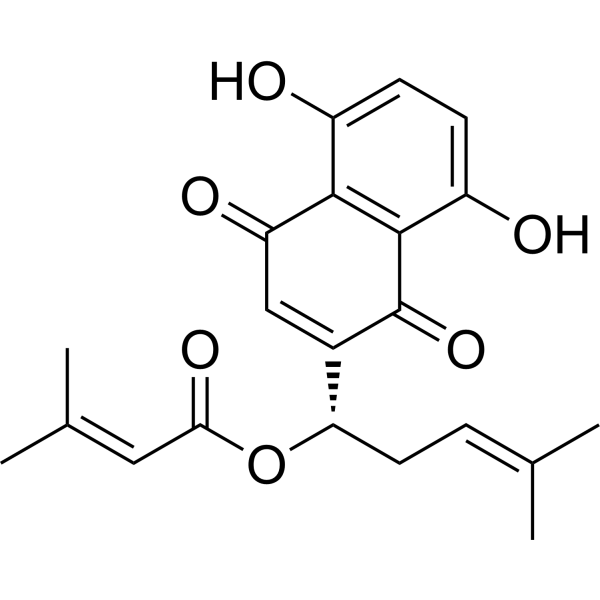
紫草素β,β-二甲基丙烯酸酯是一种羟基-1,4-萘醌。
据报道,紫草素β,β-二甲基丙烯酸酯存在于紫草属植物紫草(Alkanna euchroma)、卡帕多西亚紫草(Alkanna cappadocica)和染料紫草(Alkanna tinctoria)中,并有相关数据。 紫草素-1是一种萘醌衍生物,在紫草(一种传统伤口愈合草药)的伤口愈合特性中发挥着关键作用。研究表明,紫草素-1与血管内皮生长因子(VEGF)协同作用,对人脐静脉内皮细胞(HUVECs)具有促血管生成作用,并能加速糖尿病伤口的愈合过程。然而,紫草素-1对HUVECs的促血管生成作用及其对糖尿病伤口愈合作用的机制尚未完全阐明。本研究旨在阐明阿尼宾-1的作用机制,我们采用Western blot分析法研究了阿尼宾-1对VEGF处理的人脐静脉内皮细胞(HUVECs)中VEGF受体2(VEGFR2)和磷脂酰肌醇3-激酶(PI3K)依赖性信号通路的影响。我们通过MTT法、Transwell实验和体外成管实验评估了阿尼宾-1对HUVECs的促血管生成作用,包括其对细胞增殖和迁移的影响。我们采用Western blot分析法检测了HUVECs以及非糖尿病和糖尿病大鼠伤口组织中缺氧诱导因子(HIF)-1α、内皮型一氧化氮合酶(eNOS)和VEGF的表达水平。此外,我们还采用免疫荧光染色法评估了大鼠伤口组织中CD31的表达。我们发现,阿尼宾-1可增强VEGF诱导的VEGFR2信号通路激活。阿尼宾-1通过PI3K依赖性通路促进内皮细胞增殖、迁移和管状结构形成。此外,阿尼宾-1显著提高HUVECs中eNOS、VEGF和HIF-1α的表达水平,并通过PI3K依赖性信号通路加速糖尿病伤口愈合。与未治疗的糖尿病大鼠相比,阿尼宾-1治疗的糖尿病大鼠伤口中CD31表达显著增强。因此,本研究结果表明,arnebin-1通过诱导促血管生成反应促进糖尿病大鼠的伤口愈合过程。[1] 总之,基于本研究结果并结合我们之前的研究数据,我们证实arnebin-1在体外显著促进HUVECs的血管生成,并且局部应用arnebin-1软膏可通过PI3K依赖性信号通路诱导eNOS、VEGF和HIF-1α的表达,从而加速I型糖尿病大鼠的伤口愈合过程。因此,局部应用arnebin-1软膏可能是一种治疗糖尿病足溃疡的新型策略。有必要进行临床试验,以确定arnebin-1治疗是否能够促进糖尿病患者的伤口愈合。 arnebin-1 对成纤维细胞和角质形成细胞的确切作用仍有待研究。[1] 本研究从紫草(Arnebia nobilis Reichb.f.)的根中分离鉴定出萘醌类化合物,有望发现一种新的抗皮肤衰老成分,用于彩妆领域。通过严格的柱色谱分离纯化了四种化合物。根据光谱数据,这些化合物被鉴定为β,β-二甲基丙烯酰紫草素(AN-I)、乙酰氧基异戊酰紫草素(AAN-II)、乙酰紫草素(AN-III)和紫草素(AN-IV)。本研究首次报道了从紫草中分离得到乙酰氧基异戊酰紫草素(AAN-II)。在人皮肤细胞(人真皮成纤维细胞和人角质形成细胞)和小鼠胚胎成纤维细胞(NIH3T3)中测定的化合物IC50值在四种烷芘之间差异显著。在这四种化合物中,β-乙酰氧基异戊酰烷芘(AAN-II)显著抑制了过氧化氢(H2O2)诱导的人真皮成纤维细胞红细胞溶血和细胞衰老。AAN-II上调了人真皮成纤维细胞或角质形成细胞中I型胶原蛋白、弹性蛋白和包膜蛋白的合成。这些结果支持烷芘作为新型抗衰老成分的潜在应用价值。[2] |
| 分子式 |
C21H22O6
|
|---|---|
| 分子量 |
370.3958
|
| 精确质量 |
370.141
|
| CAS号 |
34539-65-6
|
| 相关CAS号 |
(Rac)-Arnebin 1;5162-01-6;β,β-Dimethylacrylshikonin;24502-79-2
|
| PubChem CID |
442720
|
| 外观&性状 |
Brown to reddish brown solid powder
|
| 密度 |
1.3±0.1 g/cm3
|
| 沸点 |
573.9±50.0 °C at 760 mmHg
|
| 闪点 |
201.1±23.6 °C
|
| 蒸汽压 |
0.0±1.6 mmHg at 25°C
|
| 折射率 |
1.589
|
| LogP |
5.98
|
| tPSA |
100.9
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
6
|
| 重原子数目 |
27
|
| 分子复杂度/Complexity |
706
|
| 定义原子立体中心数目 |
1
|
| SMILES |
CC(=CC[C@@H](C1=CC(=O)C2=C(C=CC(=C2C1=O)O)O)OC(=O)C=C(C)C)C
|
| InChi Key |
BATBOVZTQBLKIL-KRWDZBQOSA-N
|
| InChi Code |
InChI=1S/C21H22O6/c1-11(2)5-8-17(27-18(25)9-12(3)4)13-10-16(24)19-14(22)6-7-15(23)20(19)21(13)26/h5-7,9-10,17,22-23H,8H2,1-4H3/t17-/m0/s1
|
| 化学名 |
[(1S)-1-(5,8-dihydroxy-1,4-dioxonaphthalen-2-yl)-4-methylpent-3-enyl] 3-methylbut-2-enoate
|
| 别名 |
34539-65-6; Alkannin beta,beta-dimethylacrylate; b,b-Dimethylacrylalkannin; NCIMech_000202; [(1S)-1-(5,8-dihydroxy-1,4-dioxonaphthalen-2-yl)-4-methylpent-3-enyl] 3-methylbut-2-enoate; CHEBI:2579; CHEMBL513640; beta,beta-dimethyl-acry-lalkannin;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 本产品在运输和储存过程中需避光。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~23.75 mg/mL (~64.12 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (6.75 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL 澄清 DMSO 储备液加入900 μL 玉米油中,混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.6998 mL | 13.4989 mL | 26.9978 mL | |
| 5 mM | 0.5400 mL | 2.6998 mL | 5.3996 mL | |
| 10 mM | 0.2700 mL | 1.3499 mL | 2.6998 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。