| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| 2g |
|
||
| Other Sizes |
|

| 靶点 |
hTRPV1 (EC50 = 290 nM, HEK293 cells)[1]
|
|---|---|
| 体外研究 (In Vitro) |
辣椒素(50-300 µM;24-72 小时)以剂量和时间依赖性方式显着抑制细胞增殖。据估计,IC50 值为 150 µM[2]。在 24-72 小时内,辣椒素 (50-300 µM) 会增加促凋亡 Bad/Bax 的表达并减少抗凋亡 Bcl-2 蛋白。它还激活细胞质中的 caspase 3 和 PARP (p85) 水平[2]。辣椒素都会增加 Sub-G1 DNA 浓度、核浓缩和核 DNA 片段化 [2]。通过下调细胞周期蛋白 B1 和 D1 调节因子以及细胞周期蛋白依赖性蛋白激酶 cdk-1、cdk-2 和 cdk-4 的产生,辣椒素可阻止 FaDu 细胞中 G1/S 期的细胞周期进展 [2]。
|
| 体内研究 (In Vivo) |
通过改变细胞凋亡调节因子 p53、Bcl-2、Bax 和 caspase-3 的蛋白表达,辣椒素可预防肺癌的生长 [2]。
|
| 酶活实验 |
人TRPV1[1]的克隆与表达
如前所述(Hayes等人,2000),产生稳定表达人TRPV1的人胚胎肾细胞系(hTRPV1.HEK293细胞)。细胞在含有Earle盐的改良Eagles培养基中的塑料组织培养皿上培养,并补充10%胎牛血清、非必需氨基酸和0.2 mm l-谷氨酰胺,同时在37°C下保持在5%CO2下。对于电生理实验,将细胞以30000个细胞cm−2的密度铺在涂有聚赖氨酸的19毫米玻璃盖玻片上,并在24-48小时后进行实验。[1]
电生理技术[1] 如前所述(Hayes等人,2000),根据标准方法使用Axopatch 200B放大器进行全细胞膜片钳实验。使用电阻为1.5-4 mΩ的厚壁硼硅酸盐玻璃电极,使用自动三管溶液切换装置记录用药后的电流。细胞外溶液由(mm):NaCl,130;氯化钾,5;BaCl2,2;氯化镁1;葡萄糖,30;HEPES氢氧化钠,25;pH 7.3,电极填充细胞内溶液如下(mm):CsCl,140;氯化镁4;EGTA,10;HEPES CsOH,10;pH 7.3。通过比较激动剂测试浓度诱发的峰值反应与之前记录的对1μm辣椒素的控制电流诱发的峰值响应,生成了浓度-反应曲线。通过测量电压斜坡(-70至+70 mV)期间的净激动剂诱发电流反应,建立了电流-电压关系。从添加药物前对照溶液中两个或三个电压斜坡的平均值中获得的基线,从药物存在时峰值电流下的三到五个电压斜坡平均值中减去(见图2c)。在这些实验中,所有数据都归一化为在-70 mV的保持电位下获得的初始电流。 |
| 细胞实验 |
细胞活力测定[2]
细胞类型:人咽鳞状癌细胞 (FaDu) 测试浓度:50 µM、100 µM、200 µM 和 300 µM 孵育时间:24 小时、48 小时和 72 小时 实验结果: 显示细胞生长。 细胞凋亡分析[2] 细胞类型: FaDu 细胞 测试浓度: 50 µM、100 µM 和 200 µM 孵育持续时间:12小时 实验结果:caspase 3的活性以时间依赖性方式增加。 蛋白质印迹分析[2] 细胞类型: FaDu 细胞 测试浓度: 200 µM 孵育时间:24小时 实验结果:观察到caspase 3和PARP (p85)水平的激活。 |
| 动物实验 |
动物/疾病模型:苯并[a]芘诱导的瑞士白化小鼠(20-25 g;8-10 周龄)[3]
剂量:10 mg/kg 给药途径:腹腔注射;腹腔注射。每周一次,连续14周 实验结果:抑制小鼠肺癌的发生发展。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
口服:口服后,辣椒素可通过非活性过程从胃和全肠吸收,吸收率因动物而异,介于 50% 至 90% 之间。给药后 1 小时内即可达到血药浓度峰值。辣椒素从胃吸收进入小肠后,可能在小肠上皮细胞中发生少量代谢。虽然人体口服药代动力学信息有限,但摄入等效剂量 26.6 mg 纯辣椒素后,10 分钟即可在血浆中检测到辣椒素,并在 47.1 ± 2.0 分钟达到血浆峰浓度 2.47 ± 0.13 ng/ml。 全身吸收:动物静脉或皮下注射后,脑和脊髓中的药物浓度约为血液中的5倍,肝脏中的药物浓度约为血液中的3倍。局部用药:辣椒素在人体皮肤上能被迅速且充分吸收,但局部或经皮给药后不太可能发生全身吸收。对使用含179 mg辣椒素的局部贴剂的患者进行了群体分析,并使用一级吸收和线性消除的一室模型拟合了血浆中辣椒素的浓度。平均血浆峰浓度为1.86 ng/mL,但任何患者观察到的最高值为17.8 ng/mL。 据推测,辣椒素主要以原形和葡萄糖醛酸苷两种形式经肾脏排泄。少量原形化合物经粪便和尿液排出。体内动物研究表明,48小时后,面部检测到的给药剂量不足10%。用于局部镇痛的处方药和非处方药,包括乳膏、洗剂和贴剂,均含有辣椒素(CAP)和二氢辣椒素(DHC)。目前关于CAP和DHC的吸收、生物利用度和体内分布的体内研究较少。我们建立了一种灵敏快速的液相色谱-串联质谱(LC-MS/MS)分析方法,用于测定兔血浆和组织中CAP和DHC的含量。采用正己烷-二氯甲烷-异丙醇(100:50:5,v/v/v)混合物进行液液萃取制备生物样品,然后使用Extend C18色谱柱进行等度色谱分离。流动相为乙腈-水-甲酸(70:30:0.1,v/v/v)。对于 100 μL 生物样品,该方法在 0.125 至 50 ng/mL 范围内呈线性关系,定量下限为 0.125 ng/mL。分析每个样品的总运行时间为 3.5 分钟。我们采用该验证方法研究了局部应用辣椒素凝胶(CAP 凝胶)在兔体内的药代动力学和组织分布。极少量的辣椒素和二氢辣椒素被吸收进入体循环。血浆中最高浓度为 2.39 ng/mL,应用 CAP 凝胶 12 小时后的平均血浆峰浓度为 1.68 ng/mL。药物在治疗皮肤中的浓度相对较高,而在其他组织中的浓度较低。因此,局部应用辣椒素凝胶具有较强的局部作用和较弱的全身作用。 代谢/代谢物 口服辣椒素的代谢途径尚不明确,但预计主要在肝脏代谢,在肠腔内的代谢极少。体外研究表明,辣椒素在人肝微粒体和S9片段中代谢迅速,主要生成三种代谢物:16-羟基辣椒素、17-羟基辣椒素和16,17-羟基辣椒素,而香草醛则是一种次要代谢物。研究推测细胞色素P450(P450)酶可能在肝脏药物代谢中发挥作用。体外研究表明,辣椒素在人皮肤中的生物转化缓慢,大部分辣椒素保持不变。辣椒素和二氢辣椒素是胡椒喷雾剂的主要活性成分,胡椒喷雾剂被广泛用于执法和自卫。由于胡椒喷雾剂具有不可逆的健康危害,其使用一直备受争议。本研究利用人肝细胞、猪肝细胞组分和人肺癌细胞系(A549)在体外比较了辣椒素和二氢辣椒素的代谢和细胞毒性。采用液相色谱-串联质谱(LC-MS/MS)对代谢产物进行筛选和鉴定。在肝细胞组分中,检测到一种新型的二氢辣椒素脂肪族羟基化代谢产物(m/z 322),但未发现与辣椒素对应的结构。相反,鉴定出一种新型的辣椒素I期代谢产物,其结构对应于脂肪族脱甲基和脱氢反应(m/z 294)。此外,还鉴定出辣椒素和二氢辣椒素的两种新型结合物:甘氨酸结合物(m/z 363和m/z 365)和双谷胱甘肽(GSH)结合物(m/z 902和m/z 904)。暴露于辣椒素的A549细胞培养基中含有ω-羟基化(m/z 322)和烷基脱氢(m/z 304)形式的辣椒素,以及一种甘氨酸结合物。对于二氢辣椒素,则发现了一种烷基脱氢(m/z 306)形式、一种新型烷基羟基化形式和一种新型甘氨酸结合物。在A549细胞中,二氢辣椒素比辣椒素更能有效地诱导细胞空泡化并降低细胞活力。此外,两种化合物均能诱导p53蛋白表达和G1期细胞周期阻滞。这些代谢物作为辣椒素类物质暴露生物标志物的实用性需要通过其他毒性终点指标进行进一步研究。 ……辣椒素的脱氢是一条新的代谢途径,产生了独特的环状、二烯和酰亚胺代谢物。 1-氨基苯并三唑 (1-ABT) 可抑制微粒体对辣椒素的代谢。CYP1A1、1A2、2B6、2C8、2C9、2C19、2D6、2E1 和 3A4 可催化辣椒素的代谢。在微粒体孵育液中加入 GSH (2 mM) 可刺激辣椒素的代谢,并捕获多种活性亲电中间体,使其与 GSH 形成加合物。/本研究使用重组 P450 酶以及来自包括人类在内的多种物种的肝微粒体和肺微粒体进行。/ 本研究旨在利用肝微粒体表征辣椒素的葡萄糖醛酸化,并确定各种 UDP-葡萄糖醛酸转移酶 (UGT) 对肝脏辣椒素葡萄糖醛酸化的作用。通过将辣椒素与添加了尿苷二磷酸葡萄糖醛酸的微粒体孵育,测定了葡萄糖醛酸化速率。动力学参数通过模型拟合获得。测定了相对活性因子、表达-活性相关性和活性相关性,以鉴定参与辣椒素代谢的主要UGT酶。辣椒素在混合人肝微粒体(pHLM)中能被高效地葡萄糖醛酸化。UGT1A1、1A9和2B7(以及胃肠道酶UGT1A7和1A8)均表现出相当高的活性。在包含14个个体人肝微粒体样本的样本库中,辣椒素的葡萄糖醛酸化与β-雌二醇的3-O-葡萄糖醛酸化(r=0.637;p=0.014)以及UGT1A1蛋白水平(r=0.616;p=0.019)均显著相关。此外,辣椒素的葡萄糖醛酸化与齐多夫定的葡萄糖醛酸化(r=0.765;p<0.01)以及UGT2B7蛋白水平(r=0.721;p<0.01)均呈显著正相关。在人肝微粒体(pHLM)中,UGT1A1、1A9和2B7分别贡献了辣椒素总葡萄糖醛酸化的30.3%、6.0%和49.0%。此外,肝微粒体对辣椒素的葡萄糖醛酸化作用表现出显著的物种差异。 生物半衰期 口服等效剂量26.6 mg纯辣椒素后,其半衰期约为24.9 ± 5.0 min。局部应用3%辣椒素溶液后,辣椒素的半衰期约为24 h。使用含有 179 毫克辣椒素的局部贴剂后,平均人群消除半衰期为 1.64 小时。 |
| 毒性/毒理 (Toxicokinetics/TK) |
毒性概述
识别与用途:辣椒素是一种纯深红色固体。它可用作外用药物和神经生物学研究工具。辣椒素及其衍生物被认为具有多种健康益处,包括抗癌活性、抗炎活性、抗肥胖活性和镇痛作用。外用辣椒素用于治疗带状疱疹后神经痛、骨关节炎和糖尿病性神经痛。然而,这些物质强烈的辛辣味和潜在的神经毒性限制了它们在食品、营养补充剂和药品中的应用。人体暴露与毒性:辣椒素是一种强刺激物;初次使用会引起剧烈疼痛。长期使用会导致对疼痛刺激的敏感性降低,并诱发某些初级感觉神经元的选择性退化。接触含辣椒素的辣椒引起的疼痛是中毒控制中心接诊的最常见的植物相关中毒病例之一。它们会刺激皮肤,引起灼烧或刺痛感;成人大量摄入或儿童少量摄入,会导致恶心、呕吐、腹痛和灼烧性腹泻。接触眼睛会导致剧烈流泪、疼痛、结膜炎和眼睑痉挛。辣椒素对眼睛的刺激作用已被用于含有辣椒素的加压驱狗喷雾剂中。曾有一名男孩不慎被这种喷雾剂喷到眼睛,他的眼睛立即感到刺痛、流泪并发红,但第二天就恢复正常了。“湖南手”是一种接触性皮炎,由直接接触含有辣椒素的辣椒引起。在人类肺癌和前列腺癌细胞中,辣椒素会刺激DNA双链断裂和微核的产生。辣椒素还被发现是A549细胞中DNA高甲基化的诱导剂。动物实验:将50 μg/mL的辣椒素滴于大鼠眼内,可引起明显的疼痛和眼睑痉挛。结膜和眼睑血管对静脉注射的伊文思蓝染料的通透性异常增加。局部麻醉可缓解疼痛,但对血管反应无影响。在兔眼玻璃体内注射辣椒素可引起瞳孔缩小和血-房水屏障破坏。雄性小鼠和雌性小鼠的口服LD50值分别为118.8 mg/kg和97.4 mg/kg,雄性大鼠和雌性大鼠的口服LD50值分别为161.2 mg/kg和148.1 mg/kg。小鼠的主要毒性症状包括流涎、皮肤红斑、步态蹒跚、呼吸缓慢和紫绀。部分动物在给药后4至26分钟内出现震颤、阵挛性抽搐、呼吸困难和侧卧或俯卧位,随后死亡。小鼠存活后6小时内恢复,大鼠存活后24小时内恢复。大鼠的毒性症状与小鼠几乎相同,但大鼠出现紫绀、阵挛性或强直性抽搐、呼吸困难和侧卧位的发生率更高,且恢复时间晚于小鼠。辣椒素可引起大鼠发育神经毒性。遗传毒性试验结果证实,高纯度辣椒素在细菌突变试验和染色体畸变试验中不具有遗传毒性。此外,在大鼠骨髓微核试验中也未观察到细胞毒性或遗传毒性。在雌性小鼠单次注射7,12-二甲基苯并蒽后,反复在其剃毛背部涂抹辣椒素,与溶剂对照组相比,并未导致乳头状瘤形成以及异常增生或炎症性皮肤病变的显著增加。局部涂抹辣椒素不会诱导表皮鸟氨酸脱羧酶活性。当与肿瘤促进剂12-O-十四烷酰佛波醇-13-乙酸酯同时给药时,该化合物可减轻小鼠皮肤癌的发生。 辣椒素引起的灼烧感和疼痛感源于其与感觉神经元的化学相互作用。辣椒素作为香草醛类化合物,可与香草醛受体1 (VR1) 结合。VR1被激活后,允许阳离子穿过细胞膜进入细胞。由此产生的神经元去极化刺激其向大脑发出信号。辣椒素分子通过与 VR1 受体结合,产生与过热或磨损损伤相同的感觉,这解释了为什么辣椒素的辛辣味被描述为灼烧感。 (L1246) 毒性数据 LD50:47200 ug/kg(口服,小鼠)(T13) LD50:6500 ug/kg(腹腔注射,小鼠)(T13) LD50:9000 ug/kg(皮下注射,小鼠)(T13) LD50:400 ug/kg(静脉注射,小鼠)(T13) LD50:7800 ug/kg(肌肉注射,小鼠)(T13) LD50:1600 ug/kg(气管内注射,小鼠)(T13) 相互作用 ……在用辣椒素(0.3 uM;30 分钟)处理豚鼠气管平滑肌制剂后,最大乙酰甲胆碱刺激后气管收缩显著增强(辣椒素组:1.147 ± 0.050 g,对照组:0.717 ± 0.047 g)。预先使用辣椒素受体拮抗剂(2-[2-(4-氯苯基)乙基-氨基-硫代羰基]-7,8-二羟基-2,3,4,5-四氢-1H-2-苯并氮杂卓;一种香草醛受体拮抗剂)和YM38336(一种速激肽NK1和速激肽NK2双重受体拮抗剂)处理后,该效应完全消失。 ……用5-30 μg/mL辣椒素处理HL-60细胞72小时可抑制细胞增殖并诱导细胞分化略有增加。当辣椒素与 5 nM 1,25-(OH)₂D₃ 或 50 nM 全反式维甲酸联合使用时,观察到 HL-60 细胞分化的协同诱导作用。流式细胞术分析表明,1,25-(OH)₂D₃ 与辣椒素的组合主要刺激细胞分化为单核细胞,而全反式维甲酸与辣椒素的组合主要刺激细胞分化为粒细胞。辣椒素增强了经 1,25-(OH)₂D₃ 和全反式维甲酸处理的 HL-60 细胞中蛋白激酶 C 的活性。此外,蛋白激酶C抑制剂[双吲哚基马来酰亚胺(GF-109203X)、chelerythrine、1-(5-异喹啉磺酰基)-2-甲基哌嗪二盐酸盐(H-7)]和细胞外信号调节激酶抑制剂[2-(2'-氨基-3'-甲氧基苯基)-氧萘-4-酮(PD-098059)]显著抑制了辣椒素联合1,25-(OH)₂D₃或全反式维甲酸诱导的HL-60细胞分化。 ……辣椒素和壬酰胺显著增强了吲哚美辛在裸鼠皮肤上的转运。……组织学检查结合视觉评分表明辣椒素和壬酰胺对皮肤结构安全。与单独使用超声或增强剂相比,同时使用超声和增强剂可显著提高吲哚美辛的皮肤渗透性。 用瞬时受体电位香草酸受体1 (TRPV1) 通道激动剂辣椒素处理新生大鼠,会导致表达TRPV1通道的感觉神经元终身丢失。此前研究表明,出生后第2天接受辣椒素处理的大鼠在5-7周龄时在新环境中表现出行为过度活跃,并且大脑变化类似于精神分裂症患者的大脑变化。本研究旨在探讨新生期接受辣椒素处理的成年大鼠的大脑和行为反应。研究发现,新生期接受辣椒素处理的大鼠在5-7周龄时出现的大脑变化持续到成年期(12周龄),但在老年大鼠(16-18周龄)中有所减轻。这些大鼠在8周龄和12周龄时表现出声惊反射前脉冲抑制(PPI)增强,而非精神分裂症动物模型中常见的PPI缺陷。精神分裂症患者对烟酸和烟酸甲酯的红斑反应也减弱,这被认为是由前列腺素D2(PGD2)介导的。红斑反应伴有皮肤血浆渗出。研究发现,辣椒素处理的大鼠对烟酸甲酯和PGD2的皮肤血浆渗出反应减弱。总之,在辣椒素处理的大鼠中观察到的几种神经解剖学变化以及皮肤血浆渗出反应的减少表明,TRPV1通道在精神分裂症中的作用值得研究。 有关辣椒素的更多相互作用(完整)数据(共21项),请访问HSDB记录页面。 非人类毒性值 小鼠口服LD50 >2500 mg/kg 大鼠腹腔注射LD50 9500 ug/kg 小鼠口服LD50 47200 ug/kg 小鼠腹腔注射LD50 6500 ug/kg 有关辣椒素的更多非人类毒性值(完整)数据(共13项),请访问HSDB记录页面。 |
| 参考文献 |
[1]. McNamara FN, et al. Effects of piperine, the pungent component of black pepper, at the human vanilloid receptor (TRPV1). Br J Pharmacol. 2005 Mar;144(6):781-90.
[2]. Shin YH, et al. The Effect of Capsaicin on Salivary Gland Dysfunction. Molecules. 2016 Jun 25;21(7). [3]. Anandakumar P, et al. Capsaicin provokes apoptosis and restricts benzo(a)pyrene induced lung tumorigenesis in Swiss albino mice. Int Immunopharmacol. 2013 Jun 6;17(2):254-259. |
| 其他信息 |
治疗用途
辣椒素似乎对骨关节炎 (OA) 疼痛有效,但其疗效是否具有剂量反应关系、在不同关节间是否一致以及是否会随时间变化尚不确定。我们从 PubMed、EMBASE 和 ISI Web of Knowledge 数据库中检索了关于局部应用辣椒素治疗 OA 的随机对照试验。使用 RevMan 软件,通过标准化均数差 (SMD) 评估了辣椒素对疼痛评分、患者对治疗效果的总体评价以及用药部位灼烧感的影响。共检索到 5 项双盲随机对照试验和 1 项病例交叉试验。辣椒素制剂的浓度范围为 0.025% 至 0.075%,试验持续时间为 4 至 12 周。试验评估了膝关节 (n=3)、手部 (n=1) 和混合关节 (n=2) 的 OA。辣椒素治疗对VAS疼痛评分变化的疗效(与安慰剂相比)为中等,4周治疗后疗效为0.44(95% CI:0.25-0.62)。各研究间无异质性,表明研究间无差异,包括OA部位或治疗浓度的影响。两项研究报告了超过4周的治疗情况,结果不一。一项研究报告称,12周后效应量为-9 mm,组间差异在第4周达到最大值。另一项研究报告称,组间差异随时间推移而增大,直至20周。据报道,辣椒素安全且耐受性良好,无全身毒性。35%至100%的辣椒素治疗患者出现轻度用药部位灼烧感,风险比为4.22(95% CI:3.25-5.48,n=5项试验);发生率在第1周达到高峰,随后随时间推移而下降。对于至少中度疼痛且经临床或放射学确诊为骨关节炎的患者,无论用药部位和剂量如何,局部应用辣椒素每日四次治疗均可在长达 20 周的时间内有效减轻疼痛强度,且耐受性良好。 咳嗽过敏在呼吸系统疾病中很常见。本研究旨在确定临床稳定的成人支气管扩张患者的辣椒素咳嗽敏感性与临床参数之间的关联。我们招募了 135 例连续就诊的成人支气管扩张患者和 22 名健康受试者。所有受试者均接受了病史询问、痰培养、肺功能检查、胸部高分辨率计算机断层扫描 (HRCT)、莱斯特咳嗽问卷评分、支气管扩张严重程度指数 (BSI) 评估和辣椒素吸入激发试验。咳嗽敏感性以引起至少 2 次咳嗽 (C2) 和 5 次咳嗽 (C5) 的辣椒素浓度来衡量。尽管健康受试者和支气管扩张患者之间存在显著重叠,但后者的 C2 和 C5 水平显著低于健康受试者(所有 p<0.01)。较低的 C5 水平与支气管扩张症状持续时间更长、HRCT 评分更差、24 小时痰量更高、BSI 和痰液脓性评分更高以及痰培养铜绿假单胞菌阳性相关。与辣椒素咳嗽敏感性增加(定义为C5≤62.5 μmol/L)相关的决定因素包括:女性(OR:3.25,95%CI:1.35-7.83,p<0.01)、HRCT总评分在7-12分之间(OR:2.57,95%CI:1.07-6.173,p=0.04)、BSI评分在5-8分之间(OR:4.05,95%CI:1.48-11.06,p<0.01)以及≥9分(OR:4.38,95%CI:1.48-12.93,p<0.01)。辣椒素咳嗽敏感性在部分支气管扩张患者中升高,且与疾病严重程度相关。性别和疾病严重程度(而非痰液脓性)是辣椒素咳嗽敏感性增高的独立决定因素。目前用于诊断咳嗽敏感性的检测方法可能存在局限性,因为其与健康受试者存在重叠,但或许可以为未来的临床试验提供客观的咳嗽评估指标。 由环境刺激物引发的慢性不明原因咳嗽的特征是咳嗽反射敏感性增高,这可以通过吸入辣椒素来证实。局部应用辣椒素可以改善非过敏性鼻炎和肠道高敏感性,并减轻神经性疼痛。我们研究了口服天然辣椒素(辣椒)是否可以降低咳嗽反射敏感性并改善不明原因咳嗽。本研究纳入了24例由刺激物诱发的不明原因慢性咳嗽患者和15例健康对照者。受试者分别服用纯辣椒素胶囊4周,以及安慰剂胶囊4周。该研究采用交叉、随机、双盲设计。研究期间,通过标准化的辣椒素吸入咳嗽试验评估咳嗽敏感性,该试验测定达到两次咳嗽(C2)和五次咳嗽(C5)所需的辣椒素浓度。参与者还填写了关于咳嗽及咳嗽相关症状的问卷。三名患者在研究结束前退出,其中一名在活性治疗期退出,两名在安慰剂期退出。辣椒素治疗后,患者组(p<0.020)和对照组(p<0.0061)的C2阈值均高于安慰剂期(改善)。在患者组中,活性物质治疗后达到C2(p<0.0004)和C5(p<0.0009)所需的浓度均高于基线咳嗽阈值。活性治疗4周后,咳嗽症状评分较基线评分有所改善(p<0.0030)。口服辣椒素粉可降低辣椒素咳嗽敏感性和咳嗽症状。研究结果提示咳嗽敏感性瞬时受体电位香草酸受体1 (TRPV1) 发生脱敏。 Qutenza 是一种高剂量辣椒素贴剂,用于缓解带状疱疹后神经痛 (PHN) 和 HIV 相关神经病变 (HIV-AN) 引起的神经性疼痛。临床研究表明,部分患者对辣椒素贴剂的反应显著。我们的目标是确定最能从辣椒素贴剂治疗中获益的患者的基线特征。我们对 6 项已完成的 Qutenza 随机对照研究进行了荟萃分析,汇总了患者的个体数据。持续缓解定义为从基线到第 2 至 12 周平均疼痛强度下降 50% 以上,完全缓解定义为第 2 至 12 周平均疼痛强度评分为 1。我们采用逻辑回归分析来识别缓解和完全缓解的预测因子,以及对辣椒素贴剂反应最佳的患者亚组。基线疼痛强度评分(BPIS)=4 是带状疱疹后神经痛(PHN)和 HIV 相关神经痛(HIV-AN)患者持续缓解和完全缓解的预测因子;无痛觉过敏、存在感觉减退以及麦吉尔疼痛问卷(MPQ)感觉评分<22 是 PHN 患者持续缓解的预测因子;女性是 HIV-AN 患者持续缓解和完全缓解的预测因子。因此,与辣椒素贴剂治疗最高反应率相关的特征,对于 PHN 患者为 BPIS=4、MPQ 感觉评分=22、无痛觉过敏以及存在感觉减退;对于 HIV-AN 患者为女性和 BPIS=4。具有这些特征的患者对辣椒素贴剂的反应率显著高于其他患者。 有关辣椒素(共21种)的更多治疗用途(完整)数据,请访问HSDB记录页面。 药物警告 使用后会出现轻度至中度的灼烧感,部分患者的灼烧感可能较为严重,需要停止治疗。 必须防止辣椒素进入眼睛、开放性伤口或黏膜。 ……辣椒素仅供外用。不应涂抹于伤口、受损或受刺激的皮肤上。不应紧紧包裹。辣椒素不应接触黏膜、眼睛或隐形眼镜。如果发生这种情况,应立即用清水彻底冲洗受影响的区域。如果病情恶化或规律使用后没有改善,应停止使用本产品并咨询医疗保健专业人员。如果出现水疱或严重灼烧感持续存在,请勿在用药前后立即对治疗部位进行加热,因为这可能会加剧灼烧感。/非处方辣椒素/ 请勿将处方辣椒素涂抹于面部或头皮,以免接触眼睛或黏膜。 有关辣椒素(共14条)的更多药物警告(完整)数据,请访问HSDB记录页面。 药效学 辣椒素是TRPV1受体激动剂。TRPV1是一种跨膜受体-离子通道复合物,可被高于43摄氏度的温度、低于6的pH值和内源性脂质激活。当这些因素共同激活时,该通道可短暂开放,并由于钙离子和钠离子的内流而引发去极化。由于TRPV1主要表达于A-δ纤维和C纤维,其去极化作用会产生动作电位,并将冲动传递至大脑和脊髓。这些冲动导致辣椒素产生温热、刺痛、瘙痒、灼烧或灼烧感等反应。与环境激动剂相比,辣椒素还会导致这些受体更持久的激活,从而导致对许多感觉刺激的反应丧失,即所谓的“功能丧失”。辣椒素还会引起多种酶促、细胞骨架和渗透压变化,以及线粒体呼吸的紊乱,从而长时间损害伤害感受器的功能。 |
| 分子式 |
C18H27NO3
|
|---|---|
| 分子量 |
293.4012
|
| 精确质量 |
305.199
|
| 元素分析 |
C, 70.79; H, 8.91; N, 4.59; O, 15.72
|
| CAS号 |
404-86-4
|
| 相关CAS号 |
Capsaicinoid;404-86-4;(E/Z)-Capsaicin-d3;1185237-43-7;(Z)-Capsaicin;25775-90-0;Capsaicin-d3;1217899-52-9
|
| PubChem CID |
1548943
|
| 外观&性状 |
Pure dark red solid
Monoclinic rectangular plates or scales from petroleum ether Monoclinic, rectangular plates, crystals and scales |
| 密度 |
1.0±0.1 g/cm3
|
| 沸点 |
469.7±55.0 °C at 760 mmHg
|
| 熔点 |
65 °C
; 65 °C
; 149 °F
|
| 闪点 |
237.9±31.5 °C
|
| 蒸汽压 |
0.0±1.2 mmHg at 25°C
|
| 折射率 |
1.508
|
| LogP |
4.27
|
| tPSA |
58.56
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
9
|
| 重原子数目 |
22
|
| 分子复杂度/Complexity |
341
|
| 定义原子立体中心数目 |
0
|
| SMILES |
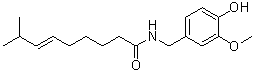
O=C(C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H])N([H])C([H])([H])C1C([H])=C([H])C(=C(C=1[H])OC([H])([H])[H])O[H]
|
| InChi Key |
YKPUWZUDDOIDPM-SOFGYWHQSA-N
|
| InChi Code |
InChI=1S/C18H27NO3/c1-14(2)8-6-4-5-7-9-18(21)19-13-15-10-11-16(20)17(12-15)22-3/h6,8,10-12,14,20H,4-5,7,9,13H2,1-3H3,(H,19,21)/b8-6+
|
| 化学名 |
8-Methyl-N-vanillyl-(trans)-6-nonenamide
|
| 别名 |
(E)-Capsaicin Capsicine Capsicin PS C (E)Capsaicin; Zostrix; CAPSAICINE; Qutenza; Styptysat; Axsain;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 本产品在运输和储存过程中需避光。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~327.43 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 20 mg/mL (65.49 mM) (饱和度未知) in 10% EtOH + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 200.0 mg/mL 澄清 EtOH 储备液加入900 μL 玉米油中,混合均匀。 配方 2 中的溶解度: ≥ 2.5 mg/mL (8.19 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (8.19 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: ≥ 2.5 mg/mL (8.19 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL 澄清 DMSO 储备液加入900 μL 玉米油中,混合均匀。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.4083 mL | 17.0416 mL | 34.0832 mL | |
| 5 mM | 0.6817 mL | 3.4083 mL | 6.8166 mL | |
| 10 mM | 0.3408 mL | 1.7042 mL | 3.4083 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。