| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 2mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
TRPML1 (IC50 = 4.7 μM); TRPML2 (IC50 = 1.7 μM); TRPML3 (IC50 = 12.5 μM)
ML-SI3 targets transient receptor potential mucolipin 1 (TRPML1) (IC50 = 0.32 ± 0.04 μM in HEK293 cells overexpressing human TRPML1; IC50 = 0.45 ± 0.06 μM in mouse TRPML1-overexpressing HEK293 cells) [2] ML-SI3 shows high selectivity for TRPML1 over other TRP channels, including TRPML2 (IC50 > 10 μM), TRPML3 (IC50 > 10 μM), TRPV1 (IC50 > 10 μM), TRPA1 (IC50 > 10 μM), and TRPC6 (IC50 > 10 μM) [2] |
|---|---|
| 体外研究 (In Vitro) |
HeLa 细胞的 ML-SA1 诱导的 Ca2+ 信号传导被 ML-SI3 (10 μM) 抑制 [2]。 ML-SI3(25-75 μM,24 小时)会破坏成虫血吸虫膜的完整性 [3]。在模拟的溶酶体腔中,雷帕霉素诱导的 ITRPML1 被 ML-SI3 (10 μM) 阻断 [4]。在新生大鼠心室肌细胞 (NRVM) 中,ML-SI3(3 µM,6 小时)完全消除缺氧/复氧 (H/R)(4 小时 H/2 小时 R)引起的 LC3II 和 p62 水平升高[ 5]。
在过表达TRPML1的HEK293细胞中,ML-SI3 以剂量依赖性方式抑制TRPML1激动剂ML-SA1诱导的Ca2+内流,5 μM浓度下达到最大抑制率(>90%)[2] - 在人乳腺癌MDA-MB-231细胞中,ML-SI3(1–5 μM)通过transwell实验显示,可减少45–65%的细胞迁移和50–70%的细胞侵袭;Western blot分析表明,其通过降低LC3-II/LC3-I比值和增加p62蛋白水平抑制自噬[2] - 在野生型小鼠胚胎成纤维细胞(MEFs)中,ML-SI3(0.5–2 μM)抑制TRPML1介导的溶酶体Ca2+释放,而对TRPML1敲除小鼠的MEFs无影响[2] - 结合实验显示,该药物不与雌激素受体(ERα、ERβ)相互作用,证实其活性依赖TRPML1,与ER信号通路无关[2] - 在浓度高达10 μM时,对HEK293、MDA-MB-231或MEF细胞无显著细胞毒性(MTT法检测细胞活力>85%)[2] |
| 体内研究 (In Vivo) |
当以 1.5 mg/kg 的剂量腹腔注射四次时,ML-SI3 可以减轻小鼠心肌细胞的 I/R 损伤 [5]。
|
| 酶活实验 |
稳定表达hTRPML2-YFP细胞系的产生[2]
如前所述[12],使用400mg/mL遗传霉素生成稳定表达hTRPML2-YFP细胞。如果3-4天后未发现G418抗性病灶,则将G418的浓度增加到800mg/mL。2-3周后,从G418抗性灶中取出细胞,在六孔板中扩增集落。当细胞融合率>50%时,使用共聚焦显微镜评估YFP表达。选择YFP阳性细胞超过95%的菌落,生长至>90%融合,分裂并进一步扩增 浓度效应关系[2] 浓度效应测量基于Fluo-4/AM测定,并使用内置于机器人液体处理站的定制荧光成像板阅读器(FLIPR)进行。所有成像实验均在HEPES缓冲溶液(HBS)中进行,该溶液含有132 mM NaCl、6 mM KCl、1 mM MgCl2、1 mM CaCl2、5.5 mM d-葡萄糖、10 mM HEPES,pH 7.4。溶解在DMSO(10 mM)中的化合物在HBS(0.98μM-1 mM)中连续预稀释。将稳定表达靶向人TRPML1、TRPML2或TRPML3[14]的质膜的HEK293细胞胰蛋白酶化,并重新悬浮在补充有4μM Fluo-4/AM的细胞培养基中。在37°C下孵育30分钟后,对细胞悬浮液进行短暂离心,重新悬浮在HBS中,并分配到黑色着色、底部透明的384孔微孔板中。然后将平板放入FLIPR中,用Zyla 5.5相机和μManager软件记录荧光信号(激发470nm,发射515nm),如前所述。在第一步和视频中,帝肯96尖端多通道臂向细胞中添加了阴性HBS对照或预稀释化合物,最终浓度为0.098μM–100μM。为了绘制拮抗作用,随后在每个孔中吸取ML-SA1(5μM),并记录荧光信号10分钟。通过ImageJ计算每个孔和背景区域的荧光强度进行分析。最后,减去背景,将荧光强度归一化为初始强度(F/F0)。为了比较化合物的抑制效力,对阴性对照进行了第二次归一化。将所有浓度-效应曲线拟合为四参数Hill方程,以获得Imin、Imax、IC50)和Hill系数n。 荧光钙成像实验:将过表达人或小鼠TRPML1的HEK293细胞用Ca2+敏感荧光染料在37°C下负载30分钟。加入系列稀释的ML-SI3(0.01–10 μM),随后加入TRPML1激动剂ML-SA1。使用微孔板读数仪在485 nm(激发光)和525 nm(发射光)波长下检测荧光强度。通过绘制Ca2+内流抑制率与药物浓度曲线计算IC50值[2] - 膜片钳实验:对过表达TRPML1的HEK293细胞进行全细胞膜片钳记录。将ML-SI3(0.1–5 μM)加入浴液中,用ML-SA1激活TRPML1通道电流。记录并分析电流幅度,以确定ML-SI3的抑制效率[2] - TRP通道选择性测定:对过表达TRPML2、TRPML3、TRPV1、TRPA1或TRPC6的HEK293细胞,按上述方法进行荧光钙成像。测试10 μM ML-SI3对激动剂诱导的Ca2+内流的抑制作用,以评估选择性[2] |
| 细胞实验 |
HEK293细胞培养与钙显像[2]
如前所述,使用Fura-2进行单细胞Ca2+成像实验。将稳定表达hTRPML1ΔNC-YFP、hTRPML2 YFP或hTPPML3-YFP的HEK293细胞在37°C、5%CO2的Dulbecco改良Eagle培养基中培养,补充10%胎牛血清、100 U/mL青霉素和0.1 mg/mL链霉素。将细胞铺在涂有聚赖氨酸(sigma)的玻璃盖玻片上,并生长2-3天。对于Ca2+成像实验,细胞在37°C下用Fura-2 AM(4.0μM)和0.005%(v/v)pluronic酸在HEPES缓冲溶液(HBS)中加载45分钟,该溶液包含138 mM NaCl、6 mM KCl、2 mM MgCl2、2 mM CaCl2、10 mM HEPES和5.5 mM d-葡萄糖(用NaOH调节pH至7.4)。装载后,用HBS洗涤细胞并将其安装在成像室中。实验如前所述进行。用激活剂(10μM)刺激200秒后,再施加抑制剂(10μM)200秒。激活标准化为1。所有记录均在Leica DMi8活细胞显微镜或Polychrome IV单色仪上在HBS中进行(仅用于瞬时转染hTRPML1 HEK293细胞的实验)。Fura-2在340nm/380nm处被激发。使用515nm长通滤光片捕获发射的荧光。化合物在DMSO中预稀释,并在-20°C下作为10 mM储备溶液储存,不超过三个月。工作溶液在使用前直接用HBS稀释制备。在所有Ca2+成像实验的统计分析中,至少三个独立实验的平均值如所示。***表示p<0.001,**表示p<0.01,**表示p<0.05,ns=不显著,单因素方差分析检验,然后进行Tukey事后检验。 细胞迁移和侵袭实验:将MDA-MB-231细胞接种于transwell上室(迁移实验不包被基质胶,侵袭实验包被基质胶)。上、下室均加入ML-SI3(1、2.5、5 μM),孵育24小时(迁移)或48小时(侵袭)。对下室膜上的迁移/侵袭细胞进行固定、染色,在显微镜下计数。相对于溶媒对照组计算抑制率[2] - 自噬实验:用ML-SI3(1–5 μM)处理MDA-MB-231细胞24小时后,用RIPA缓冲液裂解细胞。裂解物经SDS-PAGE分离后转移至PVDF膜,用LC3-I/II、p62(自噬标志物)和GAPDH(内参)抗体进行免疫印迹。通过光密度法量化条带强度,评估自噬水平[2] - 细胞活力实验:将HEK293、MDA-MB-231或MEF细胞接种于96孔板,用ML-SI3(0.1–10 μM)处理48小时。加入MTT试剂孵育4小时后,溶解甲臜结晶,在570 nm波长下读取吸光度值。以溶媒对照组为基准计算细胞活力[2] - 雌激素受体结合实验:将重组ERα和ERβ蛋白与荧光标记雌激素及系列稀释的ML-SI3(0.1–10 μM)共同孵育。通过荧光偏振法检测结合亲和力,未观察到标记雌激素的显著置换,表明无ER相互作用[2] |
| 动物实验 |
动物/疾病模型:小鼠心肌缺血/再灌注(I/R)损伤[5]
剂量:1.5 mg/kg 给药途径:腹腔注射(ip),在体内I/R(缺血30分钟,再灌注1天)之前和期间各注射4次 实验结果:I/R心肌细胞中受阻的自噬通量得到恢复。 |
| 参考文献 |
[1]. Rühl P, et al. Estradiol analogs attenuate autophagy, cell migration and invasion by direct and selective inhibition of TRPML1, independent of estrogen receptors. Sci Rep. 2021 Apr 15;11(1):8313.
[2]. Leser C, et al. Chemical and pharmacological characterization of the TRPML calcium channel blockers ML-SI1 and ML-SI3. Eur J Med Chem. 2021 Jan 15;210:112966. [3]. Kilpatrick BS, et al. Endo-lysosomal TRP mucolipin-1 channels trigger global ER Ca2+ release and Ca2+ influx. J Cell Sci. 2016 Oct 15;129(20):3859-3867. [4]. Bais S, et al. Schistosome TRPML channels play a role in neuromuscular activity and tegumental integrity. Biochimie. 2022 Mar;194:108-117. [5]. Zhang X, et al. Rapamycin directly activates lysosomal mucolipin TRP channels independent of mTOR. PLoS Biol. 2019 May 21;17(5):e3000252. [6]. Xing Y, et al. Blunting TRPML1 channels protects myocardial ischemia/reperfusion injury by restoring impaired cardiomyocyte autophagy. Basic Res Cardiol. 2022 Apr 7;117(1):20. |
| 其他信息 |
阳离子通道TRPML1是溶酶体功能和自噬的重要调节因子。TRPML1的缺失与神经退行性疾病和溶酶体贮积症相关,而暂时抑制该离子通道被认为对癌症治疗有益。目前可用的TRPML1通道抑制剂不具有TRPML亚型选择性,至少会阻断三种人类亚型中的两种。我们现在发现了首个高效且具有亚型选择性的TRPML1拮抗剂——类固醇17β-雌二醇甲醚(EDME)。通过对先导化合物进行系统的化学修饰,我们鉴定了EDME的两种类似物PRU-10和PRU-12,其特征在于它们对雌激素受体的活性降低。EDME及其类似物不仅是研究TRPML1的极具潜力的新型小分子工具化合物,而且还能选择性地影响TRPML1功能的关键特征:自噬诱导和转录因子EB(TFEB)的转位。此外,它们还能抑制三阴性乳腺癌细胞的迁移和侵袭。[1]
非选择性阳离子通道TRPML亚家族成员(TRPML1-3)参与调控重要的溶酶体和内体功能,TRPML1基因突变与神经退行性溶酶体贮积症IV型相关。为了深入研究TRPML的功能和(病理)生理作用,迫切需要膜渗透性化学工具。但迄今为止,仅有两种TRPML抑制剂ML-SI1和ML-SI3被报道,且缺乏明确的立体化学细节信息。本研究实现了这两种抑制剂的全合成。ML-SI1仅以不可分离的非对映异构体外消旋混合物的形式获得,且其抑制活性依赖于激活剂。ML-SI3是更有前景的工具,因此未对ML-SI1进行进一步研究。对于 ML-SI3,我们通过立体选择性合成证实,反式异构体的活性显著高于顺式异构体。分离反式-ML-SI3 的对映异构体进一步表明,(-)-异构体是 TRPML1 和 TRPML2 的强效抑制剂(IC50 值分别为 1.6 和 2.3 μM),也是 TRPML3 的弱抑制剂(IC50 值为 12.5 μM);而 (+)-对映异构体是 TRPML1 的抑制剂(IC50 值为 5.9 μM),但却是 TRPML2 和 TRPML3 的激活剂。因此,与外消旋体相比,纯的 (-)-反式-ML-SI3 更适合作为研究 TRPML1 和 TRPML2 的化学工具。对 ML-SI3 的 12 种类似物的分析首次揭示了该化学类型的构效关系,并表明 N-芳基哌嗪和磺酰胺部分均可耐受多种修饰。ML-SI3 的一种芳香族类似物表现出有趣的选择性特征(TRPML1 的强抑制剂和 TRPML2 的强激活剂)。[2] 瞬时受体电位 (TRP) 粘脂蛋白 (TRPML) 由 MCOLN 基因编码,是病理生理学上重要的内溶酶体离子通道,对膜转运至关重要。多项证据表明 TRPML 介导局部 Ca2+ 释放,但其在 Ca2+ 信号传导中的作用尚不明确。本文中,我们发现用合成激动剂激活内源性和重组 TRPML 可在人细胞中诱发全局 Ca2+ 信号。这些信号可被显性失活的 TRPML1 构建体和 TRPML 拮抗剂阻断。我们进一步发现,尽管TRPML1主要定位于溶酶体,但它既支持Ca2+释放也支持Ca2+内流。Ca2+释放需要溶酶体和内质网的Ca2+储存,这表明TRPML与其他内溶酶体Ca2+通道一样,能够与内质网Ca2+通道进行“交互”。我们的数据揭示了TRPML1作用的新模式。[3] ML-SI3是一种小分子选择性TRPML1通道抑制剂,其化学结构与其他TRPML1阻断剂(例如ML-SI1)不同。[2] - 其作用机制涉及直接结合TRPML1通道孔区,阻断Ca2+渗透以及随后参与细胞迁移、侵袭和自噬的下游信号通路。[2] - ML-SI3可作为研究TRPML1介导的细胞过程以及在癌症和其他TRPML1相关疾病中潜在治疗应用的宝贵工具化合物。[2] |
| 分子式 |
C23H31N3O3S
|
|---|---|
| 分子量 |
429.579
|
| 精确质量 |
429.208
|
| 元素分析 |
C, 64.31; H, 7.27; N, 9.78; O, 11.17; S, 7.46
|
| CAS号 |
891016-02-7
|
| 相关CAS号 |
(1S,2S)-ML-SI3;2563870-87-9;(1R,2R)-ML-SI3;2418594-00-8;(rel)-ML-SI3;2108567-79-7
|
| PubChem CID |
23604942
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.3±0.1 g/cm3
|
| 沸点 |
589.3±60.0 °C at 760 mmHg
|
| 闪点 |
310.2±32.9 °C
|
| 蒸汽压 |
0.0±1.7 mmHg at 25°C
|
| 折射率 |
1.629
|
| LogP |
4
|
| tPSA |
70.3Ų
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
6
|
| 重原子数目 |
30
|
| 分子复杂度/Complexity |
624
|
| 定义原子立体中心数目 |
0
|
| SMILES |
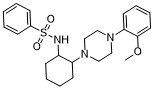
C1(OC)=C(C=CC=C1)N1CCN(C2C(CCCC2)N([H])S(=O)(=O)C2C=CC=CC=2)CC1
|
| InChi Key |
OVTXOMMQHRIKGL-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C23H31N3O3S/c1-29-23-14-8-7-13-22(23)26-17-15-25(16-18-26)21-12-6-5-11-20(21)24-30(27,28)19-9-3-2-4-10-19/h2-4,7-10,13-14,20-21,24H,5-6,11-12,15-18H2,1H3
|
| 化学名 |
N-(2-[4-(2-Methoxyphenyl)-1-piperazinyl]cyclohexyl)benzenesulfonamide
|
| 别名 |
ML SI3; ML-SI3; MLSI3; MLSI-3; N-{2-[4-(2-methoxyphenyl)piperazin-1-yl]cyclohexyl}benzenesulfonamide; ML-SI3; N-(2-[4-(2-Methoxyphenyl)-1-piperazinyl]cyclohexyl)benzenesulfonamide; N-[2-[4-(2-methoxyphenyl)piperazin-1-yl]cyclohexyl]benzenesulfonamide; N-{2-[4-(2-Methoxyphenyl)-1-piperazinyl]cyclohexyl}benzenesulfonamide; N-(2-[4-(2-METHOXYPHENYL)PIPERAZIN-1-YL]CYCLOHEXYL)BENZENESULFONAMIDE; ML-SI3?; ML SI 3
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~50 mg/mL (~116.39 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (5.82 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL 澄清 DMSO 储备液加入900 μL 玉米油中,混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.3279 mL | 11.6393 mL | 23.2786 mL | |
| 5 mM | 0.4656 mL | 2.3279 mL | 4.6557 mL | |
| 10 mM | 0.2328 mL | 1.1639 mL | 2.3279 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。