| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 5g |
|
| 靶点 |
NADP⁺ serves as a precursor for potent intracellular calcium-releasing second messengers, including nicotinic acid adenine dinucleotide phosphate (NAADP) and cyclic ADP-ribose phosphate (cADPRP), which are involved in Ca²⁺ signaling. [1]
NADP⁺ is also a substrate for NAD kinase (NADK) for the generation of NADP⁺/NADPH, and it is the oxidized form of NADPH, which acts as an essential electron donor in multiple redox reactions. [1] NADP sodium salt (NADP⁺) is the oxidized form of NADPH and serves as a substrate for NADPH-producing enzymes including glucose-6-phosphate dehydrogenase (G6PD), isocitrate dehydrogenase 1 (IDH1), and malic enzyme 1 (ME1) in the cytosol. [2] NADP⁺ is also a product inhibitor of human dihydrofolate reductase (DHFR), and its accumulation impairs DHFR activity and folate metabolism. [2] |
|---|---|
| 体外研究 (In Vitro) |
NADP⁺ 可在酸性 pH 下通过 NAD⁺ 糖水解酶(NADase)催化的碱基交换反应转化为 NAADP。[1]
NADP⁺ 也可通过 NAD 糖水解酶转化为环 ADP-核糖磷酸(cADPRP),后者是细胞内钙释放的强效诱导剂。[1] 在人工构建的人源细胞中,改变 NADK 表达水平未显著改变细胞 NADP⁺ 浓度,但强烈影响 NADPH 水平。过表达人源 NADK 使 NADPH 浓度增加 4–5 倍,提高了细胞在氧化损伤下的存活率。[1] 在 HCT116 结肠癌细胞中,敲除 G6PD(氧化磷酸戊糖途径 oxPPP 的关键酶)导致细胞 NADP⁺ 水平升高、NADPH/NADP⁺ 比值下降以及叶酸代谢受损,表现为二氢叶酸 (DHF) 和脱氧尿苷单磷酸 (dUMP) 的积累。[2] 在敲除细胞中重新表达野生型 G6PD 可恢复 NADPH/NADP⁺ 比值并使 dUMP 水平正常化,而催化失活的 G6PD 突变体 (K171Q) 无效。[2] 在 G6PD 敲除细胞中表达大肠杆菌 DHFR(而非人源 DHFR)可逆转 dUMP 积累,表明人源 DHFR 受到高浓度 NADP⁺ 的抑制。[2] 在多种癌细胞系(HEK293T、MDA-MB-468、8988T、A549、HepG2)中敲除 G6PD 均一致导致 NADP⁺ 升高、DHF 和 dUMP 积累,以及苹果酸和柠檬酸水平下降。[2] |
| 酶活实验 |
NAD 激酶(NADK)催化磷酸基团从 ATP 转移到 NAD⁺ 腺苷核糖部分的 2′-羟基,生成 NADP⁺。该酶对细胞存活至关重要,其活性依赖于 NAD⁺ 的可利用性。[1]
NAD⁺ 糖水解酶(NADase,也称为 ADP-核糖基环化酶)催化 NADP⁺ 通过碱基交换反应转化为 NAADP(以烟酸替代烟酰胺),也能催化环化反应形成 cADPRP。[1] 使用心肌黄酶-刃天青偶联法测定细胞裂解液胞质组分中 G6PD、IDH1 和 ME1 的酶活性。测定缓冲液包含 Tris pH 7.4、MgCl₂、刃天青、NADP⁺、心肌黄酶和牛血清白蛋白。反应通过添加相应底物启动:G6PD 使用葡萄糖-6-磷酸,IDH1 使用异柠檬酸,ME1 使用苹果酸。通过荧光法测定活性。[2] 使用全细胞裂解液测定 DHFR 酶活性。将裂解液与磷酸盐缓冲液、β-巯基乙醇、二氢叶酸 (DHF) 以及甲氨蝶呤或 NADP⁺(如指示)混合。通过添加 NADPH 启动反应,通过测定 340 nm 处 NADPH 吸光度下降的速率来测定活性。[2] |
| 细胞实验 |
在人工构建的人源细胞中,使用小干扰 RNA(shRNA)将 NADK 表达降至约 30%,导致细胞 NADPH 浓度显著下降(约 70%),并对过氧化氢的敏感性增加。[1]
在人源细胞中过表达 NADK 使 NADPH 水平提高 4–5 倍,并在氧化应激下提高细胞存活率,但提升程度未达 NADPH 增加所预期的水平。[1] 在 HCT116 细胞中通过 CRISPR 技术构建了 G6PD、IDH1、ME1 及其组合的克隆敲除细胞系。细胞用 Cas9 切口酶和向导 RNA 质粒转染,用嘌呤霉素筛选,并进行单细胞克隆。通过测序和免疫印迹确认功能缺失。[2] 使用 CyQUANT 增殖检测试剂盒评估细胞生长。将细胞接种于 96 孔板,连续多天测量与 DNA 含量成比例的荧光强度。对于低氧生长,氧气水平维持在 0.5%。对于氧化应激实验,在接种时加入 diamide 或 H₂O₂。[2] 通过使用含甲酸的冰冷乙腈:甲醇:水溶液提取细胞进行代谢物分析,随后使用四极杆轨道阱质谱仪在负离子模式下进行亲水相互作用色谱 LC-MS 分析。[2] 通过 LC-MS 测定 NADP⁺ 和 NADPH 水平。细胞用氘代示踪剂([3-²H]葡萄糖、[2,3,3,4,4-²H]谷氨酰胺)培养或在 D₂O 培养基中培养 2 小时,然后进行代谢物提取和针对 NADP(H) 物种的额外扫描窗口的 LC-MS 分析。[2] 通过将细胞在 [U-¹³C]葡萄糖培养基中培养多代,然后进行皂化、己烷提取和脂肪酸的 LC-MS 分析来测定脂肪酸合成。[2] 通过使用含抗坏血酸钠和醋酸铵的甲醇/水溶液提取细胞,随后与大鼠血清孵育、固相萃取和 LC-MS 分析来测定叶酸种类。[2] |
| 参考文献 | |
| 其他信息 |
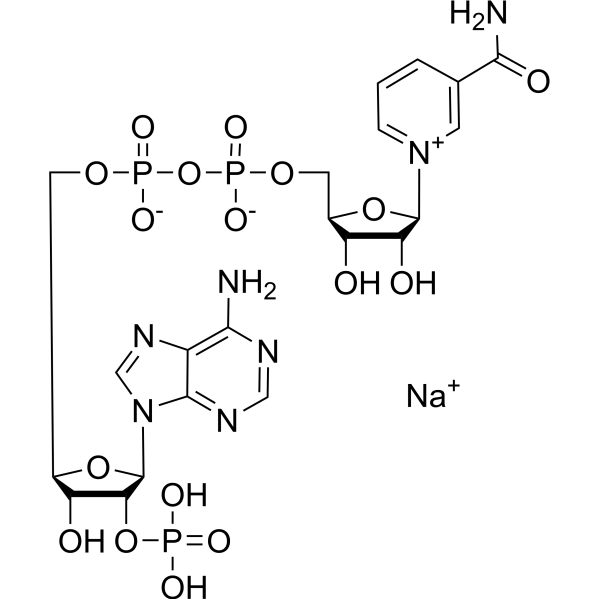
烟酰胺腺嘌呤二核苷酸磷酸(NADP)。一种辅酶,由核糖基烟酰胺5'-磷酸(NMN)通过焦磷酸键与5'-磷酸腺苷2',5'-二磷酸(A2P)偶联而成。它在多种反应中作为电子载体,交替地被氧化(NADP⁺)和还原(NADPH)。(Dorland,第27版)
NADP⁺是NADPH的氧化形式,在细胞氧化还原平衡、钙信号传导以及作为第二信使的前体方面发挥着关键作用。[1] 由于NADP⁺能迅速还原为NADPH,细胞内NADP⁺的水平维持在较低水平,而NADPH对于抗氧化防御、解毒和还原性生物合成至关重要。 [1] NADP⁺衍生的信号分子(NAADP、cADPRP)参与Ca²⁺动员,并可能将氧化应激与细胞内钙释放联系起来。[1] NADP⁺可被NADP磷酸酶(NADPase)降解。[1] NADP钠盐(NADP⁺)是一种关键代谢物,其细胞浓度受NADPH生成途径的调控。氧化磷酸戊糖途径(oxPPP)对于维持哺乳动物细胞中低NADP⁺水平和高NADPH/NADP⁺比值至关重要。[2] 由于G6PD缺乏导致的NADP⁺积累会抑制人二氢叶酸还原酶(DHFR),进而导致叶酸代谢受损、DHF和dUMP积累以及嘌呤和胸苷合成紊乱。 [2] 该机制凸显了胞质 NADPH 代谢与叶酸依赖性一碳代谢之间的关键联系,对癌细胞增殖和氧化应激反应具有重要意义。[2] |
| 分子式 |
C21H27N7NAO17P3
|
|---|---|
| 分子量 |
765.3868
|
| 精确质量 |
765.057
|
| CAS号 |
1184-16-3
|
| 相关CAS号 |
53-57-6 (reduced);604-79-5 (oxidized);53-59-8 (free);1184-16-3 (Na); 100929-71-3 (ammonium); 24294-60-2 (disodium);
|
| PubChem CID |
2724369
|
| 外观&性状 |
White to off-white solid powder
|
| 熔点 |
175-178ºC
|
| tPSA |
399.88
|
| 氢键供体(HBD)数目 |
7
|
| 氢键受体(HBA)数目 |
21
|
| 可旋转键数目(RBC) |
13
|
| 重原子数目 |
49
|
| 分子复杂度/Complexity |
1290
|
| 定义原子立体中心数目 |
8
|
| InChi Key |
JNUMDLCHLVUHFS-UHFFFAOYSA-M
|
| InChi Code |
InChI=1S/C21H28N7O17P3.Na/c22-17-12-19(25-7-24-17)28(8-26-12)21-16(44-46(33,34)35)14(30)11(43-21)6-41-48(38,39)45-47(36,37)40-5-10-13(29)15(31)20(42-10)27-3-1-2-9(4-27)18(23)32;/h1-4,7-8,10-11,13-16,20-21,29-31H,5-6H2,(H7-,22,23,24,25,32,33,34,35,36,37,38,39);/q;+1/p-1
|
| 化学名 |
sodium;[[5-(6-aminopurin-9-yl)-3-hydroxy-4-phosphonooxyoxolan-2-yl]methoxy-oxidophosphoryl] [5-(3-carbamoylpyridin-1-ium-1-yl)-3,4-dihydroxyoxolan-2-yl]methyl phosphate
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
H2O : ~100 mg/mL (~130.65 mM)
DMSO : ~3.57 mg/mL (~4.66 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 100 mg/mL (130.65 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶。
请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.3065 mL | 6.5326 mL | 13.0652 mL | |
| 5 mM | 0.2613 mL | 1.3065 mL | 2.6130 mL | |
| 10 mM | 0.1307 mL | 0.6533 mL | 1.3065 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。