| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
AT2 angiotensin II receptor (IC50 = 34 nM)
|
||
|---|---|---|---|
| 体外研究 (In Vitro) |
已证明,在多种组织中,PD 123319 可以区分 AII 受体的两个亚类。 125I-AII 选择性标记牛肾上腺肾小球细胞膜制剂中 AII 的两种结合位点。第一类(DuP-753 敏感)对 DuP-753 具有很强的亲和力(IC50 为 92.9 nM),约占所有 AII 结合位点的 85%。对于 125I-AII 与该位置的结合,PD-123319 没有影响。 PD-123319 的 IC50 为 6.9 nM,DuP-753 的 IC50 约为 10 microM,第二类结合位点表现出更高的灵敏度[2]。
血管紧张素II(AII)是肾上腺肾小球细胞分泌醛固酮的重要调节因子。All与一种与控制磷脂酶C活性的鸟嘌呤核苷酸结合蛋白偶联的特定受体相互作用。最近,新的All非肽拮抗剂(DuP-753和PD-123319)已被证明可以区分许多不同组织中All受体的两个亚类。我们的研究证实,在牛肾上腺肾小球细胞的膜制备中,125I-All特异性标记了两类All结合位点。第一类(DuP-753敏感)约占All总结合位点的85%,对DuP-753具有高亲和力(IC50为92.9+/-19.5 nM)PD-123319对125I-All与该位点的结合没有任何影响。第二类结合位点对PD-123319更敏感,IC50为6.9+/-3.7 nM,对DuP-753的亲和力要低得多(IC50约为10微M)。这两类受体对All的亲和力不同。所有样本对All 1型受体(AT1)的亲和力约为2 nM(DuP-753敏感),对All 2型受体(AT 2)的亲和力更高,约为0.3 nM(PD-123319敏感)。在3微M DuP-753存在下,所有诱导的类固醇生成都被完全消除,表明这种活性是通过DuP-753敏感受体介导的。我们还发现,聚阴离子聚硫酸乙烯酯(PVS)可以部分抑制125I-All与牛肾上腺肾小球细胞膜的结合,最大效率为17.3+/-8.2 nM。PVS对AT1的抑制作用具有选择性。PVS的抑制作用是由于受体亲和力状态的变化。出乎意料的是,PVS对All诱导的类固醇生成或All与完整牛肾上腺肾小球细胞的结合没有影响。然而,PVS对All结合的抑制作用在细胞透化后得以恢复。溶解的光亲和标记的125I-AT1吸附到肝素琼脂糖凝胶上的能力表明,聚阴离子与AT1直接相互作用。125I-AT1在肝素琼脂糖上的吸附受到溶解受体与肝素或PVS预先孵育的抑制。这些结果表明,All诱导的类固醇生成是由DuP-753敏感受体介导的,PVS通过与细胞内结构域(可能是负责与鸟嘌呤核苷酸结合蛋白偶联的带正电结构域)相互作用降低了该受体的亲和力[2]。 |
||
| 体内研究 (In Vivo) |
PD 123319 对脑血流自动调节没有影响。急性 AT2 受体阻断不会影响 CBF 的自动调节。对清醒的高血压大鼠静脉注射 PD 123319 会立即引起 MAP 的剂量依赖性增加,使用 3 mg/kg PD 123319 时这种增加可持续约 7.4 分钟。
因此,本研究探讨了PD-123319阻断自发性高血压大鼠(SHR)血管紧张素AT2受体对CBF自动调节的影响。麻醉和通气的SHR静脉注射PD 123319,0.36mg/kg/min,并与对照组进行比较。采用颈内动脉133氙注射法测量CBF,在不同的大鼠组中,通过输注去甲肾上腺素提高BP,通过控制出血降低BP。通过计算最小二乘和分析确定自动调节的极限。PD-123319不影响基线CBF,但导致血压轻微下降(10只对照组和10只治疗组大鼠)。PD 123319和对照组动物的CBF自动调节下限(8只治疗组和8只对照组)和CBF自动调整上限(8只处理组和8名对照组)没有显著差异(下限治疗组为102+/-4 mmHg,对照组为94+/-4;NS,上限治疗组为171+/-10 mmHg,控制组为162+/-7;NS)。这些发现表明,急性AT2受体阻断不影响CBF自动调节。[3] 关于健康年轻人心血管血管紧张素2型(AT2)受体的功能表达,我们知之甚少。我们对静脉注射选择性AT2受体拮抗剂PD-123319对正常志愿者血流动力学和动脉僵硬度的影响进行了一项随机、安慰剂对照的交叉研究。16名年龄为29.9+/-13.8岁(范围18-30岁)的正常受试者接受了PD-123319(10 mcg/分钟,持续5分钟)和安慰剂的静脉输注,间隔一周。使用BioZ.com胸阻抗检测系统非侵入性测量血流动力学(心脏指数、卒中指数和全身血管阻力)。使用示波法从袖带测量血压。使用脉搏描记记录仪测量动脉僵硬度指数。与安慰剂相比,PD 123319输注后血压(p=0.92)、心脏指数(p=0.52)、卒中指数(p=0.61)、全身血管阻力指数(p=3.32)或僵硬度指数(p=0.57)没有显著变化。这项研究的结果不支持心血管AT2受体在健康年轻人中介导急性血流动力学效应的功能性存在。如果该人群中存在功能性心血管AT2受体,则可能需要更高剂量的PD 123319来证明其功能[4]。 |
||
| 酶活实验 |
已证明,在多种组织中,PD 123319 可以区分 AII 受体的两个亚类。牛肾上腺肾小球细胞膜制备物中 AII 的两类结合位点被 125I-AII 特异性标记。第一类(DuP-753 敏感)对 DuP-753 具有高亲和力(IC50 为 92.9 nM),约占所有 AII 结合位点的 85%。对于 125I-AII 与该位点的结合,PD-123319 没有影响。 PD-123319 的 IC50 为 6.9 nM,DuP-753 的 IC50 约为 10 μM,第二类结合位点对前者表现出更高的敏感性。
|
||
| 细胞实验 |
通过抑制细胞外信号调节激酶信号传导,PD123319 抑制人间充质干细胞的成骨分化。
最近的证据表明,血管系统含有间充质干细胞(MSCs)。我们假设血管紧张素II(Ang II)2型受体(AT2Rs)在MSCs的成骨过程中起作用,并可能在血管钙化中起作用。人骨髓间充质干细胞分化为成骨细胞。AT2R的表达在成骨过程中显著增加,而Ang II 1型受体的表达没有显著变化。与AT2R阻断剂PD123319(含或不含Ang II)一起孵育可显著抑制钙沉积,而1型受体阻断剂缬沙坦没有显著作用。PD123319抑制了成骨过程中细胞外信号调节激酶(ERK)的磷酸化,而缬沙坦没有影响。此外,PD123319与Ang II联合使用还抑制了胰岛素诱导的MSCs中ERK的急性磷酸化。总之,AT2R在成骨过程中上调。阻断AT2R抑制人MSCs的成骨和ERK磷酸化。这些结果为钙化性血管疾病的病理生理学提供了新的见解。[J Am Soc Hypertens. 2015 Jul;9(7):517-25. https://pubmed.ncbi.nlm.nih.gov/26188399/ ] |
||
| 动物实验 |
|
||
| 参考文献 |
|
||
| 其他信息 |
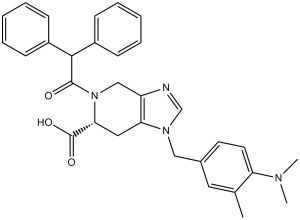
PD123319 是一种咪唑并吡啶类化合物,由 4,5,6,7-四氢-1H-咪唑并[4,5-c]吡啶组成,其 1、5 和 6 位分别连接有 4-(二甲氨基)-3-甲基苄基、二苯乙酰基和羧基。它具有血管收缩剂、内皮素受体拮抗剂和血管紧张素受体拮抗剂的作用。
本文报道了一类新型 4,5,6,7-四氢-1H-咪唑并[4,5-c]吡啶-6-羧酸衍生物的构效关系,该类衍生物能够将 125I 标记的血管紧张素 II 从大鼠肾上腺制剂中特定的血管紧张素 II (Ang II) 结合位点上置换下来。该结合位点并非介导血管收缩或醛固酮释放的血管紧张素II受体,而是一个功能尚未完全阐明的位点。它已在多种组织中被发现,并且与血管受体一样,对血管紧张素II及其肽类似物具有相似的亲和力。本文报道的非肽类化合物能够特异性地置换该结合位点上的血管紧张素II,并且在拮抗血管受体上的血管紧张素II或在测量血管效应的药理学试验中均无活性。PD 123,319 (79) 是最有效的化合物之一,其IC50值为34 nM。这些化合物中的某些可能有助于血管紧张素II受体亚型的定义和研究。[1] |
| 分子式 |
C31H32N4O3
|
|
|---|---|---|
| 分子量 |
508.61
|
|
| 精确质量 |
508.25
|
|
| 元素分析 |
C, 73.21; H, 6.34; N, 11.02; O, 9.44
|
|
| CAS号 |
130663-39-7
|
|
| 相关CAS号 |
PD 123319 ditrifluoroacetate;136676-91-0
|
|
| PubChem CID |
5311345
|
|
| 外观&性状 |
Solid powder
|
|
| 密度 |
1.2±0.1 g/cm3
|
|
| 沸点 |
775.8±60.0 °C at 760 mmHg
|
|
| 闪点 |
423.0±32.9 °C
|
|
| 蒸汽压 |
0.0±2.8 mmHg at 25°C
|
|
| 折射率 |
1.641
|
|
| LogP |
4.4
|
|
| tPSA |
78.67
|
|
| 氢键供体(HBD)数目 |
1
|
|
| 氢键受体(HBA)数目 |
5
|
|
| 可旋转键数目(RBC) |
7
|
|
| 重原子数目 |
38
|
|
| 分子复杂度/Complexity |
791
|
|
| 定义原子立体中心数目 |
1
|
|
| SMILES |
O=C([C@@H]1CC2=C(N=CN2CC3=CC=C(N(C)C)C(C)=C3)CN1C(C(C4=CC=CC=C4)C5=CC=CC=C5)=O)O
|
|
| InChi Key |
YSTVFDAKLDMYCR-NDEPHWFRSA-N
|
|
| InChi Code |
InChI=1S/C31H32N4O3/c1-21-16-22(14-15-26(21)33(2)3)18-34-20-32-25-19-35(28(31(37)38)17-27(25)34)30(36)29(23-10-6-4-7-11-23)24-12-8-5-9-13-24/h4-16,20,28-29H,17-19H2,1-3H3,(H,37,38)/t28-/m0/s1
|
|
| 化学名 |
(6S)-1-[[4-(dimethylamino)-3-methylphenyl]methyl]-5-(2,2-diphenylacetyl)-6,7-dihydro-4H-imidazo[4,5-c]pyridine-6-carboxylic acid
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|---|
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.9661 mL | 9.8307 mL | 19.6614 mL | |
| 5 mM | 0.3932 mL | 1.9661 mL | 3.9323 mL | |
| 10 mM | 0.1966 mL | 0.9831 mL | 1.9661 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。