| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| Other Sizes |
|
| 靶点 |
monoamine oxidase (MAO); KDM1/lysine-specific demethylase 1 (LSD1)
Tranylcypromine hemisulfate targets monoamine oxidase (MAO), including MAO-A with an IC50 of 0.8 μM and MAO-B with an IC50 of 0.3 μM[1] Tranylcypromine hemisulfate targets lysine-specific demethylase 1 (LSD1) with an IC50 of 2.5 μM[2,3] |
|---|---|
| 体外研究 (In Vitro) |
反苯环丙明(10 nM 至 10 μM)独立于神经胶质细胞,具有神经保护作用,可抵抗人类 Aβ (1-42) 寡聚物产生的毒性。反苯环丙胺 (100 μM) 可以显着保护 RGC 免受氧化应激和谷氨酸神经毒性诱导的细胞凋亡的影响。在谷氨酸 (Glu) 诱导的应激环境下,反苯环丙明会增加丝裂原激活蛋白激酶 12 (p38 MAPKγ) 的表达。此外,反苯环丙明可改变 p38 MAPKγ 活性以增加 RGC 存活率 [3]。
Aβ(1-42)(20 μM)处理的SH-SY5Y神经母细胞瘤细胞中,半硫酸盐反苯环丙胺(Tranylcypromine hemisulfate)(1–10 μM)剂量依赖性提高细胞活力20–45%,减少活性氧(ROS)生成30–55%,抑制细胞凋亡(膜联蛋白V阳性细胞比例降低35–60%)[1] - 蛋白质免疫印迹(Western blot)分析显示,该化合物(10 μM)在Aβ(1-42)处理的SH-SY5Y细胞中,使Bcl-2表达上调2.0倍,Bax表达下调50%,同时减少半胱天冬酶-3(caspase-3)的剪切[1] - 从子宫内膜异位症患者分离的人子宫内膜基质细胞(HESCs)中,半硫酸盐反苯环丙胺(Tranylcypromine hemisulfate)(5–20 μM)浓度依赖性抑制细胞增殖30–50%,抑制细胞迁移40–65%[2] - 氧化应激(H₂O₂,100 μM)处理的原代视网膜神经节细胞(RGCs)中,半硫酸盐反苯环丙胺(Tranylcypromine hemisulfate)(2–10 μM)提高细胞存活率25–40%,降低p38丝裂原活化蛋白激酶(p38 MAPK)的磷酸化水平(p-p38)40–55%[3] - 该化合物(10 μM)孵育正常SH-SY5Y细胞、HESCs或RGCs 24小时后,未对细胞活力产生影响[1,2,3] |
| 体内研究 (In Vivo) |
反苯环丙明治疗改善了剂量依赖性全身性痛觉过敏,并显着减小了诱发子宫内膜异位症小鼠的病变大小。此外,反苯环丙明治疗可降低对血管生成、增殖和 H3K4 甲基化等生物标志物的免疫反应,从而导致 EMT 并抑制病变生长 [2]。 NMDA 诱导的视网膜损伤后,反苯环丙胺半硫酸盐 (500 mM) 注射可抑制大鼠视网膜的形态变化,抑制 caspase 3 活性,并恢复视网膜中的 p38 MAPKγ。这些神经保护作用是在细胞内凋亡信号通路上观察到的。表达,并降低 NMDA 的神经毒性,从而提高视网膜损伤后 RGC 的存活率 [3]。 BrdU 免疫组织化学显示,反苯环丙胺半硫酸盐 (10 μg/g) 导致所检查的组合脑区域中标记细胞的近似且显着的倍增。小脑细胞增殖最显着的增加是由反苯环丙明引起的[4]。
Aβ(1-42)诱导神经毒性小鼠模型:半硫酸盐反苯环丙胺(Tranylcypromine hemisulfate) 以5 mg/kg/天剂量腹腔注射,连续7天,改善小鼠空间学习记忆能力(Morris水迷宫实验:逃避潜伏期缩短40%),减少Aβ(1-42)诱导的海马区神经元丢失35%[1] - 诱导性子宫内膜异位症小鼠模型:半硫酸盐反苯环丙胺(Tranylcypromine hemisulfate) 以10 mg/kg/天剂量口服,连续21天,使子宫内膜异位病灶体积缩小50%,缓解全身性痛觉过敏(热撤退潜伏期延长30%)[2] - 视网膜缺血再灌注(I/R)损伤大鼠模型:半硫酸盐反苯环丙胺(Tranylcypromine hemisulfate) 3 mg/kg腹腔注射(缺血前30分钟给药),保护RGC存活(存活率提高45%),改善视觉功能(闪光视觉诱发电位振幅提高35%)[3] - 视网膜组织Western blot分析显示,该化合物使p-p38水平降低50%,脑源性神经营养因子(BDNF)表达上调1.8倍[3] - 成年金鱼模型:半硫酸盐反苯环丙胺(Tranylcypromine hemisulfate) 2 mg/kg/天腹腔注射,连续14天,使端脑内细胞增殖(BrdU阳性细胞)增加30%,视顶盖内新生细胞迁移减少25%[4] |
| 酶活实验 |
单胺氧化酶(MAO)在阿尔茨海默病(AD)的发病机制中起着核心作用,而MAO抑制剂(MAOIs)是目前研究的抗抑郁药物,其对神经退行性疾病具有神经保护作用。在本工作中,测试了MAOIs,如tranylcypomine[反式-(+)-2-苯基环丙烷胺,TCP]及其酰胺衍生物,TCP丁酰胺(TCP But)和TCP乙酰胺(TCP Ac),其保护用合成淀粉样蛋白-β(Aβ)-(1-42)寡聚物(100 nM)攻击的皮层神经元48小时的能力。TCP以浓度依赖的方式显著防止了Aβ诱导的神经元死亡,并且仅在10µM时具有最大保护作用。TCP-But在1µM的混合神经元培养物中具有最大的保护作用,与TCP相比浓度较低,而新的衍生物TCP-Ac比TCP和TCP-But更有效,并在纳摩尔浓度(100 nM)下显著保护皮层神经元免受aβ毒性的影响。用硫黄素-T(Th-T)荧光测定原纤维形成的实验表明,TCP及其酰胺衍生物以浓度依赖的方式影响Aβ聚集过程的早期事件。TCP-Ac比TCP-But和TCP更有效地通过延长滞后期来减缓Aβ(1-42)聚集体的形成。在我们的实验模型中,Aβ(1-42)低聚物与TCP-Ac共同孵育能够几乎完全防止Aβ诱导的神经退行性变。这些结果表明,抑制Aβ寡聚物介导的聚集显著有助于TCP-Ac的整体神经保护活性,也增加了TCP,特别是新化合物TCP-Ac,可能代表在AD中产生神经保护的新药理学工具的可能性[1]。
MAO抑制实验:将系列浓度的半硫酸盐反苯环丙胺(Tranylcypromine hemisulfate) 与重组人MAO-A/MAO-B、荧光底物(MAO-A用酪胺,MAO-B用苯乙胺)在实验缓冲液中37°C孵育60分钟。通过荧光光谱法(激发波长340 nm,发射波长460 nm)检测荧光产物释放量,相对于溶媒对照组计算抑制率,非线性回归确定IC50值[1] - LSD1抑制实验:纯化重组LSD1与半硫酸盐反苯环丙胺(Tranylcypromine hemisulfate)(0.5–20 μM)、组蛋白H3肽底物(H3K4me2)及反应缓冲液在37°C孵育40分钟。采用特异性抗体ELISA试剂盒检测去甲基化产物,根据浓度-效应曲线计算IC50[2,3] |
| 细胞实验 |
RGCs(视网膜神经节细胞)的凋亡[3]
如前所述进行RGC细胞凋亡的评估。简言之,用含有2.4 mM CaCl2和20 mM HEPES(不含镁)的Hanks平衡盐溶液洗涤原代培养的RGCs两次(在37°C下孵育15分钟);从洗涤溶液中省略镁以避免阻断NMDA受体。32随后,将RGCs在含有2.4 mM CaCl2和20 mM HEPES的HBSS中,在37°C下,在300μM谷氨酸和10μM甘氨酸(NMDA受体的辅激活剂)中孵育2小时。用谷氨酸处理后,RGCs在不含任何神经营养因子(如毛喉素、BDNF、CNTF或bFGF)的相同培养基中在37°C下培养22小时。氧化应激诱导的细胞死亡是通过添加50μM过氧化氢(H2O2)和含有B27补充AO的营养添加剂30分钟,然后将细胞孵育24小时来实现的。与谷氨酸或H2O2同时给药特氨酰环丙胺(100μM)和沃特曼宁(100 nM),而在诱导细胞凋亡前24小时加入S2101、BIRB796(10μM,编号S1574)和SB203580(10μM)。随后,在检测细胞凋亡之前,将处理过的RGCs孵育24小时 通过将RGCs与1.0μg/mL Hoechst 33342孵育15分钟来检测细胞凋亡。使用IX71荧光显微镜观察荧光图像,并且从96孔板获得至少6个图像/孔。如前所述,30,31用Hoechst染料染色的碎裂或收缩的细胞核被算作凋亡神经元,圆形/光滑的细胞核被认为是健康的神经元。对于每种情况,使用MetaMorph成像软件对200多个神经元进行计数,以最大限度地减少测量偏差。 SH-SY5Y细胞Aβ(1-42)毒性实验:SH-SY5Y细胞以每孔5×10³个细胞接种于96孔板,过夜孵育。用半硫酸盐反苯环丙胺(Tranylcypromine hemisulfate)(1、3、10 μM)预处理细胞1小时,再加入Aβ(1-42)(20 μM)孵育24小时。MTT法检测细胞活力,DCFH-DA荧光检测ROS生成,膜联蛋白V-FITC/PI染色检测凋亡;Western blot检测Bcl-2、Bax及caspase-3表达[1] - HESC增殖迁移实验:HESCs以每孔1×10⁴个细胞接种于96孔板(增殖实验)或6孔板(迁移实验),加入半硫酸盐反苯环丙胺(Tranylcypromine hemisulfate)(5、10、20 μM)培养48小时。CCK-8法检测增殖,Transwell实验(结晶紫染色迁移细胞)检测迁移能力[2] - RGC氧化应激实验:从大鼠视网膜分离原代RGCs,接种于96孔板。用半硫酸盐反苯环丙胺(Tranylcypromine hemisulfate)(2、5、10 μM)预处理1小时,再用H₂O₂(100 μM)处理24小时。钙黄绿素-AM染色检测细胞存活,Western blot检测p-p38表达[3] |
| 动物实验 |
方法:[2]
本实验使用了47只雌性C57BL/6小鼠。除随机选择的假手术组(M)和特异性对照组(S)小鼠外,所有小鼠均接受了子宫内膜异位症诱导手术。设置S组的主要目的是确保TC治疗组小鼠全身性痛觉过敏的减轻并非由于TC的任何镇痛作用,而是由于TC对子宫内膜异位症的特异性治疗作用。术后两周,将接受手术的小鼠进一步随机分为3组:1)未治疗组(U);2)低剂量TC组(L);3)高剂量TC组(H)。S组接受与H组相同的治疗。治疗两周后,处死所有小鼠,收集其异位子宫内膜组织,并进行免疫组织化学分析。在诱导、治疗和处死前,所有小鼠均进行了热板试验。病灶大小、热板潜伏期、增殖标志物、血管生成标志物、H3K4甲基化标志物以及上皮-间质转化(EMT)标志物的免疫反应性。 结果:[2] 在诱导子宫内膜异位症的小鼠中,TC治疗显著且大幅缩小了病灶大小,并以剂量依赖的方式改善了全身性痛觉过敏。此外,TC治疗降低了增殖标志物、血管生成标志物和H3K4甲基化标志物的免疫反应性,从而抑制了EMT和病灶生长。 小鼠Aβ(1-42)神经毒性模型:将Aβ(1-42)(1 μg/只)脑室内注射到8周龄雄性C57BL/6小鼠体内以诱导神经毒性。将反式环丙胺半硫酸盐(5 mg/kg)溶于生理盐水中,每日腹腔注射一次,连续7天。对照组小鼠接受生理盐水注射。采用莫里斯水迷宫实验评估认知功能,并采集海马组织进行组织学分析[1] - 小鼠子宫内膜异位症模型:将子宫组织碎片植入6周龄雌性BALB/c小鼠体内,诱导子宫内膜异位症。术后两周,将反式环丙胺半硫酸盐(10 mg/kg/天)悬浮于0.5%羧甲基纤维素钠(CMC)溶液中,连续21天口服给药。处死小鼠后测量病灶体积,并评估热缩足潜伏期以评价痛觉过敏[2] - 大鼠视网膜缺血/再灌注损伤模型:将12周龄雄性Sprague-Dawley大鼠麻醉后,夹闭颈内动脉60分钟以诱导视网膜缺血,随后进行7天的再灌注。将反式环丙胺半硫酸盐(3 mg/kg)溶于生理盐水中,于缺血前 30 分钟腹腔注射。采用免疫荧光染色评估视网膜神经节细胞(RGC)存活率,并采用闪光视觉诱发电位评估视觉功能[3]。 - 成年金鱼神经发生模型:将成年金鱼(5-7 cm)腹腔注射反式环丙胺半硫酸盐(2 mg/kg/天),持续 14 天。在安乐死前 2 小时注射 BrdU(50 mg/kg)以标记增殖细胞。对脑组织进行切片,并通过免疫荧光检测 BrdU 阳性细胞,以评估增殖和迁移[4]。 |
| 毒性/毒理 (Toxicokinetics/TK) |
在一项为期 21 天的小鼠重复给药研究中,口服反式环丙胺半硫酸盐(10 mg/kg/天)未引起体重、食物摄入量或血清 ALT、AST、肌酐水平的显著变化[2]
- 在大鼠中,腹腔注射该化合物(3 mg/kg)7 天后,主要器官(肝脏、肾脏、大脑、视网膜)的肉眼病理检查未观察到明显异常[3] - 该化合物对 MAO 表现出轻微的可逆性抑制作用,与富含酪胺的食物同时服用可能导致高血压危象(在临床相关性讨论中提及)[1] |
| 参考文献 |
|
| 其他信息 |
硫酸反苯环丙胺是反苯环丙胺的硫酸盐形式,反苯环丙胺是一种口服生物利用度高、非选择性、不可逆、非肼类单胺氧化酶 (MAO) 和赖氨酸特异性去甲基酶 1 (LSD1/BHC110) 抑制剂,具有抗抑郁和抗焦虑活性,并可能具有抗肿瘤活性。口服后,反苯环丙胺通过抑制 MAO 发挥其抗抑郁和抗焦虑作用。MAO 是一种催化单胺类神经递质(包括血清素、去甲肾上腺素、肾上腺素和多巴胺)分解的酶。这会增加这些神经递质的浓度和活性。反苯环丙胺通过抑制 LSD1 发挥其抗肿瘤作用。抑制 LSD1 可阻止 LSD1 靶基因的转录。 LSD1 是一种黄素依赖性单胺氧化还原酶和组蛋白去甲基酶,在多种癌症中表达上调,并在肿瘤细胞增殖、迁移和侵袭中发挥关键作用。
丙胺是由苯丙胺侧链环化形成的。这种单胺氧化酶抑制剂可有效治疗重度抑郁症、心境恶劣障碍和非典型抑郁症。它对惊恐障碍和恐惧症也有效。 (摘自《美国医学会药物评价年鉴》,1994 年,第 311 页) 另见:硫酸反苯环丙胺(注释已移至)。 硫酸反苯环丙胺是一种非选择性不可逆的 MAO 抑制剂和 LSD1 可逆抑制剂[1,2,3] - 其神经保护机制包括抑制 MAO 介导的单胺降解、降低氧化应激、抑制细胞凋亡以及调节 Bcl-2/Bax/caspase-3 信号通路[1] - 该化合物通过抑制 LSD1 介导的子宫内膜间质细胞增殖和迁移发挥抗子宫内膜异位症作用[2] - 它通过抑制 p38 MAPK 磷酸化和上调 BDNF 表达来保护视网膜神经节细胞免受缺血再灌注损伤[3] - 反苯环丙胺硫酸半酯在临床上用作抗抑郁药,其其他药理活性表明其在阿尔茨海默病、子宫内膜异位症和视网膜疾病方面具有潜在的应用价值[1,2,3,4] |
| 分子式 |
C9H12NO₂S₀.₅
|
|
|---|---|---|
| 分子量 |
182.23
|
|
| 精确质量 |
133.09
|
|
| 元素分析 |
C, 59.32; H, 6.64; N, 7.69; O, 17.56; S, 8.80
|
|
| CAS号 |
13492-01-8
|
|
| 相关CAS号 |
Tranylcypromine hydrochloride;1986-47-6;Tranylcypromine;155-09-9; 13492-01-8 (sulfate); 54779-58-7 (Cis_HCl); 4548-34-9 (HCl)
|
|
| PubChem CID |
25267092
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| 密度 |
1.065g/cm3
|
|
| 沸点 |
218.3ºC at 760mmHg
|
|
| 闪点 |
90.8ºC
|
|
| 蒸汽压 |
0.127mmHg at 25°C
|
|
| LogP |
4.831
|
|
| tPSA |
135.02
|
|
| 氢键供体(HBD)数目 |
4
|
|
| 氢键受体(HBA)数目 |
6
|
|
| 可旋转键数目(RBC) |
2
|
|
| 重原子数目 |
25
|
|
| 分子复杂度/Complexity |
197
|
|
| 定义原子立体中心数目 |
4
|
|
| SMILES |
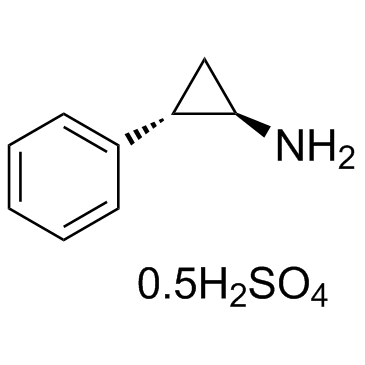
C1[C@@H]([C@H]1N)C2=CC=CC=C2.C1[C@@H]([C@H]1N)C2=CC=CC=C2.OS(=O)(=O)O
|
|
| InChi Key |
BKPRVQDIOGQWTG-FKXFVUDVSA-N
|
|
| InChi Code |
InChI=1S/2C9H11N.H2O4S/c2*10-9-6-8(9)7-4-2-1-3-5-7;1-5(2,3)4/h2*1-5,8-9H,6,10H2;(H2,1,2,3,4)/t2*8-,9+;/m00./s1
|
|
| 化学名 |
(1R,2S)-2-phenylcyclopropan-1-amine; sulfuric acid (2:1)
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 20 mg/mL (109.75 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶。 (<60°C).
请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 5.4876 mL | 27.4379 mL | 54.8757 mL | |
| 5 mM | 1.0975 mL | 5.4876 mL | 10.9751 mL | |
| 10 mM | 0.5488 mL | 2.7438 mL | 5.4876 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。