| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
sPLA2/secretory phospholipase A2 (IC50 = 9 nM)
|
|---|---|
| 体外研究 (In Vitro) |
在两个时间间隔的细胞裂解物中观察到的 RA 诱导的 MUC16 蛋白升高完全被Varespladib (LY-315920)(10 μM;24 和 48 小时;HCjE 细胞)疗法所抑制 [2]。用 Varaspladib(10 μM;24 和 48 小时;HCjE 细胞)治疗可显着减少 RA 产生的 MUC16 量,24 小时时减少 100%,48 小时时减少 99% [2]。
Varespladib(LY-315920)是重组人IIA组非胰腺分泌型PLA2(sPLA2)的强效选择性抑制剂。在显色分离酶测定中,Varespladib(LY-315920)抑制sPLA2活性,IC50为9+/-1 nM或7.3 x 10(-6)摩尔分数,接近该测定的刺激测量极限。Varespladib (LY-315920)的真实效力是通过脱氧胆酸盐/磷脂酰胆碱测定法确定的,摩尔分数为1.5 x 10(-6)。LY315920对人、IB组、胰腺sPLA2的活性低40倍,对细胞质PLA2和环氧化酶的组成型和诱导型没有活性。LY315920抑制了人sPLA2诱导的豚鼠肺支气管肺泡灌洗液细胞释放血栓素A2(TXA2),IC50为0.79微M。N-甲酰基-甲磺酰基-亮酰基-苯丙氨酸或花生四烯酸对这些细胞释放TXA2没有抑制作用。[1] 在使用广谱PLA2抑制剂ArA抑制RA诱导的MUC16上调后,我们试图确定IIA组sPLA2的特异性抑制剂Varespladib (LY-315920)是否会影响RA诱导的MUC16表达。我们通过实时PCR检测了HCjE培养物中MUC16 mRNA的表达水平,这些培养物分别用载体(DMSO)、100nM RA、100nM RA+10μmVarespladib(LY-315920)或单独使用10μm Varespladib (LY-315920)处理24和48小时。如图6所示,添加10μm LY315920显著抑制了RA诱导的MUC16表达,24小时时抑制率为100%,48小时时抑制了99%。如图7所示,添加sPLA2 IIA的特异性抑制剂LY315920可完全抑制RA诱导的MUC16蛋白在24(p<0.01)和48(p<0.0001)小时时在细胞裂解物中检测到的增加[2]。 |
| 体内研究 (In Vivo) |
Varespladib (LY-315920)治疗的 IC50 为 0.79 μM,可防止人 sPLA2 诱导的豚鼠肺支气管肺泡灌洗细胞释放血栓素 A2 (TXA2)。 Varespladib (LY-315920) 的 ED50 为 16.1 mg/kg[1]。
在采集支气管肺泡灌洗液细胞前5分钟静脉注射Varespladib(LY-315920),导致sPLA2诱导的TXA2产生受到抑制,ED50为16.1mg/kg。用sPLA2攻击豚鼠肺胸膜条产生收缩反应,这些反应被Varespladib(LY-31592 0)以浓度依赖的方式抑制,表观KB为83+/-14nM。花生四烯酸诱导的收缩反应没有改变。向表达人sPLA2蛋白的转基因小鼠静脉或口服Varespladib(LY-315920),在4小时的时间过程中以剂量相关的方式抑制血清sPLA2活性Varespladib(LY-315920)是一种强效且选择性的sPLA2抑制剂,代表了一类新的抗炎药SPI。该药物目前正在进行临床评估,应有助于确定sPLA2在各种炎症性疾病状态中的作用[1]。 ApoE−/−标准模型[3] 对照组或A-002(varespladib methyl/LY333013/S-3013处理组)动物的体重在时间0时相似(赋形剂:27.2±2.6,30mg/kg A-002:26.7±2.3,90mg/kg A-002:37.3±2.5)。在西方饮食的16周内,Vehicle, 30 mg/kga-002(varespladib methyl/LY333013/S-3013和90 mg/kg a-002组)的体重分别增加了约155%、150%和141%(图2)。使用重复测量的双向方差分析,以时间和治疗为变量,两组之间的体重没有统计学上的显著差异。 研究开始时,各组的血浆胆固醇水平没有显著差异。然而,与对照组相比,每天两次服用a-002(varespladib methyl/LY333013/S-3013,剂量为30或90 mg/kg,治疗1个月后,总胆固醇显著降低(图3)。在整个4个月的治疗期间,这种效果保持一致。每次治疗4个月后,赋形剂、30mg/kg A-002和90mg/kg A-002组的血浆胆固醇分别变化了+15%、-10%和-12%(图3)。血浆胆固醇浓度没有明显的剂量反应效应。 A-002(varespladib methyl/LY333013/S-3013)治疗对斑块含量有显著影响,斑块含量以动脉粥样硬化斑块在主动脉管腔表面的占有率表示。载体治疗的小鼠斑块覆盖率约为12.6%±0.7%,而每天两次用30mg/kg A-002治疗的小鼠为6.3%±0.6%,每天两次服用90mg/kg A-002的小鼠为6.7%±0.8%。这表明与仅接受制剂载体的治疗组相比,A-002治疗组的斑块含量显著降低(P<0.05)(图4)。 血管紧张素II ApoE−/−模型[3] 血管紧张素II在水中每天两次或在5%阿拉伯胶中每天两次配制,导致主动脉斑块覆盖率相似(分别为18%±3.3%和14.4%±4.8%,图5)A-002(varespladib methyl/LY333013/S-3013(30mg/kg)显著降低了主动脉的斑块覆盖率(8%±3%,而未经药物治疗输注血管紧张素II时为18%±3.3%,P<0.025)。在没有血管紧张素II的情况下,动脉粥样硬化的背景量(3.8%±0.6%,皮下盐水泵和每天两次水)明显低于输注血管紧张素Ⅱ的情况(18%±3.3%,P<0.025)。代表性的人脸图像如图6所示。 评估每组小鼠的主动脉瘤发生率。在未输注血管紧张素II的情况下,未观察到动脉瘤。输注水中配制的血管紧张素II导致25%的动脉瘤发生率,输注阿拉伯胶载体中配制的血管紧缩素II导致22.2%的动脉瘤发病率A-002(varespladib methyl/LY333013/S-3013治疗(30mg/kg,每天两次)在输注阿拉伯胶中配制的血管紧张素II的小鼠中完全预防了动脉瘤的形成(Prob>ChiSq=0.0096)(表1)。 |
| 酶活实验 |
sPLA2抑制[3]
根据其他地方描述的显色方法,测量了Varespladib(LY-315920)/A-001对sPLA2 V和X组酶抑制的内在活性。 磷脂酶A2抑制剂治疗[2] 为了研究RA对MUC16的调节是否与sPLA2有关,在如上所述与100 nM RA加100μM ArA(抑制剂或载体(DMSO)单独培养24和48小时的HCjE细胞中,测定了广谱PLA2抑制剂马兜铃酸(ArA)对MUC16mRNA水平的影响。在这些实验之后,测试了IIA组分泌型磷脂酶A2特异性抑制剂Varespladib (LY-315920)的效果。HCjE细胞分别用100nM RA、100nM RA加10μmVarespladib(LY-315920)、抑制剂或载体(DMSO)单独处理24和48小时。分别通过实时PCR和Western blot分析测定MUC16 mRNA和蛋白质水平。两种抑制剂都进行了两次实验,每次实验重复两次。 |
| 细胞实验 |
蛋白质印迹分析[2]
细胞类型: HCjE 细胞 测试浓度: 10 μM 孵育时间: 24 hrs(小时)和48 hrs(小时) 实验结果:在两个时间点均显着抑制RA诱导的MUC16蛋白表达。 RT-PCR[2] 细胞类型: HCjE 细胞 测试浓度: 10 μM 孵育时间:24小时和48小时 实验结果:显着抑制RA诱导的MUC16表达,24小时时为100%,48小时时为99% hrs(小时)。 |
| 动物实验 |
动物/疾病模型:雄性哈特利豚鼠(300-500 g)[1]
剂量:3 mg/kg、10 mg/kg 和 30 mg/kg 给药途径:静脉注射(药代动力学/PK 研究) 实验结果:观察到支气管肺泡灌洗液中 sPLA2 活性持续受到抑制。降低了人 sPLA2 诱导的豚鼠支气管肺泡灌洗液细胞中 TXA2 的生成。 |
| 毒性/毒理 (Toxicokinetics/TK) |
血浆浓度和剂量选择 [3]
图 1 显示了单次口服 A-002(varespladib methyl/LY333013/S-3013)后血清中 Varespladib (LY-315920)/A-001 的血浆浓度。在 10、30 和 90 mg/kg 剂量下,所有给药小鼠的样本中均可检测到 Varespladib (LY-315920)/A-001。最高两个剂量,即 30 和 90 mg/kg A-002(varespladib methyl/LY333013/S-3013),其血浆中 Varespladib (LY-315920)/A-001 的浓度均高于 IC50 值。在整个给药期间,分别检测了 sPLA2 V 组和 X 组。 血浆水平[3] 在 ApoE−/− 小鼠中进行的单剂量实验中,测定了 A-001/Varespladib (LY-315920)(A-002 (varespladib methyl/LY333013/S-3013) 的活性成分)的血浆水平。如上所述,通过灌胃法给动物分别给予 10、30 或 90 mg/kg 的 A-002 (varespladib methyl/LY333013/S-3013)。使用尾部剪取法在不同时间点采集血液样本。收集血浆并储存在 −70°C 下,用于分析 A-001/Varespladib 的存在。采用高效液相色谱-质谱法(HPLC-MS)分析LY-315920。将给药动物的血浆(25 μL)与5 μL 20 μM LY329722(内标)、25 μL异丙醇和50 μL乙腈混合于聚丙烯微量离心管中。涡旋混匀后,于37°C孵育10分钟,然后在室温下以12,000 g离心。取上清液(65 μL)倾入装有430 μL水和5 μL甲酸的800 μL玻璃自动进样器小瓶中。盖紧小瓶,涡旋混匀后置于Surveyor自动进样器中。将样品(25 μL)注入2.1 × 100 mm、5 μm、C8 Discovery反相色谱柱。色谱柱配备一根 2.1 × 4 mm 的 Phenomenex C8 保护柱。初始色谱条件设置为:流动相 A 为 95%(0.1% 甲酸的 5% 异丙醇溶液),流动相 B 为 5%(0.1% 甲酸的乙腈溶液,含 5% 异丙醇)。进样后 1 分钟,采用 6 分钟的梯度洗脱,流动相 B 的比例从 5% 升至 60%,得到 A-002(varespladib methyl/LY333013/S-3013)和内标的保留时间分别为 6.07 分钟和 6.47 分钟。采用电喷雾大气压电离离子阱质谱法检测分析物。毛细管电压为 4.5 kV,毛细管温度为 310°C。氮气鞘流速设置为 75 个任意单位。碰撞诱导解离 (CID) 的优化值为 35%(归一化)。碰撞能量。用于串联质谱检测A-001/Varespladib (LY-315920)和内标的选择性跃迁分别源于氨和一氧化碳自由基的丢失,其m/z分别为381→336和395→350。A-001和内标的峰面积用于计算响应因子,未知样品的响应因子则通过与未给药小鼠混合血浆中添加A-001的线性校准曲线进行插值计算得出。 |
| 参考文献 |
|
| 其他信息 |
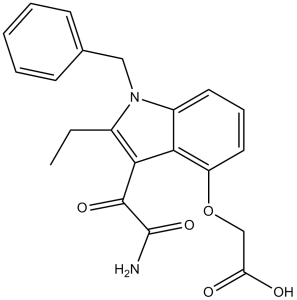
瓦瑞斯普拉地布(Varespladib)属于吲哚类化合物,其结构为1H-吲哚,分别在1、2、3和4位被苄基、乙基、草酰氧基和羧甲氧基取代。它是一种口服分泌型磷脂酶A2抑制剂,具有抗炎作用。它可作为EC 3.1.1.4(磷脂酶A2)抑制剂、抗炎药和解毒剂。它属于吲哚类、苯类、芳香醚类、二羧酸单酰胺类、单羧酸类和伯羧酰胺类化合物。它是varespladib(1-)的共轭酸。
Varespladib已被研究用于治疗和预防镰状细胞病、血管闭塞危象和急性冠脉综合征。 LY315920是一种强效、选择性的重组人IIA组非胰腺分泌型PLA2 (sPLA2)抑制剂。在显色分离酶测定中,LY315920抑制sPLA2活性的IC50为9±1 nM或7.3×10⁻⁶摩尔分数,接近该测定的化学计量极限。LY315920的真实效力通过脱氧胆酸/磷脂酰胆碱测定确定,摩尔分数为1.5×10⁻⁶。 LY315920 对人 IB 组胰腺 sPLA2 的活性降低了 40 倍,并且对胞质 PLA2 以及组成型和诱导型环氧合酶均无活性。LY315920 可抑制人 sPLA2 诱导的豚鼠肺支气管肺泡灌洗细胞释放血栓素 A2 (TXA2),IC50 为 0.79 μM。N-甲酰甲硫氨酰亮氨酰苯丙氨酸或花生四烯酸诱导的这些细胞释放 TXA2 则不受抑制。在收集支气管肺泡灌洗细胞前 5 分钟静脉注射 LY315920,可抑制 sPLA2 诱导的 TXA2 生成,ED50 为 16.1 mg/kg。用 sPLA2 刺激豚鼠肺胸膜条可产生收缩反应,该反应可被 LY315920 以浓度依赖的方式抑制,其表观 KB 值为 83 ± 14 nM。花生四烯酸诱导的收缩反应未受影响。向表达人 sPLA2 蛋白的转基因小鼠静脉或口服 LY315920,可在 4 小时内以剂量依赖的方式抑制血清 sPLA2 活性。LY315920 是一种强效且选择性的 sPLA2 抑制剂,代表了一类新型抗炎药,命名为 SPI。该药物目前正在进行临床评估,有望帮助阐明 sPLA2 在各种炎症性疾病中的作用。[1] 目的:维生素 A 如何维持眼表湿润表型尚不清楚。本研究旨在利用基因芯片分析,鉴定眼表上皮细胞中对维生素A有反应的基因。研究对象为用全反式维甲酸(RA)培养的人结膜上皮(HCjE)细胞系。分析结果显示,分泌型磷脂酶A2 IIA组(sPLA2-IIA)是RA上调最显著的基因,其次是膜相关黏蛋白MUC16,但上调时间较晚。由于PLA2家族产生的花生四烯酸产物——类花生酸已被证实能够增加黏蛋白的生成,因此本研究旨在探究sPLA2是否介导RA诱导MUC16的表达。 方法:将HCjE细胞在有或无RA的培养基中培养3、6、24和48小时。从HCjE细胞RNA制备的互补RNA与人基因芯片杂交,并使用商业软件进行分析。通过实时PCR验证了粘蛋白表达的微阵列数据。为了研究sPLA(2)是否与RA诱导的MUC16上调相关,将HCjE细胞与RA和广谱PLA(2)抑制剂马兜铃酸(ArA)或特异性sPLA(2)-IIA抑制剂LY315920孵育,然后通过实时PCR和Western blot分析MUC16 mRNA和蛋白的表达。 结果:加入RA后,在3小时和6小时(早期),有28个转录本上调,6个转录本下调超过2倍(P < 0.01)。在24小时和48小时(晚期),有80个基因转录本上调,45个基因转录本下调。 IIA组sPLA(2)在24小时显著上调,而MUC16是RA处理48小时后上调最显著的RNA。Western blot分析证实了RA对sPLA(2)的上调作用。当HCjE细胞与RA联合ArA或sPLA(2)-IIA特异性抑制剂LY315920孵育时,RA诱导的MUC16 mRNA表达显著降低(P < 0.01)。 结论:RA在后期诱导的膜相关黏蛋白MUC16的上调似乎是通过sPLA(2)-IIA介导的。这种亲水性膜相关黏蛋白的上调可能是维生素A维持眼表湿润表型的重要机制之一。 [2] 分泌型磷脂酶 A2 (sPLA2) 酶家族与炎症性疾病和组织损伤(包括动脉粥样硬化)有关。 A-001 是一种通过基于结构的药物设计发现的新型 sPLA2 酶抑制剂,而 A-002(varespladib methyl/LY333013/S-3013)是目前正在进行临床开发的口服生物利用度较高的前药。A-001 可抑制人和小鼠的 sPLA2 IIA、V 和 X 组酶,其 IC50 值在低纳摩尔范围内。在 C57BL/6J 背景中过表达人 sPLA2 IIA 组的转基因小鼠中,A-002(1 mg/kg)可使血清中 A-001 浓度升高,并抑制 PLA2 活性。此外,还使用表面分析法评估了 A-002 对两种 ApoE−/− 小鼠模型动脉粥样硬化的影响。(1) 在高脂饮食模型中,A-002(30 和 90 mg/kg,每日两次,持续 16 周)可降低主动脉粥样硬化程度。动脉粥样硬化程度降低了 50% (P < 0.05)。血浆总胆固醇在 1 个月内显著降低 (P < 0.05),并在整个研究期间保持较低水平。(2) 在血管紧张素 II 诱导主动脉病变和动脉瘤的加速动脉粥样硬化模型中,A-002(30 mg/kg,每日两次)使主动脉粥样硬化程度降低了约 40% (P < 0.05),并减轻了动脉瘤的形成 (P = 0.0096)。因此,A-002 能有效显著降低这两种 ApoE−/− 小鼠模型中的总胆固醇、动脉粥样硬化和动脉瘤形成。[3] |
| 分子式 |
C21H20N2O5
|
|---|---|
| 分子量 |
380.39
|
| 精确质量 |
380.137
|
| 元素分析 |
C, 66.31; H, 5.30; N, 7.36; O, 21.03
|
| CAS号 |
172732-68-2
|
| 相关CAS号 |
Varespladib sodium;172733-42-5;Varespladib methyl;172733-08-3
|
| PubChem CID |
155815
|
| 外观&性状 |
White to yellow solid powder
|
| 密度 |
1.3±0.1 g/cm3
|
| 沸点 |
667.9±65.0 °C at 760 mmHg
|
| 闪点 |
357.7±34.3 °C
|
| 蒸汽压 |
0.0±2.1 mmHg at 25°C
|
| 折射率 |
1.630
|
| LogP |
2.45
|
| tPSA |
111.62
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
8
|
| 重原子数目 |
28
|
| 分子复杂度/Complexity |
589
|
| 定义原子立体中心数目 |
0
|
| SMILES |
CCC1=C(C2=C(N1CC3=CC=CC=C3)C=CC=C2OCC(=O)O)C(=O)C(=O)N
|
| InChi Key |
BHLXTPHDSZUFHR-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C21H20N2O5/c1-2-14-19(20(26)21(22)27)18-15(9-6-10-16(18)28-12-17(24)25)23(14)11-13-7-4-3-5-8-13/h3-10H,2,11-12H2,1H3,(H2,22,27)(H,24,25)
|
| 化学名 |
2-((3-(2-amino-2-oxoacetyl)-1-benzyl-2-ethyl-1H-indol-4-yl)oxy)acetic acid
|
| 别名 |
A002; A 002; LY315920; Varespladib; 172732-68-2; LY315920; Varespladib (LY315,920); LY-315,920; S-5920; VAREPLADIB; 2Q3P98DATH; LY-315920; LY 315920; A-002;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 2.5 mg/mL (6.57 mM) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浮液;超声助溶。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: 30% PEG400+0.5% Tween80+5% propylene glycol:30 mg/mL View More
配方 3 中的溶解度: 1.5 mg/mL (3.94 mM) in 17% Polyethylene glycol 12-hydroxystearate in Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.6289 mL | 13.1444 mL | 26.2888 mL | |
| 5 mM | 0.5258 mL | 2.6289 mL | 5.2578 mL | |
| 10 mM | 0.2629 mL | 1.3144 mL | 2.6289 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT05717062 | Recruiting | Drug: Varespladib intravenous form Drug: varespladib-methyl- oral form |
Snakebite Envenoming, Snake |
Ophirex, Inc. | May 30, 2023 | Phase 2 |
| NCT04996264 | Completed | Drug: Varespladib Methyl Drug: Placebo |
Snakebites Envenoming |
Ophirex, Inc. | August 15, 2021 | Phase 2 |
| NCT04969991 | Terminated | Drug: Varespladib Drug: Placebo |
Coronavirus Disease 2019 | Ophirex, Inc. | June 30, 2021 | Phase 2 |
| NCT01359605 | Completed | Drug: varespladib methyl | Healthy Volunteers | Anthera Pharmaceuticals | June 2011 | Phase 1 |