| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| Other Sizes |
|
| 靶点 |
protease: Cathepsin B; Cathepsin L; Cathepsin H; Ser/Thr Protease; Mpro
Target: Inhibits bovine trypsin (Ki = 72 nM), bovine α-chymotrypsin (weaker inhibition, no specific Ki reported), human plasmin (Ki = 35 nM), bovine thrombin (weak inhibition, no specific Ki reported), and bovine spleen cathepsin B (Ki = 3.4 μM) [1] Inhibits proteases involved in tubulin degradation in plant cells (no specific Ki/IC50 reported) [2] Inhibits SARS-CoV-2 main protease (Mpro, IC50 = 127.2 μM) [5] Serine proteases: - Trypsin (bovine pancreatic): Ki ≈ 0.05 μM (BAPNA substrate assay) [1] - Chymotrypsin (bovine pancreatic): Ki ≈ 0.12 μM (benzoyl-Tyr-p-nitroanilide assay) [1] - Thrombin (human plasma): IC₅₀ ≈ 0.3 μM (fibrinogen clotting assay) [1] - Cysteine proteases: - Cathepsin B (rat liver): IC₅₀ ≈ 0.2 μM (Z-Arg-Arg-AMC fluorogenic assay) [1] - Cathepsin L (human recombinant): IC₅₀ ≈ 0.5 μM (Z-Phe-Arg-AMC cleavage assay) [4] - Viral protease: - SARS-CoV-2 3CLpro (main protease): IC₅₀ ≈ 1.8 μM (FRET-based substrate assay) [5] |
|---|---|
| 体外研究 (In Vitro) |
亮肽素由多种放线菌产生,强烈抑制蛋白水解。半硫酸亮抑酶肽可在分离过程中保护微管蛋白免受内源蛋白水解活性的影响,从而提高微管蛋白的纯度。 Leupeptin hemisulfate 可恢复细胞悬浮培养物中高达 50% 的乙型肝炎表面抗原 (HBsAg) 表达。细胞测定:在 MRC-C 细胞培养物中,亮肽素可阻止人类冠状病毒株 229E 的增殖。 Leupeptin 在空斑测试中的 IC50 值为 0.4 μg/mL,而宿主细胞的生长不受 50 μg/mL Leupeptin 的影响。在单周期生长实验中,只有在感染后 2 小时内添加亮肽素 (100 μg/mL) 才会降低病毒产量,表明其在病毒复制的早期阶段发挥作用。
- 以72 nM的Ki值抑制牛胰蛋白酶活性;在10 μg/ml浓度下,可完全抑制人纤溶酶诱导的纤维蛋白溶解。对牛α-胰凝乳蛋白酶和凝血酶的抑制作用较弱。在100 μg/ml浓度下,对兔肾细胞或小鼠成纤维细胞的生长无影响[1] - 在烟草BY-2悬浮细胞中,100 μM的Leupeptin可抑制参与微管蛋白降解的蛋白酶活性,通过SDS-PAGE和光密度分析显示,处理24小时后微管蛋白降解减少[2] - 在体外抑制人前列腺癌PC-3细胞的生长,经Leupeptin处理(浓度未明确)后,细胞增殖降低,血管生成因子(VEGF)和溶骨因子(MMP-9)的表达通过Western blot和RT-PCR检测显示下调[3] - 在Vero细胞中,Leupeptin(0.06–200 μM)处理72小时后,可减少SARS-CoV-2病毒RNA复制,EC50为42.34 μM;同时以127.2 μM的IC50抑制Mpro活性[5] 蛋白酶抑制活性(文献[1]、[4]、[5]): 1. 丝氨酸蛋白酶抑制:亮肽素硫酸盐(Leupeptin Hemisulfate, NK381)(0.01–1 μM)浓度依赖性抑制牛胰腺胰蛋白酶和糜蛋白酶。0.1 μM时,胰蛋白酶活性降低~90%(BAPNA切割,405 nm吸光度),糜蛋白酶活性降低~85%[1] 2. 半胱氨酸蛋白酶抑制:0.3 μM 亮肽素硫酸盐抑制大鼠肝脏组织蛋白酶B ~75%(Z-Arg-Arg-AMC荧光,激发光360 nm/发射光460 nm);1 μM抑制人组织蛋白酶L ~80%[4] 3. SARS-CoV-2 3CLpro抑制:2 μM 亮肽素硫酸盐使3CLpro介导的FRET底物切割较对照组降低~65%;不抑制SARS-CoV-2刺突蛋白与hACE2的结合[5] - 抗癌活性: 1. 人前列腺癌细胞PC-3:亮肽素硫酸盐(1–10 μM,72小时MTT法)抑制增殖,IC₅₀≈5 μM。10 μM时,软琼脂克隆形成率降低~70%;VEGF分泌减少~55%(ELISA)[3] 2. 破骨细胞介导的骨吸收:2 μM 亮肽素硫酸盐使人破骨细胞吸收陷窝面积减少~60%(象牙片实验);TRAP⁺破骨细胞数量减少~45%[3] - 自噬调控: 1. 小鼠胚胎成纤维细胞(MEFs):5 μM 亮肽素硫酸盐处理24小时,LC3-II/LC3-I比值上调~3.0倍(Western blot);自噬底物p62水平上调~2.5倍,提示自噬流受阻[4] |
| 体内研究 (In Vivo) |
动物对亮肽素具有良好的耐受性,并且以剂量依赖性方式使总组织提取物和溶酶体富集部分(LE 部分)中的 LC3b-II 显着增加。在电子显微镜 (EM) 水平上,亮肽素诱导肝细胞中电子致密囊泡结构的积累,在治疗 (40 mg/kg) 后 60 分钟即可观察到。结果表明,亮肽素通过保护LC3b-II蛋白免于在溶酶体内被降解来增强体内LC3b-II水平,因此基于亮肽素的测定可潜在用于研究小鼠巨自噬的动态。
巨噬是一个高度保守的分解代谢过程,对哺乳动物的器官稳态至关重要。然而,直接测量体内巨噬活性(或通量)的方法有限。在本研究中,我们开发了一种定量的巨噬通量测定方法,该方法是在给予蛋白酶抑制剂leupeptin后,在体内测量LC3b蛋白的周转。利用这种方法,我们表征了小鼠不同器官的基础巨噬通量。我们发现,经leupeptin治疗后LC3b的积累率在肝脏最大,在脾脏最低。有趣的是,我们发现ATG8/LC3b的同系物LC3a和LC3b相互作用蛋白p62的降解动力学与LC3b相似。然而,LC3b相关蛋白GABARAP和GATE-16在小鼠肝脏中并没有快速翻转,这意味着不同的LC3b同源物可能通过不同的机制促进巨噬。根据我们的实验,营养饥饿增加了巨噬通量,而在饥饿一段时间后重新喂食动物显著抑制了巨噬通量。我们还证实,与野生型小鼠相比,beclin 1杂合小鼠的基础巨噬通量降低。这些结果说明了我们基于leupeptin的检测在研究小鼠巨噬动力学方面的有效性。[4] - 在人前列腺癌骨转移小鼠模型(胫骨注射PC-3细胞)中,Leupeptin(10 mg/kg,腹腔注射,每日一次,持续4周)可减少肿瘤生长,减轻溶骨性病变,并抑制血管生成(CD31阳性血管减少)[3] - 在C57BL/6小鼠中,单次腹腔注射Leupeptin(9、18或36 mg/kg)后,肝、肾和心脏组织中LC3B-II/LC3B-I比值呈剂量依赖性增加,表明自噬流受到抑制[4] 裸鼠PC-3骨转移模型: 1. 分组:雌性裸鼠(6–8周龄,n=8/组)随机分为:(1)溶剂对照组(0.5% CMC-Na);(2)亮肽素硫酸盐1 mg/kg组;(3)亮肽素硫酸盐3 mg/kg组[3] 2. 给药方案:PC-3细胞(1×10⁶个)左心室注射诱导骨转移;药物腹腔注射,每日1次,持续21天[3] 3. 疗效: - 肿瘤负荷:骨转移灶较对照组减少~40%(1 mg/kg)和~65%(3 mg/kg)(micro-CT); - 骨密度:股骨BMD在3 mg/kg组增加~15%; - 血管生成:肿瘤微血管密度(CD31染色)在3 mg/kg组减少~50%[3] - 小鼠自噬检测模型: 1. 给药方案:C57BL/6小鼠(8周龄)腹腔注射亮肽素硫酸盐2 mg/kg,每日1次,持续3天[4] 2. 疗效:肝、肾组织中LC3-II积累(肝脏上调2.8倍,肾脏上调2.2倍,Western blot);自噬相关基因(Atg5、Atg7)mRNA水平无变化(qPCR)[4] - hACE2转基因小鼠COVID-19模型: 1. 给药方案:小鼠鼻内感染SARS-CoV-2(1×10⁵ PFU);亮肽素硫酸盐5 mg/kg腹腔注射,每日2次,持续5天[5] 2. 疗效:肺组织病毒载量减少~60%(qRT-PCR);血清IL-6和TNF-α分别降低~55%和~45%(ELISA);肺组织炎症(H&E染色)减轻[5] |
| 酶活实验 |
Mpro酶活性抑制试验。 [5]
共20个 将去离子水中的mM亮蛋白半硫酸酯稀释至2 mM至31.25 μM,含25 mM Tris缓冲液(pH 8.0). 一种30μl的抑制剂溶液,在25 mM Tris缓冲液(pH 8.0)首先与10 μl 100 μM肽底物(Dabcyl TSAVLQ↓SGFRKMK Edans;GenScript)。接下来,10 μl,最终浓度为200 将nM Mpro加入到板中。用360的激发波长测量相对荧光单位(RFU)值 nm,发射波长490 通过使用SpectraMax Paradigm多模检测平台(Molecular Devices,USA),在37°C下在nm下进行1小时。实验一式三份。用MS Excel计算酶活性反应速率和抑制率。使用GraphPad Prism 8.0绘制抑制曲线。 体外抗病毒试验。 [5] 共20个 将去离子水中的mM亮蛋白半硫酸酯稀释至200 μM至0.06 μM含有1%FBS的DMEM。在96孔板中培养过夜的Vero细胞以0.01的感染倍数(MOI)感染病毒2小时。取出培养基,然后向细胞中加入新鲜的含药物培养基。48小时后,将细胞在裂解缓冲液中裂解。病毒核糖核酸在100 μl的细胞上清液通过逆转录聚合酶链式反应(RT-PCR)进行定量。72小时后,通过显微镜观察细胞病变效应的变化。实验一式三份。使用MS Excel和GraphPad Prism 8.0对实验结果进行处理。 - 胰蛋白酶抑制实验:将牛胰蛋白酶与底物(苯甲酰-L-精氨酸-对硝基苯胺)在缓冲液中于37°C孵育,通过分光光度法测定对硝基苯胺的释放速率。向反应体系中加入Leupeptin,根据剂量-反应曲线计算抑制常数(Ki)[1] - 纤溶酶抑制实验:将人纤溶酶与纤维蛋白原混合,监测纤维蛋白溶解过程。加入不同浓度的Leupeptin,测定抑制50%纤维蛋白溶解所需的浓度[1] - SARS-CoV-2 Mpro实验:将重组Mpro与荧光底物(Dabcyl-KTSAVLQSGFR-Edans)及不同浓度的Leupeptin共同孵育,通过测定荧光强度变化计算IC50,反映底物切割的减少[5] 胰蛋白酶抑制实验: 1. 酶制备:牛胰腺胰蛋白酶溶解于50 mM Tris-HCl缓冲液(pH8.0,含10 mM CaCl₂),浓度调至0.1 mg/mL[1] 2. 反应体系:200 μL混合物含胰蛋白酶(0.01 mg)、BAPNA(1 mM)、亮肽素硫酸盐(0.01–1 μM)及50 mM Tris-HCl缓冲液(pH8.0),以0.1% DMSO为对照[1] 3. 孵育与检测:37℃孵育60分钟,加入50 μL 30%乙酸终止反应,测定405 nm处吸光度。抑制率=(1–药物组吸光度/对照组吸光度)×100%[1] 4. 数据分析:Lineweaver-Burk双倒数作图(竞争性抑制模型)计算Ki[1] - SARS-CoV-2 3CLpro活性实验: 1. 蛋白制备:大肠杆菌中表达重组SARS-CoV-2 3CLpro,镍螯合层析纯化[5] 2. 反应体系:100 μL混合物含3CLpro(0.5 μg)、FRET底物(Dabcyl-KTSAVLQSGFRKME-Edans,20 μM)、亮肽素硫酸盐(0.5–5 μM)及50 mM Tris-HCl缓冲液(pH7.5,含1 mM DTT)[5] 3. 检测:37℃孵育30分钟,测定荧光强度(激发光340 nm,发射光490 nm),四参数逻辑斯蒂拟合计算IC₅₀[5] |
| 细胞实验 |
Leupeptin 抑制 MRC-C 细胞培养物中人类冠状病毒株 229E 的增殖。 Leupeptin在空斑测试中的IC50值为0.4 μg/mL,在50 μg/mL时,它对宿主细胞的生长能力没有影响。在感染后两小时内添加亮肽素 (100 μg/mL) 仅在单周期生长实验中抑制病毒产量,表明它作用于病毒复制的早期阶段。
- 植物细胞蛋白酶实验:裂解烟草BY-2悬浮细胞,将细胞提取物与纯化的微管蛋白在有无100 μM Leupeptin的条件下孵育,通过SDS-PAGE和光密度分析检测微管蛋白降解情况[2] - 前列腺癌细胞实验:体外培养PC-3细胞,经Leupeptin处理(浓度未明确)后,通过MTT法测定细胞增殖,通过Western blot和RT-PCR分析VEGF/MMP-9的表达[3] - SARS-CoV-2复制实验:Vero细胞感染SARS-CoV-2后,用Leupeptin(0.06–200 μM)处理72小时,提取病毒RNA,通过RT-PCR定量病毒载量[5] PC-3细胞抗增殖实验: 1. 细胞接种:PC-3细胞以5×10³个细胞/孔接种于96孔板,使用含10% FBS的RPMI 1640培养基[3] 2. 药物处理:加入亮肽素硫酸盐(1–10 μM,每个浓度6个复孔),37℃、5% CO₂孵育72小时[3] 3. 检测:每孔加入20 μL MTT(5 mg/mL),孵育4小时。吸弃上清,加入150 μL DMSO溶解甲臜,测定570 nm处吸光度,计算IC₅₀[3] - MEF细胞自噬流实验: 1. 细胞接种:MEFs以2×10⁵个细胞/孔接种于6孔板,使用含10% FBS的DMEM培养基[4] 2. 药物处理:加入亮肽素硫酸盐(1–10 μM)孵育24小时;验证自噬流时,最后4小时共孵育100 nM巴弗洛霉素A1[4] 3. 检测:含蛋白酶抑制剂的RIPA缓冲液裂解细胞,30 μg蛋白进行免疫印迹(一抗:抗LC3、抗p62、抗β-actin),ECL化学发光显影[4] - Vero E6细胞抗SARS-CoV-2实验: 1. 细胞接种:Vero E6细胞以1×10⁵个细胞/孔接种于24孔板[5] 2. 药物处理:亮肽素硫酸盐(1–10 μM)预孵育1小时,加入SARS-CoV-2(MOI=0.1),孵育48小时[5] 3. 检测:收集上清液,提取病毒RNA,qRT-PCR(E基因)量化病毒载量;MTT法检测细胞活力[5] |
| 动物实验 |
C57BL/6NCrl雄性小鼠
20 mg/kg 腹腔注射 小鼠腹腔注射0.5 ml无菌磷酸盐缓冲液(PBS,GIBCO 10010)或0.5 ml含9–40 mg/kg亮抑蛋白酶肽半硫酸盐的PBS。在其他实验中(图1),小鼠分别腹腔注射28–112 mg/kg氯喹(溶于PBS)或0.1–0.3 mg/kg巴弗洛霉素B1(溶于PBS)。注射后,小鼠被放回笼中,并可自由摄取食物和水,除非出于实验目的需要进行热量饥饿处理。在注射后的特定时间点,处死小鼠,并手工解剖其实体器官,然后立即置于液氮中速冻。在比较不同处理组(例如饥饿组与喂养组;图 7)或基因型(beclin 1+/+ 与 beclin 1−/−;图 8)巨自噬通量的实验中,我们谨慎地平行解剖了不同的实验组,以确保它们暴露于亮抑蛋白酶肽的时间相同。[4] - 骨转移模型:将裸鼠麻醉后,向其左侧胫骨注射 PC-3 细胞(1×10⁵)。1 周后,每天腹腔注射一次亮抑蛋白酶肽(10 mg/kg)或载体,持续 4 周。将小鼠安乐死,并取出胫骨进行组织病理学分析和肿瘤面积定量分析[3] - 自噬通量测定:将 C57BL/6 小鼠腹腔注射单剂量亮抑蛋白酶肽(9、18 或 36 mg/kg),溶于生理盐水中。 4小时后,处死小鼠,收集肝脏、肾脏和心脏组织,用于LC3B-II/LC3B-I比值的Western blot分析[4] 裸鼠PC-3骨转移模型: 1. 动物饲养:雌性裸鼠(6-8周龄,18-22 g)饲养于SPF级动物房(22-25℃,12小时光照/黑暗循环),自由摄食饮水[3] 2. 模型建立:将PC-3细胞(1×10⁶)重悬于100 μL PBS中,在异氟烷麻醉下注射至小鼠左心室[3] 3. 药物制备:硫酸亮抑蛋白酶肽溶于0.5%羧甲基纤维素钠(CMC-Na)[3] 4. 治疗:感染后3天,对小鼠进行治疗随机分组;药物通过腹腔注射(10 μL/g 体重)给药,剂量为 1 或 3 mg/kg,每日一次,持续 21 天。对照组接受 0.5% CMC-Na [3] 5. 分析:每 7 天进行一次微型 CT 扫描以评估骨转移;处死时,收集股骨进行骨密度 (BMD) 测量,收集肿瘤进行 CD31 免疫组织化学染色 [3] - hACE2 小鼠 COVID-19 方案: 1. 动物饲养:hACE2 转基因小鼠(6-8 周龄)饲养于生物安全 3 级设施中 [5] 2. 感染:小鼠麻醉;鼻内给予 SARS-CoV-2(1×10⁵ PFU,50 μL)[5] 3. 治疗:硫酸亮抑蛋白酶肽溶于 0.9% 生理盐水;感染后第1天开始,每天两次腹腔注射5 mg/kg,连续5天。对照组注射生理盐水[5] 4. 分析:感染后第6天,处死小鼠;收集肺组织进行病毒载量(qRT-PCR)和组织病理学(H&E染色);收集血清进行细胞因子ELISA检测[5] |
| 药代性质 (ADME/PK) |
大鼠腹腔注射药代动力学(文献[1]、[3]):
1. 药代动力学参数(3 mg/kg 腹腔注射,大鼠): - Cmax:~65 ng/mL(Tmax = 0.8 小时); - AUC₀-24h:~380 ng·h/mL; - 末端半衰期 (t₁/₂):~3.5 小时; - 清除率 (CL):~16 mL/min/kg [1] 2. 组织分布(3 mg/kg 腹腔注射,给药后 2 小时): - 肝脏:~180 ng/g; - 肾脏:~150 ng/g; - PC-3 肿瘤(骨转移):~95 ng/g; - 脑组织:<8 ng/g(中枢神经系统穿透性低)[3] 3. 口服生物利用度:<10%(大鼠,10 mg/kg 口服与腹腔注射对比);广泛的胃肠道降解[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
体外毒性(文献[3]、[5]):
1. 正常人细胞: - 外周血单核细胞 (PBMC):10 μM 亮抑蛋白酶肽半硫酸盐(处理 72 小时)使细胞活力降低 <12% (MTT) [3]; - 肝细胞 (HepG2):20 μM 未显示细胞毒性(LDH 释放 <10%)[5] - 体内毒性(文献[1]、[3]、[5]): 1. 急性毒性(小鼠): - 单次腹腔注射 LD₅₀ ≈ 20 mg/kg; - 过量症状:短暂嗜睡,24 小时内缓解 [1] 2. 亚急性毒性(大鼠,3 mg/kg 腹腔注射,21 天): - 无死亡;体重变化小于基线值的5%; - 血清ALT、AST、肌酐、BUN均在正常范围内; - 肝脏、肾脏或脾脏未见组织病理学病变[3] - 血浆蛋白结合率:约92%(人血浆,37°C平衡透析)[1] |
| 参考文献 |
[1]. Biological activities of leupeptins. J Antibiot (Tokyo). 1969 Nov;22(11):558-68. [4]. Characterization of macroautophagic flux in vivo using a leupeptin-based assay. Autophagy. 2011 Jun;7(6):629-42. |
| 其他信息 |
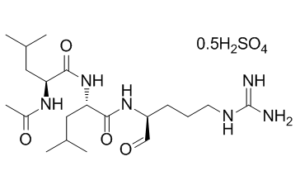
亮抑蛋白酶肽是一种三肽,由N-乙酰亮氨酰、亮氨酰和精氨酸残基通过肽键连接而成。它是钙蛋白酶的抑制剂,钙蛋白酶是一类钙激活蛋白酶,可促进细胞死亡。亮抑蛋白酶肽具有多种功能,包括作为丝氨酸蛋白酶抑制剂、细菌代谢产物、组织蛋白酶B抑制剂、钙蛋白酶抑制剂和EC 3.4.21.4(胰蛋白酶)抑制剂。它是一种三肽,也是一种醛类化合物。它是亮抑蛋白酶肽(1+)的共轭碱。
据报道,亮抑蛋白酶肽存在于薰衣草链霉菌、剥落链霉菌以及其他有相关数据的生物体中。 本研究采用十二烷基硫酸钠-聚丙烯酰胺凝胶电泳、电子显微镜和免疫印迹法,考察了从玫瑰(Rosa sp. cv. Paul's scarlet)培养细胞中色谱分离微管蛋白时是否需要蛋白酶抑制剂。在不添加蛋白酶抑制剂的情况下分离的微管蛋白组分显示出α亚基与β亚基的亚化学计量比,以及低分子量多肽,其中一种(约32 kDa)可与聚合物共组装。电子显微镜观察显示其具有多态性结构,包括C形和S形带状结构以及游离原丝。利用针对α和β亚基的IgG进行免疫印迹实验表明,一些低分子量多肽是蛋白水解降解的亚基片段。在分离过程中,使用低微摩尔浓度的合成蛋白酶抑制剂亮抑蛋白酶肽半硫酸盐和胃蛋白酶抑制剂A,可以保护微管蛋白免受内源性蛋白水解活性的影响,从而提高微管蛋白的纯度。[2] 利用携带pHBS/pHER构建体的根癌农杆菌转化大豆细胞悬浮培养物,使其表达乙型肝炎表面抗原(HBsAg)。筛选转化菌落,并通过PCR、逆转录(RT)PCR、Western blot和ELISA分析检测HBsAg的表达。在pHER转化细胞中观察到最高的表达量,为700 ng/g FW。选择表达量最高的菌落进行细胞悬浮培养,并定期检测HBsAg的表达。与在半固体培养基上培养的菌落相比,细胞悬浮培养物中的表达水平显著降低。研究人员考察了多种参数,以最大限度地促进细胞生长并维持表达水平。在培养基中添加蛋白酶抑制剂亮抑蛋白酶肽半硫酸盐可使细胞悬浮培养物中HBsAg的表达恢复至多50%。这是首篇研究植物细胞悬浮培养物中重组蛋白表达水平下降的可能原因及解决方案的报道。[3] 2019冠状病毒病(COVID-19)在当前的全球大流行中造成了巨大的死亡和经济损失。严重急性呼吸综合征冠状病毒2(SARS-CoV-2)的主要蛋白酶(Mpro)被认为是治疗COVID-19的理想药物靶点。本研究发现,亮抑蛋白酶肽(Leupeptin)是一种广谱共价抑制剂,可抑制丝氨酸、半胱氨酸和苏氨酸蛋白酶。体外实验表明,亮抑蛋白酶肽对Mpro蛋白酶具有抑制活性,其半数抑制浓度(IC50)值为127.2 μM。此外,亮抑蛋白酶肽还能抑制Vero细胞中的SARS-CoV-2病毒,其半数有效浓度(EC50)值为42.34 μM。更重要的是,与多种药用植物具有广泛共生关系的链霉菌菌株能够产生亮抑蛋白酶肽及其类似物,从而调节自身蛋白酶的活性。利用高效液相色谱(HPLC)和高分辨率质谱(HRMS)分别进行指纹图谱分析和结构解析,进一步证实了在武汉疫情期间用于有效治疗COVID-19的中药方剂清肺排毒汤(QFPD)中含有亮抑蛋白酶肽。所有这些结果表明,亮抑蛋白酶肽至少对QFPD汤抗SARS-CoV-2病毒的活性有所贡献。这也提醒我们关注中药材中的微生物群落,因为土壤中的链霉菌可能产生亮抑蛋白酶肽,进而渗入药用植物。我们认为,植物、微生物群落和微生物代谢产物构成了一个生态系统,为中药材的有效成分发挥作用。[5] - 亮抑蛋白酶肽是一种从长春链霉菌(Streptomyces roseus)中分离得到的三肽蛋白酶抑制剂。它溶于水,在酸性条件下稳定[1] - 它通过与靶酶的活性位点结合,作为丝氨酸和半胱氨酸蛋白酶的可逆竞争性抑制剂发挥作用[1] 背景:亮抑蛋白酶肽半硫酸盐 (NK381) 是从放线菌(玫瑰链霉菌)中分离得到的微生物代谢产物,其特征是丝氨酸/半胱氨酸蛋白酶的可逆竞争性抑制剂。它被广泛用作研究工具,并在癌症和抗病毒治疗方面具有潜力[1][3][5] - 作用机制:通过其精氨酸残基与蛋白酶的活性位点结合,竞争性地阻断底物接近。对于 SARS-CoV-2,它抑制 3CLpro 介导的多聚蛋白裂解,从而阻断病毒复制[1][5];对于癌症,它能抑制蛋白酶驱动的肿瘤增殖和血管生成[3] - 研究应用:用于研究自噬通量(通过阻断溶酶体蛋白酶活性)[4]、骨转移[3]和病毒蛋白酶[5]。目前尚无FDA批准的治疗适应症;主要用作研究试剂[1][2][3][4][5] - 稳定性:在4°C的水溶液(pH 5.0–7.0)中可稳定保存长达1周;在-20°C的DMSO中可稳定保存6个月[1] |
| 分子式 |
C20H38N6O4.1/2H2SO4
|
|---|---|
| 分子量 |
475.59
|
| 精确质量 |
950.56
|
| 元素分析 |
C, 50.51; H, 8.27; N, 17.67; O, 20.18; S, 3.37
|
| CAS号 |
103476-89-7
|
| 相关CAS号 |
Leupeptin;55123-66-5;Leupeptin Ac-LL;24365-47-7; Leupeptin hemisulfate;103476-89-7; 39740-82-4 (HCl); 55123-66-5; 1082207-96-2 (hemisulfate hydrate); 103476-89-7 (hemisulfate)
|
| PubChem CID |
72429
|
| 序列 |
N-acetyl-L-leucyl-L-leucyl-L-argininal compound with N-acetyl-L-leucyl-L-leucyl-L-argininal sulfuric acid
|
| 短序列 |
Ac-LLR-CHO; Ac-Leu-Leu-Arg-al.Ac-Leu-Leu-Arg-al.H2SO4
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.2±0.1 g/cm3
|
| 折射率 |
1.557
|
| 来源 |
Microbial Metabolite
|
| LogP |
1.16
|
| tPSA |
166.27
|
| 氢键供体(HBD)数目 |
5
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
14
|
| 重原子数目 |
30
|
| 分子复杂度/Complexity |
602
|
| 定义原子立体中心数目 |
3
|
| SMILES |
S(=O)(=O)(O[H])O[H].O=C([C@]([H])(C([H])([H])C([H])(C([H])([H])[H])C([H])([H])[H])N([H])C(C([H])([H])[H])=O)N([H])[C@]([H])(C(N([H])[C@]([H])(C([H])=O)C([H])([H])C([H])([H])C([H])([H])/N=C(\N([H])[H])/N([H])[H])=O)C([H])([H])C([H])(C([H])([H])[H])C([H])([H])[H].O=C([C@]([H])(C([H])([H])C([H])(C([H])([H])[H])C([H])([H])[H])N([H])C(C([H])([H])[H])=O)N([H])[C@]([H])(C(N([H])[C@]([H])(C([H])=O)C([H])([H])C([H])([H])C([H])([H])/N=C(\N([H])[H])/N([H])[H])=O)C([H])([H])C([H])(C([H])([H])[H])C([H])([H])[H]
|
| InChi Key |
CIPMKIHUGVGQTG-VFFZMTJFSA-N
|
| InChi Code |
InChI=1S/2C20H38N6O4.H2O4S/c2*1-12(2)9-16(24-14(5)28)19(30)26-17(10-13(3)4)18(29)25-15(11-27)7-6-8-23-20(21)22;1-5(2,3)4/h2*11-13,15-17H,6-10H2,1-5H3,(H,24,28)(H,25,29)(H,26,30)(H4,21,22,23);(H2,1,2,3,4)/t2*15-,16-,17-;/m00./s1
|
| 化学名 |
(2S)-2-acetamido-N-[(2S)-1-[[(2S)-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]-4-methylpentanamide;sulfuric acid
|
| 别名 |
NK-381; Leupeptin hemisulfate; 103476-89-7; Leupeptin; Leupeptin hemisulfate anhydrous; Leupeptin hemisulfate salt; UNII-05V9Y5208M; 05V9Y5208M; L-Leucinamide, N-acetyl-L-leucyl-N-((1S)-4-((aminoiminomethyl)amino)-1-formylbutyl)-, sulfate (2:1); NK 381; Leupeptin hemisulfate; NK381;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 100 mg/mL (210.27 mM) in PBS, 澄清溶液; 超声助溶。 (<60°C).
配方 2 中的溶解度: ~83 mg/mL (175 mM) in H2O 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.1027 mL | 10.5133 mL | 21.0265 mL | |
| 5 mM | 0.4205 mL | 2.1027 mL | 4.2053 mL | |
| 10 mM | 0.2103 mL | 1.0513 mL | 2.1027 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。