| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| Other Sizes |
|

| 靶点 |
Microbial Metabolite; isomer of Lithocholic acid; The targets of Isolithocholic acid involve multiple cellular signaling pathways. Studies have demonstrated its ability to inhibit multiple key steps of C. difficile spore germination and growth. Furthermore, as an agonist of GPBAR1 (G protein-coupled bile acid receptor 1), this compound may regulate intestinal L-cell differentiation and GLP-1 secretion through this receptor. Notably, its stereoisomer Isoallolithocholic acid has been shown to regulate T cell differentiation by modulating RORγt and FoxP3 expression, and although this activity has not been explicitly reported for Isolithocholic acid, the immunomodulatory functions of the bile acid family suggest it may participate in similar metabolic regulatory networks.
|
|---|---|
| 体外研究 (In Vitro) |
在无细胞和细胞体系中,Isolithocholic acid 表现出多种生物活性。它对艰难梭菌具有显著的抑制作用:在0.01%浓度下不抑制CF5和M120菌株的孢子萌发,但在较高浓度(0.1%)下可显著抑制;在0.00003%浓度下即可阻止CD196、M68、CF5、630和BI9等菌株的生长,并显著降低菌株CF5、BI9、M120和630的毒素活性;在0.0003%浓度下,除R20291和M120外,所有测试菌株的毒素活性均显著降低。此外,其立体异构体Isoallolithocholic acid在20 μM浓度下可将Th17细胞分化减少约50%,且不依赖于RORγt表达。该化合物还通过诱导线粒体活性氧(mitoROS)的产生来增强FoxP3的表达,促进调节性T细胞(Tregs)分化。
在 0.01% 的浓度下,异寡胆酸不会显着阻碍 CF5 和 M120 孢子的萌发和生长,但在 0.1% 的更高浓度下,则会显着阻碍 CF5 和 M120 孢子的萌发和生长。异石胆酸 (0.00003%) 显着降低菌株 CF5、BI9、M120 和 630 的毒素活性,并抑制 CD196、M68、CF5 和 BI9 的生长。除 R20291 和 M120 外,异石胆酸 (0.0003%) 会导致所有菌株的毒素活性显着下降[3]。 |
| 体内研究 (In Vivo) |
Isolithocholic acid 的体内活性主要通过动物模型进行研究。在高脂饮食(HFD)诱导的肥胖大鼠模型中,与正常饮食喂养的大鼠相比,从第28天起,高脂饮食组的粪便Isolithocholic acid水平显著降低,提示肥胖状态可能影响该胆汁酸的代谢或排泄。其立体异构体Isoallolithocholic acid在体内实验中显示出免疫调节活性:在B6小鼠中,通过饮食给予0.03%的Isoallolithocholic acid,连续7天,可增强调节性T细胞(Tregs)的群体。GPBAR1激动剂(如石胆酸)在体内可选择性增加L细胞密度并提高GLP-1分泌能力,改善葡萄糖耐受性,提示Isolithocholic acid可能具有类似的代谢调节功能。
与常规饮食的大鼠相比,高脂肪饮食 (HFD) 组的粪便异石胆酸水平从第 28 天开始明显下降[4]。 |
| 酶活实验 |
Isolithocholic acid与GPBAR1受体的结合可通过基于细胞的功能测定法进行评估。典型流程:将表达GPBAR1受体的细胞系接种于96孔板中,与不同浓度的Isolithocholic acid(0.1-100 μM)共孵育。通过检测细胞内cAMP的积累量来定量受体激活程度,可使用均相时间分辨荧光(HTRF)或酶联免疫(ELISA)方法检测cAMP水平。对于艰难梭菌孢子萌发抑制实验:将C. difficile孢子悬浮于含有牛磺胆酸(作为萌发诱导剂)的缓冲液中,加入不同浓度的Isolithocholic acid(0.00003%-0.1%),在37°C厌氧条件下孵育,通过显微镜计数或OD600吸光度变化评估孢子萌发率。
研究了使用3α和3β氚化胆汁酸将鹅脱氧胆酸和石胆酸细菌转化为相应的3β-羟基差向异构体的机制。在与产气荚膜梭菌孵育20小时后,3-氧代胆汁酸转化为3-α-(85%)和3-β-(15%)羟基胆汁酸。当[3β-3H]鹅脱氧胆酸或[3β3-H]石胆酸与细菌一起孵育时,在水性介质中回收了大约75%的放射性,胆汁酸部分中大约15%的放射性与异胆汁酸的3α位置有关。当[3β-3H]鹅脱氧胆酸与未标记的3-氧代-5β胆酸一起孵育时,回收了氚化的石胆酸和异石胆酸。只有当假设存在3-氧代中间体,并且在3-氧代化合物的还原过程中,胆汁酸中的3-β氢被细菌辅酶(NAD+或NADP+)转移到异胆汁酸的3-α位时,才能解释这些结果[1]。 |
| 细胞实验 |
Isolithocholic acid在细胞实验中常用于研究其对艰难梭菌的作用或免疫调节功能。典型流程(艰难梭菌生长抑制实验):将C. difficile菌株(如CD196、M68、BI9、630等)接种于BHI培养基中,加入不同浓度的Isolithocholic acid(0.00003%-0.1%),在37°C厌氧条件下培养24-48小时。通过OD600测定细菌生长密度,并使用Vero细胞毒性实验评估上清液中的毒素活性。对于T细胞分化研究(基于立体异构体的实验流程):从小鼠脾脏中分离CD4+ T细胞,在Th17极化条件(IL-6和TGF-β)下培养,加入20 μM Isolithocholic acid(或其异构体)。培养72小时后,通过流式细胞术检测IL-17A表达来评估Th17细胞比例,或通过FoxP3染色检测Treg细胞分化。
|
| 动物实验 |
Isolithocholic acid的体内研究通常采用代谢疾病动物模型。典型流程(高脂饮食诱导肥胖大鼠模型):将雄性Sprague-Dawley大鼠随机分为正常饮食组和高脂饮食(HFD)组。从第0天至第56天,定期收集粪便样本(如第0、7、14、21、28、35、42、49、56天),通过LC-MS/MS检测粪便中的Isolithocholic acid及其他胆汁酸水平。在第56天实验终点,收集血清、肝脏和肠道组织进行进一步分析。对于免疫调节研究(基于立体异构体的流程):将B6小鼠随机分组,通过饮食给予0.03%的Isolithocholic acid(或异构体),连续7天。在某些实验中,可联合抗CD3抗体处理以激活T细胞。收集脾脏和肠系膜淋巴结,通过流式细胞术检测CD4+ FoxP3+ Treg细胞比例。
|
| 药代性质 (ADME/PK) |
Isolithocholic acid作为胆汁酸家族成员,其药代动力学行为遵循胆汁酸的肠肝循环规律。计算预测的理化性质:LogP约为6.7,表明其具有较高的亲脂性;氢键供体数为2,氢键受体数为3,可旋转键数为4。该化合物在生理pH条件下主要以阴离子形式存在,需要通过特异性载体蛋白进行跨膜转运。它由肠道菌群在结肠中产生,通过门静脉被重吸收进入肝脏,随后分泌至胆汁,再进入肠道,形成肠肝循环。在肥胖状态下,粪便中的Isolithocholic acid水平显著降低,提示代谢状态可能影响其体内水平。储存条件:粉末在-20°C可稳定保存3年,4°C可保存2年;溶解后在-80°C可保存6个月,-20°C可保存1个月。在DMSO中的溶解度为20 mg/mL。
|
| 毒性/毒理 (Toxicokinetics/TK) |
根据现有材料安全数据表(MSDS),Isolithocholic acid被归类为非危险物质或混合物,在正常实验操作条件下被认为是安全的。该产品仅限科研使用,不可用于人体或兽医。作为内源性胆汁酸,在正常生理浓度下通过肠肝循环维持稳态,但高浓度胆汁酸具有潜在毒性,主要表现为对细胞膜的破坏作用。IARC、ACGIH、NTP和OSHA均未将该化合物或其组分归类为人类致癌物。操作时应由具备资质的技术人员按照标准实验室规范进行,建议佩戴个人防护装备。需要注意的是,与Isolithocholic acid结构相似的胆汁酸在高浓度下对某些细胞类型具有细胞毒性,在代谢异常状态下其异常积累可能参与病理过程。
|
| 参考文献 |
|
| 其他信息 |
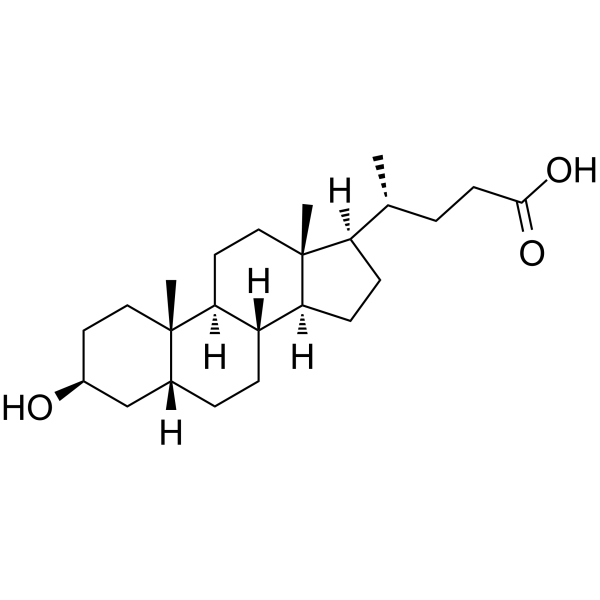
异石胆酸是一种单羟基-5β-胆烷酸,其3位上有一个β-羟基取代基。它是石胆酸的3β-羟基差向异构体。它既是人体代谢产物,也是大鼠代谢产物和外源性物质代谢产物。它是一种胆汁酸、3β-羟基类固醇、单羟基-5β-胆烷酸和C24类固醇。它是异石胆酸的结合酸。
异石胆酸是由鹅脱氧胆酸在细菌作用下形成的胆汁酸,通常与甘氨酸或牛磺酸结合。它作为一种去污剂,可以溶解脂肪以促进吸收,自身也能被吸收。它被用作利胆剂和利胆药。 过去几十年艰难梭菌感染流行病学的变化给艰难梭菌相关疾病的治疗带来了重大挑战。胃肠道菌群能够抵抗艰难梭菌的定植,越来越多的证据表明,肠道微生物来源的次级胆汁酸(SBA)在其中发挥着重要作用。我们假设,不同年龄和核糖体分型的艰难梭菌菌株,其生命周期(包括孢子萌发和生长、生长以及毒素产生)对SBA的敏感性存在差异。本研究使用艰难梭菌菌株R20291和CD196(核糖体分型027)、M68和CF5(017)、630(012)、BI9(001)以及M120(078)来研究牛磺胆酸(TCA)介导的孢子萌发和生长、生长以及毒素活性,并考察了在有无肠道微生物来源的胆汁酸(脱氧胆酸、异脱氧胆酸、石胆酸、异石胆酸、熊脱氧胆酸、ω-鼠胆酸和猪脱氧胆酸)存在的情况下,这些胆汁酸存在于人和小鼠的大肠中。结果表明,在不添加胆汁酸的情况下,不同艰难梭菌菌株的萌发率、生长动力学和毒素活性存在差异。其中,艰难梭菌M120菌株与其他菌株差异较大,其萌发和生长能力较强,但毒素活性显著低于其他菌株。许多胆汁酸(SBA)能够以剂量依赖的方式抑制三羧酸循环(TCA)介导的孢子萌发和生长、生长以及毒素活性,但不同菌株和核糖体分型的抑制程度和耐药性存在差异。本研究表明,临床相关的艰难梭菌菌株在暴露于胃肠道中存在的胆汁酸时可能产生不同的反应。[3] 肥胖已成为全球性的健康问题,并引起了公众的广泛关注。本研究旨在利用高脂饮食(HFD)诱导的大鼠肥胖模型,阐明胆汁酸及其与肠道菌群在肥胖发展过程中的作用。我们收集了粪便、血浆、肝组织和肠组织样本,并开发了一种采用超高效液相色谱-质谱联用(UPLC-MS)策略的胆汁酸定量方法。随后,我们评估了所收集生物基质中的胆汁酸通量。我们发现,无论饮食方案如何,牛磺酸结合胆汁酸都是肝脏中的主要胆汁酸种类,而非结合胆汁酸则主要存在于血浆中。然而,高脂饮食(HFD)导致总胆汁酸池略有增加,尤其是血浆和肝组织中脱氧胆酸(DCA)(对照组为138.67 ± 37.225 nmol/L,HFD组为242.61 ± 43.16 nmol/L,p = 0.014)和牛磺脱氧胆酸(TDCA)(对照组为2.8 ± 0.247 nmol/g,HFD组为4.5 ± 0.386 nmol/g,p = 0.0018)的水平显著升高,这与肠道组织和粪便中DCA水平的升高相一致。这些变化与 Blautia、Coprococcus、Intestinimonas、Lactococcus、Roseburia 和 Ruminococcus 等属的丰度增加相关。我们的研究揭示了肥胖发展过程中胆汁酸的通量及其与肠道菌群的关系,并阐明了高脂饮食对健康的不利影响。[4] |
| 分子式 |
C24H40O3
|
|---|---|
| 分子量 |
376.57
|
| 精确质量 |
376.297
|
| 元素分析 |
C, 76.55; H, 10.71; O, 12.75
|
| CAS号 |
1534-35-6
|
| 相关CAS号 |
Lithocholic acid;434-13-9;Isoallolithocholic acid;2276-93-9
|
| PubChem CID |
164853
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.1±0.1 g/cm3
|
| 沸点 |
511.0±23.0 °C at 760 mmHg
|
| 闪点 |
276.9±19.1 °C
|
| 蒸汽压 |
0.0±3.0 mmHg at 25°C
|
| 折射率 |
1.528
|
| LogP |
6.7
|
| tPSA |
57.5
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
4
|
| 重原子数目 |
27
|
| 分子复杂度/Complexity |
574
|
| 定义原子立体中心数目 |
9
|
| SMILES |
C[C@H](CCC(=O)O)[C@H]1CC[C@@H]2[C@@]1(CC[C@H]3[C@H]2CC[C@H]4[C@@]3(CC[C@@H](C4)O)C)C
|
| InChi Key |
SMEROWZSTRWXGI-WFVDQZAMSA-N
|
| InChi Code |
InChI=1S/C24H40O3/c1-15(4-9-22(26)27)19-7-8-20-18-6-5-16-14-17(25)10-12-23(16,2)21(18)11-13-24(19,20)3/h15-21,25H,4-14H2,1-3H3,(H,26,27)/t15-,16-,17+,18+,19-,20+,21+,23+,24-/m1/s1
|
| 化学名 |
(4R)-4-[(3S,5R,8R,9S,10S,13R,14S,17R)-3-hydroxy-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1H-cyclopenta[a]phenanthren-17-yl]pentanoic acid
|
| 别名 |
Isolithocholic acid; 1534-35-6; beta-Lithocholic acid; 3-Epilithocholic acid; beta-Lithocholanic acid; (4R)-4-[(3S,5R,8R,9S,10S,13R,14S,17R)-3-hydroxy-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1H-cyclopenta[a]phenanthren-17-yl]pentanoic acid; 3beta-Hydroxy-5beta-cholan-24-oic Acid; Iso-LCA;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: 28.57 mg/mL (75.87 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.86 mg/mL (7.59 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 28.6 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.86 mg/mL (7.59 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 28.6 mg/mL 澄清 DMSO 储备液加入 900 μL 20% SBE-β-CD 生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.86 mg/mL (7.59 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.6555 mL | 13.2777 mL | 26.5555 mL | |
| 5 mM | 0.5311 mL | 2.6555 mL | 5.3111 mL | |
| 10 mM | 0.2656 mL | 1.3278 mL | 2.6555 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。